17 лютого, 2023
Можливості цитиколіну в запобіганні вікових змін: фармакологічні характеристики, вплив на когнітивні показники, нейропротекторні ефекти
Населення світу старіє: майже в кожній країні спостерігається зростання кількості та частки людей похилого віку. Прогнози Організації Об’єднаних Націй про перспективи світового народонаселення показують, що до 2050 року 1 зі 6 людей (16%) у світі матиме вік >65 років (World Population Prospects, 2019). Очікуваним викликом старіння населення є підвищення рівня проблем зі здоров’ям, пов’язаних із віковими змінами, як-от зниження когнітивних функцій.
Хоча вік – важливий провісник зниження когнітивних здібностей, цей процес є складною взаємодією багатьох сприятливих факторів, у т. ч. демографічних, генетичних, соціально-економічних, екологічних параметрів і параметрів харчування (Dominguez L. J. et al., 2018). Сьогодні, на жаль, відсутні ефективні фармацевтичні методи лікування вікового зниження когнітивних функцій, що підкреслює важливість стратегій профілактики цих станів. Існує значна кількість доказів того, як окремі речовини та біологічно активні сполуки можуть впливати на зниження когнітивних функцій, пов’язане з віком (Prince M. et al., 2014).
Однією з найперспективніших біологічно активних сполук є цитиколін – фармацевтична форма ендогенної сполуки цитидин‑5’-дифосфат (CDP)-холіну; це один із препаратів, які найчастіше призначають для лікування когнітивних розладів у кількох європейських країнах (Secades J. J. et al., 1995; Hurtado O. et al., 2011). Як показано в різних експериментальних дослідженнях, цитиколін має нейропротекторні властивості, підвищує інтрасинаптичну концентрацію ацетилхоліну, сприяє синтезу фосфоліпідів, позитивно впливає на стан нейронів (Fioravanti M. et al., 2004; Cakir А. et al., 2022).
Докази ефективності цитиколіну
CDP‑холін є водорозчинною сполукою з біодоступністю ≥90%. Екзогенний CDP‑холін (введений як перорально, так і внутрішньовенно) гідролізується, поглинається у вигляді цитидину та холіну й повторно синтезується в мозку за допомогою специфічного ферменту (Secades J. J. et al., 2011). У плазмі крові спостерігаються два піки – через 1 та 24 год після прийому.
Загальні докази ефективності CDP‑холіну на функцію пам’яті та поведінку (щонайменше в коротко- і середньостроковій перспективі) були показані в огляді групи лікарів під керівництвом доктора Р. Fioravanti у 2005 році. До цього огляду було включено 14 досліджень; учасники спостерігалися в них від 20 днів до 12 міс. Учені з’ясували, що вирішальним моментом стала тривалість прийому цитиколіну; фактично виявилося, що захист клітинних мембран, нейропластичність, збільшення біосинтезу ацетилхоліну й інші важливі нейропротекторні ефекти цього препарату потребують його постійного прийому (щонайменше 6 міс для найкращих результатів). Учені дійшли висновку, що цитиколін виглядає як препарат зі здатністю сприяти безпечній нейропротекції, посилювати ендогенні захисні шляхи, одночасно готуючи сценарій для пластичності. Можливі задіяні механізми стосуються поліпшення клітинних функцій, спрямованих здебільшого на збереження функції та цілісності мембран (Hurtado O. et al., 2011).
Під час іншого дослідження вчені також звернули увагу на чіткий вплив цитиколіну на кілька когнітивних показників (García-Cobos R. et al., 2010). Зокрема, вони відзначили, що прийом цієї речовини покращує:
- як негайне, так і відтерміноване пригадування слів і предметів;
- коротко- та довгострокову пам’ять, увагу і перцептивно-моторні здібності, а також поведінковий /емоційний контроль;
- вербальну пам’ять у людей похилого віку, які попередньо спостерігали погіршення цього показника.
Схожі результати було отримано і в іншій роботі (Al-kuraishy N. et al., 2020), де здорові добровольці впродовж 2 тиж приймали цитиколін по 500 мг/день або плацебо. Вчені дійшли висновку, що цитиколін покращує психомоторну пильність людини, збудження та зорову робочу пам’ять зі значним зменшенням окислювального стресу порівняно із плацебо. Вчені контролювали можливість учасників до довготривалої підтримки уваги, зорову робочу пам’ять і маркери окисного стресу на початку та наприкінці дослідження. Виявилося, що цитиколін змінював більшість змінних психомоторних показників і робочої пам’яті (p<0,01) зі значним зменшенням окисного стресу.
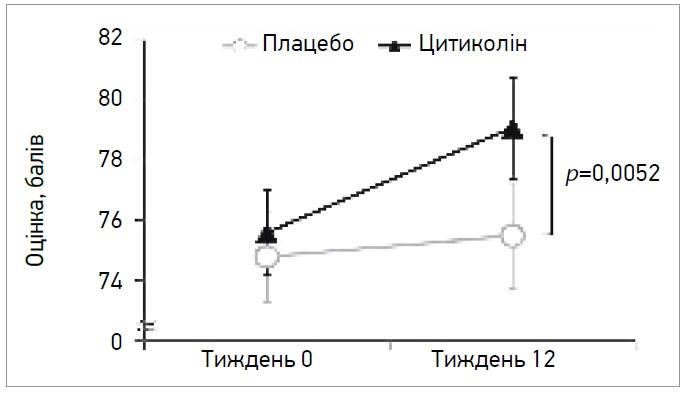
Покращення когнітивних показників, у т. ч. пам’яті, на тлі прийому цитиколіну спостерігали в своєму дослідженні вчені під керівництвом доктора Eri Nakazaki (2021). Вони пропонували учасникам (здоровим чоловікам і жінкам віком від 50 до 85 років) приймати впродовж 12 тиж 500 мг/день цитиколіну або плацебо. Виявилося, що вживання цитиколіну покращило загальну продуктивність пам’яті, особливо епізодичну пам’ять, у здорових літніх чоловіків і жінок (рис.).
Рис. Загальні показники пам’яті після 12 тиж прийому добавок цитиколіну в групі цитиколіну та плацебо
Під час оцінки отриманих результатів учені констатували, що регулярне вживання цитиколіну може бути безпечним і потенційно корисним методом профілактики погіршення пам’яті через вікові зміни.
Нейропротекторні ефекти
Вплив на експресію сиртуїнів
Один із доказів нейропротекторної активності цитиколіну походить від його ефекту, пов’язаного із сиртуїнами. Сиртуїни є висококонсервативними NAD‑залежними протеїновими деацетилазами, здатними регулювати старіння в нижчих організмах; вони відіграють важливу роль у довголітніх (Bellizzi D. et al., 2007) і у вікових захворюваннях вищих організмів (Donmez G. et al., 2013).
У ссавців існує 7 сиртуїнів (SIRT1-7), які експресуються в різних тканинах із різною локалізацією клітин і ферментативною активністю (Donmez G. et al., 2010). SIRT1 є важливим регулятором самовідновлення нервових стовбурових клітин гіпокампа / дорослих нейронних клітин-попередників і потенційним медіатором ефекту метаболічних змін (Ma C. Y. et al., 2014). Hurtado і співавт. у 2013 році під час свого дослідження показали, що CDP‑холін збільшує експресію білка SIRT1 у мозку щурів, культивованих нейронах і циркулювальних мононуклеарних клітинах крові; цей ефект значно залучено до нейропротекторної дії цього препарату.
Вплив на нейропластичність
Цитоколін є нейро- та мембранопротектором; він пригнічує синтез фосфоліпази А2 зі зменшенням накопичення жирних кислот, відновлює функціонування Na+-K+-АТФ‑ази, покращує холінергічну передачу, протидіє апоптозу.
Відомо, що цитиколін реалізує нейропротекторну дію за рахунок збереження в нейронах сфінгомієліну, кардіоліпіну й арахідонової кислоти, а також фосфатидилетаноламіну та фосфатидилхоліну, покращує активність глутатіонредуктази і доступність холіну для синтезу ацетилхоліну (Trimmel et al., 2018). Сполука знижує концентрацію глутамату в нейронах шляхом інтенсифікації поглинання глутамату астроцитами за рахунок збільшення експресії транспортерів глутамату. Коли доступність холіну є низькою, а потреба в ацетилхоліні високою, холін із нейрональних клітинних мембран фосфатидилхоліну буде пулом для синтезу ацетилхоліну (Kim et al., 2018).
Крім вищезазначених механізмів, цитиколін сприяє відновленню ушкоджених клітинних мембран за рахунок основного метаболіту холіну, що вбудовується в мітохондріальні та цитоплазматичні мембрани. Схожим чином він сприяє відновленню нервових закінчень, мембран нейронів і покращенню їхньої функціональної активності.
Нівелювання наслідків деривації сну
Сон є дуже важливим для фізичної та розумової працездатності (Tarokh L. et al., 2016). Хвороби, стрес, фактори навколишнього середовища та вікові зміни можуть викликати розлади сну або його депривацію. Під час нового дослідження на лабораторних тваринах (Cakir А. et al., 2022) виявили, що прийом цитиколіну може послабити несприятливий вплив депривації сну на синаптичне функціонування гіпокампа, нормалізуючи концентрацію специфічних білків.
Висновки
- CDP-холін (цитиколін) має сприятливу фізіологічну дію на клітинну функцію, адже він і продукти його гідролізу відіграють важливу роль у синтезі фосфоліпідів та відновленні нейронів.
- Цитиколін є ефективним при багатьох когнітивних порушеннях, він покращує довгострокову та короткострокові пам’ять, активізує увагу, зменшує поведінкову й емоційну імпульсивність, у т. ч. у разі вікових змін.
- Тривале лікування є безпечним. Застосування препарату перорально, внутрішньом’язово або внутрішньовенно (до 2000 мг/добу) не призводить до серйозних побічних ефектів.
За матеріалами: Świątkiewicz M., Grieb P. Citicoline for Supporting Memory in Aging Humans. Aging and disease. 2022 https://doi.org/10.14336/AD.2022.0913
Довідка «ЗУ»
На українському фармацевтичному ринку цитиколін представлений препаратом Роноцит (компанія World Medicine). Препарату притаманний багатогранний механізм дії, який забезпечує відновлення вмісту фосфоліпідів клітинних мембран, покращення холінергічної передачі, модуляцію дофамін- і глутаматергічної нейротрансмісії, посилення антиоксидантного захисту, протидію апоптозу, стимуляцію процесів нейро- й ангіогенезу. Роноцит представлений в ін’єкційній формі випуску (1000 мг цитиколіну в 4 мл розчину) для внутрішньовенних або внутрішньом’язових ін’єкцій і у вигляді розчину для перорального прийому (100 мг цитиколіну в 1 мл, у флаконах по 10 мл). Рекомендована доза для дорослого пацієнта становить до 2000 мг/добу.
Підготувала Юлія Котикович
Медична газета «Здоров’я України 21 сторіччя» № 1-2 (537-538), 2023 р.