19 травня, 2023
Місце цитиколіну в лікуванні черепно-мозкової травми
 Черепно-мозкова травма (ЧМТ) може виникати в будь-якій непередбачуваній ситуації – від простого удару голови до проникаючого поранення головного мозку. За балами шкали коми Глазго (GCS) ЧМТ класифікують на легку, середню та тяжку [2]. Легка ЧМТ (також відома як струс мозку) спочатку вважалася такою, шо має доброякісний перебіг; вона привернула до себе величезну увагу фахівців, адже спостерігалися деякі несприятливі нейропсихологічні наслідки в цивільних (наприклад, у спортсменів, які займаються контактними видами спорту), а також у військовослужбовців. ЧМТ середнього та тяжкого ступенів – основна причина смерті та інвалідності внаслідок травм [1].
Черепно-мозкова травма (ЧМТ) може виникати в будь-якій непередбачуваній ситуації – від простого удару голови до проникаючого поранення головного мозку. За балами шкали коми Глазго (GCS) ЧМТ класифікують на легку, середню та тяжку [2]. Легка ЧМТ (також відома як струс мозку) спочатку вважалася такою, шо має доброякісний перебіг; вона привернула до себе величезну увагу фахівців, адже спостерігалися деякі несприятливі нейропсихологічні наслідки в цивільних (наприклад, у спортсменів, які займаються контактними видами спорту), а також у військовослужбовців. ЧМТ середнього та тяжкого ступенів – основна причина смерті та інвалідності внаслідок травм [1].
Лікування ЧМТ має бути спрямованим на зниження тяжкості наслідків і покращення одужання. Важливе значення відіграють поліпшення моніторингу та знання патофізіології ЧМТ, що може змінити поточне лікування, дозволити адекватніші втручання, які могли б покращити кінцеві результати, зменшивши пов’язану з ЧМТ інвалідність [3]. Згідно з гіпотезою Монро – Келлі, загальний внутрішньочерепний об’єм (складається із тканини мозку, спинномозкової рідини, венозної та артеріальної крові) завжди має залишатися сталим, оскільки черепна коробка є жорсткою і нерозширюваною ємністю. При введенні додаткового відділу (як за гематоми) має відбуватися компенсаторне зменшення іншого відділу, щоб запобігти внутрішньочерепній гіпертензії. Церебральний перфузійний тиск (ЦПТ) визначається як середній артеріальний тиск (САТ) мінус внутрішньочерепний тиск (ВЧТ). У разі підвищення ВЧТ ЦПТ знижується, що може зумовити вторинну церебральну ішемію та інфаркт. Отже, основна мета лікування ЧМТ – запобігання вторинному ураженню [4].
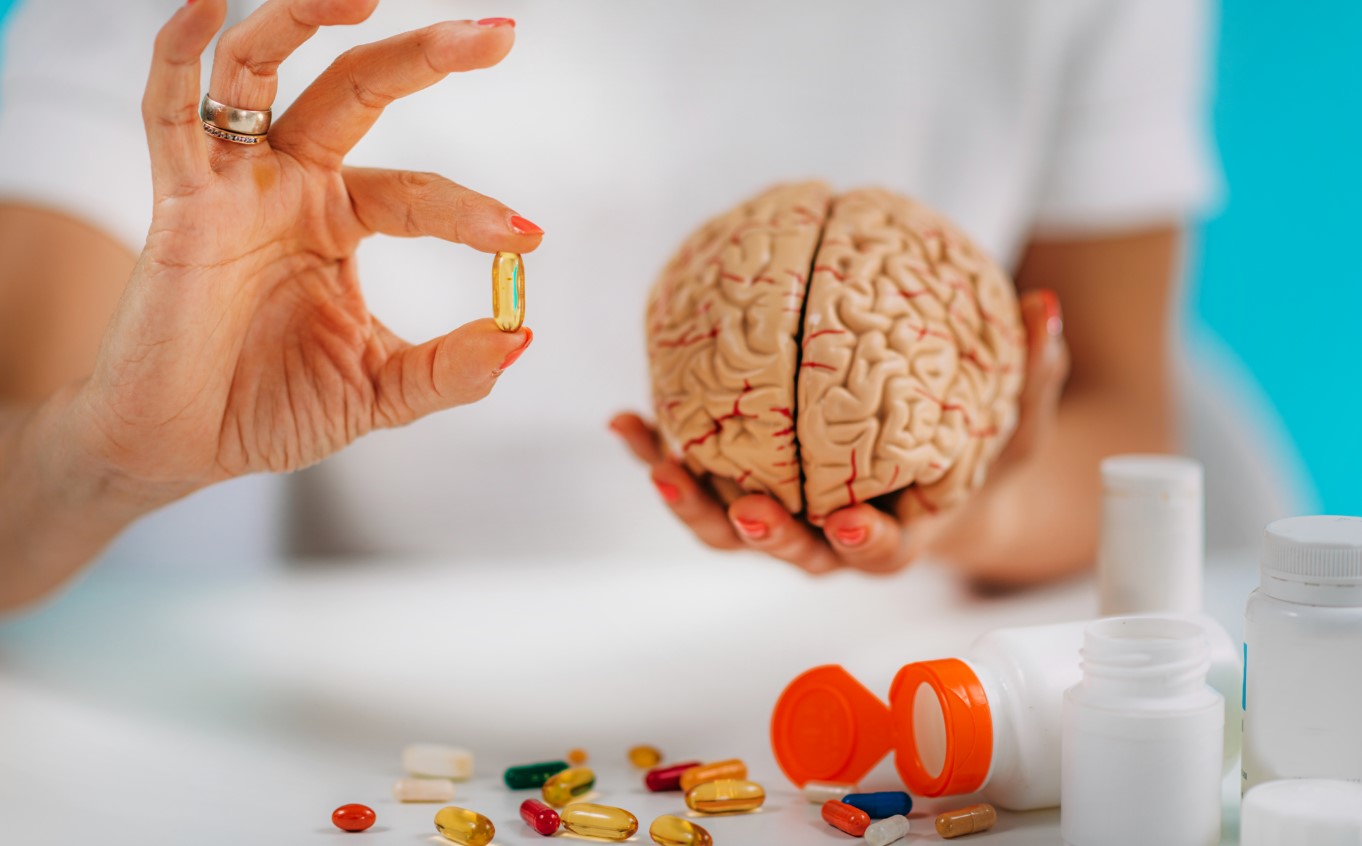
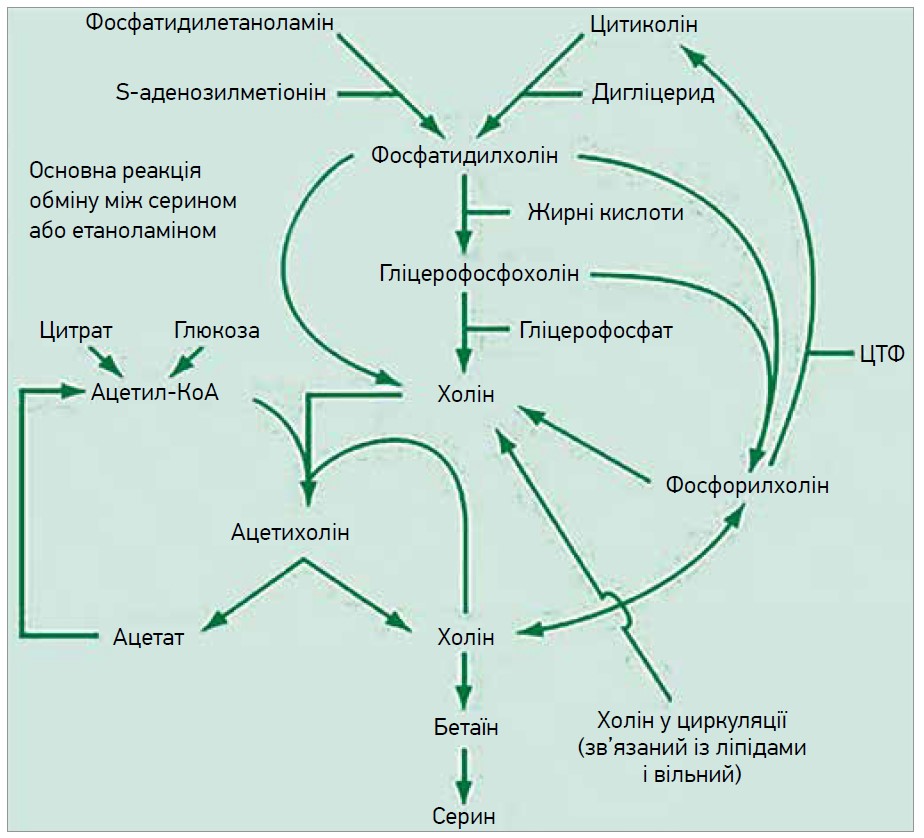
Серед біохімічних чинників у патофізіології ЧМТ провідну роль має порушення метаболізму фосфоліпідів, тому саме через ці патофізіологічні стани існує думка фахівців щодо доцільності застосування препаратів, які можуть мати захисну та відновлювальну чи репаративну дію на нервову систему [6]. Цитиколін (цитидиндифосфохолін, ЦДФ‑холін) являє собою складну органічну молекулу, яка бере участь у синтезі фосфоліпідів клітинної мембрани, синтезі ацетилхоліну, процесах нейротрансмітерної передачі [5]. За його екзогенного введення (як ліків) має широкий спектр біохімічної та фармакологічної дії, є передбачуваним засобом лікування деяких неврологічних захворювань, у т. ч. ЧМТ [2] (рис. 1).
Рис. 1. Зв’язок між метаболізмом цитиколіну та холіну, церебральними фосфоліпідами й ацетилхоліном
Експериментальні дані
За результатами нещодавніх досліджень було продемонстровано, що цитиколін здатний запобігати деградації фосфоліпідів холіну й етаноламіну під час ішемії мозку [7], а також відновлювати цілісність гематоенцефалічного бар’єра [8]. Інші експериментальні випробування довели захисну дію цитиколіну на нейрональні культури в умовах гіпокапнії [2], а також позитивний вплив на поріг реакції збудження, скорочуючи тривалість коми, спричиненої різними механізмами.
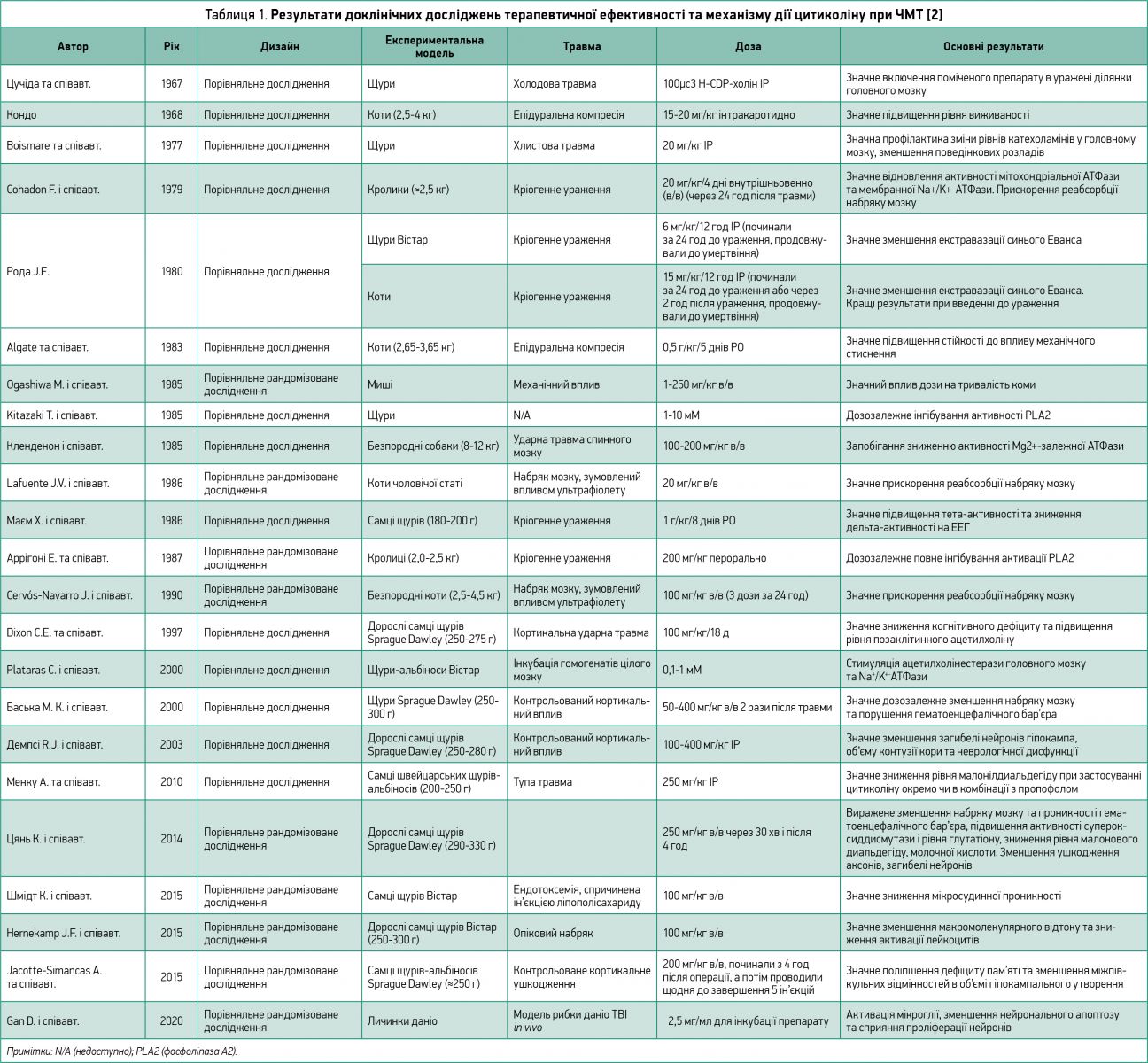
Крім того, цитиколін може покращувати метаболізм глюкози, а також знижувати рівень лактату в мозку під час ішемії. Цитиколін здатен модулювати активність деяких ферментів, як-от холінофосфотрансферази чи фосфоліпази, зокрема фосфоліпази А2 [2]. В деяких експериментальних моделях цитиколін забезпечував значний захист від летальності (табл. 1) [9].
Клінічні дослідження легких, ускладнених і тяжких травм голови
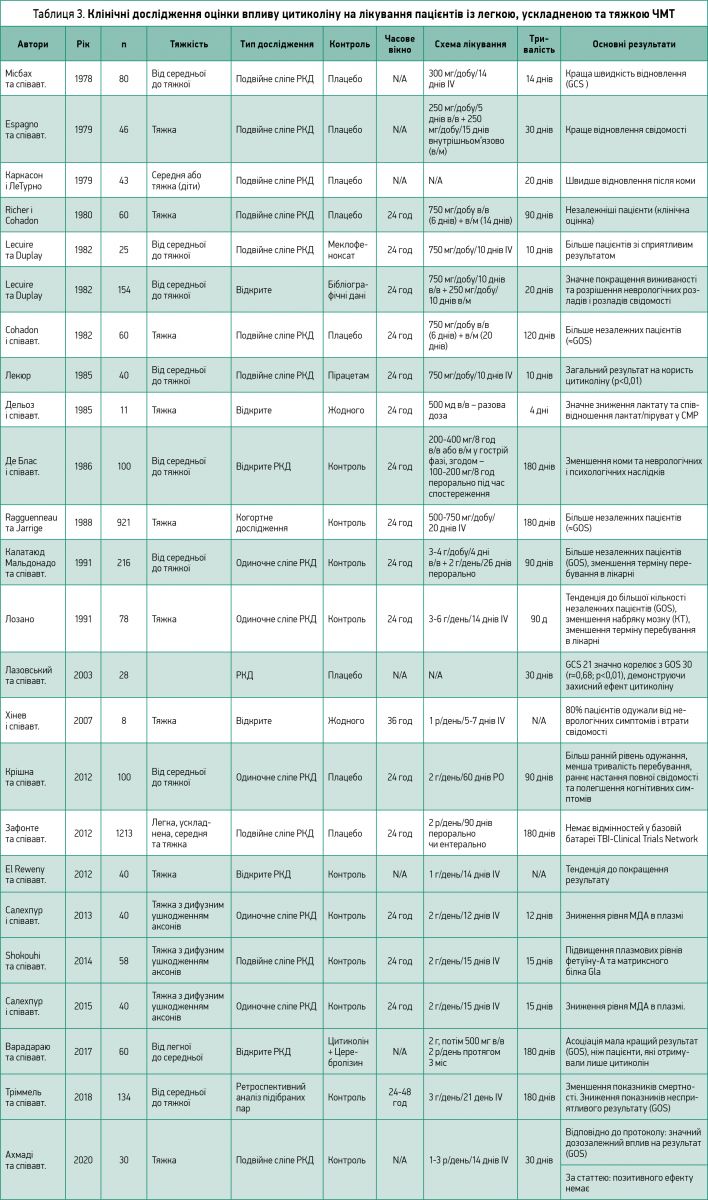
В таблиці 3 [2] за хронологічним порядком представлено всі клінічні дослідження оцінки впливу цитиколіну на лікування пацієнтів із легкою, ускладненою та тяжкою ЧМТ.
Метааналіз впливу цитиколіну в лікуванні ЧМТ
У 2014 році опубліковано метааналіз, заснований на 12 клінічних дослідженнях [10]. Для виявлення порівняльних клінічних досліджень цитиколіну в гострій фазі пацієнтів із травмами голови легкого, середнього та тяжкого ступенів було проведено систематичний пошук відповідних термінів. Основний показник ефективності – рівень незалежності чи хороший результат наприкінці запланованого періоду спостереження. До цього метааналізу залучили 2706 пацієнтів. Застосування цитиколіну було пов’язано зі значним збільшенням показників незалежності з відношенням шансів (ВШ) 1,815 (95% довірчий інтервал (ДІ) 1,302-2,530) за моделлю випадкових ефектів (рис. 2) і з ВШ 1,451 (95% ДІ 1,224-1,721) за моделлю фіксованих ефектів.
Рис. 2. Вплив цитиколіну на незалежність після ЧМТ [10]
В іншому метааналізі [11] автори виявили нейтральні ефекти цитиколіну при лікуванні пацієнтів із ЧМТ, але цей метааналіз ґрунтувався лише на дослідженнях, опублікованих англійською мовою; це є добре відомим джерелом упередженості, достатнім, щоб поставити під сумнів отримані результати.
Метааналіз, опублікований у 2023 р. (PROSPERO CRD42021238998), виявив певні корисні ефекти цитиколіну, зокрема підвищення кількості пацієнтів із незалежністю після ЧМТ. Найбільшим обмеженням цього метааналізу була гетерогенність включених досліджень [12].
Ушкодження головного мозку
Первинне ушкодження відбувається за впливу зовнішнього травмувального фактора, контактного ушкодження, лінійного та кутового прискорення голови, що викликають зміщення й ротацію мозку в порожнині черепа, кавітаційні процеси. Залежно від особливостей біомеханіки виокремлюють локальні та дифузні ушкодження мозку, при цьому відбувається запуск каскаду біохімічних та клітинних реакцій, що зрештою спричиняють вторинне ушкодження мозку.
Вторинні ушкодження мозку, що розвиваються після травми, – це утворення внутрішньочерепної гематоми, судинний та внутрішньоклітинний набряк, ішемія мозку. Отже, зона, що оточує осередок ушкодження, страждає від зниження кровотоку внаслідок крововиливів, спазму мозкових судин і порушень венозного відтоку, набряку.
Під вторинним ішемічним ушкодженням мозку розуміють погіршення стану пенумбри, а також умовно інтактної речовини мозку внаслідок будь-яких дій після розвитку первинного ушкодження. Гідроліз фосфоліпідів, що входять до складу клітинних мембран, і вільнорадикальне окислення є провідними механізмами ушкодження нервових клітин за ішемії та в постішемічному періоді, що в поєднанні з порушенням синтезу аденозинтрифосфату (АТФ), ексайтотоксичністю збуджувальних амінокислот, протеолізом порушує клітинну функцію, незворотно ушкоджує найчутливіші клітини мозку.
Розвиток вторинних ішемічних ушкоджень головного мозку підвищує ризик летального результату, а також погіршує неврологічне відновлення в постраждалих із тяжкою ЧМТ.
Терапія
Найважливішими завданнями терапії постраждалих із ЧМТ є профілактика та лікування вторинних ушкоджень, у т. ч. вторинної ішемії мозку і нейропротекції, яка зменшує дію вторинних ушкоджувальних факторів, дозволяє нервовим клітинам уникнути загибелі. При лікуванні хворих із ЧМТ необхідно враховувати багатокомпонентність патогенетичних механізмів ушкодження, а також застосовувати препарати, які мають полімодальну дію. Серед усього арсеналу схожих препаратів особливо виокремлюється один із найвивченіших нейроцитопротекторів – цитиколін (Праксіс). Механізми його дії дозволяють забезпечити як нейропротекцію, так і процес відновлення нервових клітин.
Головний ефект цитиколіну, який визначає полімодальність його дії, полягає у зниженні рівня вільних жирних кислот і зменшенні ушкоджень клітинних мембран за рахунок індукції синтезу фосфатидилхоліну та інших фосфоліпідів. Завдяки посиленню функції мембранних рецепторів та іонних транспортерів плазмолеми зменшує ступінь набряку мозку. Водночас цитиколін зменшує перекисне окиснення ліпідів, утворення вільних радикалів і лактату, відновлює активність Na+/K+-АТФази, чинить модулювальну дію на NMDA‑рецептори, регулюючи вивільнення глутамату. Значний клінічний інтерес існує при застосуванні цитиколіну під час консервативного лікування забитих місць головного мозку, тобто в разі структурних ушкоджень мозкової речовини в гострому періоді травми.
Сучасна концепція лікування хворих із ЧМТ спрямована на підтримання нормального мозкового кровотоку та збереження функції клітин у зоні пенумбри, а також передбачає ранню нейропротекцію. Дискусія щодо застосування нейропротекторної терапії наразі є однією з найгостріших. В умовах експерименту продемонстровано церебропротекторний ефект багатьох препаратів, проте триває робота з дослідження ефективності та безпеки в рандомізованих контрольованих дослідженнях. Нейропротекція сприяє зменшенню ушкоджувальних реакцій глутамат-кальцієвого каскаду, вільнорадикального окислення та блокаді прозапальних цитокінів, клітинної адгезії, зменшенню активності прооксидантних ферментів, зниженню темпу розвитку апоптозу. Вільнорадикальне окислення, ушкодження клітинних мембран за рахунок гідролізу фосфоліпідів є найважливішою ланкою комплексу ушкоджувальних механізмів при посттравматичній гіпоксії мозку; воно змінює структурну організацію нейроцитів, незворотно ушкоджує чутливіші клітини, згодом це спричиняє зниження або повне випадання певних значущих функцій. Найчутливішими до шкідливої дії посттравматичної гіпоксії є структури гіпокампа, зорового бугра, ретикулярної формації. У разі тяжкого ушкодження, в т. ч. і дислокації мозку, це зумовлює зниження ступеня неспання, виникнення парезів, мовних розладів. При менш виражених ушкодженнях у разі забоїв мозку легкого та середнього ступенів відбувається порушення тонкої регуляції рухових функцій, дисфункції інтегративних структур, що призводить до виражених інтелектуальних, астеноневротичних розладів, а це спричиняє зниження працездатності, в деяких випадках – інвалідність. Особливе значення має високий ризик розвитку посттравматичної епілепсії унаслідок низького епілептогенного порогу гіпокампа та мигдалеподібного комплексу лімбічної системи.
Висновки
Отже, експериментальні дані доклінічних досліджень і метааналіз впливу цитиколіну в лікуванні ЧМТ свідчать про те, що додавання цитиколіну до стандартної терапевтичної схеми надає переваги, оскільки цей препарат може прискорити реабсорбцію набряку мозку та одужання. Фармакологічні, біохімічні властивості та комплекс механізмів дії цитиколіну (Праксіс) обґрунтовують його застосування для лікування гострого інсульту (як ішемічного, так і геморагічного), ЧМТ різного ступеня тяжкості й когнітивних розладів різноманітного походження. Цитиколін є ефективним препаратом у терапії хворих із ЧМТ легкого та середнього ступенів тяжкості, дозволяє зменшити ступінь вираженості загальномозкової симптоматики й астеновегетативного синдрому в найближчому посттравматичному періоді, покращує показники електричної активності мозку, сприяє ранньому відновленню порушених функцій, а також дозволяє знизити терміни лікування хворих у стаціонарі.
Список літератури знаходиться в редакції.
Медична газета «Здоров’я України 21 сторіччя» № 8 (544), 2023 р.




![Рис. 2. Вплив цитиколіну на незалежність після ЧМТ [10]](/multimedia/userfiles/images/2023/ZU_8_2023/ZU_8_2023_Praxis_pic_2.jpg)