17 липня, 2023
Ефективність топічних антисептиків: фокус на повідон-йод. Роль і функція топічних антисептиків у сучасній медицині, їх перевага в умовах зростаючої антибіотикорезистентності
Місцеві антимікробні засоби – невід’ємна складова профілактики і лікування різноманітних інфекцій, їх використовують для догляду та обробки слизових та ран, що значно прискорює процес загоєння [1]. Антисептики виявляють широкий спектр дії проти бактерій, актинобактерій, грибків і вірусів, тому є хорошим вибором для лікування інфекційних процесів слизових і шкіри [2]. Висока ефективність антисептичних засобів проти планктонних і стійких бактеріальних спільнот сприяє загоєнню ран, якому часто перешкоджає утворення біоплівок – бактеріальних спільнот, стійких до дії антибіотиків [3]. Однак використання антисептиків також пов’язане з вагомими проблемами, такими як переносимість, інактивація органічними речовинами і стрімко зростаюча стійкість мікроорганізмів до антисептиків [1].
За даними Всесвітньої організації охорони здоров’я (ВООЗ), резистентність до протимікробних препаратів – пріоритетний напрям глобальної діяльності в галузі охорони здоров’я, оскільки резистентність є однією з найсерйозніших загроз здоров’ю, безпеці людини та збереженню продовольства у світі [4]. Доведено, що широка поширеність стійкості до топічних антибактеріальних засобів є наслідком безконтрольного та неправильного їх використання (зокрема, мупіроцину та фузидієвої кислоти) [5-8]. Однак стає все більш очевидним, що також набуває поширення стійкість до деяких антисептичних засобів; саме тому стійкість до антисептиків – ще одна ключова проблема, що потребує ефективних рішень [9].
Зростання поширеності антибіотикорезистентності (АБР) значною мірою завдячує появі внутрішньолікарняних інфекцій, резистентних до двох і більше антибактеріальних препаратів (АБП) – полі-, або мультирезистентність (multidrug-resistance, MDR). Список найпоширеніших нозокоміальних інфекцій в усьому світі охоплює патогени ESKAPE:
- Enterococcus faecium
- Staphylococcus aureus.
- Klebsiella pneumoniae.
- Acinetobacter baumannii.
- Pseudomonas aeruginosa.
- Enterobacter spp. [10].
Багато бактерій із цього списку стають MDR [10].
У рамках статті розглянуто основні проблеми антисептикiв: антимікробна ефективність, стійкість до антисептиків, перехресна резистентність до АБП і антисептиків, переносимість останніх, з акцентом на повідон-йод (PVP-I) у порівнянні з іншими широко використовуваними антисептичними засобами.
Методи
У січні 2019 р. на порталі PubMed було проведено 6 запитів серед наукової літератури: за допомогою фільтра здійснювався пошук даних за останніми досягненнями та актуальними проблемами в топічній антисептиці за попередні 5 років. Пошук був спрямований, зокрема, на широко використовувані антисептики – PVP-I, хлоргексидину глюконат (CHG), полігексанід (PHMB) і октенідин (OCT), у тому числі їхні синоніми.
Результати та методи дослідження
Антимікробний спектр антисептиків
Антимікробна активність антисептиків проти патогенів ESKAPE особливо актуальна, ураховуючи їхню провідну роль у розвитку нозокоміальних інфекцій [10]. PVP-I виявився ефективним проти Acinetobacter baumannii, K. pneumoniae, метицилін-чутливого S. aureus (MSSA), метицилін-резистентного S. aureus (MRSA), Ent. faecium, Enterobacter spp. і Ps. aeruginosa.
Крім того, на відміну від RNMB, CHG та OCT, PVP-І показав антимікробну активність проти актинобактерій і бактеріальних спор.
Відмінності антисептиків за спектром активності зумовлені різними механізмами дії. РНМБ, CHG і OCT переважно руйнують клітинну стінку і цитоплазматичну мембрану.
PVP-I має кілька механізмів дії (рис. 1) [31-35]. Інгібування PvP-I ферментів пояснює його ефективність проти широкого спектра вірусів і бактерій: PVP-І взаємодіє з декількома типами ферментів, у тому числі вірусних (гемаглютинін, нейрамінідаза і сіалідаза) [36]. Було також встановлено, що механізм дії CHG і PHMB, навпаки, спрямований на руйнування вірусної оболонки. Саме тому вони мають обмежену ефективність проти безоболонкових вірусів [37, 38].
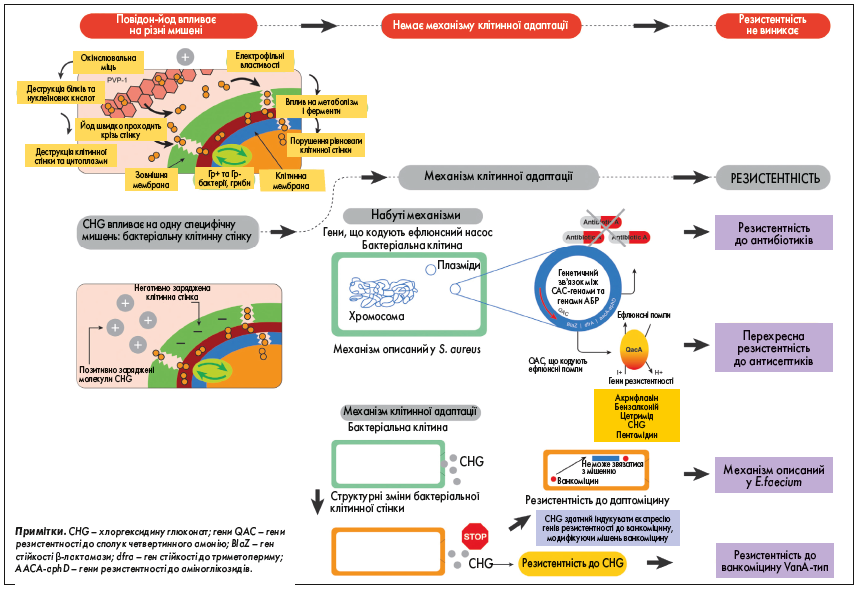 Рис. 1. PVP-І впливає на безліч мішеней у бактеріальних клітинах, тому повідомлень про резистентність або перехресну резистентність до нього немає [34, 35]. Єдиною специфічною мішенню CHG є бактеріальна клітинна стінка [47]. Експресія набутих генів призводить до підвищення резистентності мікроорганізмів до CHG, а також може призвести до перехресної резистентності до АБП [48]. Адаптація бактеріальної клітинної стінки зумовлює ще більшу стійкість мікроорганізмів до CHG поряд із ванкоміцином і даптоміцином [33, 58, 70]
Рис. 1. PVP-І впливає на безліч мішеней у бактеріальних клітинах, тому повідомлень про резистентність або перехресну резистентність до нього немає [34, 35]. Єдиною специфічною мішенню CHG є бактеріальна клітинна стінка [47]. Експресія набутих генів призводить до підвищення резистентності мікроорганізмів до CHG, а також може призвести до перехресної резистентності до АБП [48]. Адаптація бактеріальної клітинної стінки зумовлює ще більшу стійкість мікроорганізмів до CHG поряд із ванкоміцином і даптоміцином [33, 58, 70]
Йод у складі PVP-I також реагує із сульфідними (SH) і гідроксильними (ОН) групами амінокислот ферментів і структурних білків мікроорганізмів, у результаті ці білки інактивуються або руйнуються. Більшість мікроорганізмів знищуються йодом in vitro менш ніж за 1 хв, а основний руйнівний вплив відбувається в перші 15-30 секунд. При цьому знебарвлення або зниження насиченості коричневого кольору препарату свідчить про його ефективність (інактивація молекул йоду).
Вплив органічного матеріалу на антисептичну ефективність препаратів
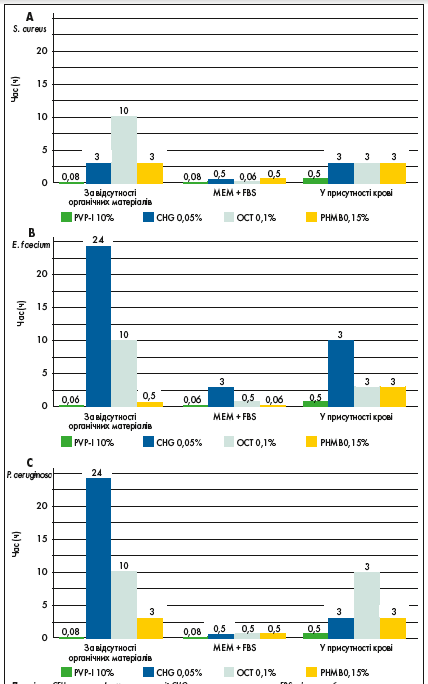
Ефективність антисептиків може знижуватися за наявності різних органічних матеріалів, наприклад крові в ранах, слизу та ін. [2]. Історично протимікробну активність топічних антисептиків випробовували in vitro в суспензійних середовищах, що моделюють умови в очагу інфекції, але не з абсолютною точністю [39]. Нещодавно було запропоновано новий метод випробування in vitro: топічні антисептики вивчали за допомогою тестових мікробних суспензій, попередньо висушених і нанесених на металеву поверхню. Такий підхід був більш репрезентативний, ніж дослідження із суспензіями [39]. Потенційно інгібуючий вплив органічних матеріалів тестували на PVP-І, CHG, PHMB та OCT. Із цього списку PVP-I показав найкоротший час ефективності проти S. aureus, E. faecium і P. aeruginosa, у тому числі в присутності крові (рис. 2) [39]. Незважаючи на широке використання CHG як антисептика, він виявився набагато менш ефективним, ніж PVP-І, як за наявності, так і за відсутності органічних матеріалів (рис. 2) [39].
Рис. 2. Необхідний час впливу для досягнення ефективності в присутності (log10 RF ≥3) і за відсутності (log10 RF ≥5) органічного матеріалу для (А) St. aureus, (В) Ent. faecium та (C) P. аeruginosa
Бактерії були розпорошені у водному розчині, розчині з органічним матеріалом (MEM [із солями Ерла та L-глутаміном] та 10% – FBS) або в органічному 30% розчині крові (MEM [із солями Ерла та L-глутаміном] та 10% FBS із людськими еритроцитами). У чашках Петрі були розміщені поверхні з нанесеними на них отриманими тестовими розчинами, попередньо висушеними протягом 60 хвилин. Потім на них наносили препарати антисептиків або негативного контролю. Антисептичну дію було припинено через 0,08 год, 0,5 год, 3 год, 10 год і 24 години. Бактерії були відновлені та інкубовані, після чого визначалися CFU і log10 RF (Schedler et al. [39]).
Ефективність антисептиків проти біоплівок
У реальних умовах бактерії переважно формують спільноти клітин у вигляді біоплівок. Біоплівки – це гетерогенні структури, що містять різні мікроорганізми, оточені захисним матриксом, який здатний приєднуватися до інертних та органічних поверхонь [40]. Нещодавно проведені систематичний огляд і метааналіз показали, що поширеність біоплівок за хронічних ран становить 78,2%. Це дає можливість припустити, що біоплівки утворюються в більшості хронічних невиліковних ран [41]. Було показано, що деякі патогени ESKAPE почали формувати біоплівки протягом 24 год, їх також часто виявляли у свіжих ранах. Біоплівки перешкоджають загоєнню ран, а мікроорганізми в їх складі особливо стійкі до протимікробної обробки і захисних механізмів організму хазяїна [3, 40]. Таким чином, потреба в топічних антисептиках, ефективних проти біоплівок, при лікуванні гострих і хронічних ран, вогнищ інфекцій слизових оболонок і шкіри вкрай висока.
Було проведено кілька досліджень для оцінки ефективності часто використовуваних антисептиків проти біоплівок, у тому числі PVP-І, CHG, РНМБ, і ОКТ. PVP-І в невеликій концентрації (0,25%) надійно усував MDR-біоплівки S. aureus, K. pneumoniae, P. aeruginosa і Candida albicans in vitro [14]. При подальшому розведенні PVP-І також виявився ефективнішим, ніж інші топічні антисептики, в ерадикації біоплівки Р. aeruginosa, C. albicans і MRSA, що містить кілька штамів [42]. Крім того, PVP-І повністю знищував біоплівки S. aureus та P. aeruginosa протягом 15 хв після нанесення, тоді як CHG – лише біоплівки S. aureus [18].
Стійкість до антисептиків
Стійкість мікроорганізмів до антисептиків може бути закладеною генетично (наприклад, непроникність поверхневих структур або генетично зумовлена інактивація) або набутою – унаслідок позитивних мутацій (наприклад, мутації рефлюксних насосів, сайтів-мішеней), формування плазмід і транспозонів [37, 46]. Незважаючи на широке клінічне використання PVP-І протягом останніх десятиліть та ретельне дослідження ізолятів, повідомлень про резистентність або підвищення стійкості бактерій до антисептичної терапії PVP-І зареєстровано не було [34, 35]. Імовірно, такий сприятливий профіль резистентності пояснюється тим, що йод має кілька механізмів дії (див. рис. 1) [34, 35].
Переносимість
Алергія на PVP-І переоцінена, здебільшого через плутанину в розумінні явищ власне алергії та подразнення [90]. У дослідженні, в якому були повторно протестовані всі пацієнти з позитивними патч-тестами на PVP-І, лише в 0,4% виникав алергічний PVP-I-асоційований контактний дерматит [90]. У порівнянні з іншими поширеними топічними антисептиками цей показник був украй рідкісним для PVP-І, OCT і PHMB і поширенішим для CHG [90]. Також було задокументовано повідомлення про кропив’янку та анафілактичні реакції внаслідок застосування CHG, анафілактичні реакції – при PHMB, і некроз асептичної тканини – при OCT [90-93].
Крім того, PVP-І 10% значно рідше чинив подразнювальну дію на шкіру, ніж CHG 5% [2]. PVP-І являє собою комплекс йоду і полімерної сполуки полівінілпіролідону (ПВП). Молекулярний йод забезпечує швидкий і виражений бактерицидний ефект, а полімер являє собою депо для йоду. При контакті зі шкірою і слизовими оболонками з препарату виділяється значна кількість йоду. У складі комплексу з ПВП йод значною мірою позбавляється місцевої подразнювальної дії, властивої спиртовим розчинам йоду. Тому PVP-І характеризується хорошою переносимістю при нанесенні на шкіру, слизові оболонки й уражені поверхні.На відміну від інших топічних антисептиків, що їх було розглянуто в цьому огляді, PVP-I іноді пов’язують з індукцією дисфункції щитоподібної залози (ЩЗ), але було продемонстровано, що вплив PVP-І на функцію ЩЗ в деяких пацієнтів із підвищеною чутливістю до препаратів йоду є тимчасовим і не має наслідків для здоров’я [98]. Крім того, подальші дослідження показали, що частота дисфункції ЩЗ в осіб, які зазнали впливу топічних йодних антисептиків, не відрізняється від показників у загальній популяції [98-103].
Висновок
Під час вибору топічних антисептиків для обробки шкіри, слизових оболонок, ран необхідно брати до уваги низку потенційних характеристик і особливостей, а саме – протимікробний спектр і ефективність в реальних умовах, стійкість до антисептичного препарату і перехресну протимікробну резистентність, вплив на загоєння ран і переносимість.
Порівняно з іншими широко використовуваними топічними антисептиками, такими як CHG, PHMB та OCT, PVP-І продемонстрував низку переваг.
PVP-I мав найширший спектр дії, був досить ефективним в усуненні патогенів ESKAPE та біоплівок, а також зберігав свою ефективність за наявності крові. Це робить PVP-І антисептиком вибору в лікуванні топічних вогнищ інфекцій і менеджменті внутрішньолікарняних інфекцій. Крім того, в епоху, коли стійкість до антисептиків і антибіотиків стрімко зростає, ключовою особливістю PVP-І, на відміну від інших антисептиків, є відсутність виникнення стійкості / перехресної резистентності серед патогенів. Це також примітно тим, що PVP-І масово використовувався протягом десятиліть.
Ідеальний топічний антисептик має не лише зменшувати мікробне навантаження, але і сприяти загоєнню тієї анатомічної ділянки, на якій його використовують. Встановлено, що PVP-І сприяє загоєнню ран за низького рівня цитотоксичності. До того ж PVP-І вирізняється хорошою переносимістю – алергічні реакції виникають лише в 0,4%. На фармацевтичному ринку України протягом багатьох років PVP-І представлений брендовим препаратом Бетадин, виробництва компанії «Егіс».
За матеріалами Barreto R. et al. Addressing the challenges in antisepsis: focus on povidone iodine. International Journal of Antimicrobial Agents 56 (2020).
Підготувала Ірина Чумак
Тематичний номер «Пульмонологія, Алергологія, Риноларингологія» № 2 (63) 2023 р.



![spp. [10].](/multimedia/userfiles/images/2023/Pulmo_2_2023/Pulmo_2_2023_%D1%80_20_tabl_1.png)