31 жовтня, 2023
Можливості фітотерапії з доведеною ефективністю в стратегії відкладеного призначення антибіотиків при гострих респіраторних інфекціях
 Надмірне та неправильне використання антибіотиків (АБ) при респіраторних інфекціях залишається актуальною проблемою. У більшості випадків гострого риносинуситу (ГРС) та гострого тонзиліту (ГТ) АБ можна вважати надмірним лікуванням, оскільки при вірусних інфекціях вони абсолютно недоречні. Антимікробна резистентність у 2019 р. спричинила приблизно 1,27 млн смертей в усьому світі. Не менш важливою проблемою є негативні зміни в мікробіоті організму пацієнта, які негативно впливають на здоров’я, а патологічні зміни можуть тривати довше та бути важчими, ніж саме захворювання. Неадекватне застосування АБ може бути згубним, особливо у дітей, оскільки їх віддалений вплив на макроорганізм та мікробіоту може сприяти проявам захворювань у дорослому віці. Фітопрепарати (ФП) з доведеною ефективністю для лікування неускладнених респіраторних інфекцій можна розглядати як альтернативу АБ і використовувати у технології їх відкладеного призначення. Дані показують, що рослинні лікарські засоби забезпечують високу ефективність і мають сприятливий профіль безпеки.
Надмірне та неправильне використання антибіотиків (АБ) при респіраторних інфекціях залишається актуальною проблемою. У більшості випадків гострого риносинуситу (ГРС) та гострого тонзиліту (ГТ) АБ можна вважати надмірним лікуванням, оскільки при вірусних інфекціях вони абсолютно недоречні. Антимікробна резистентність у 2019 р. спричинила приблизно 1,27 млн смертей в усьому світі. Не менш важливою проблемою є негативні зміни в мікробіоті організму пацієнта, які негативно впливають на здоров’я, а патологічні зміни можуть тривати довше та бути важчими, ніж саме захворювання. Неадекватне застосування АБ може бути згубним, особливо у дітей, оскільки їх віддалений вплив на макроорганізм та мікробіоту може сприяти проявам захворювань у дорослому віці. Фітопрепарати (ФП) з доведеною ефективністю для лікування неускладнених респіраторних інфекцій можна розглядати як альтернативу АБ і використовувати у технології їх відкладеного призначення. Дані показують, що рослинні лікарські засоби забезпечують високу ефективність і мають сприятливий профіль безпеки.
Украй важливо підвищити знання та обізнаність, а також забезпечити відповідну підготовку і комунікаційні стратегії серед лікарів, щоб запобігти надмірному та необґрунтованому використанню АБ. Мета огляду – підкреслити внесок ФП в ефективність лікування ГРС та ГТ і скорочення необґрунтованого призначення АБ.
ГРС і ГТ є найбільш поширеними гострими респіраторними інфекціями, особливо в дитячому віці, і, крім дискомфорту та зниження якості життя пацієнта, несуть велике соціальне та економічне навантаження. Саме ця група захворювань є однією з провідних причин значної кількості днів пропусків занять у школі серед дітей та візитів до лікаря [1-3]. ГРС, ГТ – запальні захворювання, більшість випадків яких має вірусне походження. Зазвичай вірусна інфекція запускає запальний каскад у контексті звичайної застуди.
Гострий вірусний РС (ГВРС), або застуда, має дуже високий рівень захворюваності – від двох до п’яти епізодів на людину на рік [4]. У дітей ця захворюваність в рази вища і є однією з основних причин звернення по первинну медичну допомогу [5, 6]. Гострий поствірусний РС (ГПВРС) менш поширений. У недавньому дослідженні було встановлено, що захворюваність становить 18,8 епізодів на 1000 жителів на рік [7]. ГТ виникає в усіх вікових групах, але частіше у віці від 5 до 15 років і становить близько 5% усіх візитів до лікаря [2, 8].
Найскладнішим питанням є правильна діагностика бактеріального ГРС чи ГТ. Гострий бактеріальний РС (ГБРС) розвивається в рідкісних випадках: тільки у 0,5-2% усіх ГВРС цей запальний стан може бути спричинений бактеріальною інфекцією [1]. Гострий бактеріальний тонзиліт (ГБТ) виникає в імунокомпетентних дітей у 20-30% випадків, дорослих – у 5-15%, а основна його причина – β-гемолітичний стрептокок групи А (БГСГА) [8].
Сьогодні не існує стандартного параметра для диференційної діагностики між ГБРС та ГБТ і небактеріальними їх формами. Для комплексної диференціації вірусної та бактеріальної етіології пропонуються критерії, що оцінюють наявність або відсутність ряду анамнестичних даних і клінічних симптомів. EPOS 2020 рекомендує використовувати комбінацію симптомів для визначення ймовірності бактеріального процесу та визначає ГБРС, коли наявні 3 або більше з наступних п’яти критеріїв:
- погіршення симптомів після початкового поліпшення;
- гіпертермія більше 38 °С;
- виражений локальний біль;
- виділення (переважно гнійні) з носа;
підвищення швидкості осідання еритроцитів (ШОЕ) та С-реактивний білок (СРБ). Рекомендації щодо ГТ для стратифікації пацієнтів із відсутністю потреби у призначенні АБ-терапії пропонують бальну оцінку (максимум 5 балів) згідно зі шкалою McIsaac. Усі автори клінічних рекомендацій одностайні в думці, що у звичайних ситуаціях немає потреби в додаткових діагностичних інструментах для диференційної діагностики вірусних та бактеріальних процесів, а рекомендований раніше аналіз крові для визначення СРБ/ШОЕ не допоміг зменшити надмірне призначення АБ [1, 8]. Разом з тим надійні лабораторні тести для діагностики бактеріальних інфекцій сьогодні знаходяться на стадії вивчення [9]. У реальному житті диференційна діагностика бактеріального ГРС чи ГТ з їх небактеріальними формами часто призводить до гіпердіагностики, що, в свою чергу, призводить до надмірного використання діагностичних тестів і раннього непотрібного призначення АБ [10, 11]. Згідно з даними літератури, необґрунтована АБ-терапія призначається у 54-77% випадків ГРС і ГТ [12]. В Україні при ГРС педіатри призначають АБ у 53%, лікарі загальної практики – у 32%, отоларингологи – у 77% випадків, при ГТ АБ призначають педіатри у 53% випадків, у 72% – лікарі загальної практики та у 64% випадків – отоларингологи [13].
Невиправдане призначення АБ є однією з основних причин глобальної проблеми антибіотикорезистентності (АБР), оскільки, згідно з даними ВООЗ, неадекватна терапія з використанням АБ у світі призначається в середньому у 50% випадків [14, 15]. Крім глобальної проблеми АБР, яка у 2019 р. спричинила приблизно 1,27 млн смертей в усьому світі, необґрунтоване призначення АБ може бути шкідливим для конкретного пацієнта [16]. Необґрунтоване призначення АБ при вірусному ГТ, зокрема, асоційованому з вірусом Епштейна – Барр, пов’язане з високою частотою виникнення тяжкого генералізованого висипу з ураженням кінцівок – амоксицилінасоційованої екзантеми [17]. АБ-терапія, навіть за показаннями, призводить до довготривалих змін бактеріального мікробіома організму, тому здатна порушувати симбіоз між мікробіотою та макроорганізмом. У дослідженнях показані виразні зміни бактеріального складу не тільки через 7 днів, а і через 11 тижнів після відміни АБ, що вказує на довготривале пошкодження мікробіома. Через 11 тижнів мікробний склад хоча і змінюється порівняно із 7-им днем, але не повертається до початкового рівня, а потенційно корисні види мікроорганізмів, такі як Akkermansia muciniphila, не з’являються знову, навіть при тривалому спостереженні [18]. Такі зміни в мікробіоті можуть мати потенційно небезпечні ефекти, зокрема сенсибілізацію, захворювання пародонту та карієс у дітей, розвиток опортуністичних інфекцій, вагінального кандидозу, активацію канцерогенезу тощо. Сьогодні виділена ціла група захворювань, викликаних АБ [19]. Надмірне та неправильне використання АБ і наступний вплив на мікробіоту у маленьких дітей може сприяти проявам захворювань у більш пізньому віці [20, 21]. Порушений мікробіом може сприяти хронічному системному запаленню низького ступеня, таким чином навіть сприяючи розвитку захворювань, пов’язаних із віком [22].
Порушений мікробний спектр орального та респіраторного мікробіому забезпечує порушення колонізаційної резистентності та підтримує персистуючий запальний процес із формуванням біоплівок [23]. Біоплівки здатні підвищити стійкість мікроорганізмів до АБ та антиімунні властивості бактерій у десятки разів, що створює умови для прогресування запалення і його персистенції, а також сприяє частим рецидивам. Дослідження виявили, що порушення нормального складу мікробіому носоглотки, пов’язане із формуванням біоплівок, асоціюється зі схильністю до гострих респіраторних захворювань та формування хронічних захворювань верхніх дихальних шляхів (ВДШ) [24-26].
Зважаючи на актуальність проблеми, був проведений ряд досліджень для визначення мотивації надмірного призначення АБ серед лікарів. Виявлено, що лікарі, які лікують ГРІ в амбулаторних умовах, добре знають про дію АБ і АБ-резистентність і демонструють відповідальність при призначенні АБ. Однак кількість неналежних призначень велика [27, 28]. Були проведені додаткові дослідження для вивчення факторів невідповідної практики призначення АБ і недотримання рекомендацій. Визначено, що основними мотивами були тиск на лікаря через недостатність у пацієнтів чи їх батьків знань про АБ, складнощі у диференційній діагностиці бактеріальних та небактеріальних процесів, недостатня впевненість лікаря, побоювання розвитку ускладнень, відсутність інформативних тестів, звернення до лікаря з уже придбаним АБ внаслідок вільного їх продажу в аптеках, а також неадекватна медична підготовка [29-31].
З метою зменшення неналежного використання АБ при респіраторних інфекціях опубліковані дослідження, в яких підкреслюється важливість розвитку комунікаційних навичок лікаря щодо використання АБ, включаючи допомогу в прийнятті клінічних рішень, відповідального їх обґрунтування та навчання лікарів [32, 33].
Однією зі стратегій скорочення необґрунтованого призначення АБ при неускладнених ГРІ є відкладене призначення АБ [34], що показує практично аналогічний рівень задоволеності пацієнта лікуванням порівняно із призначенням його на першому визиті (86 проти 91%). Ця технологія дозволила знизити частоту використання АБ-терапії до 31% і не призводить до збільшення кількості ускладнень [35, 36].
Суть тактики відкладеного призначення полягає в тому, що фахівець припускає, що негайне призначення АБ не є необхідним, очікуючи, що симптоми будуть усунуті без їх використання, але залишає можливість призначення при невідповідності стану пацієнта критеріям позитивної динаміки. Пацієнти та лікарі можуть бути більш схильними погодитися з таким курсом лікування порівняно з негайним призначенням або відсутністю призначення АБ пацієнтам із респіраторними інфекціями [37].
Основною умовою можливості реалізації стратегії відкладеного призначення АБ є лікування з доведеною ефективністю. Згідно з рекомендаціями, симптоматична фармакотерапія ГРС та ГТ включає топічні і системні стероїдні та нестероїдні протизапальні препарати (НПЗП) або жарознижувальні. Проте зазначені симптоматичні засоби не охоплюють всього спектра патогенетичних механізмів ні ГРС, ні ГТ, а призначення таких широко використовуваних засобів, як антигістамінні, гомеопатичні, БАД тощо, при ГРІ не обґрунтовано, оскільки їх користь не доведена [38, 39]. Очікування призначення АБ найвищі у пацієнтів із низькою ефективністю лікування, особливо в перші дні хвороби. Виходячи з цього, виникає необхідність у використанні препаратів з комплексною дією на основні ланки патогенезу та доведеною ефективністю при гарному профілі безпеки. Саме тому за 8-річний період між EPOS 2012 та EPOS 2020 перелік препаратів із доведеною ефективністю для лікування ГРС розширився за рахунок ФП [1].
Лікарські засоби на основі рослинних препаратів або їх екстрактів, як правило, демонструють позитивне співвідношення користь/ризик і є життєздатною альтернативою для лікування неускладнених респіраторних інфекцій [40]. На відміну від АБ або НПЗП, варіанти лікування сучасними комплексними фітоніринговими засобами, такими як Синупрет® та Імупрет®, зазвичай не спрямовані на конкретні патогени, хоча і проявляють противірусну та помірну АБ-активність. Швидше їхня ефективність базується на багатоцільовому підході із впливом на основні патогенетичні механізми захворювання [41-45]. Для багатьох поширених і рецидивуючих інфекцій, таких як інфекції ВДШ, доступні ефективні та безпечні варіанти лікування з використанням фітопрепаратів [46, 47].
В EPOS 2020 доказові схеми лікування з використанням конкретних рослинних засобів розглядаються окремо для вірусного і поствірусного РС [1]. Так, при ГВРС робоча група рекомендує такі рослинні засоби, як BNO 1016 (Синупрет®), Cineole (компонент евкаліптової олії) та Andrographis paniculata SHA-10 (в Україні не зареєстрований), оскільки вони мають істотний вплив на симптоми без важливих побічних явищ. При ГПВРС рекомендуються BNO 1016, Pelargonium sidoides та Myrtol, що також мають суттєвий вплив на симптоми без значних побічних явищ. Суттєвим недоліком використання більшості рослинних засобів є відсутність універсального впливу на патогенез кількох форм ГРС, зокрема ГВРС та ГПВРС, тому вони показані тільки при конкретних нозологічних одиницях: вірусному чи поствірусному РС. Це значно утруднює призначення appropriate medical therapy (кращої медичної терапії), оскільки лікарю, особливо первинної ланки, не завжди легко провести диференційну діагностику. Таким чином, згідно з рекомендаціями щодо лікування як ГВРС і поствірусного РС, показаний тільки BNO 1016.
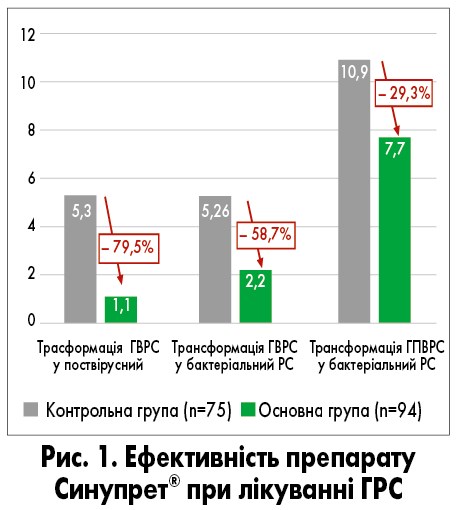 Дослідження показали, що при призначенні препарату Синупрет® з першого дня у пацієнтів із ГВРС його трансформація у поствірусний зменшується на 79,5%, на 58,7% – у бактеріальний (рис. 1). Аналогічно призначення препарату Синупрет® з першого дня лікування пацієнтам із ГПВРС зменшує його трансформацію у бактеріальний на 29,3% [48, 49].
Дослідження показали, що при призначенні препарату Синупрет® з першого дня у пацієнтів із ГВРС його трансформація у поствірусний зменшується на 79,5%, на 58,7% – у бактеріальний (рис. 1). Аналогічно призначення препарату Синупрет® з першого дня лікування пацієнтам із ГПВРС зменшує його трансформацію у бактеріальний на 29,3% [48, 49].
У контексті цільового впливу на зменшення клінічних проявів ГТ застосування ФП могло би бути цікавим, оскільки, згідно з дослідженнями, фітотерапію при запальних захворюваннях глотки призначають 28% лікарів [50]. Найбільш вивченими у цьому відношенні є препарати ехінацеї та Pelargonium sidoides. Однак рандомізовані дослідження не довели їх ефективності у лікуванні пацієнтів із ГТ [51, 52]. Рандомізоване клінічне дослідження у дітей показало, що додаткове використання фітонірингового препарату BNO 1030 (Imupret®) для лікування ГТ значно зменшує клінічні симптоми, забезпечує достовірні відмінності у виразності клінічних симптомів, починаючи з 3-го дня лікування (рис. 2) [53]. Із 6-го дня пацієнти в групі прийому препарату Імупрет® не мали потреби у використанні НПЗП для усунення гіпертермії та болю в горлі. Вказані пацієнти на 6-й день лікування демонстрували таку виразність симптомів, як пацієнти контрольної групи тільки на 10-й день (рис. 2). Таким чином, використання препарату Імупрет® забезпечує терапевтичний виграш у 4 дні при лікуванні небактеріального ГТ.
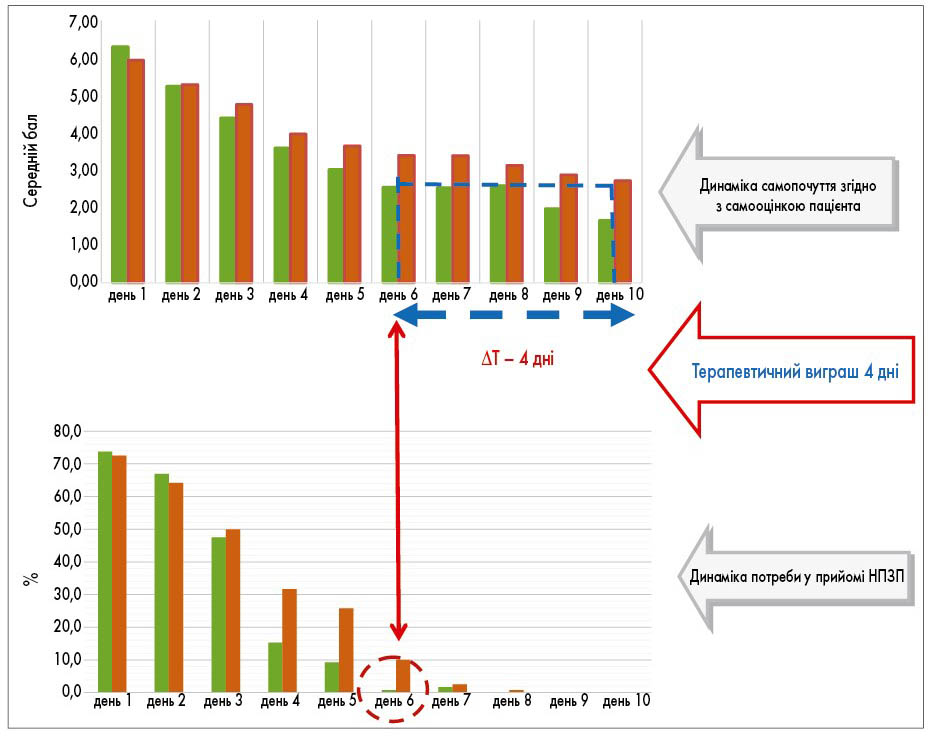 Рис. 2. Ефективність препарату Імупрет® при лікуванні ГТ
Рис. 2. Ефективність препарату Імупрет® при лікуванні ГТ
Як ми писали вище, одна зі стратегій скорочення кількості необґрунтованих призначень АБ – відкладене їх призначення. Основною умовою можливості реалізації такої стратегії є призначення лікування з доведеною ефективністю. З точки зору стратегії відкладеного призначення АБ стартове лікування повинно мати високу ефективність, особливо в перші дні після призначення. При недостатній ефективності стартової терапії, при повторному огляді, як правило, на 3-й день лікування, виникає необхідність призначення АБ. Проведені дослідження демонструють, що використання фітонірингових препаратів Синупрет® та Імупрет® має доведений терапевтичний ефект вже у перші дні лікування. Тому метою подальших досліджень була оцінка ефективності додаткового застосування фітонірингових фітоекстрактів Синупрет® та Імупрет® у технології відкладеного призначення АБ у пацієнтів із ГРС та ГТ, порівняно зі стандартною симптоматичною терапією згідно з клінічними рекомендаціями.
Показано, що в умовах контрольованого дослідження відкладене призначення АБ пацієнтам зі стандартним лікуванням ГРС було у 8,26% випадків, а пацієнтам, що приймали Синупрет®, – у 3,4% випадків (рис. 3) [54]. 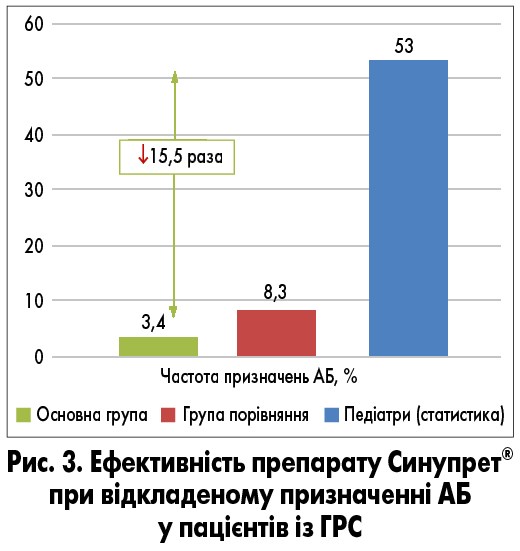
Така частота призначень в цілому відповідає існуючим рекомендаціям щодо необхідності призначення АБ-терапії при цьому захворюванні [1, 10]. Водночас, згідно з даними літератури, в Україні при ГРС педіатри призначають АБ у 53% випадків, лікарі загальної практики – у 32%, отоларингологи – у 77% [13]. Таким чином, застосування препарату Синупрет® у стратегії відкладеного призначення АБ у пацієнтів із ГРС дозволяє зменшити обґрунтоване призначення АБ у 1,81 та 15,5 раза (з 53 до 3,4%) порівняно зі статистичними даними.
Рандомізоване дослідження ефективності препарату Імупрет® порівняно зі стандартною терапією, згідно з клінічними рекомендаціями в рамках тактики відкладеного призначення АБ, проводилося у пацієнтів із тяжким ГТ (4-5 балів за оціночною шкалою Mclsaac) [8]. У дослідженні показано, що АБ за технологією відкладеного призначення виписано 23,46% пацієнтів, які отримували стандартну терапію згідно з клінічними рекомендаціями (14,28% – на 3-й день лікування і 9,18% – на 5-й; рис. 4) [55].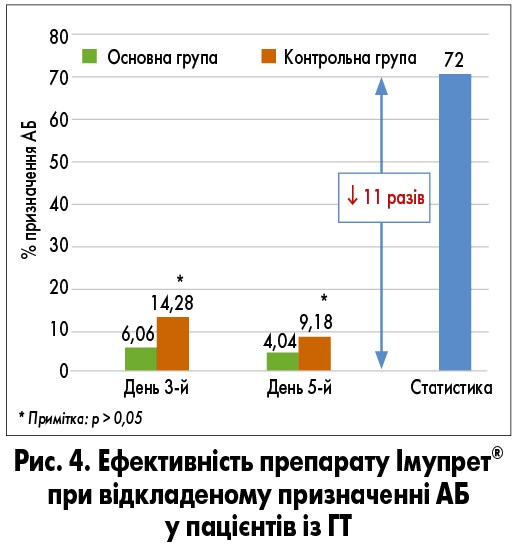
Кількість призначень в умовах контрольованого дослідження відповідає середній частоті поширеності бактеріального ГТ [8, 11]. Пацієнтам, які додатково приймали Імупрет®, АБ-терапія призначена в 10,12% випадків (6,06% – на 3-й день лікування і 4,04% – на 5-й; рис. 4). Таким чином, важливий висновок полягає в тому, що в умовах контрольованого дослідження застосування препарату Імупрет® у пацієнтів із тяжким ГТ на 43,7%, або в 2,3 раза знижує необхідність призначення АБ-терапії при використанні технології відкладеного призначення АБ порівняно з пацієнтами, що отримують стандартне лікування. Разом з тим в Україні при ГТ педіатри призначають АБ у 53% випадків, у 72% їх призначають лікарі загальної практики, у 64% – отоларингологи [13]. Отримані результати показують зниження в 11 разів кількості призначених АБ порівняно із середньостатистичним рівнем їх призначення серед лікарів загальної практики.
Таким чином, застосування препарату Імупрет® у стратегії відкладеного призначення АБ у пацієнтів із ГТ дозволяє зменшити обґрунтоване призначення АБ у 2,3 та в 11 разів порівняно зі статистичними даними.
Як відомо, АБ-терапія призводить до довготривалих змін бактеріального мікробіома організму. У зв’язку з цим проведене вивчення впливу фітонірингових препаратів Синупрет® та Імупрет® на зміни мікробіома, оскільки збереження мікробіоти відповідає стратегії раціонального застосування АБ. В експериментальному дослідженні показано, що бактеріальний склад кишечнику лабораторних мишей, які отримували BNO 1011 (Синупрет®), показав високу схожість з нелікованими мишами, що свідчить про відсутність впливу на мікробіом [18]. В іншому, клінічному, дослідженні показано, що використання препарату Імупрет® у пацієнтів із хронічним назофарингітом і неодноразовим призначенням АБ-терапії в анамнезі сприяє нормалізації складу мікробіома носоглотки, який асоціюється із покращенням клінічної симптоматики [56].
Отже, дослідження з фітоніринговими препаратами Синупрет® та Імупрет® демонструють, що лікування ФП є ефективним у зменшенні симптомів ГРС та ГТ і дає можливість зменшити призначення пацієнтам АБ, водночас забезпечуючи сприятливі профілі безпеки. Крім того, вказані дослідження призвели до визнання рослинних лікарських засобів в офіційних рекомендаціях щодо риносинуситу [1].
Таким чином, актуальною проблемою залишається надмірне та неправильне використання АБ і розвиток АБ-резистентності, що спричинило приблизно 1,27 млн смертей в усьому світі у 2019 р. АБ можуть спричинити шкідливі зміни в мікробіоті та макроорганізмі з подальшим негативним впливом на здоров’я, який може тривати довше та бути важчим, ніж саме захворювання. У більшості випадків ГРС та ГТ АБ можна вважати надмірним лікуванням, оскільки при вірусних інфекціях вони абсолютно недоречні. Неадекватне застосування АБ може бути згубним, особливо у дітей, оскільки їх вплив на макроорганізм та мікробіоту може сприяти проявам захворювань у дорослому віці. Крім того, часті медичні консультації, які також пов’язані з більшим призначенням АБ, можуть відволікати ресурси від лікування потенційно більш серйозних захворювань.
Рослинні екстракти із доведеною ефективністю можна розглядати як альтернативу АБ для лікування неускладнених респіраторних інфекцій. Дані свідчать, що рослинні лікарські засоби забезпечують ефективність і загалом мають сприятливий профіль безпеки. Однак лікарські засоби рослинного походження не можуть замінити АБ в усіх випадках, тому їх відкладене призначення зі стартовим лікуванням ФП корисне для зменшення надмірного і необґрунтованого призначення АБ.
Украй важливо підвищити знання та обізнаність, а також забезпечити відповідну підготовку і комунікаційні стратегії серед лікарів, щоб запобігти надмірному та необґрунтованому призначенню АБ. У той час як обізнаність про ефективне використання АБ зростає, формування більш широкого розуміння відповідального використання АБ у рутинній практиці залишається важливим, щоб зменшити ризик побічних ефектів і АБ-резистентності, а також сприяти більш свідомому вибору лікування запальних захворювань ВДШ.
Загалом цей огляд має на меті підкреслити внесок ФП в ефективність лікування ГРС та ГТ і скорочення необґрунтованого призначення АБ.
Повний список літератури знаходиться в редакції.
Тематичний номер «Педіатрія» № 4 (70) 2023 р.



