28 грудня, 2023
Фосфоміцин у лікуванні інфекцій сечових шляхів
Інфекції сечових шляхів (ІСШ) є найпоширенішими бактерійними інфекціями у світі (McLellan L.K., Hunstad D.A., 2016; Saint S. et al., 2008). Вони являють собою гетерогенну групу хвороб різної етіології та тяжкості. На ризик розвитку ІСШ впливає низка вроджених та набутих факторів, як-от затримка сечі, везикоуретеральний рефлюкс, часті статеві зносини, застосування сперміцидів, збільшення розміру передміхурової залози, вульвовагінальна атрофія, сімейний анамнез (Storme O. et al., 2019; Craven B.C. et al., 2019).
ІСШ виникають тоді, коли уропатогени, що знаходяться в кишечнику, колонізують уретру, а згодом – сечовий міхур. Якщо фізіологічна запальна відповідь організму-господаря є недостатньою для елімінації усіх бактерій, вони починають розмножуватися, продукуючи токсини та ферменти, які сприяють їхній виживаності. Подальша колонізація нирок із проходженням патогенів через нирковий епітеліальний бар’єр може спричинити бактеріємію. Уропатогени схильні до утворення біоплівок; у разі відсутності лікування здатні викликати пієлонефрит (Mancuzo G. et al., 2023).
Класифікація ІСШ передбачає розподіл залежно від місця виникнення (уретрит, цистит, пієлонефрит) і перебігу (неускладнені, ускладнені). Ускладнені ІСШ відрізняються від неускладнених наявністю функціональних або структурних змін сечовидільної системи (Huang L. et al., 2021; Li X. et al., 2022; Gomila A. et al., 2018). Типовим для ускладнених ІСШ є достовірно вища частка невдач лікування і системне / інвазивне залучення тканин та органів до патологічного процесу (Luu T., Albarillo F.S., 2022). За наявності ≥3 епізодів неускладненої ІСШ упродовж 12 міс або ≥2 епізодів протягом 6 міс діагностують рецидивувальну ІСШ (Rando E. et al., 2022; Nicolle L.E., 2005).
Стан, за якого специфічні симптоми ІСШ відсутні, а в культурі сечі виділяють ≥105 колонієутворювальних одиниць бактерій/мл, називають асимптоматичною бактеріурією. Він зазвичай минає спонтанно, не потребує лікування (Wiley Z. et al., 2020). Лікувати асимптоматичну бактеріурію варто лише в певних випадках: у вагітних, осіб із нейтропенією та в пацієнтів, які підлягають генітоуринарним хірургічним втручанням (Luu T., Albarillo F.S., 2022; Ourani M. et al., 2021).
Найпоширеніший уропатоген – E. coli (80% випадків), але інші ентеробактерії (насамперед K. pneumoniae) також нерідко спричиняють ІСШ (Hooton T.M. et al., 2012; Walker E. et al., 2016). Часто інфекція здається нетяжкою (особливо на ранніх стадіях), але за наявності ускладнювальних факторів стан пацієнта може значно погіршитися. Такими ускладнювальними факторами є здатність уропатогенів утворювати біоплівки, стаз сечі та застосування сечових катетерів (Mancuzo G. et al., 2023). За невдачі лікування ІСШ можуть завершитися висхідними інфекціями, включаючи пієлонефрит, і сепсисом. Основна причина невдач лікування – резистентність до призначуваних антибіотиків. Зазвичай при ІСШ призначають β-лактами, триметоприм і триметоприм/сульфаметоксазол (Abou Heidar N.F. et al., 2019; Lopez Romo A., Quirós R., 2019). Також широко застосовують фторхінолони, які вже не є рекомендованими ні в європейських, ні в міжнародних керівних рекомендаціях (Tutone M. et al., 2022).
Проблема антибіотикорезистентності в поєднанні з відсутністю нових препаратів цієї групи обумовлює потребу в переоцінці давно відомих препаратів (Bergen P.J. et al., 2012), зокрема фосфоміцину. Фосфоміцин застосовується вже >40 років і наявний як у пероральній (фосфоміцину трометамол), так і в парентеральній формі. Системний огляд і метааналіз T. Cai та співавт. (2020) продемонстрували, що одна доза фосфоміцину трометамолу була такою самою ефективною в лікуванні неускладнених ІСШ у жінок, як і триваліші курси інших препаратів.
Загальноєвропейське дослідження SURF (2022), покликане оцінити чутливість та резистентність до фосфоміцину порівняно з іншими антимікробними засобами, виявило, що до фосфоміцину були чутливими 96,4% ізолятів E. coli, в т. ч. >90% цефалоспорин-резистентних E. coli. Антибіотиками, активними щодо >90% ізолятів E. coli, виявилися лише 3 препарати: фосфоміцин, нітрофурантоїн і мецилінам. Резистентність до них склала 3,6; 1,5 та 8,2% відповідно. Активними щодо >90% цефподоксим-резистентних E. coli були лише фосфоміцин і нітрофурантоїн. Для цефалоспоринів, амоксициліну/клавуланату та ципрофлоксацину було продемонстровано значно меншу ефективність: ≈80% (79,2-83,1%), а для триметоприму й ампіциліну – ще меншу (<70%) (Tutone M. et al., 2022).
Порівняння фосфоміцину та нітрофурантоїну в жінок із неускладненими ІСШ, проведене A. Shafrir і співавт. (2023), виявило, що в групі нітрофурантоїну спостерігалася вища частота реінфекцій (9,21 проти 7,76%; р<0,0001), тобто фосфоміцин забезпечує кращу профілактику рецидивів. Переваги фосфоміцину були вираженішими в групі молодих пацієнток (віком <40 років).
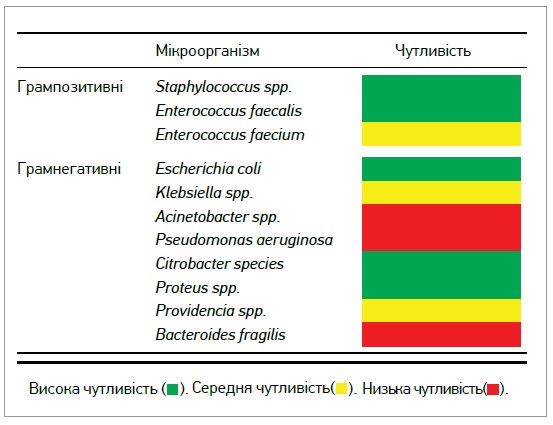
Фoсфоміцин належить до бактерицидних антибіотиків. Він пригнічує фермент УДФ-ацетилглюкозамін‑3-енолпірувілтрансферазу, яка бере участь у синтезі стінки бактерійної клітини. Цей нетиповий механізм дії обумовлює низький потенціал перехресної резистентності, забезпечує фосфоміцину значну активність щодо багатьох грампозитивних і грамнегативних патогенів, включаючи мультирезистентні штами E. coli та клебсієли, здатні продукувати β-лактамази, а також карбапенем-резистентні ентеробактерії (рис.) (Avent M.L. et al., 2018).
Рис. Спектр активності фосфоміцину
Фосфоміцин може застосовуватися в педіатрії. Так, описано успішне застосування доз 100-200 мг/кг/добу (за 3-4 прийоми), яке не супроводжувалося токсичними проявами. Побічні явища застосування фосфоміцину є нетиповими також у вагітних. За класифікацією Управління з контролю за якістю продуктів харчування і лікарських засобів США (FDA), фосфоміцин належить до категорії вагітності В, тобто доведені ризики застосування відсутні. Хоча препарат проникає через плаценту, призначення фосфоміцину не асоціюється з тератогенним впливом (Avent M.L. et al., 2018; Cimolai N., Cimolai T., 2008).
Фосфоміцину притаманний хороший розподіл у тканинах організму з досягненням клінічно значущих концентрацій у сироватці крові, нирках, стінці сечового міхура та простаті (Frimodt-Moller N., 2010; Michalopoulos A.S. et al., 2011; Gardiner B.J. et al., 2014). Більшість наявної літератури підтверджує сприятливий профіль безпеки фосфоміцину. Найпоширенішими побічними ефектами цього препарату є пронос і блювання (Avent M.L. et al., 2018).
Більшість досліджень ефективності фосфоміцину передбачали вивчення його дії при неускладнених циститах у дорослих жінок. Порівняння із фторхінолонами, триметопримом/сульфаметоксазолом, нітрофурантоїном, амоксициліном/клавуланатом і пероральними цефалоспоринами (всі ці препарати застосовуються в режимі 5-7-денних курсів лікування на відміну від фосфоміцину, який приймається одноразово) виявили аналогічну частку клінічного та мікробіологічного успіху (в межах 75-95%) (Falagas M.E. et al., 2010; Pullukcu H. et al., 2007; Rodriguez-Bano J. et al., 2008).
Систематичний огляд M.E. Falagas і співавт. (2010) виявив, що пероральна терапія фосфоміцином була клінічно ефективною за циститу та пієлонефриту, спричинених E. coli, здатними продукувати β-лактамази. Запропоновано застосовувати фосфоміцин і як альтернативний засіб для лікування простатиту, оскільки цей препарат має високу біодоступність при пероральному застосуванні, здатність досягати високих концентрацій у тканинах передміхурової залози (Gardiner B.J. et al., 2014). Лікування простатиту зазвичай потребує множинних доз фосфоміцину (Grayson M.L. et al., 2015; Los-Arcos I. et al., 2015).
Отже, в умовах наростання антибіотикорезистентності та асоційованих із нею невдач лікування виникає потреба в переосмисленні застосування давно відомих і добре вивчених антибактеріальних медикаментів. Одним із таких препаратів є фосфоміцин, який успішно застосовується з 1960-х рр. Незважаючи на 60-річну історію, фосфоміцин відповідає сучасним клінічним настановам, зокрема рекомендаціям Європейської асоціації урологів (2023). Дуже вагома перевага фосфоміцину – зручність застосування: для лікування використовується лише одна доза препарату. Важливо також те, що фосфоміцин можна застосовувати у вагітних та для лікування пієлонефриту і простатиту. Урофосцин виробництва АТ «Київмедпрепарат» (фармацевтична корпорація «Артеріум», лідер* роздрібного ринку антибактеріальних препаратів) являє собою вітчизняний фосфоміцин у формі гранул для орального розчину в пакеті-саше (1 пакет-саше містить 5,631 фосфоміцину трометамолу, що еквівалентно 3 г фосфоміцину). Мандариновий ароматизатор забезпечує препарату хороші смакові якості, що покращує прихильність пацієнтів (насамперед за потреби декількаразового прийому). Показання до застосування Урофосцину – лікування гострих неускладнених інфекцій нижніх сечовивідних шляхів, спричинених чутливими до фосфоміцину мікроорганізмами, в чоловіків, дівчат віком >12 років і жінок, а також профілактика під час діагностичних процедур, хірургічних втручань у дорослих пацієнтів.
Експертна думка
 Завідувачка кафедри нефрології та нирковозамісної терапії Національного університету охорони здоров’я України ім. П.Л. Шупика (м. Київ), доктор медичних наук, професор Стелла Вікторівна Кушніренко
Завідувачка кафедри нефрології та нирковозамісної терапії Національного університету охорони здоров’я України ім. П.Л. Шупика (м. Київ), доктор медичних наук, професор Стелла Вікторівна Кушніренко
– Інфекції сечових шляхів (ІСШ) є небезпечними не лише самі собою, а і як фактор ризику хронічної хвороби нирок та термінальної стадії ниркової недостатності. П’ятірка основних етіологічних чинників ІСШ включає E. coli, K. pneumoniae, E. faecalis, E. faecium і P. aeruginosa.
Відповідно до концепції розподілу ІСШ, цистити, пієлонефрити та рецидивуючі ІСШ можуть бути як неускладненими, так і ускладненими; натомість катетер-асоційовані ІСШ та ІСШ у чоловіків завжди вважаються ускладненими. Ускладнені інфекції часто виникають також у вагітних і жінок віком >65 років; в осіб із цукровим діабетом на тлі прийому інгібіторів натрійзалежного котранспортера глюкози 2 типу; при сечокам’яній хворобі; в осіб з імуносупресією тощо.
Більшій частоті ІСШ у жінок порівняно із чоловіками сприяють анатомічні фактори (коротка та широка уретра, близькість уретри до вагіни), генетичні (наявність специфічних рецепторів) і гінекологічні фактори (запальні, інфекційні процеси вагіни й вульви, гормональні розлади, ранній початок статевого життя, аборти, застосування сперміцидів).
Відповідно до настанов Європейської асоціації урологів (2023), точний діагноз неускладненого циститу може ґрунтуватися на сфокусованому анамнезі симптомів нижніх сечових шляхів і відсутності виділень з вагіни чи подразнення. Симптомами нижніх сечових шляхів вважаються дизурія (пекучий біль під час сечовипускання), підвищена частота сечовипускань та невідкладні позиви до сечовипускання. На відміну від Європейської асоціації урологів, Національний інститут охорони здоров’я та досконалості надання медичної допомоги Сполученого Королівства Великої Британії та Північної Ірландії вважає симптомами нижніх сечових шляхів дизурію, появу ніктурії та каламутність сечі.
Для діагностики циститу також доцільним є проведення загального аналізу сечі; натомість посів сечі потрібен за підозри на гострий пієлонефрит; при симптомах, які не минають або рецидивують упродовж 4 тиж після завершення лікування; в жінок з атиповими симптомами; у вагітних.
У рекомендаціях Європейської асоціації урологів надано пораду призначати фосфоміцину трометамол, півмецилінам або нітрофурантоїн як першу лінію терапії неускладненого циститу в жінок. Амінопеніциліни чи фторхінолони застосовувати не рекомендовано.
Фосфоміцин блокує синтез клітинної стінки бактерій, зменшує їхню адгезію, порушує функціонування фімбрій, руйнує біоплівки, які утворюють уропатогенні штами E. coli, та сприяють їхній загибелі. Фосфоміцин накопичується в нирках у концентрації 2500-3500 мкг/мл, а його мінімальна інгібувальна концентрація для E. coli становить 128 мкг/мл. Виражена бактерицидна й антиадгезивна дія щодо найпоширеніших збудників гострого циститу забезпечує фосфоміцину високу клінічну ефективність (ерадикація E. coli до 99%). Після одного прийому терапевтична концентрація препарату в сечовій системі зберігається протягом 48 год (на прикладі препарату Урофосцин виробництва АТ «Київмедпрепарат» (фармацевтична корпорація «Артеріум», лідер* роздрібного ринку антибактеріальних препаратів)).
У гострій фазі захворювання приймають 1 пакет-саше (3 г фосфоміцину), розчинивши вміст у склянці води. З метою профілактики інфікування сечових шляхів при хірургічних втручаннях і трансуретральних діагностичних обстеженнях приймають уміст 1 пакета за 3 год до втручання і 2-го – через 24 год після втручання.
Окремим питанням у веденні осіб з ІСШ є рецидивуючі інфекції, тобто ІСШ, які виникають із частотою не менше 3 епізодів на рік або 2 епізодів на 6 міс. Рецидивуючі ІСШ – поширений патологічний стан, який асоціюється зі значним погіршенням стану здоров’я та великими фінансовими витратами; може виникати в жінок усіх вікових категорій, расових та етнічних груп, будь-якого соціально-економічного статусу чи рівня освіти. При рецидивуючих ІСШ слід ретельно збирати анамнез, звертаючи увагу на частоту інфекцій, застосування медикаментів, дані щодо культури сечі тощо. Для виявлення будь-яких структурних або функціональних порушень, зокрема вагінальної атрофії чи випадіння тазових органів, проводиться фізикальне обстеження черевної порожнини, органів малого таза.
Загальне резюме щодо діагностики та лікування рецидивуючих ІСШ (Європейська асоціація урологів, 2023) включає такі тези:
1) розширене рутинне обстеження, включаючи цистоскопію, візуалізаційні дослідження тощо, має низьку діагностичну цінність для діагностики рецидивуючих ІСШ;
2) підвищення споживання води – ефективна стратегія зменшення вживання антибактеріальних засобів для запобігання рецидивуючим ІСШ у жінок у предменопаузі з високим ризиком рецидиву, які п’ють невеликий об’єм води (<1,5 л) щодня;
3) вагінальна замісна терапія естрогенами продемонструвала тенденцію щодо запобігання рецидивуючим ІСШ у жінок у постменопаузі;
4) в декількох рандомізованих контрольованих дослідженнях імуноактивна профілактика була активнішою за плацебо в запобіганні рецидивуючим ІСШ;
5) пробіотики, що містять L. rhamnosus, L. reuteri, L. casei shirota або L. crispatus, ефективні для відновлення вагінальної флори та профілактики рецидивуючих ІСШ;
6) сучасні наукові дані щодо ефективності продуктів із журавлини для профілактики ІСШ є суперечливими;
7) на підставі обмежених даних D-манноза може значно зменшити кількість епізодів ІСШ в окремих пацієнтів;
8) згідно з обмеженими даними, внутрішньоміхурова терапія глікозаміногліканами може зменшити кількість ІСШ на рік, збільшити інтервал часу між рецидивами;
9) рандомізоване контрольоване дослідження продемонструвало не меншу ефективність прийому метенаміну гіпурату 2 р/добу порівняно зі стандартною антибіотикопрофілактикою;
10) було показано таке: як безперервна антимікробна профілактика низькими дозами, так і посткоїтальна антимікробна профілактика знижують частоту рецидивуючих ІСШ;
11) проспективне когортне дослідження продемонструвало, що періодична терапія, яку пацієнт розпочинає самостійно, є ефективною, безпечною та економічно доцільною для жінок із рецидивуючими ІСШ.
Визначення і діагностична оцінка рецидивуючих ІСШ, а також стратегії антибіотикопрофілактики є узгодженими в більшості наявних настанов, а також підкреслюють важливість отримання посіву сечі й обмеженість ролі цистоскопії та візуалізаційних досліджень верхніх сечових шляхів у жінок без факторів ризику. Запропоновані схеми безперервної антимікробної профілактики (AUA/CUA/SUFU, 2022) включають фосфоміцину трометамол 3 г кожні 10 діб (на прикладі препарату Урофосцин виробництва АТ «Київмедпрепарат» (фармацевтична корпорація «Артеріум», лідер* роздрібного ринку антибактеріальних препаратів)), нітрофурантоїн 50 або 100 мг 1 р/добу, триметоприм 100 мг 1 р/добу, а під час вагітності – цефалексин 125 або 250 мг 1 р/добу чи цефаклор 250 мг 1 р/добу.
Червоними прапорцями щодо раннього скерування до уролога жінок із рецидивуючими ІСШ і симптомами циститу є розбіжність між результатами посіву сечі, клінічною картиною; стійка гематурія, незважаючи на адекватний контроль інфекції; стійка піурія; постійний біль; стійка бактеріурія, незважаючи на відповідну антибіотикотерапію; наявність бактерій, які розщеплюють сечовину, в повторних культурах сечі; доведений візуалізацією конкремент у сечовому міхурі чи нирці; рецидивуючий пієлонефрит; попереднє хірургічне втручання на сечовивідних шляхах (у т. ч. щодо нетримання сечі); травма сечових шляхів; анамнез злоякісної пухлини органів черевної порожнини або малого таза; анамнез опромінення органів малого таза; неврологічні захворювання (травма спинного мозку, розсіяний склероз); симптоми обструктивного сечовипускання (слабкий струмінь сечі, неповне спорожнення сечового міхура); ознаки незадовільного спорожнення сечового міхура під час ультразвукового обстеження; аномалії сечового тракту; ослаблений імунітет; симптоми фістули між сечовим міхуром та кишечником (пневматурія, фекалурія); відсутність відповіді на профілактичні заходи.
З огляду на погляди провідних урологічних асоціацій щодо призначення фосфоміцину (на прикладі препарату Урофосцин виробництва АТ «Київмедпрепарат» (фармацевтична корпорація «Артеріум», лідер* роздрібного ринку антибактеріальних препаратів)) можна сказати, що при симптоматичному епізоді ІСШ він призначається одноразово, за повторних симптоматичних епізодів – 3 доби (1 р/добу), а для безперервної низькодозової антимікробної профілактики в разі рецидивуючих ІСШ – 1 р/10 діб протягом 3-6 міс (EAU, 2023).
Підготувала Лариса Стрільчук