4 січня, 2024
Інфекційно-запальні захворювання сечової системи та їхні ускладнення
 Сепсис розглядають як спричинений інфекцією небезпечний для життя стан, що асоціюється з високим ризиком смерті. Захворюваність на сепсис протягом останніх десятиліть постійно зростає, але ефективність лікування не покращується передусім через поширення резистентності до антибіотиків серед клінічно значущих патогенів. Сьогодні сепсису приділяють чималу увагу на міжнародних і вітчизняних медичних форумах. Проблемним питанням діагностики та лікування сепсису було присвячено науково-практичну конференцію «Сепсис: виклики сьогодення», що відбулася 24 листопада в онлайн-форматі. Професор кафедри урології Одеського національного медичного університету, доктор медичних наук Михайло Іванович Ухаль розповів про інфекційно-запальні захворювання сечової системи, які часом можуть ускладнюватися розвитком сепсису.
Сепсис розглядають як спричинений інфекцією небезпечний для життя стан, що асоціюється з високим ризиком смерті. Захворюваність на сепсис протягом останніх десятиліть постійно зростає, але ефективність лікування не покращується передусім через поширення резистентності до антибіотиків серед клінічно значущих патогенів. Сьогодні сепсису приділяють чималу увагу на міжнародних і вітчизняних медичних форумах. Проблемним питанням діагностики та лікування сепсису було присвячено науково-практичну конференцію «Сепсис: виклики сьогодення», що відбулася 24 листопада в онлайн-форматі. Професор кафедри урології Одеського національного медичного університету, доктор медичних наук Михайло Іванович Ухаль розповів про інфекційно-запальні захворювання сечової системи, які часом можуть ускладнюватися розвитком сепсису.
Доповідач зазначив, що інфекції сечовивідних шляхів (ІСШ) є досить поширеними. Найчастішими з них є хронічний пієлонефрит (46,5%), гострий цистит (31,9%), хронічний цистит (11%), гострий пієлонефрит – ГП (8,1%).
ІСШ класифікують за локалізацією (інфекції верхніх сечових шляхів: пієлонефрит, пієліт, уретрит; інфекції нижніх сечових шляхів: цистит, уретрит), за клінічним перебігом (гострі – перший епізод, рецидив, нова інфекція; хронічні – загострення, ремісія; безсимптомна бактеріурія), за розвитком ускладнень (ускладнені: абсцес, карбункул, паранефрит, уросепсис, шок, гостра ниркова недостатність).
До неускладнених ІСШ відносять епізоди гострої інфекції нижніх або верхніх сечових шляхів (частіше в жінок) за відсутності яких-небудь порушень відтоку сечі з нирок і сечового міхура, структурних порушень в органах сечової системи та серйозних супутніх захворювань, які можуть призвести до ускладнень або неефективності застосованої терапії.
Ускладнені ІСШ розвиваються на тлі структурних або анатомічних аномалій сечових органів, а також супутніх захворювань, які знижують захисні сили організму та підвищують ризик висхідної інфекції або неефективності лікування. До ускладнених інфекцій ІСШ відносять також внутрішньолікарняні (нозокоміальні) інфекції, ІСШ у вагітних.
Чинники ризику ускладнених ІСШ
Розрізняють низку чинників, що підвищують ризик розвитку ускладнених ІСШ. До них належать:
- наявність постійного катетера чи стента (уретрального, сечовідного, ниркового) або періодична катетеризація сечового міхура;
- об’єм залишкової сечі >100 мл;
- обструктивна уропатія будь-якої етіології, наприклад обструкція вічка сечового міхура (включаючи нейрогенний сечовий міхур), камені та пухлини;
- сечовідний рефлюкс або інші функціональні порушення;
- реконструктивні операції сечовідних шляхів із використанням сегмента клубової кишки;
- хімічні або променеві пошкодження уроепітелію;
- пері- чи післяопераційні ІСШ;
- ниркова недостатність або трансплантація нирок, цукровий діабет й імунодефіцити.
Зазвичай ІСШ спричиняються одним збудником. Найчастіше це ентеробактерії (70-95% випадків) і Staphylococcus saprophyticus (5-20% випадків). Значно рідше це інші грамнегативні бактерії (клебсієли, протеї та ін.).
Одним із найпоширеніших ІСШ, що супроводжується високим ризиком ускладнень, є ГП. Це гострий запальний процес, який характеризується бактеріальним пошкодженням ниркової паренхіми та чашково-мискової системи нирки. У більшості випадків ГП перебігає як тяжка інфекційна хвороба з вираженою інтоксикацією. Захворювання трапляється в усіх вікових групах. Середня поширеність ГП у популяції становить близько 10-12%. Частіше хворіють дівчата та молоді жінки, особливо вагітні. У віці 60-80 років різко зростає захворюваність на ГП серед чоловіків у зв’язку зі збільшенням поширеності гіперплазії та раку передміхурової залози, порушеннями гемо- й уродинаміки. Серед хворих похилого віку частіше спостерігаються тяжкі та загрозливі для життя форми захворювання (гнійний пієлонефрит, апостематоз нирок, сепсис).
У більш ніж 80% випадків етіологічним агентом ГП є Escherichia coli. Інші етіологічні причини включають аеробні грамнегативні бактерії, S. saprophyticus та ентерококи. Поширене використання катетерів серед цих пацієнтів зумовлює їх інфікування грамнегативними мікроорганізмами, як-от Proteus, Klebsiella, Serratia, Pseudomonas.
Клінічні прояви і діагностика ГП
Спектр проявів ГП досить широкий. Пієлонефрит зазвичай характеризується гострим початком з ознаками системного запалення (лихоманка, озноб і нездужання). Часто відзначається біль у попереку, переважно однобічний.
Розрізняють такі клінічні форми перебігу ГП: найгостріша (тяжкий стан, лихоманка, озноб, загальні ознаки сепсису, незначні місцеві прояви захворювання); гостра (вираженіші місцеві прояви захворювання, озноб зазвичай відсутній); підгостра (загальні симптоми стерті, вираженіші місцеві прояви захворювання); латентна (перебіг захворювання з мінімальними місцевими симптомами).
Обов’язковими методами дослідження за підозри на ГП є загальний аналіз сечі та крові. Їх слід виконати до початку емпіричної антибактеріальної терапії. Піурія присутня майже в усіх пацієнтів із ГП. Окрім того, в сечі можуть визначатися висока бактеріурія (105-106), мікрогематурія, протеїнурія. Для загального аналізу крові характерними є лейкоцитоз зі зсувом уліво, підвищення показника ШОЕ.
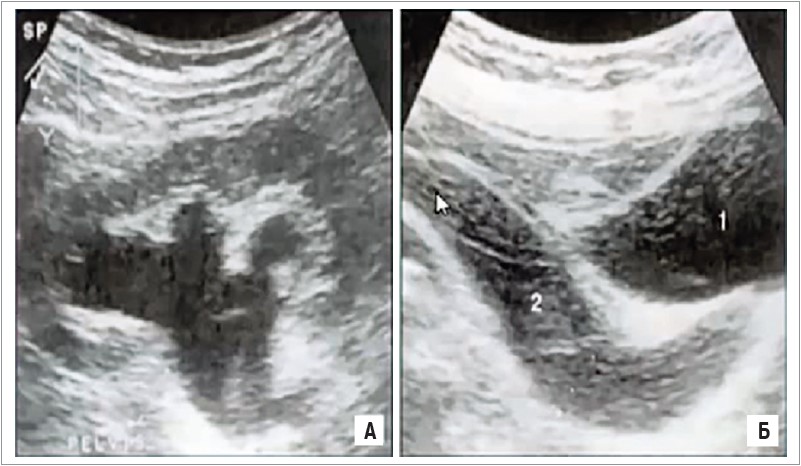
На оглядовій рентгенограмі (комп’ютерній томограмі) уражена нирка має збільшені розміри (на ≥1,5 см). При ультрасонографії нирок спостерігаються збільшена уражена нирка з посиленням ехосигналу, розширення чашково-мискової системи нирки (рис.).
Рис. Ультрасонограма нирки при обструктивному пієлонефриті: А – розширення чашково-мискової системи нирки; Б – розширення сечоводу на тлі сечового міхура
Примітки: 1 – сечовий міхур; 2 – сечовід.
Ускладнення ГП
Найтяжчими ускладненнями гострого гнійного пієлонефриту є бактеріотоксичний (септичний) шок і сепсис.
Близько 95% випадків бактеріотоксичного шоку мають ятрогенне походження та розвиваються внаслідок призначення потужної протимікробної терапії на тлі порушеного відтоку сечі від нирок. Тому при обструктивному пієлонефриті першочерговим завданням є відновлення відтоку сечі від ураженої нирки.
Чому це так важливо? Добре відомо, що на тлі гіпертензії в чашково-мисковій системі нирки формується каліковенозний шунт. Це призводить до надходження інфікованої сечі безпосередньо в кровоток. У разі призначення антибактеріальної терапії в кровоток починають масово потрапляти бактеріальні ендотоксини й інші продукти руйнування мікроорганізмів, які й спричиняють бактеріотоксичний шок. Спостерігаються генералізована вазодилатація, депонування крові на периферії, зниження серцевого викиду.
На тлі гострого гнійного запального процесу в нирці розвиваються гіпоальбумінемія та дефіцит ендогенного гепарину.
Клінічні прояви і лікування бактеріотоксичного шоку
На початку розвитку бактеріотоксичного шоку спостерігаються короткочасний сильний озноб із наростанням тахікардії, різке зниження артеріального тиску, гостра серцево-судинна недостатність. Характерними є множинні крововиливи в шкіру та підшкірну клітковину, слизові покриви, паренхіматозні органи, можливі носові кровотечі. Застосування інфузійної терапії та вазопресорів зазвичай не дає достатнього ефекту.
Лікування хворих на бактеріотоксичний шок передбачає болюсне введення гепарину в дозі 10 тис. ОД внутрішньовенно. Надалі переходять на призначення підтримувальних доз гепарину (по 1250 ОД що 6 год підшкірно). Для швидкого відновлення рівня альбумінемії застосовують масивні трансфузії нативної або замороженої плазми, альбуміну. Вазопресори слід застосовувати за умови компенсації об’єму циркулювальної крові. Після стабілізації стану пацієнта призначають дезінтоксикаційну та симптоматичну терапію.
Сепсис
Дефініція сепсису впродовж певного періоду часу зазнала низки змін. До 2016 р. поняття «сепсис» визначали як синдром системної запальної відповіді (ССЗВ) за наявного або підтвердженого вогнища інфекції. У 2016 р. більшість наукових товариств переглянули критерії визначення сепсису. На сьогодні ССЗВ разом із наявним або підтвердженим вогнищем інфекції не вважається більше критерієм для встановлення діагнозу «сепсис», оскільки ознаки ССЗВ не обов’язково вказують на зміни, небезпечні для життя. Нині сепсис визначають як життєзагрозливу органну дисфункцію внаслідок порушення відповіді хазяїна на інфекцію. Термін «тяжкий сепсис» у нових рекомендаціях виключено, оскільки поліорганна недостатність, на думку експертів, має розглядатись як складова сепсису, а не його ускладнення.
Отже, сепсис є надмірною реакцією організму на інфекцію за участю компонентів мікроорганізму та його ендотоксинів, а також продукованих організмом господаря медіаторів запальної відповіді (цитокінів, хемокінів, ейкозаноїдів та ін.) і речовин, які пошкоджують клітини (наприклад, вільні кисневі радикали).
Сепсис є мікробіологічно підтвердженим діагнозом, що потребує виявлення патогенних мікроорганізмів (або їхніх антигенів чи генетичного матеріалу) з тканин або рідин організму, які в нормі є стерильними. Слід зазначити, що тип мікроорганізму не визначає перебігу сепсису. У більшості випадків немає попередніх порушень імунітету, хоча вони є важливим чинником ризику сепсису.
Клінічна картина та перебіг сепсису
Симптоми сепсису залежать від первинно уражених органів. Якщо прогресування інфекції не вдається зупинити на початковій стадії сепсису, починають з’являтися симптоми порушення функцій інших органів: дихальної системи (гостра дихальна недостатність), системи кровообігу (гіпотензія, шок) нирок (гостре пошкодження нирок), порушення гемостазу (синдром дисемінованого внутрішньосудинного зсідання, тромбоцитопенія), метаболічні порушення (лактацидоз). Якщо не розпочати ефективного лікування, перебіг захворювання поглиблюватиметься, що надалі призведе до розвитку поліорганної недостатності та смерті.
Клініко-лабораторні показники сепсису
- Температура тіла >38 або <36 ºС.
- Тахікардія >90/хв.
- Тахіпное >30/хв (або механічна вентиляція легень).
- Раптове порушення свідомості.
- Значні набряки або позитивний водний баланс (>20 мл/кг/добу).
- Гіперглікемія (>7,7 ммоль/л, або 140 мг/дл), незважаючи на відсутність цукрового діабету.
- Лейкоцитоз >12 000/мкл або лейкопенія (число лейкоцитів <4000/мкл).
- Наявність >10% незрілих форм нейтрофілів.
- С-реактивний білок >2 стандартні відхилення від середнього значення.
- Прокальцитонін >2 відхилення від середнього значення.
- Зниження артеріального тиску (систолічний <90 мм рт. ст., середній <70 мм рт. ст., падіння систолічного тиску на >40 мм рт. ст. в осіб з артеріальною гіпертензією).
- Подовження часу капілярного наповнення та прогресування симптомів дисфункції органів.
- Гіпоксемія (PaO2/FiO2 <300 мм рт. ст., а за наявності первинних захворювань дихальної системи <200).
- Гостра олігурія (діурез <0,5 мл/кг/год протягом >2 год за достатньої гідратації).
- Підвищення креатинінемії на >44,2 мкмоль/л (0,5 мг/дл) протягом 48 год.
- Порушення гемостазу (кількість тромбоцитів <1×105/мкл, міжнародне нормалізоване відношення >1,5, активований частковий тромбопластиновий час >60 с).
- Концентрація загального білірубіну в плазмі >70 мкмоль/л (4 мг/дл).
- Паралітична кишкова непрохідність (перистальтичні шуми не вислуховуються).
Мікробіологічне дослідження
Для мікробіологічного дослідження потрібно взяти не менш як 2 зразки крові. При цьому як мінімум 1 зразок має бути взятий з окремо пунктованої вени та по 1 – з кожного судинного катетера, встановленого раніше 48 год.
Залежно від імовірної етіології сепсису мікробіологічному дослідженню підлягає матеріал із дихальних шляхів, сечі, інших біологічних рідин (у тому числі ліквору, плевральної рідини), мазків чи виділень із ран.
Лікування
Антибактеріальна терапія. Відповідно до чинних настанов хворим із сепсисом або септичним шоком після встановлення діагнозу показано якнайшвидше (протягом 1 год) довенне введення антибактеріальних препаратів, оскільки з кожною наступною годиною запізнення ризик смерті суттєво зростає.
Призначення емпіричної комбінованої антибактеріальної терапії спрямоване на найімовірнішого збудника на початковому етапі лікування септичного шоку, що обумовлює застосування щонайменше 2 препаратів різних класів. Також одним із принципів проведення антибактеріальної терапії є рання деескалація (згідно з результатами антибіотикограми).
Не рекомендується рутинне застосування ≥2 антибіотиків із різних груп, спрямованих на той самий патоген, який підтверджений або підозрюється, при сепсисі чи бактеріємії з нейтропенією або при тяжких інфекціях із бактеріємією чи сепсисом без шоку. Втім, це не виключає в таких випадках полівалентної терапії з метою розширення спектра протимікробної дії (наприклад, використання ≥2 антибіотиків різних активних груп, які скеровані проти ≥2 бактерій, що підтверджені або підозрюються). За підтвердження чи підозри інфекції Pseudomonas або Acinetobacter (особливо в разі виявлення штамів, стійких до лікарських форм) застосовують комбіновану терапію.
Із метою деескалації протимікробної терапії в пацієнтів із сепсисом і септичним шоком рекомендоване щоденне оцінювання стану. Рівень прокальцитоніну може бути використаний для прийняття рішення щодо припинення антибактеріальної терапії у хворих із початковими проявами сепсису, які згодом мають обмежені клінічні прояви інфекційного процесу.
Стан пацієнта контролюють щодня, оцінюючи можливість переходу на антибіотик вужчого спектра дії або монотерапію. Тривалість антибактеріальної терапії, навіть для серйозних інфекцій, пов’язаних із сепсисом і септичним шоком, у більшості випадків не має перевищувати 7-10 діб. Триваліші курси показані хворим, які мають повільну клінічну відповідь, вогнища інфекції, MRSA-бактеріємію, деякі грибкові або вірусні інфекції, імунодефіцит, у тому числі нейтропенію.
Коротший курс лікування може бути доцільним у деяких пацієнтів, особливо при швидкому покращенні клінічного стану після усунення вогнища уросепсису та в разі неускладненого (тобто за відсутності анатомічного підґрунтя) пієлонефриту.
Лікування порушень кровообігу. Згідно з рекомендаціями SSC (2016) у хворих із підозрою на гіповолемію інфузійну терапію слід починати з інфузії кристалоїдів або розчину NaСl 0,9% у кількості ≥30 мл/кг протягом перших 3 год, з одночасним моніторингом показників гемодинаміки. Зазвичай перевага віддається збалансованим розчинам, особливо за потреби внутрішньовенного переливання великих об’ємів.
Деякі пацієнти можуть потребувати швидкого переливання більшої кількості розчинів (>30 мл/кг). У такому випадку великі об’єми розчинів варто вводити порційно (по 200-500 мл), після переливання кожної з них слід оцінювати відповідь на лікування.
У пацієнтів, які потребують переливання великих об’ємів кристалоїдів, пропонується також переливання розчинів альбуміну (зазвичай у концентрації 4 або 5%) на початку інфузійної терапії.
Переливання препаратів крові. За рівня гемоглобіну <7 г/дл рекомендується застосування еритроцитарної маси до досягнення концентрації 7,0-9,0 г/дл.
Профілактична трансфузія тромбоцитів показана хворим у таких випадках:
- рівень тромбоцитів <10×109/л за відсутності явної кровотечі;
- рівень тромбоцитів <20×109/л, якщо пацієнт має значний ризик розвитку кровотечі;
- рівень тромбоцитів ≥50×109/л за активної кровотечі, операції або інвазивних процедур.
Трансфузію свіжозамороженої плазми та кріопреципітату застосовують переважно при активній кровотечі або плануванні інвазивних утручань.
Лікування ниркової недостатності. Основне значення має стабілізація гемодинаміки (нормалізація артеріального тиску). За потреби проводять нирковозамісну терапію. Наразі не встановлено, чи ранній початок такої терапії є ефективнішим.
Корекція ацидозу. За рівня pH крові <7,15 рекомендується внутрішньовенне введення NaHCO3.
Кортикостероїди. Якщо гіпотензія зберігається, незважаючи на адекватну інфузійну терапію та застосування вазопресорних препаратів у середніх або високих дозах, можна розглянути введення гідрокортизону внутрішньовенно в дозі <400 мг/добу впродовж ≥3 днів (зазвичай 200 мг/добу принаймні до ліквідації шоку).
Контроль глікемії. У разі розвитку спричиненої тяжким сепсисом гіперглікемії (>10 ммол/л у 2 послідовних вимірюваннях) рекомендоване застосування внутрішньовенної інфузії інсуліну. Цільовим значенням є радше глікемія <10 ммоль/л, аніж <6,1 ммоль/л. На ранніх етапах лікування інсуліном слід визначати рівень глікемії що 1-2 год, а після її стабілізації – що 4-6 год. Результати досліджень, отримані з капілярної крові, можуть бути хибними, тому в пацієнтів із наявним артеріальним катетером рекомендується проводити забір крові через цей катетер для виконання глікемічних експрес-тестів.
Харчування. У пацієнтів із сепсисом і септичним шоком слід віддавати перевагу ентеральному харчуванню, якщо це можливо. Не рекомендовано застосування раннього лише парентерального харчування; або парентеральне + ентеральне харчування (слід якнайшвидше розпочинати ентеральне), навіть у критичних хворих, які можуть харчуватися ентерально. Не обов’язково покривати повну потребу в калоріях.
Профілактика стресових виразок шлунка. За наявності чинників ризику шлунково-кишкової кровотечі рекомендовано проведення профілактики стрес-індукованих виразок. Із цією метою застосовують інгібітори протонної помпи або антагоністи Н2-гістамінових рецепторів. У хворих без чинників ризику шлунково-кишкових кровотеч рутинна профілактика стресових виразок не рекомендована.
Підготував В’ячеслав Килимчук
Медична газета «Здоров’я України 21 сторіччя» № 21 (558), 2023 р