2 липня, 2024
Ведення пацієнтів із гіперурикемією та дисліпідемією
За матеріалами майстеркласу Української кардіологічної школи «Серцево-судинні та ревматичні захворювання» (19 квітня 2024 року)
 У межах заходу Української кардіологічної школи «Серцево-судинні та ревматичні захворювання», який відбувся у квітні поточного року, провідні українські науковці розглядали актуальні проблеми в кардіології та ревматології. Зокрема, йшлося про диференційоване ведення пацієнтів із коморбідними захворюваннями, яке потребує міждисциплінарної та узгодженої співпраці фахівців різних спеціальностей задля досягнення якісного контролю клінічного стану хворого, успіху в лікуванні та уникнення поліпрагмазії. Під час заходу д.мед.н., професорка Ірина Юріївна Головач та д. мед.н., професорка Лариса Анатоліївна Міщенко представили спільну доповідь «На прийомі в лікаря пацієнт із гіперурикемією та дисліпідемією. Як обрати правильну тактику?». На прикладі клінічного випадку пацієнта із суглобовим синдромом і коморбідними метаболічними станами спікерки, спираючись на дані доказової медицини, обґрунтували відповідні рекомендації щодо його обстеження та лікування.
У межах заходу Української кардіологічної школи «Серцево-судинні та ревматичні захворювання», який відбувся у квітні поточного року, провідні українські науковці розглядали актуальні проблеми в кардіології та ревматології. Зокрема, йшлося про диференційоване ведення пацієнтів із коморбідними захворюваннями, яке потребує міждисциплінарної та узгодженої співпраці фахівців різних спеціальностей задля досягнення якісного контролю клінічного стану хворого, успіху в лікуванні та уникнення поліпрагмазії. Під час заходу д.мед.н., професорка Ірина Юріївна Головач та д. мед.н., професорка Лариса Анатоліївна Міщенко представили спільну доповідь «На прийомі в лікаря пацієнт із гіперурикемією та дисліпідемією. Як обрати правильну тактику?». На прикладі клінічного випадку пацієнта із суглобовим синдромом і коморбідними метаболічними станами спікерки, спираючись на дані доказової медицини, обґрунтували відповідні рекомендації щодо його обстеження та лікування.
Клінічний випадок
Пацієнт Х., 43 роки, підприємець. Звернувся на консультацію до лікаря-ревматолога через гостре запалення в ділянці І плесно-фалангового суглоба (І ПФС) та склепіння правої стопи. У чоловіка трапився гострий напад артриту серед повного здоров’я, раніше таких випадків не було. Напад виник вночі, супроводжувався гострим інтенсивним болем із різким набряком стопи в ділянці I пальця, що збільшувався «на очах», та значним почервонінням шкіри. А вже зранку пацієнт не зміг стати на ногу. Приймання нестероїдних протизапальних препаратів (НПЗП) мало помірний ефект.
Як зазначає пацієнт, через п’ять днів інтенсивність болю зменшилась, ознаки запалення почали регресувати, і він звернувся до ревматолога. Подібний гострий напад суглобового болю виник уперше. Наявність хронічних захворювань заперечував. Він курить, є епізоди зловживання алкоголем. Сімейного лікаря відвідує нерегулярно. Раніше в біохімічному аналізі крові фіксували підвищені показники сечової кислоти (СК) та холестерину (ХС), але відповідної медичної документації з цього приводу немає.
Огляд: набряк і почервоніння І ПФС правої стопи, незначні ознаки болю за пальпації суглобів склепіння стопи. Рухи в стопі обмежені. Інші суглоби візуально не змінені, рухи не обмежені. Індекс маси тіла (ІМТ) 32,6 кг/мІ, артеріальний тиск (АТ) 130/75 мм. рт. ст., частота серцевих скорочень (ЧСС) 68 на хвилину. З боку внутрішніх органів – без патологічних змін.
Як заначила Ірина Юріївна, ведення пацієнта з гострим суглобовим нападом потребує дотримання послідовних кроків:
Крок 1. Втамування гострого нападу суглобового болю, диференційне діагностування та встановлення причини гострого суглобового нападу.
Крок 2. Лабораторне та інструментальне обстеження для встановлення основного діагнозу.
Крок 3. Виявлення коморбідних станів та їх корекція, визначення потреби в уратзнижувальній терапії (УЗТ), визначення плану лікування пацієнта.
Лабораторні дослідження
Загальний аналіз крові (ЗАК): еритроцити (Еr) 4,1Ч10 12/л, гемоглобін (Нb) 128 г/л, лейкоцити (L) 10,2Ч109/л, тромбоцити (Tr) 223Ч109/л, швидкість осідання еритроцитів (ШОЕ) 38 мм/год; лейкоцитарна формула: паличкоядерні 4%, сегментоядерні 71%, еозинофіли 1%, базофіли 0%, лімфоцити 19%, моноцити 5%.
Коагулограма: протромбіновий індекс 92%, фібрин 8,66 г/л.
Біохімічний (б/х) аналіз крові: загальний білок 72 г/л, сечовина 6,7 ммоль/л, креатинін 95 мкмоль/л, СК 438 мкмоль/л, загальний холестерин (ЗХ) 7,3 ммоль/л, тригліцериди (ТГ) 2,1 ммоль/л, холестерин ліпопротеїдів високої щільності (ЛПВЩ) 1,0 ммоль/л, білірубін загальний 17,7 мкмоль/л, білірубін непрямий 17,7 мкмоль/л, аланінамінотрансфераза (АЛТ) 49 Од/л, аспартатамінотрансфераза (АСТ) 13 Од/л, γ-глутаміл-транспептидаза (ГГТП) 78 Од/л, креатинфосфокіназа (КФК) 34 Од/л, КФК МВ-фракція 8,9%, кальцій загальний 2,32 ммоль/л, ревматоїдний фактор негативний, С-реактивний білок (СРБ) 38 мг/дл, глюкоза крові 5,2 ммоль/л.
Загальний аналіз сечі: колір жовтий, прозора, pH слаболужна, питома вага 1017, глюкози не виявлено, білок 0,6 г/л, лейкоцити 6‑8 у полі зору (п/з), епітелій плаский небагато в п/з, епітелій перехідний 2‑3 у п/з.
Швидкість клубочкової фільтрації (ШКФ) (за формулою CKD-EPI) 84 мл/хв/1,73м2.
Результати лабораторних досліджень пацієнта Х. свідчать про відхилення щодо показників лабораторних досліджень. Зокрема, дані ЗАК підтвердили легке зниження Er та Hb, що може вказувати на можливу анемію. Показник L – у межах норми, проте рівень ШОЕ збільшений, що підтверджує наявність запального процесу.
За даними б/x аналізу крові виявлено підвищені рівні СК, ЗХ і ТГ. Також є підвищення рівнів АЛТ і ГГТП, що може свідчити про можливе ураження печінки. ШКФ – у межах норми, що вказує на здоровий функціональний стан нирок.
Інші показники б/х аналізу крові – без відхилень. Скарги пацієнта Х., дані огляду та результати лабораторного дослідження дають підставу запідозрити в пацієнта діагноз подагри.
Для визначення точного діагнозу слід послуговуватися покроковими класифікаційними критеріями щодо подагри Американського коледжу ревматології та Європейського альянсу ревматологічних асоціацій (ACR/EULAR, 2015):
Крок 1. Вхідний критерій – ≥1 епізод активного запалення в периферичному суглобі / бурсі.
Крок 2. Достатній критерій – наявність кристалів моноурату натрію (МУН) у синовіальній рідині / тонусі.
Якщо немає змоги виконати дослідження синовіальної рідини, необхідно застосовувати систему балів для підрахунку патернів характерних для подагри:
А. Патерн залучення суглоба / бурси: + 1‑2 бали.
А. Характерні симптоми: +1‑3 бали.
B. Час перебігу: +1‑2 бали.
C. Тофус: +4 бали.
D. Лабораторний: від -4 до +4 балів – залежить від рівня СК.
E. Аналіз синовіальної рідини: немає кристалів – 0 балів, негативність щодо кристалів моноурату натрію (МУН) – -2 бали.
F. Візуалізація: «подвійний контур» за ультразвукового дослідження (УЗД) / DECT скан: +4 бали.
G. Рентгенологічні ознаки ураження кистей / стоп (ерозії): +4 бали (Neogi et al., 2015).
Крок 3. Система на основі балів: ≥8 балів із 23 можливих відповідає діагнозу подагри.
Пацієнту Х. не виконували дослідження синовіальної рідини, тому підраховували показники патернів, характерних для подагри. У чоловіка наявний клінічний патерн залучення суглоба / бурси І ПФС як моноартикулярне ураження +2 бали; три характеристики епізоду +3 бали; уперше виниклий типовий перебіг епізоду +1 бал; рівень уратів від 6 до 8 мг/дл (360‑480 мкмоль/л) +2 бали.
Під час УЗД ураженого суглоба виявлено типові для подагри ознаки +4 бали. Загалом отримано 16 балів, що дає підстави встановити клінічний діагноз: Подагра, гострий напад подагри (І), інтермітуючий перебіг. Ожиріння І ступеня. Синдром дисліпідемії.
Лікування гострого нападу подагри
Головний принцип терапії гострого нападу подагри – розпочати його якомога раніше. Вибір лікування такого пацієнта має бути індивідуалізованим, зважаючи на характеристики кожного конкретного випадку та наявні протипоказання.
Як зазначила пані І.Ю. Головач, за безсимптомної ГУ ревматологічні товариства (EULAR, 2016; BSR, 2017; ACR, 2020) не рекомендують призначення медикаментозної уратзнижувальної терапії (УЗТ). І навпаки, в усіх сучасних настановах ревматологічних асоціацій рекомендовано модифікацію способу життя.
Ірина Юріївна наголосила, що гіперурикемія (ГУ) і подагра це два абсолютно різні клінічні стани. Сьогодні ГУ позиціонується як метаболічний розлад, що може стати основою для розвитку різних захворювань, зокрема і подагри. Часто ГУ має безсимптомний перебіг, хоча асоціюється із субклінічним запаленням і ерозуванням кісток. Відкладення кристалів МУН у суглобі провокує гострий напад подагричного артриту.
Постійне утворення кристалів може призвести до хронічного перебігу захворювання, зокрема до хронічного запалення, збільшення кількості нападів, зростання тофусів, структурного ураження суглобів.
Власне, через механізми оксидативного стресу, запалення, ендотеліальної дисфункції ГУ спричиняє розвиток подагричного артриту, хвороб нирок, серцевої недостатності (СН), інсульту, артеріальної гіпертензії (АГ), атеросклерозу та метаболічного синдрому (МС) (Yao et al., 2022).
Також доведено зв’язок ГУ з розвитком супутніх захворювань (Chaudhary et al., 2013).
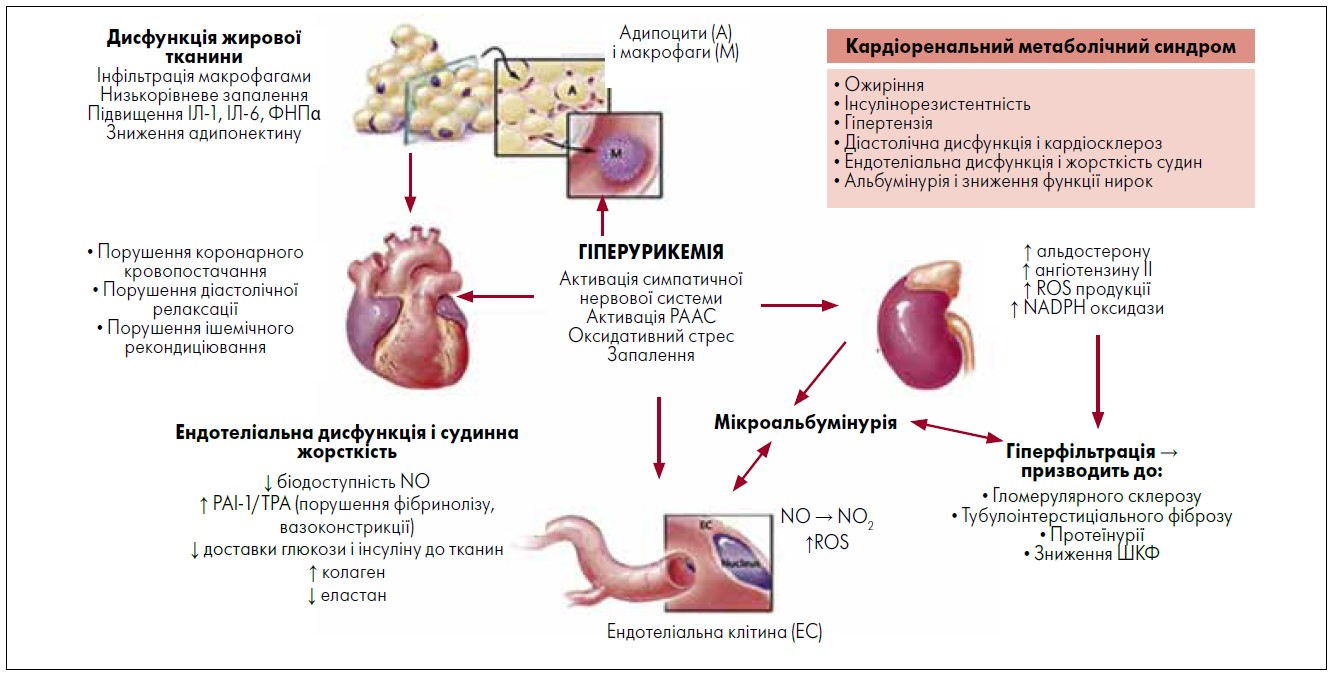
На рисунку представлено дані дослідження впливу ГУ на розвиток кардіоренального та метаболічного синдромів.
Рис. Вплив гіперурикемії на розвиток кардіоренального та метаболічного синдромів
Примітка: ІЛ – інтерлейкін; ФНПα – фактор некрозу пухлин альфа; РААС – ренін-ангіотензин-альдостеронова система; ШКФ – швидкість клубочкової фільтрації; ROS – reactive oxygen species – aктивні форми кисню; NADPH – nicotinamide adenine dinucleotide phosphate – нікотинамід-аденін-динуклеотид-фосфат; NO – nitric oxide – оксид азоту; NO2 – діоксид азоту; PAI‑1 – Plasminogen activator inhibitor‑1 – інгібітор активатора плазміногену‑1; TPA – tissue plasminogen activator – тканинний активатор плазміногену.
Адаптовано за S. Chaudhary et al., 2013.
Уратзнижувальна терапія
Відповідно до рекомендацій EULAR (2016) показаннями до початку УЗТ є:
- Наявність тофусів.
- Хоча б два гострі напади на рік.
- Один гострий напад подагри плюс:
- із дебютом подагри віком до 40 років;
- з артритом при дуже високому сироватковому рівні СК (>8,0 мг/дл або 480 мкмоль/л);
- за супутніх захворювань (ниркова недостатність, АГ, ішемічна хвороба серця [ІХС], СН) (Richette et al., 2017).
У пацієнта Х. на момент огляду немає потреби в призначенні УЗТ, тому йому було рекомендовано застосування всіх можливих шляхів немедикаментозного зниження рівня СК. Окрім ГУ, у чоловіка виявлено порушення ліпідного обміну.
Відповідаючи на запитання: чи потрібно лікувати дисліпідемію (ДЛП) у пацієнта Х. і яку тактику обрати, професорка Л.А. Міщенко запропонувала насамперед проаналізувати дані виконаних досліджень.
Ліпідний спектр у пацієнта Х.: ЗХ 7,3 ммоль/л, ХС ЛПНЩ 4,3 ммоль/л, ХС ЛПВЩ 1 ммоль/л, ТГ 2,1 ммоль/л. Показники ліпідограми свідчать про ДЛП, тож тактика лікування залежить від того, який серцево-судинний ризик (ССР) має пацієнт.
За рекомендаціями Європейського товариства кардіологів (ESC, 2021), Лариса Анатоліївна порадила використовувати для цього покрокове оцінювання стану:
Крок 1. Визначення ССР за шкалою SCORE2 (шкала оцінювання ССР для осіб віком 40‑69 років). Пацієнт Х. належить до категорії високого ризику (зокрема, 7% свідчить про помаранчеву зону), це передбачає медикаментозний вплив на чинники ССР (ESC, 2021).
Для пацієнта Х. було рекомендовано обрати відразу медикаментозну терапію статинами. Крім того, за рекомендаціями Європейського товариства з атеросклерозу (ESC/EAS, 2019) за такого випадку необхідно виконати діагностичну візуалізацію для визначення ризику ССЗ.
Наявність атеросклеротичного ураження артерій (каротидних або феморальних) слід розглядати як модифікувальний чинник наявного ризику в пацієнтів низького та помірного ризику (клас рекомендацій ІІа, рівень доказовості В).
Індекс кальцію за даними спіральної комп’ютерної томографії також належить до модифікувальних чинників наявного ризику за його оцінювання в асимптомних пацієнтів низького і помірного ризику (клас рекомендацій ІІа, рівень доказовості В).
Пацієнту Х. було виконано доплерографічне дослідження артерій голови та шиї, за результатами якого не виявлено ознак ураження сонних артерій, без потовщень інтими-медіа (до 0,8 мм), що свідчить про можливість відтермінування медикаментозної гіполіпідемічної терапії та переходу до наступного кроку настанов ESC (2021).
Крок 2. Обговорення з пацієнтом ССР (пожиттєвий) і користі терапії, яка відповідатиме індивідуальним потребам, зважаючи на його вік, коморбідність, крихкість, поліформації. Ухвалення персоналізованих рішень щодо лікування.
Крок 3. Втручання на індивідуальному рівні. Терапевтичні цілі нацьому етапі передбачають зміни способу життя пацієнта (насамперед правильне харчування, зниження маси тіла, відмову від паління та вживання алкоголю, належний рівень фізичної активності); психотерапію; лікування АГ, гіперхолестеринемії, цукрового діабету (ЦД); антитромботичну терапію та додаткові специфічні заходи (ESC, 2021).
У таблиці наведено показники впливу окремих заходів модифікації способу життя на рівні ХС ЛПНЩ, ХС ЛПВЩ і ТГ (ESC/EAS, 2019).
|
Таблиця. Вплив окремих заходів модифікації способу життя на ЛПНЩ, ЛПВЩ і ТГ |
||
|
Заходи |
Ефект |
Рівень доказів |
|
Зниження рівнів ЗХ і ХС ЛПНЩ |
||
|
Виключення з раціону трансжирів |
5‑10% |
A |
|
Зниження вживання насичених жирів |
>10% |
A |
|
Збільшення вживання клітковини |
5‑10% |
A |
|
Функціональна їжа з фітостеролами |
5‑10% |
A |
|
Добавки із червоним рисом |
5‑10% |
A |
|
Зменшення індексу надмірної ваги |
5‑10% |
А |
|
Зменшення вживання холестеролу |
<5% |
В |
|
Збільшення рівня фізичної активності |
<5% |
В |
|
Зниження рівня ТГ |
||
|
Зменшення надмірної ваги |
<5% |
A |
|
Зменшення вживання алкоголю |
>10% |
A |
|
Збільшення рівня фізичної активності |
5‑10% |
A |
|
Зменшення вживання вуглеводів |
5‑10% |
A |
|
Добавки з ПНЖК (поліненасичені жирні кислоти) |
5‑10% |
A |
|
Зменшення моно- і дисахаридів |
5‑10% |
В |
|
Збільшення рівня ХС ЛПВЩ |
||
|
Виключення з раціону трансжирів |
5‑10% |
A |
|
Збільшення рівня фізичної активності |
>10% |
A |
|
Зменшення індексу надмірної ваги |
5‑10% |
A |
|
Зменшення вживання вуглеводів і заміна їх насиченими жирами |
5‑10% |
A |
|
Помірне вживання алкоголю (2-4 «стандартні дози»), для чоловіків – до 4 доз, для жінок – до 2 доз |
5‑10% |
В |
|
Відмова від куріння |
<5% |
В |
|
Примітки: ЗХ – загальний холестерин, ПНЖК – поліненасичені жирні кислоти, ХС ЛПНЩ – холестерин ліпопротеїдів низької щільності, ХС ЛПВЩ – холестерин ліпопротеїдів високої щільності Адаптовано за ESC/EAS Guidelines for the management of dyslipidemias: lipid modification to reduce cardiovascular risk, 2019. |
||
Лариса Анатоліївна зауважила, що модифікація способу життя, як-от збільшення рівня фізичної активності та відмова від вживання алкоголю, у комбінації з додаванням до раціону добавок червоного ферментованого рису (RYR) має найбільший антиатерогенний ефект.
За рекомендаціями Міжнародної експертної ліпідної панелі (ILEP) щодо використання RYR у клінічній практиці, такий підхід можливо розглядати як частину підтримувальної стратегії для управління ДЛП і ССР у пацієнтів із підтвердженою непереносимістю статинів (клас рекомендації ІІа, рівень доказовості В).
Також RYR рекомендовано розглянути для пацієнтів, які мають неоптимальний ліпідний профіль, попри дотримання дієти та модифікацію способу життя (клас рекомендації ІІа, рівень доказовості В). Крім того, добавки RYR, окремо або в комбінації з іншими доступними ліпідознижувальними препаратами, рекомендовано для первинної профілактики пацієнтам, які не бажають приймати статини.
Комплексом на основі RYR є Атеродінол. В одній його капсулі міститься екстракт RYR100 мг, що еквівалентно 3 мг моноколіну К, екстракт бергамоту 250 мг, 5-метилтетрагідрофолат 0,2 мг. Така комбінація має статиноподібний механізм дії і чинить позитивний вплив на ТГ (↓30‑40%), ХС ЛПНЩ, ХС ЛПВЩ, глюкозу крові, та функцію ендотелію, незалежно від рівня гомоцистеїну в плазмі крові.
Співробітники відділу артеріальної гіпертензії та коморбідної патології ДУ «ННЦ Інститут кардіології, клінічної та регенеративної медицини імені академіка М.Д. Стражеска» НАМН України вивчали гіполіпідемічний вплив комплексу Атеродінол. У дослідженні взяли участь 60 осіб із чинниками ризику ССЗ (90% жінки), віком 48,1±0,7 років.
На тлі приймання Атеродінол спостерігалось достовірне зниження рівня ЗХ від 7,2 до 6,6 ммоль/л; ХС ЛПНЩ – від 5,2 до 4,4 ммоль/л та ХС не-ЛПВН – від 5,8 до 5,1 ммоль/л через три місяці вживання (р=0,0001). Також виявлено позитивний вплив на рівень ТГ в осіб із гіпертригліцеридемією (ТГ >1,7 ммоль/л), зниження рівня ТГ від 2,7 до 2,2 ммоль/л через три місяці вживання (p=0,046).
Як зазначила Лариса Анатоліївна, разом із пацієнтом Х. було узгоджено немедикаментозну корекцію ДЛП комплексом Атеродінол. Ірина Юріївна зауважила, що через наявність ГУ пацієнту Х. було також рекомендовано дотримання тактики модифікації способу життя, насамперед коригування режиму харчування (Sautner et al., 2022).
Модифікація способу життя та харчування для пацієнтів із подагрою та гіперурикемією
Щодо модифікації способу життя та харчування для пацієнтів із подагрою та ГУ запропоновано десять рекомендацій (зокрема рекомендації 1‑3 мають загальний характер; 4‑7 – містять заборонені продукти; 8‑10 – бажано додавати до харчування):
- Збільшення ваги та ожиріння можуть призвести до підвищення рівня СК та подагри. У разі ожиріння поступове зменшення ваги (принаймні в чоловіків) може допомогти знизити рівень СК і в такий спосіб запобігти розвитку подагри (клас рекомендації ІІb, рівень доказовості В).
- Як подагра, так і ГУ пов’язані з кардіометаболічними та нирковими супутніми патологіями. Рекомендовано виконувати регулярні фізичні вправи та кардіотренування (150‑300 хвилин на тиждень помірної інтенсивності) на додаток до контролю ваги та відповідної дієти (клас рекомендації ІІа, рівень доказовості В).
- Здорове харчування, зокрема дієтичні заходи для зменшення ризику гіпертензії (DASH), у поєднанні зі зниженням ваги (за наявності зайвої ваги / ожиріння) може мати позитивний вплив на захворюваність на подагру, підвищений рівень СК і кардіометаболічний ризик (клас рекомендації ІІb, рівень доказовості В).
- Червоне м’ясо, субпродукти та ковбасні вироби можуть підвищувати рівень СК і в такий спосіб збільшувати ризик розвитку подагри. Тому слід обмежити вживання червоного м’яса та пов’язаних із ним продуктів (щонайбільше двічі на тиждень) і лише в невеликих кількостях (клас рекомендації ІІb, рівень доказовості В).
- Морепродукти, особливо ракоподібні та мідії, можуть підвищити рівень СК і ризик подагри, тому їх слід вживати у помірних кількостях. Рибу рекомендовано вживати регулярно (щонайменше 1‑2 рази на тиждень) як частину здорової дієти, а також для запобігання ССЗ (клас рекомендації ІІІ, рівень доказовості В).
- Зловживання алкоголем (залежно від дози) також збільшує ризик розвитку подагри. Особливо слід уникати пива та міцних алкогольних напоїв, тоді як червоне вино має найменший потенціал для підвищення ризику подагри (клас рекомендації ІІа, рівень доказовості В).
- Солодкі безалкогольні напої, фруктові соки та продукти з високим вмістом фруктози (фруктовий цукор) можуть також підвищувати рівень СК, тому необхідно уникати їх вживання. Тоді як свіжі фрукти та «легкі напої» без фруктози не підвищують ризик подагри (клас рекомендації ІІІ, рівень доказовості В).
- Регулярне вживання молока / молочних продуктів (із низьким вмістом жиру) може знизити рівень СК, тому їх вживання рекомендовано всім пацієнтам із подагрою. (клас рекомендації Іb, рівень доказовості А).
- Регулярне вживання кави також може допомогти знизити рівень СК у поєднанні з правильною дієтою та ліками (клас рекомендації ІІb, рівень доказовості В).
- Плоди вишні, особливо сорту Монморансі, можуть допомогти знизити рівень СК. Однак досі не з’ясовано, у якій дозі різні продукти (сік, концентрат, екстракт) мають найбільший ефект (клас рекомендації ІІb, рівень доказовості В).
Було проведено дослідження впливу вживання вишні на ризик загострення подагри за участю 533 пацієнтів із рецидивною подагрою. Так, 224 (35%) пацієнти вживали тільки свіжі плоди вишні, 15 (2%) – екстракт вишні і 33, (5%) – плоди і екстракт. Вживання однієї склянки вишні протягом двох днів знижувало ризик нападу подагри на 35% порівняно з тими, хто не мав її у раціоні. Аналогічний ефект зафіксовано під час приймання екстракту вишні. Вплив вживання цих ягід утримувався незалежно від статі, ІМТ, вживання алкоголю та застосування діуретиків.
У пацієнтів, які поєднували вживання плодів вишні з антигіперукемічними засобами (алопуринол), ризик нападів подагри знижувався достовірно на 75%. Вживання близько 20 ягід (одна чашка) є тією дозою, яка може знизити ймовірність нападу подагри (Zhang et al., 2012).
В іншому дослідженні 18 жінок і 8 чоловіків, віком 41±11 років, ІМТ 31,3±6,0 (12 осіб мали ожиріння, 14 – зайву вагу) вживали терпкий вишневий сік по 8 унцій на день (240 мл) або плацебо протягом восьми тижнів (Martin and Coles, 2019).
Таке вживання вишневого соку допомогло зменшити концентрацію СК на 19,2% (p<0,05), рівень СРБ – на 19,4% (р=0,09) і рівень моноцитного хемоатрактантного білку‑1 – на 6,3% (p=0,08). За даними дослідження, вживання 100% терпкого вишневого соку зменшувало концентрацію СК, пом’якшуючи ГУ, пов’язану з подагричним артритом.
Узагальнені результати шести досліджень щодо впливу вживання плодів вишні на подагру вказують на кореляцію між прийманням її екстракту та згаданими захворюванням. Антоціани, які містяться у плодах вишні, пригнічують ключові ферменти запалення, як-от циклооксигенази- 1 і 2. Продемонстровано, що екстракт вишні зменшує рівні різних цитокінів, наприклад ІЛ‑1b, ФНПa, ІЛ‑6 та ІЛ‑17. Також вживання плодів вишні може зменшувати утворення прозапальних речовин, як-от NО і СРБ (Chen et al., 2019).
Ірина Юріївна зауважила, що при лікуванні пацієнтів із подагрою та ГУ важливо використовувати антиоксидантний, протизапальний і гіпоурикемічний ефекти ягід вишні (Collins et al., 2019).
Вживання плодів вишні та вишневого екстракту чинить вплив на блокування канальцевої реабсорбції уратів і збільшення їх екскреції із сечею, запобігаючи загостренням подагри. Також вживання вишневого соку може блокувати дію ксантинооксидази і зменшувати утворення СК.
У вишні, як і в інших червоних і пурпурових фруктах і овочах (червонокачанній капусті, буряках, чорниці, малині, фіолетовому винограді), міститься антиоксидантний пігмент антоціан, який має протизапальний ефект.
На фармринку України сьогодні представлений фітокомплекс Монморол, застосування якого сприяє зниженню рівня СК, зменшенню ризиків нападів подагри, збільшенню міжрецидивних періодів; чинить антиоксидантну дію, знижує запальну активність, має безпечний профіль, що дає змогу комбінувати його зі стандартною УЗТ, підсилюючи її дію (Schlesinger et al., 2012; Zhang et al., 2012; Bell et al., 2014; Jacob et al., 2003).
Монморол містить концентрований порошок терпкої вишні сорту Монморансі (1:50) CherryPure (440 мг) та сухий екстракт кори верби (45 мг) в одній капсулі. Монморол застововують як засіб комплементарної корекції подагри та ГУ при ССЗ, ЦД, МС, хворобах нирок.
Підсумовуючи, пацієнтові Х. було рекомендовано:
- Для втамування гострого чи затяжного нападу до НПЗП додати колхіцин (0,5 мг тричі на добу), щоб повністю усунути напад артриту, із подальшим зменшенням дози препарату (до 0,5 мг раз на добу протягом трьох місяців).
- Дотримуватись спеціальної дієти, яка допомагає тримати хворобу під контролем, ці заходи слід виконувати протягом усього життя.
- Утриматися від застосування УЗТ.
- Фітокомплекс Монморол (по 1 капсулі двічі на добу протягом трьох місяців).
- Контролювати рівень СК у міжрецедивний період.
- Комплекс Атеродінол (по 1 капсулі двічі на добу протягом трьох місяців).
- Контролювати показники ліпідограми в динаміці.
Підготувала Ірина Климась