20 вересня, 2024
Розувастатин: підтверджені переваги для різних груп пацієнтів
Атеросклеротичні серцево-судинні захворювання (АССЗ) – одна із провідних причин смерті у світі. Важливою стратегією профілактики АССЗ є оптимізація рівня холестерину (ХС) у крові за допомогою зміни способу життя та/або ліпідознижувальної терапії. Необхідність тривалого, а часто пожиттєвого приймання препаратів для зменшення вмісту ХС потребує ретельного дослідження всього комплексу їх ефектів, а також профілю безпеки й ризику медикаментозних взаємодій.
Визначення та епідеміологія
ХС – один із найбільш клінічно значущих ліпідів плазми крові, що утворюється переважно в результаті печінкового синтезу; від 15 до 20% ХС надходить з їжею. Синтез ХС de novo відбувається у багато етапів, і лімітуючим ферментом у цьому процесі є 3-гідрокси‑3-метилглутарил-коензим А редуктаза (ГМГ-КоА-редуктаза). ХС циркулює у гідрофобному ядрі сферичних ліпопротеїнових частинок, що складаються також із тригліцеридів (ТГ), фосфоліпідів та аполіпопротеїнів.
За функцією, розміром, щільністю, відносним вмістом ліпідів і визначальним для них аполіпопротеїном розрізняють хіломікрони, ХС ліпопротеїнів дуже низької щільності (ЛПДНЩ), ліпопротеїнів низької щільності (ЛПНЩ), ліпопротеїнів проміжної щільності, ліпопротеїнів (а) і ліпопротеїнів високої щільності (ЛПВЩ). Визначення розрахункового показника ХС не-ЛПВЩ (дорівнює загальному ХС мінус ХС ЛПВЩ) дозволяє оцінити всі фракції ліпідів крові, які беруть участь в утворенні атеросклеротичних бляшок в судинах. Це забезпечує точнішу оцінку ризику АССЗ в осіб із високим рівнем ТГ, цукровим діабетом (ЦД), ожирінням чи дуже низьким ХС ЛПНЩ (ESC/EAS, 2019).
Надмірна кількість частинок ХС ЛПНЩ і ЛПДНЩ, особливо після окислення, стимулює в артеріальній стінці синтез молекул адгезії та запальних цитокінів, а також може ініціювати Т-опосередковану імунну відповідь і запалення. При розриві бляшки ймовірне виникнення оклюзивної судинної події, що призводить до інфаркту міокарда (ІМ), інсульту або ішемії нижніх кінцівок (Lusis, 2000). Основним фактором ризику розвитку АССЗ є концентрація атерогенних ліпопротеїнів, яку найкраще відображає концентрація аполіпопротеїну B або не-ЛПВЩ.
Епідеміологія гіперхолестеринемії та загалом дисліпідемій залежить від регіону, віку, статі й етнічної належності, на неї також впливають генетичні та екологічні фактори (Pirillo al., 2021). Згідно з даними Всесвітньої організації охорони здоров’я (ВООЗ), у 2008 р. глобальна поширеність підвищеного загального ХС серед дорослого населення становила 39% (37% для чоловіків і 40% для жінок). Поширеність дисліпідемії серед дітей та підлітків зростає, особливо у розвинених країнах, через збільшення кількості випадків ожиріння, малорухливого способу життя та нездорового харчування (Xia et al., 2023; Pappan et al., 2024).
За оцінками, підвищений рівень ХС є причиною 2,6 млн смертей у світі (4,5% від загальної кількості). У 2017 р. великий вміст ХС не-ЛПВЩ був причиною приблизно 3,9 млн летальних випадків у світі від ішемічної хвороби серця (ІХС) та ішемічного інсульту, що становить третину смертей із цих причин (NCD Risk Factor Collaboration, 2020).
Стратегія терапії гіперхолестеринемії
В усіх сучасних настановах щодо профілактики АССЗ йдеться про необхідність визначення загального серцево-судинного (СС) ризику. Що вищий показник, то інтенсивнішими мають бути профілактичні заходи, зокрема, спрямовані на модифікацію ліпідних факторів.
Особи із документованим АССЗ, ЦД 1-го та 2-го типу, дуже високим рівнем індивідуальних чинників ризику або хронічною хворобою нирок (ХХН) мають високий та дуже високий рівень СС-ризику. Ці категорії пацієнтів потребують активної корекції всіх факторів ризику. Для інших хворих може бути використана система SCORE, яка дозволяє врахувати декілька наявних чинників ризику і визначити кумулятивну ймовірність виникнення першої атеросклеротичної події протягом наступних 10 років життя з оцінкою загального СС-ризику (ESC/EAS, 2019).
На додаток, за допомогою SCORE є нагода оцінити 10-річний ризик фатальних ССЗ на основі різних факторів, як-от вік, стать, куріння, систолічний артеріальний тиск та показник загального ХС. Отриманий результат дозволяє також визначити загальну ймовірність розвитку фатальних і нефатальних СС-подій.
У 2021 р. з’явилися два нових алгоритми, які можуть бути використані для визначення стратегії втручання з метою зниження ризику АССЗ (доступні за посиланням: www.heartscore.org):
- SCORE2 – модель для оцінки 10-річного ризику виникнення СС-подій в Європі;
- SCORE2-OP – модель для оцінки ризику виникнення СС-подій в осіб похилого віку в чотирьох географічних регіонах.
- За результатами оцінки загальний рівень СС-ризику в пацієнта визначається як дуже високий, високий, помірний або низький.
Стратегія лікування дисліпідемій передбачає корекцію загального СС-ризику та рівня ХС ЛПНЩ (ESC/EAS, 2019). Вона включає немедикаментозні методи, як-от дієта з низьким вмістом насичених жирів, корекція маси тіла, підвищення фізичної активності, припинення куріння, та медикаментозні, серед яких застосування статинів, езетимібу, інгібіторів пропротеїнової конвертази субтилізин-кексинового типу 9 (PCSK9). Пацієнт має бути обов’язково залучений у прийняття рішень щодо зниження СС-ризику.
Терапевтичні цілі лікування щодо рівня ХС ЛПНЩ і не-ЛПВЩ наведені в таблиці 1 (ESC/EAS, 2019).
Лікарськими засобами 1-ї лінії в терапії дисліпідемій є статини. Вони знижують синтез ХС у печінці за рахунок конкурентного інгібування ферменту ГМГ-КoA-редуктази.
|
Таблиця 1. Терапевтичні цілі лікування щодо рівня ХС ЛПНЩ і не-ЛПВЩ |
||
|
Рівень ризику |
Цільовий рівень ХС ЛПНЩ |
Цільовий рівень ХС не-ЛПВЩ |
|
Дуже високий |
<1,4 ммоль/л |
<2,2 ммоль/л |
|
Високий |
<1,8 ммоль/л |
<2,6 ммоль/л |
|
Помірний |
<2,6 ммоль/л |
<3,4 ммоль/л |
|
Низький |
<3,0 ммоль/л |
<3,8 ммоль/л |
Серед ефектів статинів варто відзначити (Davignon J., 2004):
- Основні – зниження рівнів ХС, ХС ЛПНЩ, ТГ.
- Додаткові (плейотропні) – стабілізація атеросклеротичної бляшки, протизапальна, антитромботична, антиоксидантна та імуномодулювальна дія, здатність до підвищення еластичності артерій та поліпшення ендотеліальної функції.
До плейотропних ефектів статинів відносять такі, що пов’язані з блокадою активності ферменту ГМГ-КоА-редуктази, але не безпосередньо зі зниженням рівня ХС ЛПНЩ.
Статини ефективні для первинної та вторинної профілактики АССЗ. У метааналізі 26 рандомізованих контрольованих досліджень впливу статинів за участю більш ніж 170 тис. осіб було показано, що зниження на 1 ммоль/л показника ХС ЛПНЩ зменшувало кількість великих судинних подій (як-то ІМ, смерть від ІХС, будь-який інсульт або коронарна реваскуляризація) приблизно на 22%, великих коронарних подій – на 23%, смерті від ІХС – на 20%, загалом інсульту – на 17% та загальну летальність – на 10% протягом п’яти років (Cholesterol Treatment Trialists Collaboration, 2010).
Високоінтенсивна терапія статинами у максимально переносимій дозі рекомендована для досягнення цільових рівнів ХС ЛПНЩ залежно від ступеня СС-ризику (ESC/EAS, 2019). Якщо при цьому не вдається досягти цільового значення ХС ЛПНЩ, пацієнту доцільно призначити комбінацію статину з інгібітором абсорбції ХС езетимібом. Якщо терапія статинами не переноситься за будь-якого дозування (навіть після повторного приймання), може бути розглянутий езетиміб.
Слід зазначити, що інтенсивність статинотерапії визначається відсотком зниження рівня ХС ЛПНЩ для конкретного статину і дози (табл. 2). Розрахунок проводили за результатами метааналізу даних 26 рандомізованих клінічних досліджень (РКД) із залученням 170 тис. пацієнтів (Cholesterol Treatment Trialists, 2010).
|
Таблиця 2. Статинотерапія високої, середньої та низької інтенсивності |
||
|
Статин високої інтенсивності |
Статин середньої інтенсивності |
Статин низької інтенсивності |
|
Аторвастатин, 40‑80 мг Розувастатин, 20‑40 мг |
Аторвастатин, 10‑20 мг Розувастатин, 5‑10 мг Симвастатин, 20‑40 мг Пітавастатин, 2‑4 мг |
Симвастатин, 10 мг Пітавастатин, 1 мг |
Переваги розувастатину
Одним із найефективніших статинів щодо зниження рівня ХС ЛПНЩ вже понад 20 років залишається розувастатин (Adams et al., 2014). Переваги препарату зумовлені його фармакологічними і фармакокінетичними властивостями. Розувастатин – це синтетична сполука, що має вищу афінність до активного центру ферменту ГМГ-КоА-редуктаза, ніж інші представники даної групи препаратів (Rubba et al., 2009). Гідрофільність розувастатину забезпечує його вищу селективність стосовно гепатоцитів, ніж інших тканин (зокрема м’язової), що потенційно може знижувати частоту побічних реакцій (ПР).
Серед усіх статинів розувастатин має найдовший період напіввиведення (19 год). До того ж це єдиний статин, який метаболізується переважно через ізоформи CYP 2С9 і CYP 2С19 цитохрому Р450 із мінімальним залученням ізоформи 3А4, за участю якої метаболізується значна кількість ліків. У результаті в розувастатину відсутні клінічно значущі медикаментозні взаємодії (McKenney, 2005). Фармакокінетичні особливості розувастатину не залежать від віку, статі чи наявності помірно вираженої печінкової недостатності. Препарат можна приймати у будь-який час доби, незалежно від вживання їжі, що сприяє прихильності пацієнта до лікування.
Клінічні переваги розувастатину для різних популяцій пацієнтів були доведені в численних РКД, серед яких:
- STELLAR (порівняння гіполіпідемічної ефективності розувастатину та інших статинів);
- JUPITER (ефективність розувастатину в первинній профілактиці АССЗ);
- MERCURY II (порівняльна ефективність розувастатину та інших статинів у досягненні знижених цільових рівнів ХС ЛПНЩ);
- METEOR (ефективність розувастатину в осіб із низьким ризиком ССЗ);
- VOYAGER (порівняльна ефективність розувастатину та інших статинів у зниженні рівня тригліцеридів);
- ASTEROID (здатність розувастатину забезпечувати зворотний розвиток атеросклерозу);
- CORONA (безпека застосування розувастатину в пацієнтів із серцевою недостатністю).
Згідно з результатами дослідження STELLAR, розувастатин у дозі 10‑40 мг за шість тижнів лікування знижував рівень ХС ЛПНЩ на 46‑55% порівняно з 37‑51%, 28‑39% і 20‑30% при застосуванні аторвастатину (10‑80 мг), симвастатину (10‑40 мг) та правастатину (10‑40 мг) відповідно. Також розувастатин підвищував показник ХС ЛПВЩ на 8‑10% (порівняно із 2‑6%, 5% і 3‑6% відповідно) і знижував вміст ТГ на 20‑26% (порівняно із 20‑28%, 12‑15% і 8‑13% відповідно) (Jones et al., 2003). Отримані результати були підтверджені у дослідженні VOYAGER – об’єднаному метааналізі на основі даних 32 258 пацієнтів (Nicholls et al., 2010), а також у великих метааналізах X. Zhang еt al. (2020) і M. Jaam et al. (2023).
Що стосується профілю безпеки, згідно з результатами РКД, частота ПР під час застосування високоінтенсивних статинів є подібною і дозозалежною (Brewer et al., 2003). Проте важливо зауважити, що дослідження у реальному житті демонструють дещо інший результат, а саме нижчий ризик виникнення ПР при застосуванні розувастатину порівняно з аторвастатином, при цьому дозозалежність не завжди має місце (Stein еt al., 2020).
У ретроспективному когортному дослідженні порівнювали пацієнтів, які отримували 20‑40 мг розувастатину із січня 2009 р. по листопад 2011 р. (n=4165) та 40‑80 мг аторвастатину і з травня 2012 р. по червень 2016 р. (n=5852). Між групами аторвастатину та розувастатину було виявлено різницю у загальних ПР (4,59 vs 2,91%; відносний ризик [ВР] 1,61; р<0,05). Також статистично значущі відмінності спостерігалися щодо печінкової токсичності, маркером якої було підвищення рівня аланінамінотрансферази (АЛТ) утричі від верхньої межі норми (ВМН) – 3,99% аторвастатину та 1,39% розувастатину (ВР 2,95; р<0,05). Також статистично значиму різницю було зареєстровано щодо статин-асоційованих міопатій, маркером яких було підвищення рівня креатинфосфокінази (КФК) >10ЧВМН (1,14% аторвастатину та 0,5% розувастатину; ВР 2,29; р<0,05).
Порівняння частоти виникнення будь-яких ПР, печінкових (АЛТ >3ЧВМН), м’язових порушень (КФК >10ЧВМН) і статин-асоційованих м’язових симптомів (САМС), які включали міалгію та/або підвищення рівня КФК, при застосуванні розувастатину й аторвастатину в різних дозах наведене на рисунку 1. Аналіз підгруп не виявив різниці у показниках ПР між 40 мг аторвастатину та 20 мг розувастатину. Однак у пацієнтів, які отримували 40 мг аторвастатину, мали місце вищі показники АЛТ і САМС порівняно із групою 20 мг розувастатину. Аналогічно, у хворих на лікуванні 80 мг аторвастатину була вища частота виникнення ПР, підвищення рівня АЛТ та САМС порівняно із групою 40 мг розувастатину.
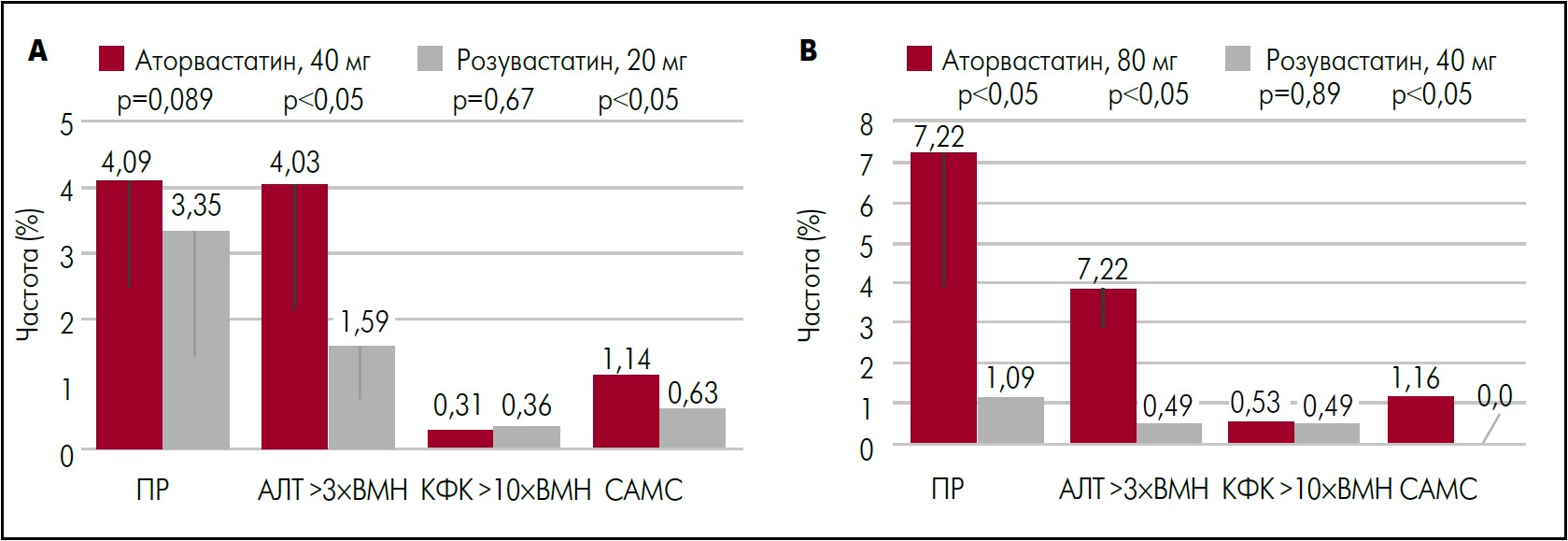
Рис. 1. Частота побічних реакцій, що виникли на тлі застосування аторвастатину і розувастатину в різних дозах
Адаптовано за Stein et al. (2020)
Протизапальні властивості
Плейотропні ефекти розувастатину заслуговують на особливу увагу, адже можуть забезпечувати комплексну профілактику ССЗ та позитивно впливати на прогноз пацієнта.
Так, важливі переваги розувастатину були підтверджені у клінічному дослідженні JUPITER (Ridker et al., 2009). Приводом до дослідження став той факт, що певна частка ІМ та інсультів трапляються у здорових осіб із середнім або низьким рівнем ХС ЛПНЩ (<3,4 ммоль/л), тобто серед тих, хто формально не має показань для статинотерапії. Отже необхідним є встановлення інших факторів з метою оцінки та мішеней для корекції СС-ризику. Зокрема, важливим фактором атерогенезу може виступати запалення, а його маркером – високочутливий С-реактивний білок (вчСРБ), що може незалежно прогнозувати судинні події.
У дослідженні JUPITER було перевірено, чи є статинотерапія ефективною для запобігання першим СС-подіям в осіб, які за рівнем ХС ЛПНЩ не є кандидатами для отримання лікування статинами, але мають підвищений рівень вчСРБ. До участі були залучені 17 802 чоловіків і жінок із 26 країн без встановлених ССЗ, які мали підвищений вміст вчСРБ >2 мг/л та середній або низький ХС ЛПНЩ (<3,4 ммоль/л). Вони були випадковим чином розподілені на дві групи: для отримання розувастатину в дозі 20 мг та плацебо.
Випробування було достроково припинене після середнього періоду спостереження 1,9 року (максимальний становив 5 років) через отримання цілком переконливих даних:
- зниження частоти всіх СС-подій на 44% (р<0,00001);
- зниження частоти ІМ на 54% (р=0,0002);
- зниження частоти інсульту на 48% (р=0,002);
- зменшення потреби в артеріальній реваскуляризації на 46% (р<0,001);
- зниження смертності від усіх причин – на 20% (р=0,02).
У дослідженні JUPITER користь від застосування розувастатину отримали всі попередньо визначені підгрупи учасників, зокрема особи групи низького ризику, жінки, пацієнти з індексом маси тіла <25 кг/м2, без метаболічного синдрому, які не курять, не страждають на артеріальну гіпертензію, а також ті, хто за фремінгемською шкалою мають СС-ризик <10%.
Висока ефективність розувастатину спостерігалася у 6375 осіб із підвищеним рівнем вчСРБ, але без інших факторів СС-ризику. Зокрема, під час дослідження мало місце зниження показника вчСРБ на 37%, що підтверджує протизапальні властивості розувастатину. В різних підгрупах результати були незмінними і не залежали від віку, статі, вихідного СС-ризику, а також наявності ЦД або ХХН, що свідчить про переваги розувастатину в усій категорії пацієнтів із дисліпідемією (Koenig еt al., 2011; Ridker et al., 2012).
Вплив на ризик тромбоемболій
Плейотропні ефекти розувастатину, зокрема протизапальний та антикоагулянтний, забезпечують зниження ризику венозної тромбоемболії (ВТЕ), яка включає тромбоемболію легеневої артерії та тромбоз глибоких вен. Тривалий час відкритим залишалося питання, чи мають артеріальний і венозний тромбоз спільні шляхи розвитку, а також чи є лікування, ефективне стосовно одного патологічного процесу, корисним щодо іншого. Пізніше в низці досліджень та метааналізів було достовірно підтверджено, що статини здатні знижувати ризик венозного тромбозу (Agarwal et al., 2020; Kunutsor et al., 2017).
Нещодавно було опубліковано дані метааналізу, що включав не лише плацебо-контрольовані випробування, але й такі з активними речовинами порівняння. У дослідженнях вивчали, які саме гіполіпідемічні препарати (розглядалися різні статини та фібрати) є ефективнішими щодо зниження ризику ВТЕ (Birdal et al., 2023).
Метааналіз включав 28 РКД, що загалом охоплювали 137 тис. пацієнтів. Парний метааналіз виявив статистично значуще нижчу частоту ВТЕ при застосуванні статинів, ніж плацебо (0,79 та 0,99% відповідно; ВР 0,87; 0,77‑0,98; р=0,022). Проте гіполіпідемічні засоби по-різному впливали на ризик ВТЕ. Зокрема, розувастатин виявився найкращим вибором для зниження ризику ВТЕ порівняно із плацебо (ВР 0,56; 0,42‑0,75), аторвастатином (ВР 0,64; 0,44‑0,95), правастатином (ВР 0,50; 0,34‑0,74), симвастатином (ВР 0,60; 0,42‑0,86) і фенофібратом (ВР 0,37; 0,25‑0,56).
Отже, зниження ризику ВТЕ на тлі статинотерапії було переважно асоційоване із застосуванням розувастатину. Інші статини продемонстрували вплив на ймовірність ВТЕ, зіставний із таким плацебо. Своєю чергою фенофібрат корелював із підвищенням ризику ВТЕ порівняно із плацебо та статинами. Варто підкреслити наступні отримані висновки: розувастатин порівняно із плацебо знижував ризик ВТЕ приблизно на 45%, а фенофібрат підвищував ризик ВТЕ на 65%.
Профіль користь/ризик
Розувастатин у дозі 10‑40 мг знижує рівень ХС ЛПНЩ та забезпечує досягнення цільового показника ХС ЛПНЩ, а також поліпшує низку важливих ліпідних показників, зокрема рівні ХС ЛПВЩ, ТГ, загального ХС, ХС не-ЛПВЩ, аполіпопротеїну B, а також співвідношення атерогенних і неатерогенних ліпопротеїнів. Аналіз у підгрупах підтверджує ефективність 10‑40 мг розувастатину в пацієнтів, визначених за віком (≥65 років), статтю (жінки), постменопаузальним статусом, артеріальною гіпертензією, атеросклеротичним захворюванням, ЦД та ожирінням (індекс маси тіла ≥30).
Що стосується потенційного несприятливого впливу статинів на функцію м’язів і печінки, було проаналізовано оцінку користі й ризику лікування статинами, а саме частоту підвищення АЛТ >3ЧВМН і КФК >10ЧВМН зіставлено з відсотком зниження рівня ХС ЛПНЩ для різних статинів залежно від дози (рис. 2) (Brewer Jr., 2003).
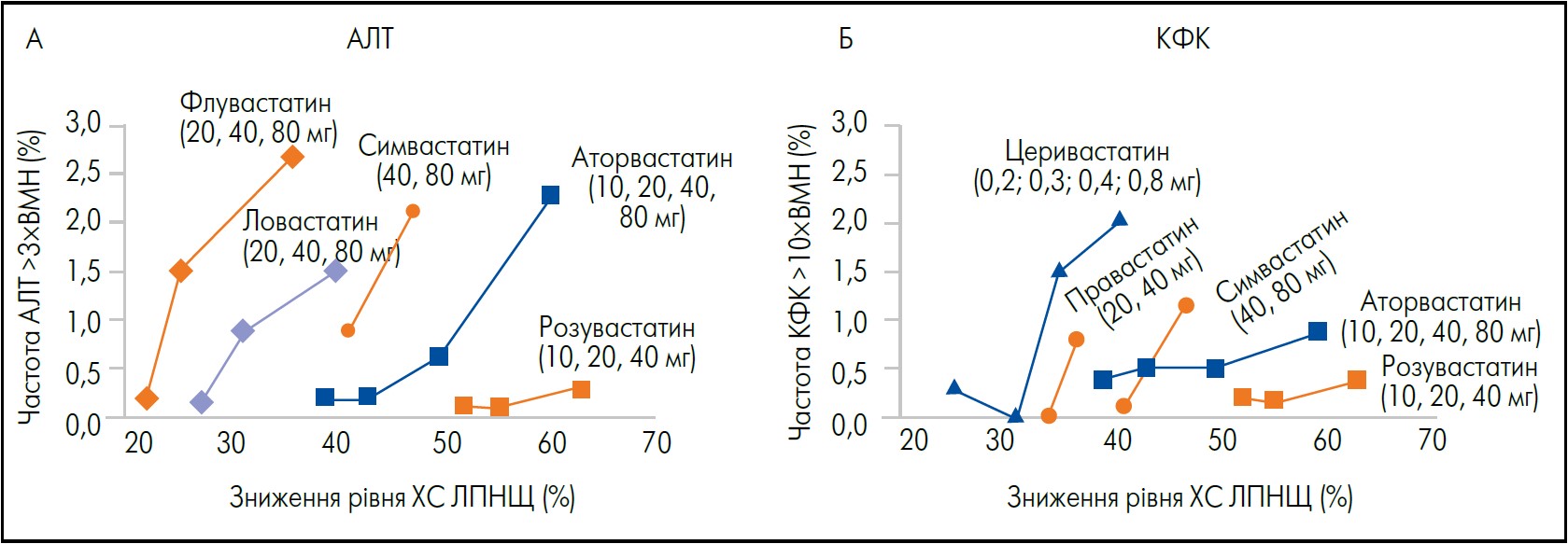
Рис. 2. Сприятливий профіль користі та ризику розувастатину порівняно з іншими статинами відповідно до зниження ХС ЛПНЩ та частоти підвищення АЛТ і КФК
Адаптовано за Brewer Jr. (2003)
За отриманими даними, рівні КФК або АЛТ зростали із більшим зниженням ХС ЛПНЩ при підвищенні доз аторвастатину і симвастатину. У пацієнтів, які отримували 10‑40 мг розувастатину, частота підвищення КФК або АЛТ зі зростанням ліпідознижувального ефекту залишалася низькою, з мінімальними змінами на тлі збільшенні дози. Так, міопатія внаслідок приймання розувастатину в дозі 10‑40 мг спостерігалася у ≤0,03% пацієнтів. Ці дані свідчать про дуже сприятливий профіль користь/ризик у всьому діапазоні доз розувастатину (Brewer Jr., 2003).
Порівняльна користь розувастатину та дієтичних добавок
Щорічно у світі продажі дієтичних добавок (ДД) сягають десятків мільярдів доларів, і багато ДД позиціонуються як засоби для зниження рівня ХС та профілактики АССЗ. Але справа в тому, що до реклами ДД не висуваються такі суворі вимоги, як до такої ліків, і вона часто містить недоказові дані. Зокрема, реклама ДД нерідко заявляє, що вони не поступаються статинам за ефективністю, але переважають за безпекою. Як наслідок, пацієнти можуть самостійно замінювати призначені статини на ДД, що становить серйозну проблему для охорони здоров’я.
Для отримання доказових даних щодо ефективності поширених ДД порівняно зі статинами у низьких дозах було проведене одноцентрове проспективне рандомізоване сліпе клінічне дослідження SPORT (Laffin et al., 2023). Первинною кінцевою точкою виступала відсоткова зміна рівня ХС ЛПНЩ при застосуванні розувастатину в дозі 5 мг/добу порівняно із плацебо та низкою ДД, як-от риб’ячий жир, кориця, часник, куркума, рослинні стероли та червоний дріжджовий рис. Вторинні кінцеві точки включали зміну рівня вчСРБ, ХС ЛПВЩ, загального ХС та ТГ у сироватці крові для кожної досліджуваної групи порівняно з розувастатином.
В учасників (199 осіб віком 40‑75 років) рівень ХС ЛПНЩ становив 70‑189 мг/дл (1,8‑4,9 ммоль/л), вони не мали в анамнезі АССЗ, до початку дослідження не приймали статини або інші ліпідознижувальні препарати, а також жодної з досліджуваних ДД. Для осіб без ЦД в анамнезі 10-річний ризик АССЗ був 5‑20%. Пацієнти із ЦД і ризиком <20% могли бути включені у дослідження, якщо були віком 40‑50 років (чоловіки) або 50‑60 років (жінки).
Згідно із результатами дослідження, розувастатин у низькій дозі забезпечував суттєвіше зниження ХС ЛПНЩ порівняно із плацебо, риб’ячим жиром, корицею, часником, куркумою, рослинними стеролами та червоним дріжджовим рисом (рисунок). Жодна із ДД не продемонструвала достовірного зниження ХС ЛПНЩ. На відміну від плацебо та ДД, на тлі приймання низьких доз розувастатину спостерігалося поліпшення інших ліпідних біомаркерів, а саме загального ХС та ТГ. Небажані явища були мінімальними в усіх групах.
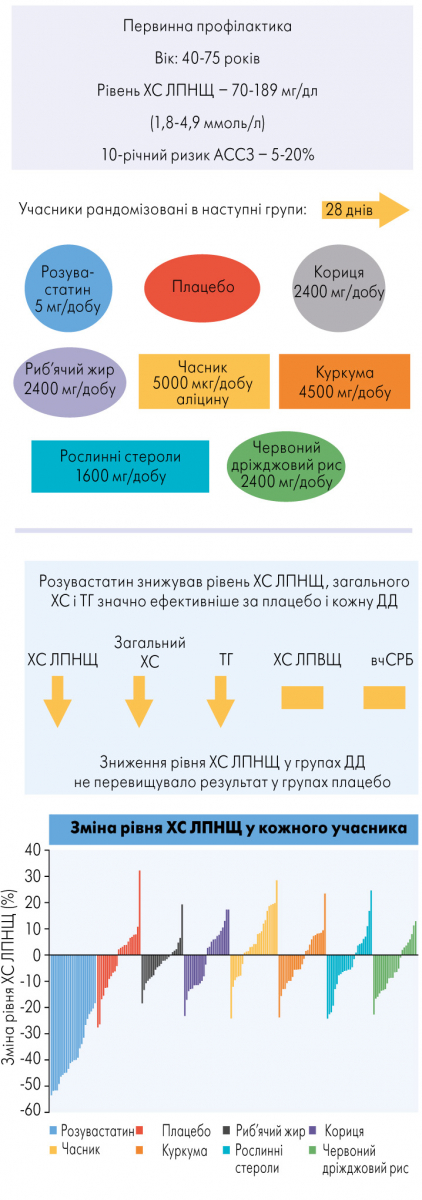
Рисунок. Зміна рівня ХС ЛПНЩ в учасників дослідження SPORT
Адаптовано за Laffin et al. (2023)
Таким чином, були отримані докази того, що певні ДД, які рекламуються як засоби для зниження ХС, достовірно не зменшують ХС ЛПНЩ порівняно із плацебо і поступаються за ефективністю статинам. Ці дані також демонструють очікуване поліпшення інших ліпідних біомаркерів при застосуванні низьких доз розувастатину, але не виявляють різниці для ДД порівняно із плацебо.
Сьогодні на фармринку України розувастатин доступний у вигляді препарату Розуліп® (фармацевтичний завод «Егіс», Угорщина) та представлений у найчастіше застосовуваних дозах 10 і 20 мг. Також у цій лінійці препаратів наявний Розуліп® Плюс – комбінація 10 або 20 мг розувастатину із 10 мг езетимібу. Наявність різних доз розувастатину та підсиленої езетимібом гіполіпідемічної комбінації надає лікареві можливість обрати оптимальну для кожного пацієнта інтенсивність ліпідознижувальної терапії.
Підготувала Тетяна Ткаченко
Тематичний номер «Кардіологія. Ревматологія. Кардіохірургія» № 4 (95) 2024 р.


