5 серпня, 2024
Рекомендації IWGDF/IDSA щодо діагностики і лікування інфекцій стопи, пов’язаних із цукровим діабетом (2023)
 Поширеність діабету продовжує зростати. За оцінками Міжнародного фонду цукрового діабету, у 2021 р. у світі з діабетом жило 537 млн дорослих віком від 20 до 79 років [1]. Це зумовлює зростання частоти виникнення ускладнень із боку стопи, у тому числі інфекцій [1]. Діабет-асоційовані інфекції стопи (ДІС) пов’язані з високою захворюваністю, що потребує частих візитів до лікаря, щоденного догляду за ранами, застосування антимікробних препаратів, виконання хірургічних утручань, а також значних витрат на охорону здоров’я [2]. Особливо важливо те, що ДІС лишаються найчастішим ускладненням діабету, що потребує госпіталізації пацієнтів, та найчастішою причиною ампутації нижніх кінцівок [3, 4].
Поширеність діабету продовжує зростати. За оцінками Міжнародного фонду цукрового діабету, у 2021 р. у світі з діабетом жило 537 млн дорослих віком від 20 до 79 років [1]. Це зумовлює зростання частоти виникнення ускладнень із боку стопи, у тому числі інфекцій [1]. Діабет-асоційовані інфекції стопи (ДІС) пов’язані з високою захворюваністю, що потребує частих візитів до лікаря, щоденного догляду за ранами, застосування антимікробних препаратів, виконання хірургічних утручань, а також значних витрат на охорону здоров’я [2]. Особливо важливо те, що ДІС лишаються найчастішим ускладненням діабету, що потребує госпіталізації пацієнтів, та найчастішою причиною ампутації нижніх кінцівок [3, 4].
Є кілька настанов, мета яких – допомогти клініцистам у лікуванні ДІС. У 2004 р. IDSA (Іnfectious Diseases Society of America – Американське товариство фахівців з інфекційних хвороб) опубліковало рекомендації, оновлені у 2012-му [10, 11]. Група експертів, скликана IWGDF (International Working Group on the Diabetic Foot – Міжнародна робоча група з діабетичної стопи), починаючи з 2004 року кожні чотири роки публікує широко використовувані рекомендації [12]. Нинішнє видання 2023 року рекомендацій IWGDF щодо лікування ДІС являє собою новий перегляд видання 2019 року про діагностику й лікування ДІС та є частиною вищезазначеного гайдлайну [13]. IWGDF і IDSA погодилися створити спільні рекомендації з діагностики і лікування ДІС; у результаті до групи експертів, що брала участь у створенні нової версії, уперше увійшли члени як IWGDF, так і IDSA, які працювали над створенням єдиного документу.
В одному великому проспективному дослідженні результати лікування пацієнтів з інфікованою діабетичною виразкою стопи (ДВС) наприкінці 1-го року були субоптимальними: виразка загоїлася лише в 46% (і пізніше у 10% із них рецидивувала), тоді як 15% пацієнтів померли, а 17% було призначено ампутацію нижньої кінцівки [5].
Ведення ДІС потребує пильної уваги, щоб правильно діагностувати стан, отримати відповідні зразки для посіву, обмірковано підібрати антимікробну терапію, швидко визначити, коли потрібне оперативне втручання, і забезпечити будь-який необхідний додатковий догляд за раною та загальний догляд за пацієнтом.
Систематичний, заснований на доказах підхід до лікування ДІС, імовірно, поліпшує результати лікування, зокрема забезпечує розрішення складних випадків інфекції та допомагає уникнути ускладнень, таких як небезпечні для життя інфекції та втрата кінцівки. Найкраще це роблять міждисциплінарні групи, у складі яких, якщо можливо, мають бути спеціалісти з інфекційних хвороб або клінічні/медичні мікробіологи [6], аби забезпечити оптимальний місцевий догляд за раною (наприклад, очищення та обробка), зменшення навантаження на кінцівку, оцінку стану периферичних судин (із проведенням реваскуляризації, якщо необхідно) і метаболічний контроль (зокрема, контроль глікемії).
Загальна інформація
Інфекції шкіри і м’яких тканин стопи в пацієнтів із цукровим діабетом (ЦД) найчастіше виникають унаслідок порушення цілісності шкіри. Найпоширенішим таким порушенням цілісності шкірного бар’єра є ДВС, яка охоплює щонайменше епідерміс і частину дерми. Це ускладнення найчастіше виникає в пацієнтів із периферичною нейропатією та часто – у пацієнтів із захворюваннями периферичних артерій (ЗПА) [14]. Інфекційний процес виникає як наслідок колонізації рани різноманітною мікрофлорою. Колонізація рани бактеріями є постійним явищем, яке визначається наявністю бактерій на поверхні рани за відсутності доказів інвазії в тканини хазяїна. Ранова інфекція – це патологічний стан, спричинений інвазією та розмноженням мікроорганізмів у тканинах хазяїна, що спричинює запальну реакцію, яка зазвичай супроводжується ушкодженням тканин. Оскільки всі рани колонізовані (часто потенційно патогенними мікроорганізмами), ранову інфекцію неможливо діагностувати лише за допомогою результатів посіву рани. Натомість діагноз ДІС встановлюють клінічно за наявності ознак запального процесу із залученням рани стопи, розташованої нижче щиколотки. Проте в осіб із діабетичними ускладненнями з боку стопи ознаки і симптоми запалення можуть маскуватися внаслідок периферичної нейропатії, ЗПА або імунної дисфункції. Хворий з ускладненнями ЦД може потребувати ампутації нижньої кінцівки для контролю інфекції, або в нього може розвинутися поліорганна недостатність без місцевих клінічних проявів ДІС, але таке ускладення виникає вкрай рідко. Хоча ЗПА нечасто виступають основною причиною виразок стопи, їх наявність підвищує ризик інфікування виразки [4, 15-17] і погіршує прогноз інфекції [4, 18, 19]. Оскільки поєднання інфекції і ЗПА асоціюється зі значно вищим ризиком поганого загоєння та ампутації, лікарі мусять якомога раніше оцінювати стан перфузії рани та потенційну потребу в проведенні реваскуляризації в усіх пацієнтів із ДІС [7].
Факторами, що сприяють інфікуванню стопи, є наявність глибокої давньої рецидивної рани або рани травматичної етіології; наявність діабет-асоційованих імунологічних порушень, зокрема дисфункції нейтрофілів; супутньої хронічної ниркової недостатності [16, 18-23]. Хоча хронічна гіперглікемія як чинник, що сприяє розвитку ДІС, вивчалася лише в кількох дослідженнях, відомо, що вона може провокувати розвиток ДІС; крім того, наявність гіперглікемії при первинному зверненні по медичну допомогу може свідчити про швидко прогресуючу або деструктивну (некротичну) інфекцію [24, 25].
Незважаючи на те що більшість випадків ДІС під час первинного звернення по медичну допомогу є відносно неглибокими, мікроорганізми можуть безперервно поширюватися на підшкірні тканини, зокрема фасції, сухожилля, м’язи, суглоби та кістки. Анатомія стопи, яка розділена на кілька окремих, але сполучених відділів, сприяє поширенню інфекції в проксимальному напрямі [26]. Запальна реакція, спричинена інфекцією, може призвести до того, що тиск у відділі перевищить капілярний тиск, а це призведе до ішемічного некрозу тканин ураженого відділу і, таким чином, до прогресування інфекції [27, 28]. Сухожилля в межах відділу сприяють поширенню інфекції в проксимальному напрямі, яке зазвичай відбувається від ділянок із вищим тиском до ділянок із нижчим тиском. Фактори вірулентності бактерій також можуть відігравати певну роль у цих складних інфекційних процесах [29, 30]. Системні симптоми (наприклад, гарячка або озноб), виражений лейкоцитоз або серйозні метаболічні порушення в пацієнтів із ДІС спостерігаються рідко, але їх наявність свідчить про більш серйозну, потенційно небезпечну для кінцівок (або навіть небезпечну для життя) інфекцію [4, 31, 32]. Якщо вчасно не діагностувати та не розпочати належне лікування, ДІС мають тенденцію прогресувати, іноді дуже швидко [33]. Таким чином, пацієнта з тяжкими ДІС упродовж 24 год має оглянути досвідчений спеціаліст (або команда) з досвідом лікування інфекційних захворювань [34]. Скупчення гнійних виділень, особливо під тиском або з некрозом, потребує негайної (зазвичай протягом 24 год) хірургічної декомпресії та дренування. Хоча для успішного лікування остеомієліту може знадобитися резекція кістки і/або суглоба (переважно з використанням консервативного підходу, з обмеженою резекцією та уникненням ампутації, якщо це можливо), як правило, така інфекція м’яких тканин потребує термінового початку антимікробної терапії та хірургічного втручання.
Цей документ має на меті надати вичерпний, заснований на доказах огляд рекомендацій із діагностики і лікування інфекції стопи в осіб із ЦД. Наведені рекомендації призначені для практичного використання лікарями-клініцистами на основі всіх доступних наукових доказів.
Рекомендації
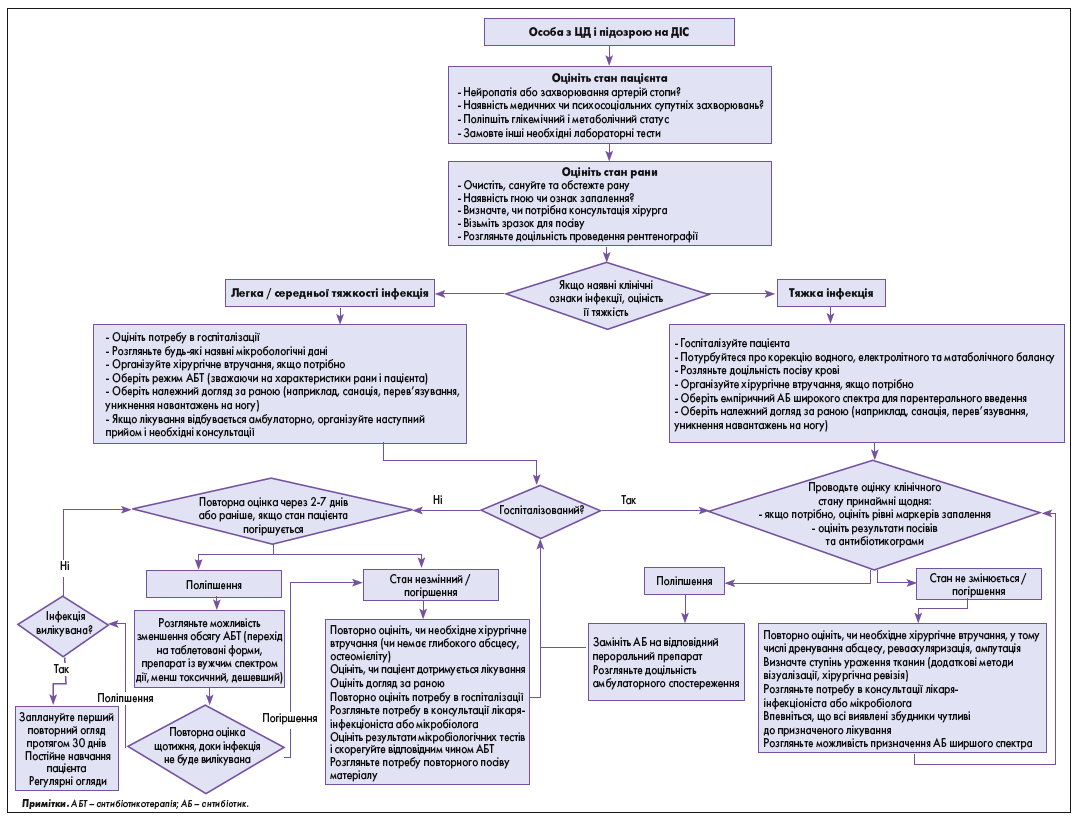
На рисунку наведено загальну схему діагностики і лікування пацієнтів із ДІС, у тому числі діабет-асоційованим остеомієлітом стопи (ДОС).
Рис. Схема діагностики і лікування пацієнтів із ДІС (Lipsky et al. DMRR2019). Виконайте неінвазивний тест для діагностики ЗПА
Діагностика
Клінічне запитання
Чи дає можливість класифікація IWGDF/IDSA передбачити прогноз захворювання?
Рекомендація 1.
(a) Діагностика діабет-асоційованих інфекцій м’яких тканин ґрунтується на наявності місцевих або системних клінічних ознак і симптомів запалення. (Сильна рекомендація; низька достовірність доказів.)
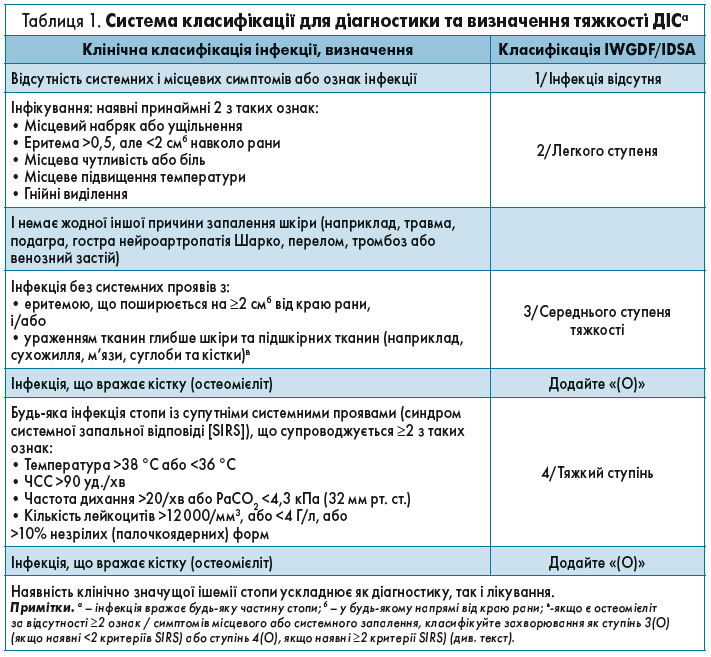
(b) Для оцінки ступеня тяжкості ДІС рекомендовано використовувати класифікаційну схему IWGDF/IDSA. (Сильна; низька.)
Обґрунтування. Клініцист, який приймає пацієнта з ЦД і виразкою стопи, завжди має перевіряти наявність інфекції і, якщо вона є, визначати ступінь її тяжкості [42, 43]. Експерти запропонували багато класифікаційних схем ДВС, багато з яких ураховують лише наявність або відсутність «інфекції» [9]. Попередні проспективні і ретроспективні дослідження повністю або частково підтвердили класифікацію ДІС IWGDF/IDSA як частину більшої Системи класифікації діабетичних захворювань стоп (PEDIS) (табл. 1) [4, 15]. Для тяжкої інфекції були розроблені інші класифікації, наприклад National Early Warning Score (Національна шкала раннього запобігання) [44, 45] або швидка динамічна оцінка органної недостатності [46], з метою виявлення пацієнтів із сепсисом або прогнозування результатів їх лікування.
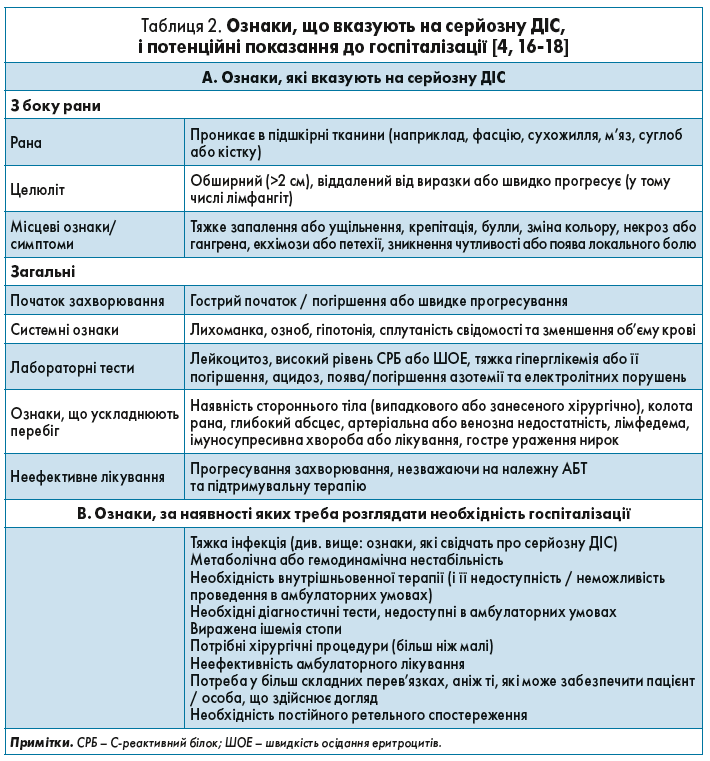
Рекомендація 2. Розгляньте можливість госпіталізації осіб із ЦД і інфекцією стопи, які за класифікацією IWGDF/IDSA мають тяжку форму ДІС або інфекцію середньої тяжкості зі значущими супутніми захворюваннями. (Умовна; низька.)
Обґрунтування. Система класифікації діабетичної стопи IWGDF/IDSA полегшує стратифікацію ризиків під час прийняття рішення про госпіталізацію хворого [4]. Госпіталізація є дорогим і обмеженим ресурсом і може наражати пацієнта на серйозні незручності та потенційні нозокоміальні ризики. Але хоча багато пацієнтів із діабетичною стопою не потребують госпіталізації, деякі з них, безумовно, мають бути госпіталізовані. Необхідно розглядати госпіталізацію всіх осіб із тяжкою інфекцією стопи, щоб забезпечити своєчасне й ефективне лікування, а також госпіталізацію пацієнтів з інфекцією середньої тяжкості за наявності значущих супутніх захворювань, зокрема ЗПА (табл. 2).
Це пов’язано з вищим ризиком несприятливого прогнозу в таких випадках, особливо ампутації або смерті [4, 16, 17, 19]. Треба зазначити, що наявність остеомієліту не обов’язково свідчить про потребу в госпіталізації, оскільки багато з таких пацієнтів клінічно стабільні та можуть бути виліковані пероральними АБ. Госпіталізація може бути рекомендована (принаймні на початку) пацієнтам, які потребують внутрішньовенної АБТ, мають значущу супутню інфекцію м’яких тканин, потребують спеціального діагностичного обстеження або термінового хірургічного лікування. На щастя, майже всі пацієнти з легкою інфекцією, а також багато пацієнтів із ДІС помірної тяжкості, але без будь-яких значущих супутніх захворювань, можуть отримувати лікування в амбулаторних умовах. Доступність у деяких країнах програм для отримання парентеральних АБ в амбулаторних умовах є ще одним фактором, що залежить від локації і впливає на необхідність госпіталізації.
Рекомендація 3. Оцініть сироваткові рівні біомаркерів запалення, таких як СРБ, ШОЕ або прокальцитонін у людини з ЦД і можливою інфікованою ДВС, в якої результати клінічного обстеження є діагностично сумнівними або невизначеними. (Положення найліпшої практики.)
Рекомендація 4. Для діагностики діабет-асоційованої інфекції м’яких тканин стопи ми пропонуємо не використовувати вимірювання температури стопи (незалежно від способу вимірювання) або кількісний мікробний аналіз. (Умовна; низька.)
Клінічне запитання
Які аналізи дають можливість визначити збудника(-ів) і чутливість до АБ у людини з ДІС?
Рекомендація 5. У людини з підозрою на ДІС з ураженням м’яких тканин потрібно зібрати зразок для посіву з метою визначення мікроорганізмів-збудників, бажано – шляхом асептичного забору зразка тканини (шляхом кюретажу або біопсії) з рани. (Умовна; помірна.)
Рекомендація 6. Використовуйте звичайні, а не молекулярні мікробіологічні методи для першої лінії ідентифікації збудників у зразках м’яких тканин або кісток у пацієнта з ДІС (Сильна; помірна.)
Клінічне запитання
Які тести найліпше корелюють із результатами BonE BiOPsy (BeBoP) під час діагностики ДОС, зокрема залишкового/післяопераційного остеомієліту в людини з ЦД і підозрою на інфекцію кісток або суглобів стопи?
Рекомендація 7. Для первинного обстеження пацієнта з ЦД і підозрою на остеомієліт стопи розгляньте можливість поєднання тесту зондування кістки (ТЗК) тупим стерильним інструментом, звичайної рентгенограми та визначення ШОЕ, або рівня СРБ, або прокальцитоніну. (Умовна; низька.)
Обґрунтування. Діагностика ДОС може бути складною, частково – через відсутність загальновизнаного визначення або стандартних критеріїв діагностики, частково – через низький рівень узгодженості між різними широко використовуваними тестами [87]. Остеомієліт може супроводжувати будь-яку рану стопи, особливо в разі її наявності протягом багатьох тижнів або якщо вона широка, глибока, розташована над кістковим виступом, оголюючи кістку, або супроводжується еритемою, набряком пальця ноги (у вигляді «сосиски») [88].
Діагностика інфекції кістки стопи має першочергове значення, оскільки її наявність значно підвищує ризик необхідності низької чи високої ампутації. Обстеження пацієнта з діабетичною раною стопи та підозрою на інфекцію кістки зазвичай передбачає фізикальне обстеження та звичайну рентгенограму, також становлять інтерес рівні деяких біомаркерів у крові; ці питання обговорюються нижче. Точний діагноз ДОС є важливим для того, щоб розпочати відповідну терапію та уникнути необґрунтованого тривалого лікування АБ та хірургічного втручання в пацієнтів, в яких остеомієліту немає.
Тест зондування кістки тупим стерильним інструментом
Серед клінічних обстежень стопи ТЗК є найбільш корисним, але техніка проведення та досвід клініциста, розташування виразки та її етіологія можуть вплинути на надійність результатів тесту [89, 90]. Загалом, при діагностиці ДОС ТЗК підтверджує діагноз, якщо він позитивний у пацієнта з високим ризиком, і допомагає виключити діагноз, якщо він негативний у пацієнта з низьким ризиком. Процедура проста для освоєння, вивчення та виконання, потрібен лише стерильний тупий металевий зонд (обережно вводиться в рану, результат тесту позитивний, якщо відчувається тверда зерниста структура), є недорогою і по суті нешкідливою, але результати тесту в різних клініцистів не завжди збігаються [92]. Треба зазначити, клініцистам без достатнього досвіду виконання ТЗК не можна покладатися на його результати, оскільки тест міг бути виконаний неправильно, що могло призвести до неточних результатів.
Рентгенограма
Будь-якому пацієнту з можливою інфекцією кістки спочатку необхідно провести звичайну рентгенографію стопи. За умови опису знімка досвідченим рентгенологом характерні зміни кістки (табл. 3) з високою ймовірністю свідчать про наявність остеомієліту, проте схожі знахідки можуть бути зумовлені остеоартропатією Шарко та іншими захворюваннями. Оскільки звичайне рентгенівське дослідження є відносно недорогим, широко доступним і завдає мінімальної шкоди, ми рекомендуємо його як частину рутинного обстеження пацієнтів із ДІС. Цей візуалізаційний метод надає корисну інформацію, особливо про стан підлеглих кістково-суглобових тканин, наявність газу в глибоких тканинах і будь-якого рентгеноконтрастного стороннього тіла. Крім того, зображення можна використовувати для порівняння з новими знімками, якщо пацієнт має інші проблеми з ногами. Оскільки звичайні рентгенівські знімки не є діагностичними при гострому остеомієліті, часто доцільно повторити обстеження через 2-3 тиж, якщо зберігається підозра на остеомієліт [93].
Сироваткові біомаркери
У систематичному огляді, опублікованому у 2019 р., виявлено, що ШОЕ ≥70 мм/год була чутливим специфічним маркером із площею під кривою (AUC) 0,81; 0,8 і 0,84 відповідно, тоді як значення прокальцитоніну неможливо було оцінити через брак даних [62].
Масштабне ретроспективне одноцентрове дослідження з високим ризиком похибки, в якому як еталонний стандарт використовували результати посівів і/або гістологічного дослідження зразків кісток, виявило, що ШОЕ >60 мм/год і CРБ ≥80 мг/л мали високу позитивну прогностичну цінність, але помірну негативну прогностичну цінність для діагностики ДОС [96]. В іншому дослідженні поєднання підвищеної ШОЕ (>43 мм/год) із позитивним результатом ТЗК показало високу кореляцію з позитивними результатами посіву з кісток і/або гістологічного дослідження [97].
Загалом, ані звичайне рентгенівське дослідження, ані рівні запальних біомаркерів (ШОЕ, CРБ і прокальцитоніну), ані ТЗК не можуть самі по собі однозначно і надійно підтвердити або виключити діагноз ДОС стопи. Якщо діагноз залишається сумнівним після клінічного обстеження та рентгенографії стопи, ми рекомендуємо визначати ШОЕ, рівень СРБ або прокальцитоніну. Однак ця рекомендація є умовною через ризик гіпер- або гіподіагностики інфекційного ураження кісток, базується на доказах низької якості із суперечливими даними щодо їхньої діагностичної точності.
Рекомендація 8. Магнітно-резонансна томографія (МРТ) показана для діагностики ДОС, якщо діагноз залишається сумнівним, незважаючи на клінічні, рентгенологічні та лабораторні обстеження. (Сильна; помірна.)
Рекомендація 9. Розгляньте можливість проведення позитронної емісійної томографії (ПЕТ), лейкоцитарної сцинтиграфії або однофотонної емісійної комп’ютерної томографії (ОФЕКТ) як альтернативу МРТ для діагностики ДОС. (Умовна; низька.)
Рекомендація 10. У разі підозри на остеомієліт стопи (до або після лікування) розгляньте можливість отримання для посіву зразків кісток (а не м’яких тканин), інтраопераційно або черезшкірно. (Умовна; помірна.)
Лікування
Клінічне запитання
Яку конкретну схему лікування АБ (препарат(и), шлях введення, тривалість терапії) потрібно обрати для пацієнтів із ЦД та інфекцією м’яких тканин стопи, щоб врахувати розрішення або рецидив інфекції, а також розвиток антибіотикорезистентності?
Рекомендація 11. Не лікуйте виразки стопи без клінічних ознак інфекції за допомогою системної або місцевої антибактеріальної терапії (АБТ), якщо метою є зменшення ризику виникнення нової інфекції або сприяння загоєнню виразки. (Положення найліпшої практики.)
Рекомендація 12.
(a) Використовуйте будь-яку зі схем системного лікування АБ, ефективність якої було продемонстровано в рандомізованих контрольованих дослідженнях при стандартному дозуванні для лікування людини з ДІС та інфекцією м’яких тканин стопи. (Сильна; висока.)
(b) Призначайте АБТ пацієнту з ЦД та інфекцією шкіри або м’яких тканин стопи курсом 1-2 тижні. (Сильна; висока.)
(c) Розгляньте можливість продовження лікування, скажімо, до 3-4 тиж, якщо є позитивна динаміка, але інфекцією уражено великі ділянки та загоєння відбувається повільніше, ніж очікувалося, або за наявності тяжкого ЗПА. (Умовна, низька.)
(d) Якщо ознаки інфекції не зникли після 4 тиж відповідної терапії, повторно оцініть стан пацієнта та перегляньте необхідність проведення додаткових діагностичних досліджень або призначення альтернативних методів лікування. (Сильна; низька.)
Рекомендація 13. Обирайте АБ для лікування ДІС з урахуванням імовірного або доведеного збудника(-ів) та його (їхньої) чутливості до АБ; клінічної тяжкості інфекції; опублікованих доказів ефективності препарату при ДІС; ризику побічної дії, у тому числі супутнього ураження коменсальної мікрофлори; імовірності міжлікарської взаємодії; наявності і вартості АБ. (Положення найліпшої практики.)
Рекомендація 14. У пацієнтів із легким перебігом ДІС, які незадовго до цього не отримували АБТ та проживають у Північній Америці чи Західній Європі, розглядайте лише аеробні грампозитивні патогени (бета-гемолітичні стрептококи та золотистий стафілокок, у тому числі метицилінрезистентні штами, якщо є відповідні показання). (Положення найліпшої практики.)
Рекомендація 15. Не використовуйте емпіричну АБТ проти Pseudomonas aeruginosa у разі ДІС у пацієнтів, які проживають у помірних кліматичних зонах, але призначайте емпіричну АБТ проти P. aeruginosa, якщо збудника було виділено при посіві з ураженої ділянки протягом кількох попередніх тижнів у тих пацієнтів із помірною або тяжкою інфекцією, які проживають в Азії чи Північній Африці. (Положення найліпшої практики.)
За даними багатьох досліджень (більшість обмежені через методологічні недоліки), які порівнювали різні пероральні або парентеральні АБ в пацієнтів із ДІС, застосування будь-якого відповідним чином обраного препарату з більшості класів АБ із будь-яким шляхом уведення в переважній більшості випадків виявлялося ефективним [135-141]. Вибір схеми АБТ має ґрунтуватися на:
- імовірному або доведеному збудник(у) та його (їх) чутливості до АБ;
- наявності АБ;
- опублікованих доказах ефективності засобу для лікування ДІС;
- клінічній тяжкості інфекції;
- досвіді команди лікарів і наявності місцевих протоколів;
- наявності факторів із боку пацієнта, зокрема таких, як алергія на ліки в анамнезі, нещодавня госпіталізація та супутні захворювання, наприклад порушення функції нирок або перебування на діалізі;
- імовірності побічних ефектів або потенційної взаємодії лікарських засобів;
- ризику супутнього ураження коменсальної мікрофлори;
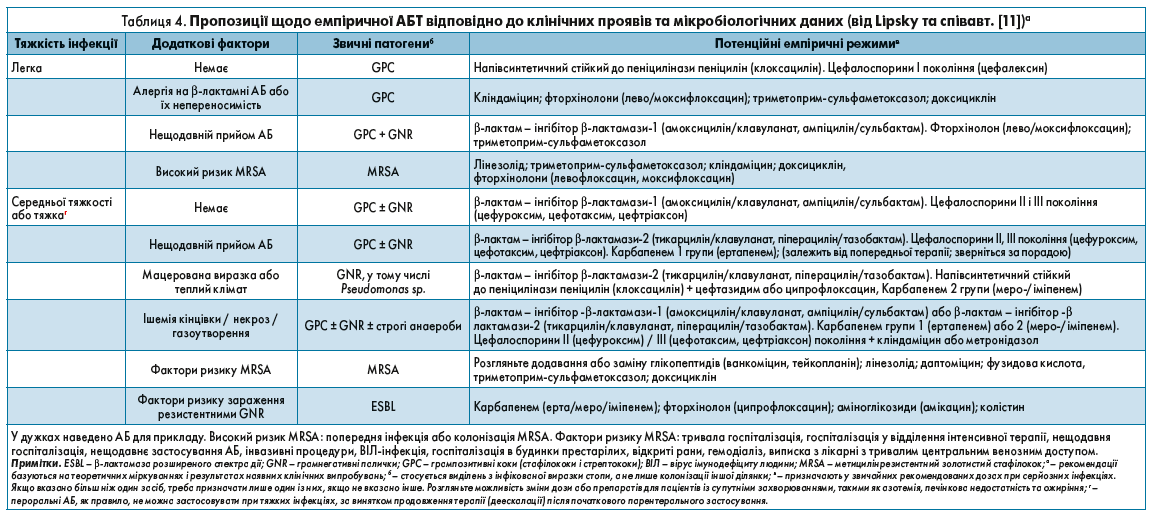
- вартості (дивіться наші пропозиції щодо АБТ в таблиці 4).
При правильно підібраній АБТ (у поєднанні з будь-яким необхідним оперативним утручанням, належним метаболічним контролем і доглядом за раною) більшість випадків ДІС можна успішно лікувати з незначними ускладненнями лікування [140-142]. Найімовірнішими збудниками легких інфекцій є грампозитивні мікроорганізми (бета-гемолітичні стрептококи і S. aureus) [11]. У цьому разі є час для корегування АБТ, якщо під час посіву буде виділено резистентні мікроорганізми або підтвердиться, що інфекція спричинена не грампозитивними коками. Якщо інфекція не реагує на лікування, терапію потрібно скорегувати відповідно до отриманих результатів посівів. Пропозиції щодо емпіричної АБТ помірно тяжких або тяжких ДІС наведено в таблиці 4.
Клінічне запитання
Чи є якась конкретна схема АБТ (певний препарат (и), шлях введення, тривалість загального курсу та парентерального застосування) ефективнішою щодо розрішення інфекції та ймовірності рецидиву в людини з ЦД та інфекцією кісток або суглобів стопи?
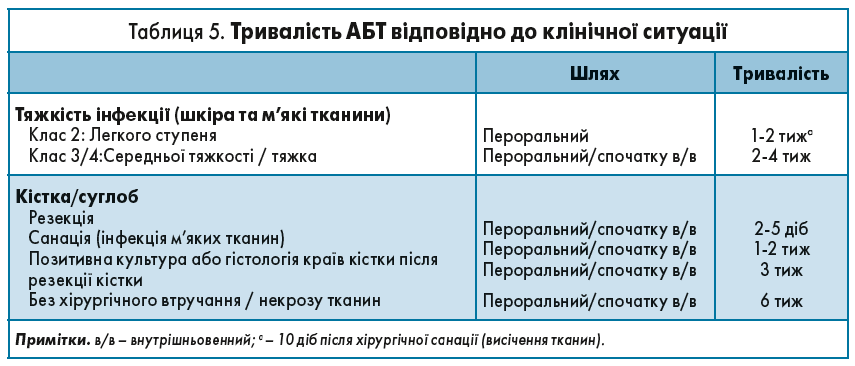
Рекомендація 16. Розгляньте призначення АБТ курсом до 3 тиж після низької ампутації з приводу ДОС і за позитивних результатів посіву з країв кістки і 6 тиж у разі ДОС, якщо не було проведено резекції кістки або ампутації. (Умовна; низька.)
Обґрунтування. При призначенні АБТ для лікування ДОС клініцист має врахувати кілька аспектів, зокрема досягнення достатньо високих рівнів препарату в сироватці крові, щоб забезпечити його проникнення в кістку. Особливо важливо враховувати біодоступність пероральних засобів (тобто всмоктування з шлунково-кишкового тракту у кров), якщо обрано такий шлях застосування препарату. Проникнення АБ із крові в кістку в різних препаратів варіює, але більшість класів АБ забезпечують досягнення відповідної концентрації препарату в зараженій кістці [146]. Ми пропонуємо застосовувати АБ в найвищих рекомендованих дозах, і, як правило, загальна тривалість лікування (табл. 5) має бути значно довшою, аніж для лікування інфекцій м’яких тканин. Призначення довготривалої супресивної АБТ зазвичай виправдане лише в осіб з ортопедичними засобами або обширним некрозом кістки, який не вдається повністю видалити.
Рекомендація 17. Ремісія ДОС може бути діагностована щонайменше через 6 міс після закінчення АБТ. (Повідомлення найліпшої практики.)
Клінічне запитання
В яких випадках у людини з ЦД і помірною або тяжкою інфекцією стопи, у тому числі ДОС, нехірургічне лікування (лише АБТ) є так само безпечним і ефективним методом для досягнення ремісії, як хірургічне лікування (у поєднанні з АБТ)?
Рекомендація 18. Термінова хірургічна консультація необхідна в разі тяжкої ДІС або ДІС середньої тяжкості, ускладнених обширною гангреною, некротичною інфекцією, ознаками, що свідчать про глибокий (нижче фасції) абсцес, компартмент-синдром або тяжку ішемію нижніх кінцівок. (Положення найліпшої практики.)
Рекомендація 19. Розгляньте раннє (протягом 24-48 год) проведення хірургічного втручання в поєднанні з АБТ для лікування ДІС помірного і тяжкого ступеня з метою видалення інфікованих і некротичних тканин. (Умовна; низька.)
Рекомендація 20. У разі ЦД, ЗПА та виразки або гангрени стопи з інфекцією, що зачіпає будь-яку частину стопи, необхідна термінова консультація хірурга, а також судинного хірурга для визначення показань і термінів виконання дренування і/або реваскуляризації. (Положення найліпшої практики.)
Рекомендація 21. Розгляньте можливість проведення хірургічної резекції інфікованої кістки в поєднанні із системною АБТ у пацієнтів із ДОС. (Умовна; низька.)
Рекомендація 22. Розгляньте можливість лікування АБ без оперативного втручання в разі (i) остеомієліту переднього відділу стопи без негайної необхідності розрізу та дренажу для контролю інфекції, (ii) без ЗПА та (iii) без оголеної кістки. (Умовна; низька.)
Клінічне запитання
Чи поліпшує результати лікування пацієнта з ЦД і ДІС будь-яка додаткова специфічна терапія або місцеве лікування АБ на додачу до системної АБТ та оперативного лікування?
Рекомендація 23. Ми не рекомендуємо використовувати нижченаведені методи для лікування ДІС: (a) гранулоцитарний колонієстимулювальний фактор (G-CSF) або (b) місцеві антисептики, препарати срібла, мед, бактеріофаги або терапія ран негативним тиском (з або без інстиляцій). (Умовна; низька.)
Рекомендація 24. Ми не рекомендуємо використовувати АБ для місцевого застосування (губки, креми і мазі) в поєднанні із системними АБ для лікування інфекцій м’яких тканин або ДОС. (Умовна; низька.)
Рекомендація 25. Ми не рекомендуємо використовувати гіпербаричну оксигенацію або місцеву кисневу терапію як допоміжне лікування в разі ДІС. (Умовна; низька.)
Ключові протиріччя
Деякі аспекти менеджменту ДІС все ще потребують доопрацювання. Нижче наведені питання, які, на нашу думку, становлять найбільший інтерес.
- Яким чином і коли можна встановити, що інфекція, у тому числі інфекція м’яких тканин та остеомієліт, вилікувана?
- Які біомаркери сироватки крові є найбільш корисними для визначення того, що ДВС інфікована і є супутній остеомієліт, особливо коли клінічні та візуалізаційні дані є непереконливими?
- Наскільки можна скоротити рекомендовану на сьогодні тривалість АБТ при інфекції м’яких тканин та остеомієліті?
- Коли та які доступні сучасні візуалізаційні методи дослідження треба призначати пацієнту з ДІС?
- Чи поліпшує використання даних, отриманих за допомогою BeBoP, у тому числі в місці ампутації, результати лікування ДОС?
- Яке місце посідають нові АБ в лікуванні ДІС?
- Чи існує визначення та практичне клінічне застосування поняття хронічних біоплівок у разі ДВС?
- Чи допомагає молекулярне (генотипічне) мікробіологічне дослідження на ДІС у виборі антимікробної терапії та поліпшенні результатів лікування?
- Який є потенціал місцевого застосування антимікробних препаратів для скорочення використання системних АБ при ДІС?
Реферативний огляд статті Eric Senneville et al. IWGDF/IDSA Guidelines on the Diagnosis and Treatment of Diabetes-related Foot Infections (IWGDF/IDSA 2023), Clinical Infectious Diseases, ciad527, 02 October 2023.
Повну версію статті дивіться: https://onlinelibrary.wiley.com/doi/10.1002/dmrr.3687
Підготувала Христина Ключківська
Тематичний номер «Діабетологія. Тиреоїдологія. Метаболічні розлади» № 2 (66) 2024 р.