11 грудня, 2021
Лікування гострого больового синдрому: реалії та перспективи
За матеріалами конференції
У статті розглянуто особливості гострого больового синдрому, схеми його лікування у відділенні реанімації та інтенсивної терапії й поза ним, нові підходи до терапії гострого болю, а також найбільш застосовувані знеболювальні препарати.
Ключові слова: біль, гострий больовий синдром, опіоїди, нестероїдні протизапальні препарати, кеторолаку трометамін.
На Шостій молодіжній анестезіологічній конференції «Тріщинські читання», що відбулась 20-22 жовтня, доповідь на тему «Лікування гострого больового синдрому: реалії та перспективи» представив доцент кафедри анестезіології та інтенсивної терапії Національного університету охорони здоров’я України ім. П.Л. Шупика, кандидат медичних наук Олексій Едуардович Доморацький.
Незважаючи на те що основними знеболювальними препаратами у пацієнтів відділення реанімації та інтенсивної терапії (ВРІТ) залишаються опіоїди, для зменшення потреби в них застосовують й інші медикаменти. Так, поза межами реанімації лікування гострого болю починають із нестероїдних протизапальних препаратів (НПЗП) та парацетамолу.
Доповідач окреслив основні аспекти в лікуванні больового синдрому:
- найкращою профілактикою хронічного болю є лікування гострого болю;
- необхідність виділення і моніторингу груп ризику;
- лікування болю поза ВРІТ має починатися за схемою «НПЗП + парацетамол»;
- застосування опіоїдів у якості основної терапії у пацієнтів ВРІТ;
- призначення ад’ювантів для зниження дозування опіоїдів;
- застосування профілактичної аналгезії;
- врахування різних факторів, що модифікують біль;
- створення служб лікування болю як перспективний етап у стратегії лікування больового синдрому.
Післяопераційний біль є очікуваним для пацієнта і триває недовго, хоча іноді може переходити у хронічний. Парадоксально, що ділянки малих хірургічних втручань є більш болісними, ніж такі при значних операціях. Післяопераційний біль оцінювати доволі складно, особливо у пацієнтів окремих категорій, до яких належать: пацієнти ВРІТ, особи похилого віку й ослаблені пацієнти, іншомовні особи, пацієнти із хронічним болем, політравмою або тяжкою тупою травмою грудної клітки, із тяжкою дисфункцією органів, із толератністю до опіоїдів, особи із психічними розладами або деменцією, фізичними вадами або порушеннями сприйняття, особи, що вживають наркотики чи алкоголь, вагітні та жінки, що годують грудьми (Royal College of Anaesthetists, 2021).
Факторами ризику виникнення ригідного післяопераційного болю можуть бути:
- нелікований передопераційний біль;
- тривалий прийом опіоїдів;
- генетичні, хірургічні й психологічні чинники;
- висока інтенсивність післяопераційного болю;
- застосування великих періоперативних доз реміфентанілу;
- вік пацієнта (в осіб похилого віку низька ймовірність виникнення персистуючого болю);
- жіноча стать.
Доповідач прокоментував деякі фактори ризику. Він зауважив, що раніше при гострому болю у животі уникали інтенсивного доопераційного знеболення, щоб зберегти клінічну картину гострого апендициту чи іншого захворювання. У сучасному хірургічному стаціонарі достатньо діагностичних інструментів, тому всі пацієнти із гострим болем потребують передопераційної аналгезії. Щодо реміфентанілу, то оскільки українські клініцисти його не застосовують, автор не зміг спростувати або підтвердити ризик його застосування. Хірургічні, психологічні чинники та інтенсивний післяопераційний біль заслуговують на особливу увагу, адже їх можна модифікувати, застосовуючи нові хірургічні методики, покращуючи контакт із пацієнтом і призначаючи відповідні медикаменти.
Доповідач навів дані нещодавнього дослідження (Cachemaille M., Grass F., Fournier N., 2020), у якому лікарі оцінювали біль у 1278 пацієнтів протягом 96 год після абдомінального втручання. Для оцінки інтенсивності болю застосовували візуально-аналогову шкалу. У ході дослідження було виявлено, що біль посилюється при подовженні тривалості операції, застосуванні епідуральної аналгезії та призначенні лідокаїну. Однак, за результатами багатоваріантного аналізу, залишився тільки один незалежний фактор ризику інтенсивного болю: вік пацієнта. Пацієнти віком <70 років мали вищу больову чутливість, ніж старші особи.
В іншому дослідженні (Kranke P., Jokinen J., Pace N.L. et al., 2015) учені відзначили, що більшість пацієнтів були задоволені лікуванням болю. Особливо інтенсивний біль був асоційований із мобілізацією, наявністю в особи баріатричного чи колоректального втручання. Автори дослідження встановили, що лікарі, які використовували один і той самий протокол, призначали різні НПЗП через неоднакові проміжки часу. Тому актуальним є питання більш стандартизованого підходу до знеболення. Крім того, дослідники припустили, що лікарі недооцінюють біль після невеликих хірургічних втручань (що може пояснювати більш інтенсивний біль після малих операцій). Цікаво, що результати не виявили відмінностей болю за статтю.
У згаданому дослідженні була застосована наступна медикація (Kranke P. et al., 2015):
- фентаніл/суфентаніл (на розсуд анестезіолога);
- парацетамол – 1 г наприкінці операції;
- НПЗП (ібупрофен, кеторолак, анальгін);
- реміфентаніл – після операції;
- клонідин – 0,5-1 мкг/кг;
- кетамін – 0,25 мг/кг болюсно з подальшим введенням у дозі 0,25 мг/кг/год, максимальна доза – 1 мг/кг;
- лідокаїн – 1 мг/кг для індукції, згодом – 2 мг/кг/год до виписки з післяопераційної палати.
Доповідач звернув увагу на основні помилки в лікуванні гострого больового синдрому. Насамперед, хибним є ігнорування болю, лікування його за потребою і відсутність оцінки його інтенсивності. До того ж лікарі часто ігнорують біль, який виник не в ділянці втручання. Це особливо актуально у травматологічних й ортопедичних пацієнтів, які тривало перебувають у вимушеному положенні, відчуваючи дискомфорт і біль. Наступною помилкою є надмірне або недостатнє призначення опіоїдів. Помилки медикації означають недотримання дозування й часу введення препаратів, у зв’язку із чим знижується їхня ефективність. Ще однією помилкою є невикористання ад’ювантів, наприклад лідокаїну, кетаміну, габапентину (при цьому максимальна передопераційна доза габапентину не має перевищувати 600 мг, щоб запобігти надмірному седативному ефекту). Нарешті, при лікуванні болю дуже важливо враховувати психологічний стан пацієнта і наявність у нього порушень циркадного ритму.
Основою лікування гострого болю у ВРІТ є призначення опіоїдів. Препарати мультимодальної аналгезії застосовують для зменшення кількості призначених опіоїдів. За рекомендацією Королівського коледжу анестезіологів Великої Британії, термін дії рецепта на опіоїд, виданого під час виписки, не має перевищувати 5 днів. По закінченні цього періоду, перш ніж знову призначити опіоїдний препарат, лікар повинен оглянути пацієнта. Осіб, які тривало приймають опіоїди, слід виявляти на передопераційному етапі й направляти до спеціалізованих служб, щоб зменшити споживання ними опіоїдів і полегшити больовий синдром (Royal College of Anaesthetists, 2021).
Для усунення болю у ВРІТ призначають:
- фентаніл – 20-50 мкг/год;
- морфін – 2-5 мг/год;
- парацетамол – 1 г/6 год;
- препарати для регіонарної аналгезії;
- НПЗП;
- кетамін;
- лідокаїн.
Наведена фармакотерапія відповідає міжнародним настановам PADIS (Настанови із профілактики та лікування болю, терапії збудження/седації, лікування делірію, іммобілізації та корекції порушень сну в дорослих пацієнтів у ВІТ) і протоколам ERAS (Протоколи прискореного відновлення після операції). Кетамін і лідокаїн рідко застосовують за межами реанімаційного відділення, на відміну від НПЗП, що визначені початковими препаратами для лікування гострого болю.
Одним із НПЗП, який призначають у складі хірургічної аналгезії, є кеторолак. Серед препаратів кеторолаку в Україні, у тому числі, знайшов визнання препарат Кетанов® (1 мл розчину для ін’єкцій містить 30 мг кеторолаку трометаміну). Кеторолак – відносно безпечний препарат за умови його застосування у стандартній дозі. Дані про безпечність цього препарату отримані в одному з досліджень, у ході якого встановлено (Maslin B., Lipana L., Roth B., Kodumudi G., 2017):
- застосування кеторолаку не перешкоджає післяопераційному загоєнню кісткової тканини;
- кеторолак безпечний у пацієнтів із нормальною функцією нирок;
- призначення кеторолаку зменшує потребу в опіоїдах у всіх пацієнтів;
- при застосуванні кеторолаку можливе підвищення кровоточивості після тонзилектомії у дорослих (але не в дітей);
- за даними наступних досліджень не виявлено зв’язку між лікуванням кеторолаком та виникненням кровотечі.
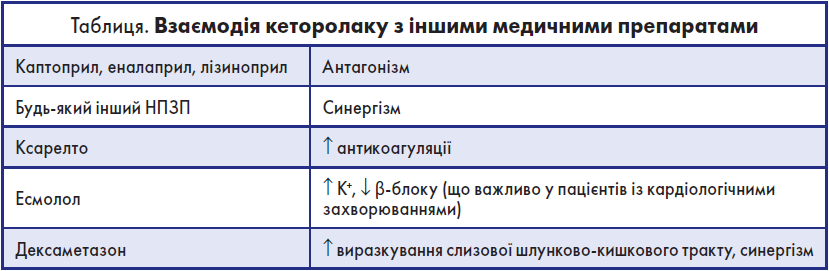
Якщо знеболювальна дія кеторолаку є недостатньою, його не слід поєднувати з іншим НПЗП, оскільки аналгезуючий ефект суттєво не зміниться, але виникне сумарна побічна дія. Таким чином, призначення кеторолаку має враховувати його взаємодію з іншими препаратами (таблиця).
Доповідач наголосив, що, призначаючи будь-який препарат для знеболення, наприклад НПЗП, слід оцінювати гастроінтестинальний ризик (ризик виникнення у пацієнта шлунково-кишкової кровотечі), адже анальгетиків із низьким гастроінтестинальним ризиком не існує. Результати дослідження (Bhala N., Emberson J., Merhi A., 2013) показали, що всі схеми НПЗП посилювали ускладнення з боку верхніх відділів шлунково-кишкового тракту: целекоксиб (відношення ризиків [ВР] 1,81, 95% довірчий інтервал [ДІ] 1,17-2,81, p=0,0070), диклофенак (ВР 1,89, 95% ДІ 1,16-3,09, p=0,0106), ібупрофен (ВР 3,97, 95% ДІ 2,22-7,10, p<0,0001), напроксен (ВР 4,22, 95% ДІ 2,71-6,56, p<0,0001).
О.Е. Доморацький навів особливості застосування кеторолаку трометаміну (De Oliveira G.S., Agarwal D., Benzon H.T., 2012):
- однократне парентеральне введення кеторолаку трометаміну знижує потребу в опіоїдах у післяопераційному періоді;
- максимальна доза препарату становить 90 мг/добу у вигляді ін’єкцій;
- при однократному застосуванні кеторолаку трометаміну відмічено зниження частоти післяопераційної нудоти і блювання.
Автор доповіді резюмував, що для вирішення проблеми усунення гострого больового синдрому слід звернутись до міжнародної практики, а саме запровадження в лікарнях чи поза ними служб лікування болю. Протягом останніх років клініцисти дотримуються протоколів ERAS, що передбачають виконання малоінвазивних втручань де це можливо, застосування новітніх знеболювальних методик, ранню мобілізацію і виписку пацієнта. Проте датські вчені відзначили, що з моменту впровадження у практику протоколів ERAS лікарі практично перестали звертатися до служб лікування болю. За статистикою, 20-30% госпіталізованих пацієнтів мають складні діагнози, толерантність до опіоїдів і хронічний біль, тому терапія за протоколами ERAS для них є недостатньою (Romundstad L., Breivik H., 2012). Саме служба лікування болю могла б забезпечити потреби у знеболенні для всіх категорій пацієнтів.
Підготувала Анна Сакалош