27 липня, 2021
Антибіотикорезистентність як глобальна проблема в умовах пандемії COVID-19 та способи її подолання
Експертна думка
На думку багатьох представників медичної спільноти, найближчим часом після завершення пандемії COVID-19 слід очікувати різкого зростання рівня антибіотикорезистентності, адже у сьогоднішніх реаліях ми спостерігаємо ситуацію, за якої для лікування вірусної пневмонії призначається два-три антибактеріальних препарати, що є абсолютно необґрунтованим і не відповідає міжнародним та вітчизняним рекомендаціям. Для визначення критеріїв вибору правильної терапевтичної стратегії застосування антибіотиків у період пандемії COVID-19 ми запросили поділитися власним досвідом та обговорити існуючі світові напрацювання у цій сфері провідних вітчизняних експертів у галузі інфектології, мікробіології, клінічної фармакології, анестезіології та інтенсивної терапії дітей та дорослих. Такий міждисциплінарний підхід дозволив визначити основні принципи та умови оптимальної антибактеріальної терапії, розглянути різні схеми та комбінації призначених препаратів у контексті стримання подальшого росту кількості антибіотикорезистентних патогенів в умовах стаціонару.
Ключові слова: антибіотикорезистентність, COVID‑19, карбапенем-резистентні патогени, цефтазидим/авібактам.
Проблеми використання антибактеріальних препаратів в умовах пандемії COVID-19.
Світовий та вітчизняний досвід на прикладі відділень реанімації та інтенсивної терапії
Завідувач кафедри анестезіології та інтенсивної терапії Національного медичного університету ім. О.О. Богомольця (м. Київ), доктор медичних наук, професор Сергій Олександрович Дубров.
– За даними Всесвітньої організації охорони здоров’я (ВООЗ), проблема стійкості до антибактеріальних препаратів являє собою глобальну загрозу для здоров’я і розвитку населення. Неправильне та надмірне застосування антибіотиків призводить до більш тривалого перебігу інфекційних захворювань, подовження терміну госпіталізації і, як наслідок, веде до значних економічних витрат.
Відсутність ефективних протимікробних препаратів створює підвищену загрозу успіху сучасної медицини в лікуванні інфекцій, у тому числі при виконанні високотехнологічних хірургічних втручань і проведенні хіміотерапії в онкологічних хворих.
У 2015 році ВООЗ був прийнятий глобальний план дій (ГПД) по боротьбі зі стійкістю до протимікробних препаратів. До нього долучилося багато країн світу із зобов’язанням розробити і здійснювати багатосекторальні плани дій на національному рівні відповідно до рамкових принципів ГПД. У березні 2019 року Національний план дій по боротьбі зі стійкістю до протимікробних препаратів був схвалений та прийнятий урядом нашої країни.
Ставлячи на меті пріоритетні розробки нових антибіотиків задля подолання проблеми антибіотикорезистентності, у 2017 році ВООЗ визначила 12 найнебезпечніших бактерій. Перше місце серед них, із критичним рівнем пріоритетності, займають карбапенем-резистентні штами Acinetobacter baumannii, Pseudomonas aeruginosa та представники Enterobacteriaceae, такі як Klebsiella pneumoniae та Escherichia сoli, що продукують β-лактамази розширеного спектра дії.
Слід відзначити, що в Україні A. baumannii на сьогодні займає перше місце серед збудників нозокоміальних інфекційних ускладнень у відділеннях реанімації та інтенсивної терапії, на відміну від статистики 12-15 річної давності, коли домінуючим патогеном була синьогнійна паличка. До того ж останнім часом у вітчизняних стаціонарах спостерігається зростання питомої ваги резистентних до карбапеменів штамів E. сoli.
Так, відповідно до бази даних ВООЗ з епіднадзору за стійкістю до антимікробних препаратів у Центральній Азії та Європі (CAESAR), в Україні частота виявлення E. сoli, резистентної до карбапенемів, у 2018 році становила менше 1%, а у 2019 році питома вага її виявлення зросла до 10-25%.
На жаль, пандемія COVID-19 дещо завадила ефективному й повномасштабному впровадженню принципів інфекційного контролю, закладених ГПД, зі стримання антибіотикорезистентності як у світі, так і в нашій країні. Відповідно до результатів міжнародних досліджень, на сьогодні 70% пацієнтів із COVID-19 отримують антибіотики на амбулаторному етапі лікування й у стаціонарі (ISARIC, 2020; Langford et al., 2021). Утім до 95% призначень останніх є недоцільним.
Нами проведений ретроспективний аналіз призначення антибактеріальних препаратів від початку пандемії до сьогодні у трьох лікувальних закладах м. Києва. Так, у двох із трьох лікарень практично 100% пацієнтів, хворих на коронавірусну інфекцію, отримували антибіотики, причому досить часто це була комбінація двох чи трьох різних препаратів. У третьому закладі частота призначення антибактеріальних препаратів не перевищувала 5% в інфекційних відділеннях без ВІТ (відділення інтенсивної терапії) та 16,7% – із ВІТ.
Якщо звернутися до даних американських колег Мічиганського університету, які провели велике ретроспективне дослідження 1700 хворих, госпіталізованах у 38 лікарень із підозрою на COVID-19, більше 50% пацієнтів отримували антибіотики (Vaughn V.M., 2021). Притому що реальні підстави, тобто показання для призначення цих препаратів (наявність бактеріальної коінфекції), були лише у 3,5% хворих. У 96,5% із них виділили лише SARS-CоV-2, на який антибіотики не діють. Навіть у США, де працює страхова медицина і всі призначення сурово контролюються, має місце поліпрагмазія лікарських засобів і необґрунтоване призначення.
Лікування нозокоміальної інфекції в умовах прогресуючої мультирезистентності.
Погляд інфекціоніста
Завідувач кафедри інфекційних хвороб Національного медичного університету ім. О.О. Богомольця, доктор медичних наук, професор, Ольга Анатоліївна Голубовська.
– Основними причинами стійкості до антибіотиків є надмірне і неправильне їх застосування, чому сприяє:
- застосування антибактеріальних препаратів у лікуванні небактеріальних інфекцій;
- безрецептурне відпускання антибіотиків;
- низький інфекційний контроль;
- застосування антибіотиків у якості стимулятора росту тварин і для запобігання захворюваності останніх на нозокоміальні інфекції.
Чутливі до антибактеріальних препаратів бактерії можуть стати стійкими у результаті генетичної мутації в їхніх ДНК (хромосомна резистентність) або, що спостерігається частіше, у результаті набуття мобільних елементів генів від інших бактерій, які вже мають стійкість до антибіотиків (горизонтальне перенесення генів резистентності). Нерідко один ген резистентності здатний передавати стійкість до двох чи більше препаратів, що належать до одного класу (перехресна резистентність). Крім того, антибіотикорезистентність може розвиватись і до препаратів інших класів, якщо гени резистентності, що детермінують стійкість до антибіотиків різних класів, знаходяться у ДНК бактерії поряд і можуть передаватись одночасно (корезистентність).
Останнім часом тривогу викликає швидке розповсюдження штамів E. coli, які продукують β-лактамази розширеного спектра, що володіють стійкістю до цефалоспоринів 3-4-го покоління й здатні її передавати. Це небезпечно тим, що внаслідок такої передачі розвивається резистентність і до фторхінолонів. Даний штам E. coli за останні 10 років швидко почав розповсюджуватись не лише країнами Європи, а й усього світу. Стійкість його до колістину визначається наявністю гена MCR‑1, який було виділено не тільки в E. сoli, а й у Klebsiella pneumoniaе та Pseudomonas aeruginosa (Comparative analysis of food and nutrition policies in the WHO European, 2011).
Одним із важливих шляхів розповсюдження антибіотикорезистентності є застосування антибіотиків у тваринництві, м’ясомолочній і харчовій промисловості, що пов’язано не лише з лікуванням тварин, а й зі стимуляцією їх росту. Так, за статистичними даними, у Китаї із продуктами харчування люди щороку споживають близько 30 кг антибіотиків, що сприяє невпинному росту антибіотикорезистентності.
Salmonella та Campylobacter є на сьогодні найпоширенішими бактеріями, що викликають хвороби харчового походження, із прогресуючою резистентністю до макролідів, цефалоспоринів 3-го покоління та фторхінолонів (ципрофлоксацину).
В Україні 20-50% ізолятів Е.соli резистентні до фторхінолонів, 25-50% – до цефалоспоринів 3-го покоління, 5-10% – до карбапенемів, а 50% ізолятів К. pneumoniaе резистентні до цефалоспоринів 3-го покоління і 50% – до карбапенемів. Це вказує на найгіршу ситуацію у Європі (Westblade L., et al., 2019).
Згідно з міжнародними рекомендаціями з ведення хворих на COVID‑19, для виявлення вторинної бактеріальної інфекції слід провести наступні додаткові обстеження:
- гемограму;
- візуалізацію грудної клітки (ГК-рентген), комп’ютерну томографію (КТ) або ультразвукове дослідження (УЗД);
- мікробіологічне обстеження зразків із органів дихання та крові;
- аналіз сечі для тестування на легіонели та пневмококовий антиген;
- аналіз слизу із ротоглотки для тестування на респіраторні віруси та атипові збудники.
Показаннями до призначення антибіотиків у лікарні є клінічна підозра на вторинну бактеріальну інфекцію або її підтвердження впродовж 4 год після надходження до стаціонару, а також підозра на сепсис або належність пацієнта до групи високого ризику розвитку сепсису (рекомендації NICE).
Основні принципи, якими слід керуватися при використанні антибактеріальних препаратів, передбачають наступне:
- обираючи вид антибіотика, слід враховувати місцеві дані стійкості останніх;
- віддавати перевагу слід пероральній формі антибіотиків, якщо пацієнт має змогу їх приймати;
- слід переглянути тактику лікування, якщо через 48-72 год від початку прийому антибіотиків не спостерігається очікуваних результатів;
- у випадку клінічної неефективності або розвитку нозокоміальних (внутрішньолікарняних) ускладнень вибір режиму антимікробної терапії необхідно проводити на підставі виявлення факторів ризику резистентних штамів, результатів моніторингу антибіотикорезистентності та результатів мікробіологічної діагностики.
Для терапії нозокоміальних бактеріальних інфекцій у стаціонарі, залежно від результатів чутливості збудників, у конкретного пацієнта можуть застосовуватись такі антибактеріальні препарати, як азтреонам (у комбінації із цефтазидимом/авібактамом), іміпенем/циластатин, лінезолід, меропенем, піперацилін/тазобактам, поліміксин (лише в комбінації), телаванцин, тайгециклін, фосфоміцин (лише в комбінації), цефтазидим/авібактам, цефтолозан/тазобактам, цефепім/сульбактам.
22-й перегляд життєво необхідних лікарських засобів ВООЗ, що відбувся у квітні 2019 року, виділив наступний перелік ліків:
- цефтазидим/авібактам;
- колістин;
- фосфоміцин;
- лінезолід;
- меропенем/ваборбактам;
- поліміксин B;
- плазоміцин.
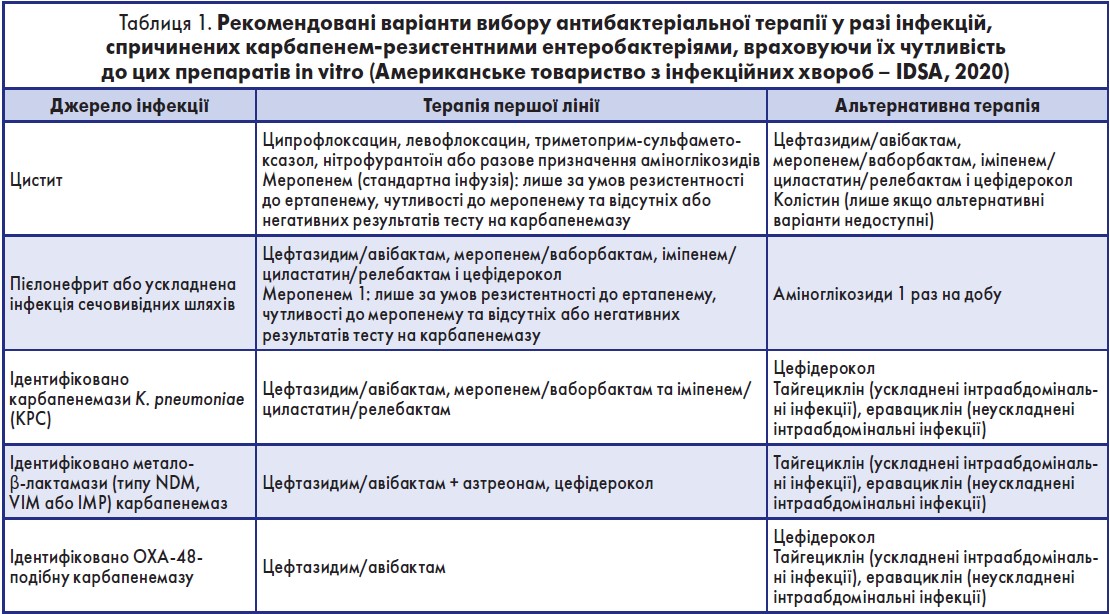
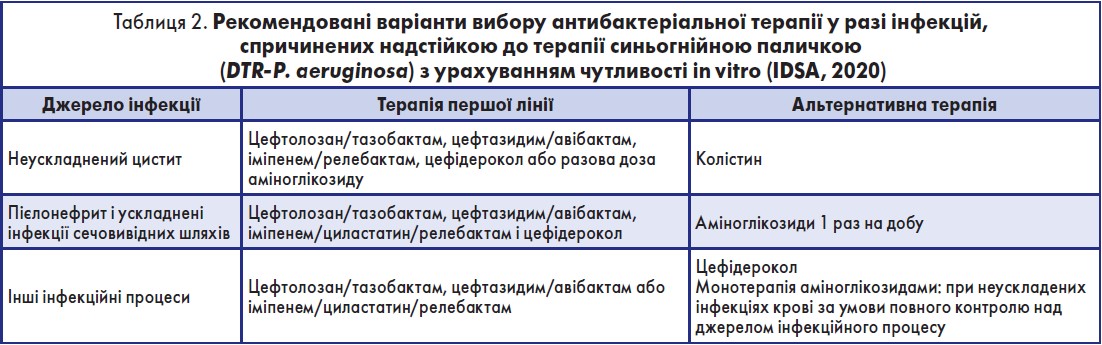
Дані препарати та їх комбінації використовуються для лікування інфекцій, викликаних карбапенем-резистентними збудниками, за наступними схемами (табл. 1, 2).
Таким чином, за даними IDSA (2020), при використанні антибіотиків слід враховувати дані локального мікробіологічного пейзажу та діяти згідно із принципом «збереження» нових антибіотиків. IDSA рекомендує цефідерокол як препарат вибору тільки у якості альтернативи, коли інші методи лікування не дають результату або до останніх виникає резистентність. Поліміксин В і колістін призначають при лікуванні інфекцій, викликаних карбапенем-резистентними ентеробактеріями. Колістин може розглядатись як альтернативний препарат при неускладненому циститі, викликаному карбапенем-резистентними ентеробактеріями. Меропенем/ваборбактам не рекомендуються для лікування інфекцій, викликаних P. aeruginosa. Найоптимальнішим варіантом лікування карбапенем-резистентної P. аeroginosa та ускладненої інфекції сечовивідних шляхів є цефтазидим/
авібактам.
Можливості застосування комбінацій антибіотиків в умовах тотальної антибіотикорезистентності грамнегативних мікроорганізмів.
Погляд мікробіолога
Завідувач Референс-центру молекулярної діагностики інфекційних хвороб МОЗ України, кандидат медичних наук Валентина Володимирівна Яновська.
– До основних грамнегативних збудників внутрішньолікарняних інфекцій належать P. aeruginosa, K. pneumoniaе та A. baumanii. Однак неадекватне призначення антибіотиків та неправильне проведення досліджень щодо визначення чутливості до останніх невпинно веде до зростання антибіотикорезистентності. Наприклад, помилка у визначенні чутливості до колістину полягає у тому, що її неможливо визначити диско-дифузійним методом або методом серійних розведень в агарі й напіврідкому агарі, оскільки колістин має досить велику молекулу, яка не проникає в агар рівномірно.
Дедалі частіше у клінічній практиці зустрічаються антибіотикограми збудників, стійких до більшості антибіотиків. У таких випадках для ефективного лікування пацієнтів використовується ефект синергічної дії комбінацій антибіотиків різних груп.
Так, при лікуванні станів, викликаних резистентною флорою, можна використовувати наступні комбінації антибактеріальних препаратів:
Однак для успішної реалізації стратегії боротьби з антибіотикорезистентністю слід мати систему інфекційного контролю та мікробіологічну лабораторію, яка може забезпечити її функціонування.
Нормативні документи, які на сьогодні стосуються контролю за внутрішньолікарняними інфекціями, включають:
- Наказ МОЗ України від 04.04.2012 № 236 «Про організацію контролю та профілактики післяопераційних гнійно-запальних інфекцій, спричинених мікроорганізмами, резистентними до дії антимікробних препаратів»;
- Наказ МОЗ України від 04.04.2008 № 181 «Про затвердження методичних рекомендацій “Епідеміологічний нагляд за інфекціями ділянки хірургічного втручання та їх профілактика”»;
- Наказ МОЗ України від 10.05.2007 № 234 «Про організацію профілактики внутрішньо-лікарняних інфекцій в акушерських стаціонарах»;
- A Guide to Infection Control in the Hospital, 5th edition.
Однак актуальність даних протоколів слід переглянути, зважаючи на давність їх оновлення, зміни, пов’язані з пандемією COVID‑19 та невпинне зростання антибіотикорезистентності загалом.
Конкретні кроки на шляху до подолання антибіотикорезистентності в Україні.
Практика дитячого відділення інтенсивної терапії
Професор кафедри дитячої анестезіології та інтенсивної терапії Харківської медичної академії післядипломної освіти, професор Маріне Акопівна Георгіянц.
– Розповсюдження нозокоміальних інфекцій, у т.ч. у дитячих відділеннях інтенсивної терапії (ВІТ), продовжує зростати. Проте на сьогодні немає універсальних нормативних документів щодо їх лікування.
Кожне ВІТ повинне мати індивідуальний мікробний паспорт, що буде найточніше відповідати актуальній на даний момент поширеності мікробних агентів у конкретному відділенні. А для створення останнього та просування проекту подолання антибіотикорезистентності в Україні слід вжити наступних заходів:
- регулярно проводити дослідження для визначення мікробного пейзажу ВІТ у стаціонарах педіатричного профілю та формування напрямку інфекційного контролю;
- організовувати для лікарів та медичних сестер відділень проведення освітніх програм, зокрема щодо правильності забору біологічного матеріалу;
- призначати та змінювати антибактеріальні препарати суворо за показаннями;
- розглянути можливість використання визначення прокальцитоніну для призначення або відміни антибіотиків;
- працювати над створенням Реєстру нозокоміальних інфекцій на рівні регіонів та МОЗ України.
Щоб дані пропозиції стали робочими інструментами, було заплановано та запущено національне мультицентрове дослідження поширеності полірезистентних штамів мікроорганізмів у ВІТ педіатричного профілю. Основні його завдання включають виявлення найбільш поширених полірезистентних штамів мікроорганізмів, оцінку чутливості виявлених патогенів до антибактеріальних препаратів, аналіз ефективності лабораторного забезпечення ВІТ педіатричного профілю, визначення впливу даних мікробіологічних досліджень на тактику антибіотикотерапії, а також визначення залежності поширення антибіотикорезистентних штамів від дотримання принципів раціональної антибіотикотерапії. Результати даного дослідження будуть опубліковані в національних та міжнародних профільних друкованих виданнях.
Проблема антибіотикотерапії у педіатричній популяції.Погляд клінічного фармаколога
Завідувач кафедри фармакології Національного медичного університету ім. О.О.Богомольця, доктор медичних наук, професор Ганна Володимирівна Зайченко.
– Половина всіх лікарських засобів, які використовуються у педіатричній практиці, офіційно не дозволені для застосування у дітей або використовуються не у відповідності до інструкції (off-label), оскільки клінічні дослідження цих препаратів у дітей не проводилися. Серед дітей зростає частота розвитку інфекцій, спричинених збудниками із множинною стійкістю до антибіотиків, що пов’язано з підвищеним ризиком смертності. Разом із тим частота нерегламентованих призначень антибіотиків у педіатрії становить близько 50% при лікуванні у стаціонарі й >10% при проведенні фармакотерапії в амбулаторних умовах. Педіатрична когорта пацієнтів не застрахована від зростаючої загрози, яку несуть стійкі до карбапенемів ентеробактерії. Інфекції, викликані цими збудниками, важче піддаються лікуванню через обмеженість варіантів антибіотикотерапії й спричиняють зростання смертності серед дітей.
Важливо відзначити, що вибір оптимального лікування залишається складним, враховуючи обмеженість даних про фармакокінетику та фармакодинаміку в дітей та обмежений клінічний досвід щодо оцінки нових антибіотиків. Фармакологічна відповідь у них може значно відрізнятись від такої у дорослих, насамперед через незрілість систем абсорбції, розподілу, метаболізму та виведення лікарських засобів. Вікові особливості цих процесів впливають на чутливість до антибіотиків, що необхідно враховувати при виборі самого препарату, шляху введення та режиму його дозування.
Ефективність та безпечність комбінації цефтазидиму та авібактаму – інгібітора β-лактамаз широкого спектра дії була вивчена у дев’яти клінічних дослідженнях на території Європейського Союзу як у дорослих, так і в дітей.
Дані дослідження вже завершені і демонструють докази ефективності цефтазидиму/авібактаму в лікуванні ускладнених інтраабдомінальних інфекцій (уІАІ) та інфекцій сечовивідних шляхів (ІСШ) у педіатричних пацієнтів старше 3 місяців. Про серйозні несприятливі явища або настання летальних випадків під час досліджень не повідомлялося. Комбінація цефтазидим/авібактам + метронідазол добре переносилась у педіатричних пацієнтів з уІАІ. Це зумовлено тим, що загальний профіль безпеки цефтазидиму/авібактаму відповідав профілю безпеки дорослих пацієнтів з уІАІ згідно з даними рандомізованих клінічних досліджень ІІІ фази RECLAIM. У ході дослідження також підтвердилась ефективність цефтазидиму/авібактаму проти грамнегативних патогенів у дітей з ускладненими ІСШ. До того ж цефтазидим/авібактам добре проникає в легені, де його концентрація є пропорційною концентрації у плазмі крові, й не проявляє потенційної здатності подовжувати інтервал QT. Вищеописані дані дозволяють зробити висновок, що поява нового інгібітор-захищеного цефалоспорину 3-го покоління для лікування дітей від 3 міс до 18 років – важлива подія для педіатричної фармакології. Комбінація цефтазидиму/авібактаму допоможе стримати використання антибіотиків резерву – карбапенемів, а з огляду на його фармакологічні та фармакокінетичні переваги може розширити спектр антибіотиків для педіатричних пацієнтів, які мають протипоказання до амінопеніцилінів та макролідів.
Проблема мультирезистентної флори в умовах дитячого стаціонару.
Досвід НДСЛ «Охматдит»
Завідувач відділення анестезіології та інтенсивної терапії новонароджених ДУ «Науково-практичний медичний центр дитячої кардіології та кардіохірургії МОЗ України», медичний директор НДСЛ «Охматдит» Сергій Сергійович Чернишук.
– У НДСЛ «Охматдит» проводились пілотні дослідження, які дозволили виявити проблему внутрішньолікарняних інфекцій, визначити причини їх виникнення та створити локальні формуляри щодо епіднагляду та сповіщення про випадки появи мультирезистентної флори, шляхи ізоляції пацієнтів цієї категорії.
Була проаналізована частота виникнення різних видів внутрішньолікарняної інфекції та порівняна з аналогічними показниками у зарубіжних літературних джерелах:
- катетер-асоційовані інфекції кровотоку виявлялись із частотою 9,6 випадку на 1000 катетер-днів, що значно перевищувало ці показники в інших країнах світу (Тайвань – 3,9 випадку на 1000 катетер-днів);
- вентилятор-асоційовані пневмонії – 14,3 випадку на 1000 днів інтенсивної терапії, тобто цей показник наближається до такого у європейських країнах (13,6 випадку на 1000 днів інтенсивної терапії), є нижчим, ніж у країнах Азії (3,5-46 випадків на 1000 днів інтенсивної терапії), однак вищим, ніж у США (1,2-8,5 випадку на 1000 днів інтенсивної терапії);
- катетер-асоційовані інфекції сечової системи – 8,1 випадку на 1000 катетер-днів, що порівняно із цим показником у США, який становить 3,1 випадку на 1000 катетер-днів, є значно вищим;
- інфекції ділянки хірургічного втручання – 5% випадків, натомість як у США – 3%.
Окрім інфекційного контролю, безумовно, важливою є раціональна передопераційна профілактика із застосуванням антимікробних препаратів (АМП). У ході даного дослідження, метою якого було виявити нераціональність призначення АМП, пролонгацію періоду їх уведення, проаналізовано 179 медичних карт та отримано наступні результати:
- у 56% пацієнтів передопераційна профілактика не проводилася;
- при проведенні АМП у 48% випадків її застосування перевищувало допустимі 48 год, у 0,6% випадків – 24-48 год, у 6% – введення припинене одразу після операції;
- тривалість введення АМП варіювалась від 0 до 90 діб;
- середня тривалість терапії АМП після операції становила 11,4 доби.
З огляду на отримані дані зафіксовано нераціональне призначення лікарських засобів, що вказує на необхідність покращення обізнаності лікарів щодо особливостей призначення антибіотикотерапії.
Для раціонального призначення АМП слід користуватись класифікацією BOO3, що була розроблена у рамках проекту AWaRe (2019) з виокремленням наступних категорій лікарських засобів:
- категорія доступу (амікацин);
- категорія спостереження (тобраміцин, ванкоміцин, піперацилін/тазобактам, меропенем, ципрофлоксацин, цефалоспорини 3-4-го покоління);
- категорія резерву (колістин, фосфоміцин).
У ході оцінки коректності призначення АМП були виявлені відхилення схеми лікування від настанов ВООЗ. Згідно із рекомендаціями, для передопераційної профілактики не є можливим призначення антибіотиків нагляду та резерву. Утім навіть антибіотики резерву, що не призначаються в більшості клінік без рішення комісії, застосовувались із метою передопераційної антибіотикопрофілактики одноразово у вигляді монопрофілактики та в комбінації з іншими препаратами.
Основні проблеми сучасної антибіотикотерапії:
- відсутність уведення АМП як стратегічного компоненту підготовки пацієнта до оперативного втручання;
- застосування нераціональних комбінацій АМП, включаючи препарати з категорії спостереження та резерву;
- неадекватно тривале застосування АМП із категорії спостереження та резерву у післяопераційному періоді;
- порушення часових термінів для проведення передопераційної антибіотикопрофілактики;
- застосування протигрибкових препаратів у комбінації з АМП перед оперативним втручанням;
- надзвичайно поширене тривале застосування цефалоспоринів без попереднього введення АМП перед оперативним втручанням.
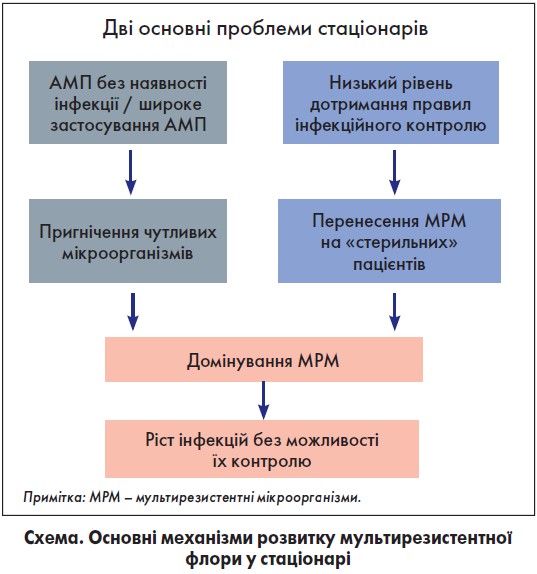
Основні механізми розвитку мультирезистентної флори у стаціонарі представлені на схемі.
Отже, окреслені вище проблеми вказують на необхідність опрацювання механізмів запобігання виникненню мультирезистентності та проведення освітньої роботи серед лікарів.
Проблема антибіотикорезистентності у терапії неонатального сепсису.
Практичні рекомендації фахівця з інтенсивної терапії новонароджених
Завідувач відділення анестезіології та інтенсивної терапії новонароджених КП «Дніпропетровська обласна дитяча клінічна лікарня Дніпропетровської обласної ради», доктор медичних наук Денис Миколайович Сурков.
– Сепсис – загрозлива для життя органна дисфункція, викликана порушенням реакції хворого на інфекцію. Етіологічним чинником розвитку раннього неонатального сепсису перш за все є стрептококи групи В, натомість як збудники пізнього неонатального сепсису не відрізняються від таких будь-якого госпітального сепсису.
Діагностика сепсису у новонароджених має складнощі, оскільки клінічна картина є неспецифічною. Диференціальну діагностику із сепсисом слід проводити у випадку будь-якого порушення загального стану дитини й звертати увагу на наступні діагностичні маркери:
- наявність центральних венозних катетерів;
- тривале перебування у стаціонарі;
- виділення бактеріальної культури із крові, ліквору;
- зміна характеристик сечі (надлобкова пункція), абдомінального і плеврального аспірату;
- зміна кількості лейкоцитів і зсуви лейкоцитарної формули;
- наявність тромбоцитопенії, коагулопатії;
- зміни рівнів С-реактивного білка, прокальцитоніну, інтерлейкіну 6.
Відповідно до настанов Surviving Sepsis Campaign, за наявності септичного шоку емпірична комбінована антибіотикотерапія має передбачати застосування принаймні двох антибіотиків різних класів. Комбіновану терапію не слід призначати рутинно для постійного лікування більшості інфекцій, включаючи бактеріємію та сепсис без шоку. Крім того, не рекомендована вона для рутинного лікування нейтропенічного сепсису/бактеріємії. Тривалість терапії протягом 7-10 днів є достатньою для усунення більшості інфекцій, у т.ч. сепсису та септичного шоку.
Лікування інфекції, викликаної грампозитивними коками, передбачає призначення β-лактамів у випадку, якщо збудник є оксацилін-чутливим, за наявності резистентності рекомендовано використовувати ванкоміцин або лінезолід.
При грибковому сепсисі показаний флуконазол у профілактичному режимі (двічі на тиждень), однак у випадку стійкості недоцільно призначати інші препарати групи азолів. У такій ситуації рекомендованим є використання амфотерицину В або ехінокандинів. Сучасним підходом у профілактиці антибіотикорезистентності є комбінована медикаментозна терапія, оскільки дозволяє розширити спектр дії антибактеріальної терапії у пацієнтів у критичному стані, відкриває можливість до її деескалації й має синергічний ефект, що особливо важливо у випадку полімікробної інфекції.
Для профілактики антибіотикорезистентності необхідне використання комбінацій наступних груп препаратів у високих дозах:
- захищені цефалоспорини 3-го покоління;
- аміноглікозиди 4-го покоління;
- високодозові карбапенеми;
- колістин;
- гліцилциклін.
На фармакологічному ринку України наявні комбіновані препарати, що мають у своєму складі цефтазидим та авібактам. Авібактам інгібує більшість класів бактеріальних ензимів (окрім металопротеїназ) і показаний за наявності продуцентів β-лактамаз розширеного спектра. Оскільки авібактам є новою молекулою, рекомендовано призначати цефтазидим/авібактам у дозуванні, аналогічному такому препаратів цефтазидиму, що становить 50 мг/кг у дітей від 6 міс та 40 мг/кг у дітей від 3 до 6 міс кожні 8 год із тривалістю введення 2 години.
Активність цефтазидиму/авібактаму проти карбапенем-резистентних мікроорганізмів.
Практикум від фахівця лабораторної діагностики
Завідувач бактеріологічної лабораторії НДСЛ «Охматдит» Оксана Михайлівна Головня.
– Безумовно, проблема антибіотикорезистентності надзвичайно актуальна у щоденній лабораторній діагностиці. Скринінг носійства мультирезистентної мікрофлори (МРМ) у 2020 році показав, що 45,5% пацієнтів госпіталізуються у НДСЛ «Охматдит» із наявністю МРМ і за час перебування на лікуванні їх відсоток збільшується до 65-70%.
Основну проблему вибору антибіотиків для лікування являють грамнегативні мікроорганізми, стійкі до карбапенемів, зокрема K. pneumoniae, P. aeruginosa та A. baumannii.
Виходячи з особливостей структури і властивостей цефтазидим/авібактаму, у якому інгібітор не є β-лактамом, цей препарат проявляє активність проти мультирезистентних штамів, продуцентів β-лактамаз розширеного спектра i набутих AmpC, а також продуцентів карбапенемаз класу А (KPC) та класу D (OXA-48). Разом із тим у нього відсутня активність проти штамів, що продукують карбапенемази класу В (метало-β-лактамази) і класу С (за винятком OXA-48).
Було проаналізовано чутливість 271 штаму K. pneumoniae та 178 штамів P. aeruginosa, ізольованих від пацієнтів відділень інтенсивної терапії, хірургічного, педіатричного та онкогематологічного профілів. Штами в діагностичних значеннях виділені з наступних біологічних матеріалів: 59,9% – виділення нижніх дихальних шляхів, 25,4% – виділення інфікованих ранових поверхонь і гною, 11,4% – кров і ліквор та 3,3% – сеча.
У ході аналізу порівняльної активності цефтазидим/авібактаму та колістину проти карбапенем-резистентної K. pneumoniae та P. aeruginosa були отримані наступні результати.
- Резистентність K. pneumoniae до меропенему виявлено у 71,6% штамів, до цефтазидим/авібактаму – у 23,6%. Таким чином, 48% штамів були чутливими до цефтазидим/авібактаму при резистентності до карбапенемів.
- Розглядаючи чутливість цефтазидим/авібактаму та фенотипи карбапенемаз у K. pneumoniae, виявлено, що 93,8% продуцентів КРС та 90,5% продуцентів OXA-48 були чутливі до цефтазидим/авібактаму, натомість у продуцентів метало-β-лактамаз чутливість виявлено лише у 5,5% штамів.
У дану вибірку увійшло 28 штамів K. pneumoniae, стійких до колістину, 75,0% з яких були чутливими до цефтазидим/авібактаму, серед них продуценти OXA-48 склали 19,1%, продуценти КРС – 15,0% та продуценти метало-β-лактамаз – 12,7%. Таким чином, це дає можливість для використання цефтазидим/авібактаму у пацієнтів, інфікованих штамами, що є стійкими до карбапенемів та колістину.
У штамів P. aeruginosa резистентність до меропенему виявлено у 66,3% штамів, до цефтазидим/авібактаму – у 57,9%. Таким чином, 8,4% штамів були чутливими до цефтазидим/авібактаму при резистентності до меропенему.
Усі виявлені штами P. aeruginosа, що продукували метало-β-лактамази, були стійкими до цефтазидим/авібактаму, натомість серед штамів P. aeruginosа з іншими механізмами стійкості (втрата пуринів чи ефлюкс) чутливих виявлено 19,5%. Це вказує на те, що залишається невеликий відсоток стійких до карбапенемів штамів, для яких цефтазидим/авібактам може бути препаратом вибору.
Впровадження сучасних методів визначення чутливості збудників, виявлення фенотипів їх резистентності та аналіз поширення в межах стаціонару дає можливість для прогнозування та проведення успішної антибіотикотерапії у пацієнтів із МРМ.
В умовах зростаючої антибіотикорезистентності дуже важливо дотримуватися правил раціональної антибіотикотерапії, що передбачає врахування не тільки резистентності збудників, а й також фармакодинамічних та фармакокінетичних характеристик препарату. Поширення карбапенем-резистентних штамів мікроорганізмів веде до втрати можливості використання карбапенемів у якості антибіотиків резерву, що значно ускладнює лікування інфекцій. Саме тому цефтазидим/авібактам, зареєстрований для лікування бактеріальних інфекцій, викликаних грамнегативними збудниками, у рамках карбапенем-зберігаючої стратегії має бути препаратом вибору у відділеннях, де кількість карбапенем-резистентних штамів складає/перевищує 20%.
Тематичний номер «Хірургія, Ортопедія, Травматологія, Інтенсивна терапія» № 3 (46), 2021 р.