15 березня, 2025
Принципи використання жарознижувальних засобів у пацієнтів різного віку
 Гарячка – це стан організму, який характеризується високою температурою тіла (>38 °C), що визначається при проведенні вимірювання термометром у пахвовій ділянці. Гарячка відрізняється від гіпертермії принципово іншим механізмом розвитку. З погляду сучасної української мови термін «лихоманка» не слід використовувати в професійній медичній термінології. Необхідно послуговуватися саме терміном «гарячка», оскільки лихоманка є патофізіологічним механізмом, який допомагає організму боротися насамперед з інфекцією. При гарячці температура тіла перевищує норму. Зазвичай це означає, що в організмі відбуваються аномальні процеси. Фізичні вправи, спекотна погода та звичайне щеплення також можуть спричинити підвищення температури тіла.
Гарячка – це стан організму, який характеризується високою температурою тіла (>38 °C), що визначається при проведенні вимірювання термометром у пахвовій ділянці. Гарячка відрізняється від гіпертермії принципово іншим механізмом розвитку. З погляду сучасної української мови термін «лихоманка» не слід використовувати в професійній медичній термінології. Необхідно послуговуватися саме терміном «гарячка», оскільки лихоманка є патофізіологічним механізмом, який допомагає організму боротися насамперед з інфекцією. При гарячці температура тіла перевищує норму. Зазвичай це означає, що в організмі відбуваються аномальні процеси. Фізичні вправи, спекотна погода та звичайне щеплення також можуть спричинити підвищення температури тіла.
Гарячка представляє собою захисно-пристосувальну реакцію організму, що виникає у відповідь на дію патогенних подразників. Для неї є характерною перебудова процесів терморегуляції, що призводить до підвищення температури тіла і стимулює природну реактивність організму. Саме гарячка є одним із найчастіших симптомів у дітей і становить приблизно третину від усіх випадків у клінічній практиці лікаря-педіатра. З нею пов’язане широке використання безрецептурних антипіретиків. Про це свідчать рекомендації Американської академії педіатрії (2011).
У педіатрії ібупрофен є найкраще вивченим і найчастіше застосовуваним нестероїдним протизапальним засобом (НПЗП) у лікуванні гарячки та больового синдрому. Крім того, це єдиний НПЗП, схвалений для лікування дітей віком >6 міс. Знеболювальний, протизапальний та антипіретичний ефекти ібупрофену вивчені в дітей із травмами й іншими м’язово-скелетними патологічними станами, після тонзилектомії та/або аденектомії чи інших хірургічних втручань тощо.
Після завершення первинного патенту в 1985 р. на фармацевтичний ринок світу вийшла значна кількість генеричних препаратів ібупрофену (Kuchar E. et al., 2014). Наразі світовий обсяг виробництва ібупрофену становить у межах 15 000 т/рік. Ібупрофен виробляють у таких лікарських формах, як таблетки, капсули, сиропи. Рідка форма ібупрофену 200 мг у м’яких капсулах, яку можна застосовувати в дітей із масою тіла >20 кг (приблизно з віку 6 років), набуває усе більшої популярності через полегшене всмоктування, кращу біодоступність малорозчинної активної речовини та вищі показники прихильності до лікування (Dousa M. et al., 2017).
Важливість фармакокінетики: таблетки чи капсули?
Для більшості аналгетиків, включаючи ібупрофен, стартове зростання концентрації активної речовини в плазмі крові після перорального прийому є ключовим фактором у визначенні часу до початку знеболювальної дії. Ібупрофен досить швидко всмоктується, досягаючи пікової концентрації у плазмі та максимального аналгетичного ефекту вже через 1,5-2 год після вживання. Концентрація ібупрофену корелює зі ступенем знеболювання та жарознижувальним ефектом.
Отже, для пероральних форм ібупрофену швидке всмоктування має ключове значення (Dewland P.M. et al., 2009). Фармакокінетичні характеристики (максимальна концентрація, час до її досягнення, площа під кривою «концентрація – час») ібупрофену залежать від лікарської форми. Загалом розчинні форми ібупрофену забезпечують швидше та краще усунення болю; натомість сповільнене всмоктування або менша концентрація активної речовини в плазмі крові можуть зумовити невдачу в лікуванні (Shin D. et al., 2017).
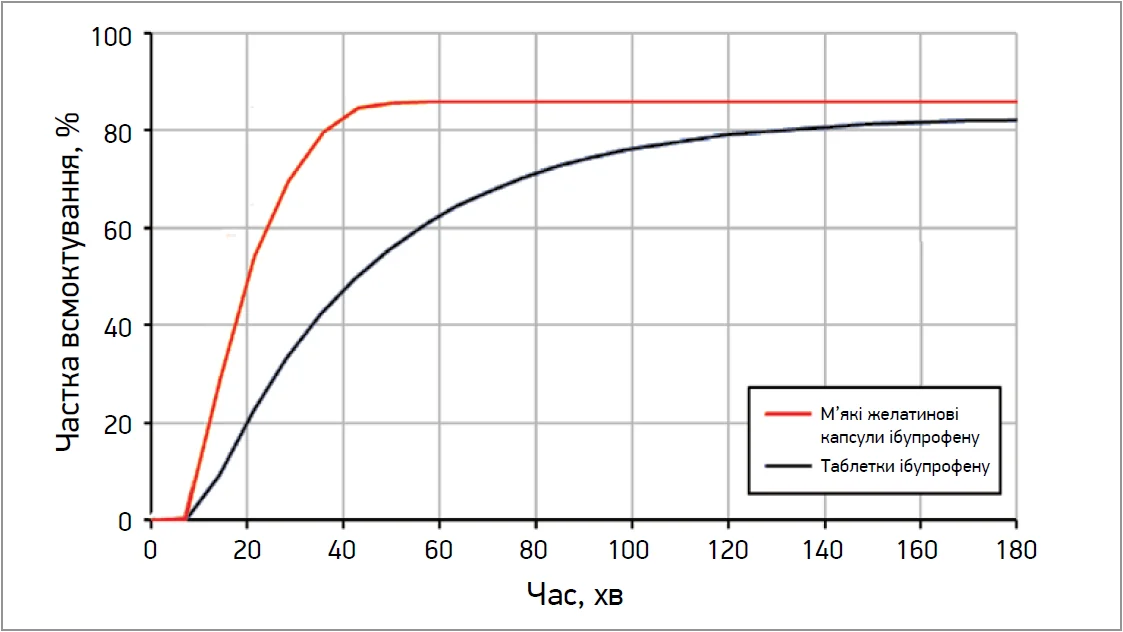
Відповідно до біофармацевтичної класифікації, ібупрофен належить до класу ІІа, тобто до препаратів із низькою розчинністю та високою проникністю. Такі сполуки погано розчиняються в кислому середовищі шлунка, де їхні молекули наявні в неіонізованій формі вільних кислот. Однак після іонізації сполуки класу ІІа, зокрема ібупрофен, легко розчиняються при вищих показниках рН тонкого кишечнику, що в поєднанні з високою здатністю до проникнення в біологічні тканини забезпечує повне або майже повне всмоктування. Експериментальне дослідження показало, що рідкий ібупрофен у м’яких желатинових капсулах забезпечує не лише швидшу абсорбцію активної речовини, а й більший відсотковий обсяг усмоктування (рис. 1) (Katona M.T. et al., 2023).
Рис. 1. Відсоткова частка всмоктування активної речовини з м’яких желатинових капсул і таблеток ібупрофену
У рандомізованому перехресному дослідженні було показано, що медіана часу до досягнення максимальної концентрації для рідкого ібупрофену в м’яких желатинових капсулах становила 0,5 год, а для звичайного таблетованого – 1,25 год, що є свідченням достовірно швидшої дії капсульованого ібупрофену.
Крім того, ібупрофен у м’яких капсулах забезпечував вищу максимальну концентрацію активної речовини в плазмі крові – 119,1% порівняно зі стандартним препаратом (рис. 2).
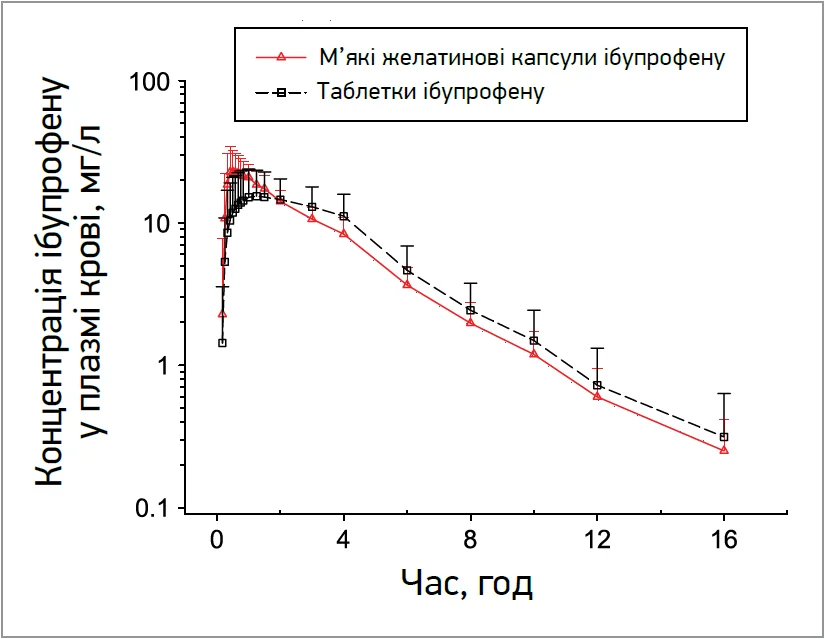 Рис. 2. Профіль «час – концентрація» для рідкого ібупрофену в м’яких капсулах і стандартного таблетованого ібупрофену
Рис. 2. Профіль «час – концентрація» для рідкого ібупрофену в м’яких капсулах і стандартного таблетованого ібупрофену
Це має велике значення для клінічної медицини, оскільки відомо, що концентрація ібупрофену прямо корелює з його знеболювальною ефективністю. Автори також зазначили, що через 8 год після вживання препарату інгібування простагландину E2 в групі рідкого ібупрофену в м’яких капсулах становило 18,4%, а в групі стандартного ібупрофену – лише 11,6% (рис. 3).
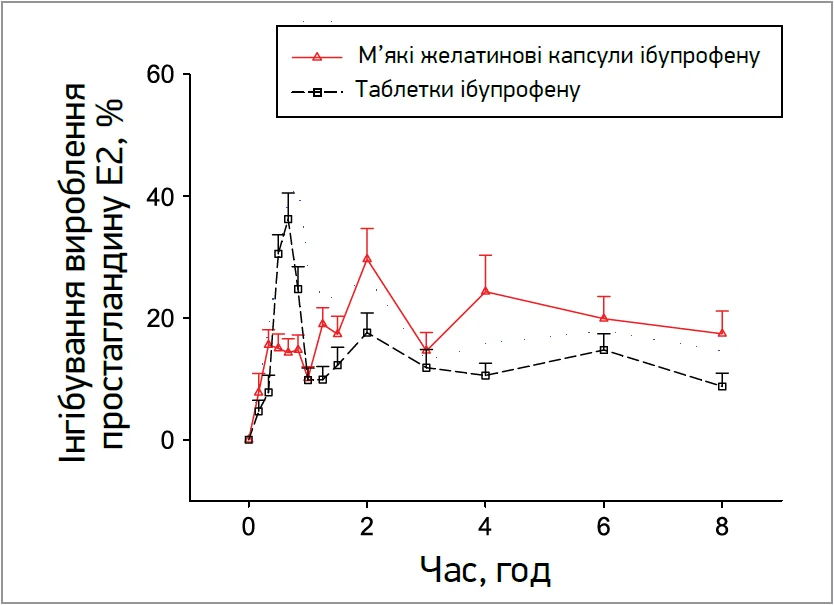 Рис. 3. Відсоткова частка інгібування вироблення простагландину Е2 порівняно з початковим рівнем через 0-8 год після прийому 200 мг рідкого ібупрофену в м’яких капсулах і стандартного таблетованого ібупрофену
Рис. 3. Відсоткова частка інгібування вироблення простагландину Е2 порівняно з початковим рівнем через 0-8 год після прийому 200 мг рідкого ібупрофену в м’яких капсулах і стандартного таблетованого ібупрофену
Отже, рідкий ібупрофен швидкої дії у формі м’яких желатинових капсул забезпечує швидше всмоктування та вищу пікову концентрацію порівняно зі стандартною таблетованою формою препарату. Такий інгібувальний вплив цієї форми на циклооксигеназу-2 є потужнішим (Shin D. et al., 2017).
Переваги рідкого ібупрофену в м’яких желатинових капсулах було підтверджено і в метааналізі 22 клінічних досліджень. Автори з’ясували, що саме рідкий ібупрофен забезпечував вираженіше зниження болю та більший жарознижувальний ефект порівняно з таблетованим через 60, 90 та 120 хв після вживання препарату (Lawati H., Jamali F., 2016).
Переваги м’яких желатинових капсул Clear Caps
Капсули для перорального застосування характеризуються хорошою прихильністю пацієнтів до лікування, оскільки є легкими для ковтання та маскують неприємний смак і запах активного інгредієнта.
Крім того, в разі застосування капсул пацієнт не може самостійно зменшити призначену дозу препарату. Рідкий уміст капсули забезпечує більшу гомогенність активної речовини порівняно з іншими твердими лікарськими формами, а також полегшує усмоктування погано розчинних медикаментів, підвищує їхню біодоступність та зменшує варіабельність концентрації активної речовини в плазмі крові.
Ці ефекти дозволяють застосовувати меншу дозу порівняно з таблетками чи капсулами із твердим умістом. Варто зауважити, що при виробництві капсул із рідким умістом шкода для довкілля є меншою.
До того ж, оскільки виробництво цих капсул – єдиний технологічний процес, під час якого активна речовина герметично інкапсулюється в еластичній оболонці, працівники фармацевтичного заводу менше контактують з активною речовиною порівняно з виробництвом таблеток або капсул із твердим порошкоподібним умістом (Naharros-Molinero A. et al., 2023).
Додатковою перевагою капсульної лікарської форми є те, що виробництво капсул передбачає використання меншої кількості допоміжних речовин і не потребує застосування компресії, яка може ушкодити структуру складників таблетки (Kruk K., Winnicka K., 2024).
Під час обрання ібупрофену в капсулах слід звернути увагу і на саму капсулу. Так, деякі капсули містять шкідливі допоміжні речовини; натомість технологія виготовлення капсул Clear Caps робить їх безпечнішими для організму людини.
Желатинові капсули використовуються в усьому світі вже >100 років, їхня безпека добре вивчена. На відміну від синтетичних матеріалів для капсул, желатин – це речовина природного походження, яка утворюється під час гідролізу колагену. За хімічною структурою желатин – це біополімер, який на 84-90% складається з водорозчинних білків, на 1-2% – із мінеральних солей і на 8-15% – із води (Prakash A. et al., 2017; Naharros-Molinero A. et al., 2023). Желатинові капсули вважаються однією із найстабільніших лікарських форм, оскільки желатинова оболонка надійно захищає активну речовину від таких зовнішніх чинників, як температура або вологість. Оболонка м’яких желатинових капсул містить переважно сам желатин (40-45%), воду та нелетючі речовини-пластифікатори (Naharros-Molinero A. et al., 2023).
Небезпеки допоміжних речовин у лікарській формі сиропу
В педіатрії ключове значення має прийнятний смак лікарського засобу, оскільки саме незадовільні смакові властивості є ключовою перешкодою до прихильності дітей до лікування. Водночас більшість активних фармацевтичних інгредієнтів мають неприємний смак. У випадку лікарських форм для дорослих препарат покривають плівковою оболонкою, але в педіатрії таку тактику унеможливлює часта дисфагія, тому на перший план виходять рідкі пероральні форми. У випадку цих форм маскування смаку є особливо важливим. З цією метою застосовуються різноманітні допоміжні речовини (Walsh J. et al., 2014).
Зазвичай до складу лікарського засобу включають декілька різних допоміжних речовин, що значно підвищує ризик непереносимості та реакцій гіперчутливості (Reker D. et al., 2019). Поширеною лікарською формою в педіатрії виступають сиропи – рідини з підсолоджувачами, барвниками та загущувачами, які зазвичай являють собою майже насичені розчини сахарози. Форма сиропу потребує маскування смаку діючої речовини та включення консервантів (Rouaz K. et al., 2021). Наприклад, один із видів сиропу парацетамолу містить пропіленгліколь, метилгідроксибензоат, пропілгідроксибензоат, ксантанову камідь, розчин сорбітолу 70%, сахарозу, ароматизатор.
Слід зазначити, що фармацевтичні компанії не завжди розкривають повний список допоміжних речовин (Lee Q.U. et al., 2017). За даними дослідження К. Зупанець та співавт. (2021), лише один з 22 проаналізованих фітомуколітичних сиропів не містив жодних потенційно шкідливих речовин. Автори зазначають, що лікарі та фармацевти більше турбуються про основні діючі речовини препаратів, не звертаючи уваги на допоміжні речовини, які не є абсолютно неактивними і здатні провокувати небажані реакції.
Кожній допоміжній речовині притаманний особливий профіль ризику. Так, вживання препаратів, які містять сахарозу, слід уникати особам із цукровим діабетом 1 типу та спадковою непереносимістю фруктози, крім того, сахароза може сприяти карієсу й ожирінню. Аспартам не можна вживати за наявності фенілкетонурії; він також спричиняє алергічні реакції, кропив’янку, ангіонабряк. Бензоат і цитрат натрію потенційно здатні підвищувати артеріальний тиск (Bobillot M. et al., 2024). Таких підсолоджувачів, як цикламат і сахарин, слід уникати дітям з алергією на сульфонамідні засоби (Walsh J. et al., 2014).
Небезпечними можуть бути й хімічні барвники. Наприклад, тартразин провокує у схильних осіб анафілаксію, бронхоспазм та ангіонабряк. Загалом до складу приблизно третини лікарських засобів входить щонайменше один барвник, асоційований з розвитком алергічних реакцій (Rouaz K. et al., 2021; Reker D. et al., 2019). Реакції гіперчутливості можуть виникати й у відповідь на азобарвники, зокрема метиловий оранжевий, метиловий червоний, Судан І, Судан ІІІ, Конго червоний (Soremekun R. et al., 2019).
Знеболювальні сиропи і сиропи для лікування кашлю, застуди та алергії можуть бути джерелом червоного барвника № 40 і не лише при хронічному чи субхронічному, а й при епізодичному застосуванні. За тривалого вживання таких сиропів надходження барвника до організму може значно перевищувати допустимі показники, встановлені для дітей FDA. Варто зауважити, що для деяких барвників продемонстровано зв’язок із синдромом дефіциту уваги і гіперактивністю (Lehmkuhler A.L. et al., 2020), який нерідко діагностують у сучасних дітей та навіть дорослих.
Деякі допоміжні речовини, які можна безпечно застосовувати в дорослій популяції, наприклад бензиловий спирт, етанол, пропіленгліколь, парабени, характеризуються підвищеним токсикологічним ризиком для дітей, навіть у разі застосування в адаптованих до віку нижчих концентраціях (Buckley L.A. et al., 2017).
Окрім широкого спектра допоміжних речовин, у випадку рідких лікарських форм (сиропів, суспензій) небезпеку становить помилка у дозуванні. Так, аналіз даних великої бази даних США за 2009-2016 рр. виявив 4756 випадків побічних явищ, спричинених препаратами для лікування кашлю та застуди. З них 10,8% (513) випадків були зумовлені помилкою у дозуванні, причому в 45,8% випадків помилка стосувалася дітей віком 2-6 років (Wang G.S. et al., 2020). За результатами опитування, 76% матерів давали дітям удвічі більшу дозу, ніж потрібно (Kigen G. et al., 2015). Інше дослідження виявило, що 84,4% батьків та доглядальників зробили щонайменше одну помилку, відмірявши 9 доз препарату у формі сиропу за допомогою мірної чашки або шприца (Yin N.S. et al., 2016).
Отже, під час обрання фармакологічного препарату необхідно враховувати не лише активну речовину, а й лікарську форму та вміст допоміжних речовин. У педіатрії перевагу доцільно віддавати засобам з мінімальною кількістю та концентрацією допоміжних речовин, а також у максимально зручній формі, яка виключає/мінімізує імовірність помилки дозування.
Гофен – сучасний ібупрофен у м’яких желатинових капсулах
Гофен 200 («Мега Лайфсайенсіз», Таїланд) – рідкий ібупрофен швидкої дії в невеликих м’яких желатинових капсулах, які легко ковтати. До складу капсул Гофену, вироблених за технологією Clear Caps, входять лише желатин, розчин сорбіту та очищена вода. Вмістом капсули є прозора безбарвна масляниста рідина, оскільки Гофен не містить барвників і консервантів, що дозволяє зменшити ймовірність небажаних побічних явищ. Застосування цього препарату дозволено дітям із масою тіла >20 кг.
Низька біодоступність ібупрофену у водному середовищі та преципітація активної речовини при контакті навіть з незначною кількістю води несприятливо впливає на всмоктування препарату. З метою подолання цієї проблеми до вмісту капсули додають гідрофільні речовини-носії, зокрема поліетиленгліколь (ПЕГ). Слід зауважити, що застосування ПЕГ низької молекулярної маси (ПЕГ 200, ПЕГ 300) у вмісті капсули обмежене, оскільки ці речовини здатні дифундувати в оболонку капсули та діяти як пластифікатори. Ступінь дифузії ПЕГ із вмісту в оболонку зменшується паралельно зі збільшенням молекулярної маси речовини. Застосування ПЕГ дозволяє підвищити розчинність ібупрофену на 40-400% (Lodha A. et al., 2012). Саме ПЕГ є однією з допоміжних речовин умісту капсул Гофену, що забезпечує цьому препарату високий ступінь розчинності.
Доза 200 мг дозволяє з легкістю застосовувати Гофен для дорослих і дітей з різною масою тіла. Так, для дорослих і дітей із масою тіла ≥40 кг рекомендована початкова доза становить 1-2 капсули, згодом (за потреби) – по 1-2 капсули (200-400 мг ібупрофену) кожні 4-6 год. Не слід застосовувати >6 капсул протягом доби. Для дітей із масою тіла 30-39 кг рекомендована початкова доза становить 1 капсулу, максимальна добова доза – 4 капсули, а для дітей із масою тіла 20-29 кг – також 1 капсулу, натомість максимальна добова доза – 3 капсули. Гофен доцільно приймати під час вживання їжі, не розжовуючи та запиваючи водою.



 Дуда О.К.
Дуда О.К.