24 березня, 2025
Від наукових досліджень до клінічної практики: оновлення стандартів діагностики та лікування на основі даних доказової медицини
За матеріалами навчального циклу «Академія сімейного лікаря»
11-12 березня в рамках навчального циклу «Академія сімейного лікаря» відбувся майстер-клас, у ході якого розглядалися шляхи впровадження наукових досліджень у клінічну практику. Під час заходу лікарі широкого кола спеціальностей ознайомилися з доповідями відомих вітчизняних експертів щодо профілактики та лікування різних патологічних порушень. Було представлено нові напрями у формуванні здоров’я людини, розглянуто захворювання, що супроводжуються болем, та багато іншої корисної інформації.
Безпечне й ефективне застосування НПЗП у сучасній медицині
 Професор кафедри терапії Української військової медичної академії Міністерства оборони України (м. Київ), кандидат медичних наук Мар’яна Миколаївна Селюк у своєму виступі закцентувала увагу на безпеці й ефективності застосування нестероїдних протизапальних препаратів (НПЗП) у сучасній медицині.
Професор кафедри терапії Української військової медичної академії Міністерства оборони України (м. Київ), кандидат медичних наук Мар’яна Миколаївна Селюк у своєму виступі закцентувала увагу на безпеці й ефективності застосування нестероїдних протизапальних препаратів (НПЗП) у сучасній медицині.
НПЗП – група різних за хімічною структурою лікарських препаратів (переважно похідні кислот), що мають протизапальну, аналгезивну та жарознижувальну дію. Основний вплив НПЗП полягає у блокуванні ферменту циклооксигенази (ЦОГ), що обумовлює позитивні клінічні ефекти препаратів цієї групи, тоді як причини ускладнень певною мірою залишалися загадкою до кінця минулого сторіччя. Саме тоді було виділено другий (згодом і третій) тип ЦОГ, крім того, встановлено, що пригнічення «патологічної» ЦОГ‑2 обумовлює вплив на всі ланки запального процесу, пригнічуючи біль та запалення і відновлюючи функцію. Своєю чергою, пригнічення «фізіологічної» ЦОГ‑1 гальмує захисні реакції: виникає кровоточивість через вплив на згортання крові; з’являються ерозії та виразки через порушення цілісності слизової оболонки, зниження функції нирок – за рахунок порушення в них кровотоку. Водночас дезагрегантні властивості ацетилсаліцилової кислоти використовують і сьогодні. В низьких дозах вона діє як дезагрегант і лише в дозі >500 мг діє як неселективний блокатор ЦОГ, виявляючи протизапальний вплив.
Класифікація НПЗП залежно від ступеня пригнічення ізоферментів ЦОГ представлена в таблиці 1.
|
Таблиця 1. Класифікація НПЗП залежно від ступеня пригнічення ізоферментів ЦОГ |
|||
|
Переважне пригнічення ЦОГ‑1 |
Приблизно однакове інгібування ЦОГ‑1 та ЦОГ‑2 |
Переважне пригнічення ЦОГ‑2 |
Специфічне інгібування ЦОГ‑2 |
|
Ацетилсаліцилова кислота Індометацин Напроксен Ібупрофен Кетопрофен |
Диклофенак Ациклофенак Піроксикам |
Німесулід Мелоксикам |
Целекоксиб Еторикоксиб |
Різні представники групи НПЗП мають різний протизапальний, аналгезивний, жарознижувальний і, що дуже важливо, хондропротекторний ефекти. За тривалістю прийому розрізняють короткочасне та хронічне (≥4 тиж) застосування. Короткочасне застосування НПЗП або в режимі за потреби рекомендоване, наприклад, для купіювання гострого неспецифічного болю в спині, гострого нападу подагри, загострення остеоартриту, коли в пацієнтів наявний інтенсивний больовий синдром.
Доволі жорсткі підходи до тривалості застосування препаратів зумовлені насамперед можливістю шлунково-кишкових кровотеч. Це обумовило розробку більш селективних інгібіторів ЦОГ‑2, які не чинять підвищеного негативного впливу на шлунково-кишковий тракт (ШКТ), але виявилося, що зі збільшенням цієї селективності можуть збільшуватися також кардіоваскулярні ризики. Саме тому під час обрання препарату групи НПЗП слід зважувати ті чи інші ризики.
До факторів ризику виникнення НПЗП-гастропатій належать:
- виразка шлунка та дванадцятипалої кишки з ускладненнями в анамнезі;
- прийом ≥2 НПЗП і глюкокортикоїдів;
- супутній прийом ацетилсаліцилової кислоти й антикоагулянтів;
- супутній прийом селективних інгібіторів зворотного захоплення серотоніну;
- інфекція Helicobacter pylori;
- вік >60 років;
- куріння;
- диспепсія в анамнезі.
Вибір НПЗП здійснюють залежно від гастроінтестинального ризику (табл. 2).
|
Таблиця 2. Вибір НПЗП залежно від гастроінтестинального ризику |
||
|
Гастроінтестинальний ризик |
Визначення |
Вибір НПЗП |
|
Низький |
Відсутні фактори ризику |
Будь-які НПЗП |
|
Помірний |
Наявний хоча б один із нижчезазначених факторів ризику:
|
Неселективні НПЗП + інгібітори протонної помпи або монотерапія селективними / високоселективними НПЗП |
|
Високий |
Наявний хоча б один із нижчезазначених факторів ризику:
|
Селективні / високоселективні НПЗП + інгібітори протонної помпи |
За лікування пацієнтів із високим серцево-судинним ризиком необхідно дуже виважено ставитися до застосування НПЗП, особливо тривалого (табл. 3).
|
Таблиця 3. Алгоритм призначення НПЗП залежно від серцево-судинного ризику [1] |
||
|
Серцево- |
Визначення |
Вибір НПЗП |
|
Дуже високий |
|
Уникати хронічного застосування НПЗП |
|
Високий |
Спостерігають такі показники:
|
Застосовувати НПЗП з обережністю – в мінімальних дозах і нетривалим курсом |
|
Помірний |
|
Застосовувати з обережністю будь-які НПЗП |
|
Низький |
|
Застосовувати будь-які НПЗП |
Серед препаратів групи НПЗП золотим стандартом вважають диклофенак. Із метою покращення переносимості з боку ШКТ у 1991 р. був синтезований ацеклофенак – похідне диклофенаку. За механізмом дії ацеклофенак займає проміжне положення між неселективними НПЗП і високоселективними інгібіторами ЦОГ.
Встановлено, що ацеклофенак перевершує диклофенак за вираженістю аналгезивної дії у пацієнтів із гострим болем. Так, його переваги перед диклофенаком продемонстровані в систематичному огляді проспективних порівняльних досліджень. До аналізу було включено 9 досліджень, у т. ч. за участю пацієнтів з остеоартритом, ревматоїдним артритом, різними захворюваннями опорно-рухового апарату, болем у попереку та болем після видалення зуба. Ацеклофенак перевершував диклофенак за ефективністю або не поступався йому, а також мав перевагу щодо переносимості [2].
Для оцінки знеболювальної ефективності ацеклофенаку та задоволеності терапією проведено багатоцентрове європейське дослідження (Австрія, Бельгія, Німеччина, Греція) за участю 23 407 пацієнтів із болем, спричиненим різними запальними або дегенеративними ревматологічними захворюваннями. Причиною призначення ацеклофенаку в понад половини випадків було незадоволення пацієнтів попередньою терапією іншими НПЗП [3]. До кінця дослідження стан хворих (параметр, що включає як знеболювальну ефективність, так і переносимість) оцінювався пацієнтами й лікарями як такий, що «значно покращився» або «покращився», у 84% випадків. Частина пацієнтів спостерігала зменшення сильного болю із 41 до 2% при застосуванні ацеклофенаку. Результати були схожими в різних країнах і не залежали від наявності гострого чи хронічного болю. Задоволеність пацієнтів ацеклофенаком і показники прихильності виявилися однаково вражаючими: 90% пацієнтів були задоволені терапією та >90% дотримувалися схеми лікування.
У великому метааналізі 44 рандомізованих контрольованих досліджень із загальною кількістю 19 045 пацієнтів з остеоартритом до 3 найефективніших НПЗП із найбільшою вираженістю знеболювального ефекту належать ацеклофенак, еторикоксиб, целекоксиб [4].
Результати іншого дослідження продемонстрували сприятливий вплив ацеклофенаку на метаболізм протеогліканів і гіалуронової кислоти в хрящовій тканині в пацієнтів із тяжким та помірним остеоартритом, якого не спостерігали після прийому диклофенаку. Встановлено, що ацеклофенак не чинить значного впливу на проліферацію клітин сухожиль на відміну від індометацину та напроксену, які пригнічують поділ клітин, що обумовлює вибір ацеклофенаку при лікуванні болю після травм сухожиль і хірургічних втручань [5].
Після отримання цих даних НПЗП було розподілено на 3 групи:
- ті, що стимулюють синтез позаклітинного матриксу;
- ті, що не мають впливу на позаклітинний матрикс;
- ті, що пригнічують синтез хрящового матриксу.
Більшість НПЗП належать до 2 або 3 груп, тоді як ацеклофенак має значний позитивний вплив на синтез глікозаміногліканів і колагену в хрящах пацієнтів з остеоартритом та ревматоїдним артритом.
Властивості ацеклофенаку:
- пригнічення синтезу цитокінів;
- інгібування інтерлейкінів;
- інгібування фактора некрозу пухлини;
- вплив на молекули адгезії нейтрофілів;
- синтез глікозаміногліканів;
- синтез 4-гідроксиацеклофенаку, який бере участь у хондропротекції.
Отже, яким безпечним буде препарат за таких потужних клінічних позицій? Установлено, що за частотою кровотеч у верхніх відділах ШКТ серед різних НПЗП ацеклофенак є відносно безпечним, також він є вдалим вибором, якщо йдеться про тяжкі побічні реакції з боку печінки, нирок, прояви з боку шкіри [6]. Що стосується впливу на госпіталізацію через серцеву недостатність, то ацеклофенак може бути НПЗП вибору в пацієнтів, у яких наявна серцево-судинна патологія [7].
Результати численних рандомізованих клінічних досліджень та метааналізів підтверджують високу аналгезивну і протизапальну активність, хорошу переносимість, сприятливе співвідношення «користь/ризик» ацеклофенаку, що свідчить про доцільність його широкого застосування як лікарського засобу першої лінії при поширених захворюваннях суглобів, а також хребта. Рекомендована доза препарату ацеклофенаку Аертал® становить 100 мг (1 таблетка) 2 р/добу (максимальна рекомендована доза – 200 мг/добу).
«Від скарг до клінічних рішень»: говоримо про міорелаксанти
 Професор кафедри клінічної фармакології Інституту підвищення кваліфікації спеціалістів фармації Національного фармацевтичного університету (м. Харків), доктор медичних наук Наталія Володимирівна Бездітко представила доповідь, присвячену особливостям застосування такої украй важливої групи лікарських засобів, як міорелаксанти.
Професор кафедри клінічної фармакології Інституту підвищення кваліфікації спеціалістів фармації Національного фармацевтичного університету (м. Харків), доктор медичних наук Наталія Володимирівна Бездітко представила доповідь, присвячену особливостям застосування такої украй важливої групи лікарських засобів, як міорелаксанти.
Спастичність – це аномальне напруження м’язів через їхнє тривале скорочення; виникає через відсутність гальмування мотонейронів і пов’язана з підвищеною активністю збуджувальних нейромедіаторів або зниженою активністю гальмівних нейромедіаторів. Спазм м’язів – це мимовільні локальні скорочення м’язів, що виникають унаслідок гострої травми чи м’язової перенапруги. В усьому світі через спастичність страждає >12 млн людей.
Спастичність м’язів спостерігають за дитячого церебрального паралічу, розсіяного склерозу, інсульту, травматичного ушкодження головного чи спинного мозку. Спазм м’язів – одна з основних причин такого поширеного стану, як біль у спині. Основними симптомами є постійна скутість, спазми та мимовільні скорочення м’язів, болючість м’язів, проблеми з ходьбою (хворому складно ходити чи виконувати певні рухові завдання).
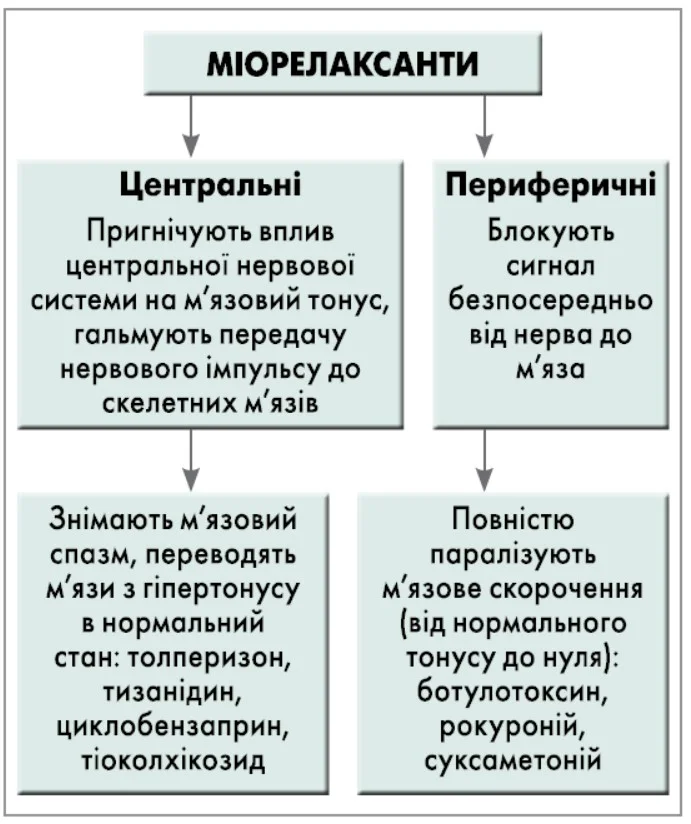
Важливим компонентом лікування спастичності є міорелаксанти – група лікарських засобів із декількох різних хімічних класів, із різними механізмами дії (рис.).
Рис. Міорелаксанти – засоби, що розслаблюють поперечно-смугасті м’язи та знижують тонус скелетних м’язів
Під час обрання оптимального міорелаксанту необхідно обов’язково враховувати індивідуальні характеристики пацієнта (особливо в осіб літнього віку з коморбідною патологією).
Важливі властивості препарату:
- ефективне зменшення м’язового спазму;
- зменшення больового синдрому;
- відсутність надлишкової м’язової слабкості;
- відсутність седативної дії;
- безпека тривалого / періодичного застосування;
- можливість безпечного поєднання з іншими лікарськими препаратами;
- наявність як ін’єкційних, так і пероральних лікарських форм;
- доказова база щодо ефективності та безпеки застосування.
Саме із цього кута зору доповідачка запропонувала подивитися на добре відомий препарат Мідокалм (толперизон) – міорелаксант центральної дії для лікування спастичності центрального (наприклад, при розсіяному склерозі, бічному аміотрофічному склерозі, інсульті) та периферичного генезу (наприклад, за люмбоішіалгії, артриту). У клінічній практиці толперизон застосовують протягом >60 років [8].
Хімічна структура толперизону схожа на таку лідокаїну. Препарат має високу афінність до нервової тканини, досягаючи найбільшої концентрації у стовбурі головного мозку, спинному мозку та периферичній нервовій системі. Толперизон дозозалежно гальмує активність потенціалозалежних натрієвих каналів, потенціалозалежних кальцієвих каналів, вихід нейромедіатора ацетилхоліну, крім того, як і лідокаїн чинить мембраностабілізувальну дію, знижує електричну збудливість рухових нейронів і первинних аферентних волокон. Також толперизон сприяє зменшенню нейропатичного болю шляхом зниження чутливості больових рецепторів і гальмування передачі ноцицептивних імпульсів. На відміну від інших основних представників класу толперизону, крім міорелаксувального ефекту, притаманні знеболювальний та місцево анестезувальний вплив. Толперизон (Мідокалм) надає комплексну терапевтичну дію при спастичності: зменшує м’язовий спазм, усуває біль, покращує кровообіг, перешкоджаючи хронізації болю.
Ефективність толперизону вивчали за різних клінічних станів і захворювань: біль у попереку, спастичність після церебрального інсульту, хворобливий рефлекторний м’язовий спазм (включаючи біль у попереку), захворювання периферичних судин, розсіяний склероз.
Згідно з інструкцією до застосування препарат показаний:
- у разі наявності м’язової спастичності, включаючи постінсультну спастичність, у випадках, коли ін’єкційна форма є методом вибору;
- для симптоматичного лікування м’язового спазму в дорослих після перенесеного інсульту.
Підтверджено ефективність препарату щодо м’язового тонусу та больового синдрому, при цьому пацієнти спостерігають задоволення ефектом, тобто це не лише об’єктивна реєстрація з боку лікарів, а й суб’єктивне відчуття покращення в пацієнтів.
Доведено, що комбінація НПЗП і антиспастичних засобів є дієвішою при гострому неспецифічному болю в спині [9]. Додавання толперизону до НПЗП суттєво покращує стан хворих із болем у спині, впливає на тривалість лікування болю і термін непрацездатності. Існують докази рівня 1B щодо доцільності застосування толперизону для зменшення спастичності та прискорення процесу одужання після інсульту [10].
Дослідження щодо безпеки свідчать про хорошу переносимість препарату з мінімальними протипоказаннями, що надає можливість його широкого застосування, включаючи пацієнтів похилого віку із супутніми захворюваннями [11, 12].
Отже, толперизон (Мідокалм) має багатокомпонентний механізм дії на спастичність та больовий синдром, поєднуючи 3 ефекти: міорелаксувальний, знеболювальний та місцевоанестезувальний. Препарат чинить позитивний вплив на периферичний кровообіг. Седативний ефект за його застосування практично відсутній. Мідокалм представлений у різних лікарських формах: ін’єкції, таблетки. Препарат має тривалий досвід клінічного застосування та численні докази щодо клінічної ефективності (післяінсультна спастичність) і безпеки.
Список літератури знаходиться в редакції.
Підготувала Віталіна Хмельницька
Медична газета «Здоров’я України 21 сторіччя» № 5 (591), 2025 р