8 грудня, 2020
Потенційні можливості лікування COVID-19: протидія надмірному запаленню, антиоксидантний вплив і цитопротекція
 Зважаючи на небезпеку пандемії, що й досі не стихає, існує потреба в розробленні нових схем лікування коронавірусної хвороби (COVID-19), у тому числі в переосмисленні вже знайомих, добре вивчених препаратів і застосуванні їх у новому контексті.
Зважаючи на небезпеку пандемії, що й досі не стихає, існує потреба в розробленні нових схем лікування коронавірусної хвороби (COVID-19), у тому числі в переосмисленні вже знайомих, добре вивчених препаратів і застосуванні їх у новому контексті.
Причиною мультиорганного пошкодження та смерті при тяжких випадках COVID-19 є надмірне та некероване вивільнення певних прозапальних цитокінів і хемокінів (Huang C. et al., 2020), тому зменшення цієї агресивної запальної відповіді потенційно здатне знизити смертність і пошкодження органів.
На думку S. E. Reznik і співавт. (2020), препаратом, який може протидіяти запаленню при COVID‑19, є едаравон (як у вигляді монотерапії, так і в комбінації з одним або кількома противірусними препаратами). Відповідно до інструкції для медичного застосування, едаравон уводиться внутрішньовенно з метою лікування бічного аміотрофічного склерозу й інфаркту мозку в гострій фазі. Едаравон є ліпофільною речовиною, що легко проникає в низку тканин організму та має значну антиоксидантну та протизапальну активність (Watanabe T. et al., 2008). Системне призначення едаравону сприяє протекторній протизапальній дії в експериментальних моделях хімічного пошкодження легень, нирок, кишечнику, підшлункової залози, мозку та печінки (Kikuchi K. et al., 2012). Едаравон також здатен знижувати вміст певних цитокінів (інтерлейкінів (ІЛ) 2, 6, 1β, фактора некрозу пухлини), хемокінів (ІЛ‑8, моноцитарного хемоатрактантного білка‑1, макрофагального запального білка‑1α тощо), печінкових ферментів, активних форм кисню (АФК) й оксиду азоту – NO (Kikuchi K. et al., 2012).
Ефективність едаравону при COVID‑19 доцільно довести в подвійному сліпому рандомізованому плацебо-контрольованому клінічному дослідженні за участю дорослих пацієнтів із цим захворюванням, підтвердженим за допомогою полімеразної ланцюгової реакції (ПЛР), і тяжким перебігом, визначеним за критеріями G. Chen і співавт. (2020). Оптимальним режимом призначення едаравону в цьому випадку може бути введення 60 мг препарату внутрішньовенно 1 раз на добу протягом 10 днів. Первинними кінцевими точками мають виступати смертність і клінічне покращення (Grein J. et al., 2020). У разі успішного застосування едаравону для зменшення мультиорганного пошкодження, кількості ускладнень і смертності при тяжких випадках COVID‑19 доцільно вивчити його ефективність за умови інших інфекційних захворювань, які супроводжуються надмірною запальною відповіддю (Reznik S. et al., 2020).
Сьогодні українські науковці можуть поділитися власним досвідом застосування цього препарату в клінічній практиці. Зокрема, результати своїх досліджень і спостережень вони представили в рамках IV Міжнародного конгресу з інфузійної терапії, що відбувся в режимі онлайн 12-13 жовтня.
 Досвідом застосування препарату едаравон у лікуванні пневмоній коронавірусної етіології поділилася завідувачка пульмонологічного відділення Чернівецької обласної клінічної лікарні, лікар-пульмонолог вищої кваліфікаційної категорії, доктор медичних наук, професор Світлана Вікторівна Коваленко. З початком пандемії саме до очолюваного нею відділення почали надходити перші пацієнти з COVID‑19. У дослідження було включено пацієнтів (n=30 в основній групі та n=30 у групі контролю), котрі захворіли на COVID‑19. Діагноз підтверджували за допомогою КТ та ПЛР‑тестування. Пацієнти мали приблизно однакову площу ураження легень за даними КТ (від 50 до 70% площі легеневої тканини). Як контрольні точки були обрані кількість ліжко-днів, сатурація крові, температура тіла, рівні феритину, D‑димеру, С‑реактивного білка, загальний клінічний аналіз крові з визначенням кількості еритроцитів, лейкоцитів, тромбоцитів, ШОЕ, лейкоцитарної формули, вмісту гемоглобіну.
Досвідом застосування препарату едаравон у лікуванні пневмоній коронавірусної етіології поділилася завідувачка пульмонологічного відділення Чернівецької обласної клінічної лікарні, лікар-пульмонолог вищої кваліфікаційної категорії, доктор медичних наук, професор Світлана Вікторівна Коваленко. З початком пандемії саме до очолюваного нею відділення почали надходити перші пацієнти з COVID‑19. У дослідження було включено пацієнтів (n=30 в основній групі та n=30 у групі контролю), котрі захворіли на COVID‑19. Діагноз підтверджували за допомогою КТ та ПЛР‑тестування. Пацієнти мали приблизно однакову площу ураження легень за даними КТ (від 50 до 70% площі легеневої тканини). Як контрольні точки були обрані кількість ліжко-днів, сатурація крові, температура тіла, рівні феритину, D‑димеру, С‑реактивного білка, загальний клінічний аналіз крові з визначенням кількості еритроцитів, лейкоцитів, тромбоцитів, ШОЕ, лейкоцитарної формули, вмісту гемоглобіну.
Пацієнти основної групи поряд зі стандартним лікуванням (антибіотики, антикоагулянти, протизапальні препарати) отримували препарат едаравону Ксаврон (із метою впливу на так званий цитокіновий шторм), Реосорбілакт (препарат, здатний зменшувати частоту легеневих ускладнень і тривалість перебування на штучній вентиляції легень), Тіворель (комбінація L‑аргініну та L‑карнітину для нормалізації вмісту NO в легеневих артеріях і пригнічення медіаторів запалення).
У пацієнтів основної групи спостерігалося більш швидке й істотне зниження рівня С‑реактивного білка, що свідчить про виражене пригнічення запального процесу в легенях. Зменшення вмісту D‑димеру в пацієнтів основної групи також свідчило про поліпшення їхнього загального стану порівняно з учасниками контрольної групи в динаміці лікування. Як відомо, високий рівень D‑димеру у хворих на COVID‑19 є прогностичним маркером тяжкого перебігу захворювання, а також збільшує ризик тромботичних ускладнень.
Терапія препаратами Ксаврон, Тіворель і Реосорбілакт сприяла вираженішому насиченню крові киснем, супроводжувалася прискоренням нормалізації температури тіла. Загалом термін госпіталізації пацієнтів основної групи становив 13 ліжко-днів, натомість хворих контрольної групи – 15 ліжко-днів. Побічних ефектів лікування не спостерігалося.
Отже, застосування препаратів Ксаврон, Тіворель і Реосорбілакт у комплексному лікуванні пневмонії коронавірусної етіології дає змогу зменшити тяжкість перебігу захворювання та прискорює одужання.
 Завідувачка кафедри інфекційних хвороб із курсом епідеміології Вінницького національного медичного університету ім. М. І. Пирогова, доктор медичних наук, професор Лариса Василівна Мороз представила власний досвід ведення пацієнтів із COVID‑19 з акцентом на пневмонії. Доповідачка нагадала, що коронавіруси являють собою РНК‑віруси з характерною оболонкою у формі корони, котрі мають тропність до рецепторів епітелію дихальної системи. Серед найвідоміших коронавірусів, здатних уражати організм людини, – SARS-CoV (коронавірус тяжкого гострого респіраторного синдрому), MERS-CoV (коронавірус близькосхідного респіраторного синдрому) та новий SARS-CoV‑2.
Завідувачка кафедри інфекційних хвороб із курсом епідеміології Вінницького національного медичного університету ім. М. І. Пирогова, доктор медичних наук, професор Лариса Василівна Мороз представила власний досвід ведення пацієнтів із COVID‑19 з акцентом на пневмонії. Доповідачка нагадала, що коронавіруси являють собою РНК‑віруси з характерною оболонкою у формі корони, котрі мають тропність до рецепторів епітелію дихальної системи. Серед найвідоміших коронавірусів, здатних уражати організм людини, – SARS-CoV (коронавірус тяжкого гострого респіраторного синдрому), MERS-CoV (коронавірус близькосхідного респіраторного синдрому) та новий SARS-CoV‑2.
Патогенез COVID‑19 передбачає розмноження вірусу в епітелії верхніх і нижніх дихальних шляхів із подальшим дифузним ураженням альвеолоцитів, що призводить до вірусної пневмонії чи гострого респіраторного дистрес-синдрому (ГРДС) із 40% летальністю. Основними симптомами є лихоманка (83-99%), втрата апетиту (40-84%), кашель (59-82%), підвищена втомлюваність (44-70%), аносмія (15-30%), біль у м’язах (11-35%). Окрім того, коронавірусна інфекція часто супроводжується коагулопатіями, що зумовлюють венозний тромбоз, інфаркт міокарда, дисеміноване внутрішньосудинне згортання крові. Факторами ризику коагулопатій виступають сепсис, хронічне обструктивне захворювання легень та ураження печінки, онкологічні захворювання, гіпертермія та гострий перебіг COVID‑19.
У 40% пацієнтів із коронавірусною інфекцією відзначається легкий перебіг, іще в 40% – середньотяжкий, у 15% – тяжкий і в 5% – критично тяжкий. У 94% пацієнтів, у яких це захворювання закінчилося летально, спостерігалася щонайменше одна з таких ознак: наявність злоякісної пухлини, патологічне ожиріння, цукровий діабет, хвороби серця та судин, нирок, легень, гіпоальбумінемія, вік понад 60 років.
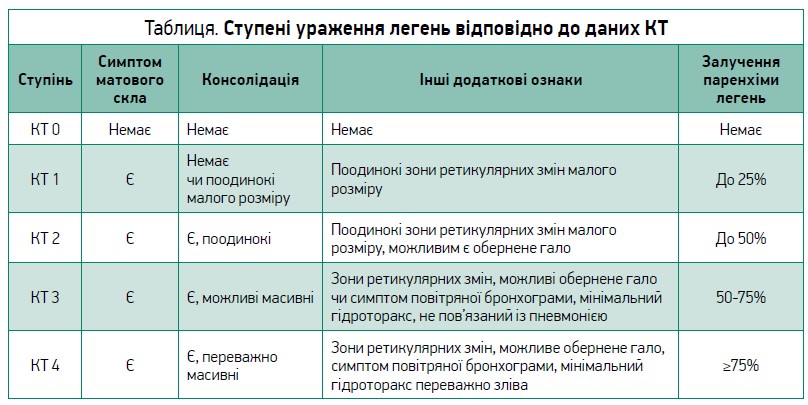 У діагностиці коронавірусного ураження легень провідне місце належить комп’ютерній томографії (КТ). Цей метод візуалізації необхідно застосовувати при первинному обстеженні чи госпіталізації, далі – повторно через 2-3 дні та що 2-3 дні за відсутності потрібного терапевтичного ефекту чи в разі клінічного погіршення з метою оцінки прогресування ураження легень, через 5-7 днів за відсутності позитивної динаміки симптомів. Ураження легень за даними КТ поділяється на 4 основні ступені (табл.).
У діагностиці коронавірусного ураження легень провідне місце належить комп’ютерній томографії (КТ). Цей метод візуалізації необхідно застосовувати при первинному обстеженні чи госпіталізації, далі – повторно через 2-3 дні та що 2-3 дні за відсутності потрібного терапевтичного ефекту чи в разі клінічного погіршення з метою оцінки прогресування ураження легень, через 5-7 днів за відсутності позитивної динаміки симптомів. Ураження легень за даними КТ поділяється на 4 основні ступені (табл.).
Допоки не розроблена вакцина від COVID‑19, пріоритетною задачею клініцистів є зниження ризику фатальних ускладнень. Із цією метою може застосовуватися патогенетичне лікування, проте варто зауважити, що всі препарати патогенетичної дії застосовуються off-label, тобто поза межами показань відповідно до офіційних інструкцій. Так, едаравон (Ксаврон, ТОВ «Юрія-Фарм», Україна) являє собою низькомолекулярний антиоксидантний засіб, який має протизапальну дію за рахунок пригнічення цитокінового шторму (зменшення продукції фактора некрозу пухлини, ІЛ‑6), а також чинить інгібувальний вплив на проникність ендотеліоцитів мікроциркулярного русла легень. Едаравон швидко нейтралізує вільні радикали; гальмує перекисне окиснення ліпідів, захищаючи клітини від руйнування; активує ферменти антиоксидантного захисту (супероксиддисмутазу, каталазу, глутатіонпероксидазу). Ці властивості роблять доцільним застосування едаравону при ГРДС.
Порівняння едаравону з дексаметазоном виявило, що обидва препарати здатні запобігати розвитку підвищеної проникності ендотеліоцитів мікроциркуляторного русла легень, однак у зв’язку з меншою кількістю побічних явищ перевагу варто віддавати едаравону (Saitoa Y. et al., 2015).
Іншими діючими речовинами, вплив яких при COVID‑19 активно вивчається, є L‑аргінін і L‑карнітин. Ці речовини є складниками вітчизняного препарату Тіворель (ТОВ «Юрія-Фарм»). L‑аргінін покращує мікроциркуляцію, забезпечуючи стійку вазодилатацію, зміцнює імунну систему й активує Т‑клітинний імунітет, чинить мембраностабілізувальну, цитопротекторну й антиоксидантну дії, збільшує вміст NO в легеневій тканині, зменшуючи спазм бронхів і легеневих артерій. Своєю чергою, L‑карнітин сприяє отриманню енергії з жирних кислот, чинить імуномодулювальну дію, пригнічуючи вивільнення прозапальних цитокінів, виступає прямим антиоксидантом, запобігає апоптозу клітин, є відомим кардіопротектором. За рахунок аргініну препарат Тіворель виступає донатором NO, основна функція котрого пов’язана з вазодилатацією та гальмуванням процесів агрегації й адгезії тромбоцитів. Цей препарат інгібує здатність коронавірусів прикріплятися до клітин, протидіє реплікації вірусів, сприяє зменшенню ендотеліальної дисфункції.
Для підтвердження наведених теоретичних даних професор Л. В. Мороз представила клінічний випадок 63-річного чоловіка з двобічною полісегментарною пневмонією, спричиненою вірусом SARS-CoV‑2 (підтверджено за допомогою ПЛР і КТ). При надходженні пацієнт скаржився на загальну слабкість, малопродуктивний кашель, утруднений вдих, задишку під час незначного фізичного навантаження. Температура тіла становила 39,0 °C, сатурація артеріальної крові киснем – 88% (96% на тлі оксигенотерапії). Пацієнту було призначено меропенем, левофлоксацин, фраксипарин, інфузії парацетамолу (Інфулган, ТОВ «Юрія-Фарм»), а наступного дня додано Ксаврон (10 мл 2 рази на добу) та Тіворель. Через 7 днів лікування сатурація артеріальної крові киснем становила вже 96%, а на тлі оксигенотерапії – 99%. Позитивна динаміка також спостерігалася на КТ, а повторна ПЛР виявилася негативною. У зв’язку з клінічним і рентгенологічним покращенням було відмінено левофлоксацин і парацетамол.
У другому клінічному випадку, представленому доповідачкою, фігурував 56-річний чоловік, у якого також була діагностована двобічна полісегментарна пневмонія, спричинена вірусом SARS-CoV‑2. Скаргами цього хворого були загальна слабкість, пітливість, сухість у носі, малопродуктивний кашель, погіршення апетиту. Температура тіла становила 38,4 °C. Пацієнту призначили меропенем, моксифлоксацин, фраксипарин, Ксаврон і Тіворель у стандартних дозуваннях. Через тиждень сатурація крові киснем нормалізувалася, а повторна ПЛР була негативною.
Отже, теоретичні дані та клінічний досвід свідчать, що включення до схеми комплексного лікування пневмонії, спричиненої SARS-CoV‑2, препаратів Ксаврон і Тіворель чинить сприятливий вплив за рахунок протидії надмірній продукції цитокінів та окисним реакціям.
 Завідувач кафедри внутрішньої медицини, фізичної реабілітації та спортивної медицини Буковинського державного медичного університету (м. Чернівці), доктор медичних наук, професор Віктор Корнійович Тащук представив доповідь «Органопротекція кардіологічного хворого в епоху COVID‑19».
Завідувач кафедри внутрішньої медицини, фізичної реабілітації та спортивної медицини Буковинського державного медичного університету (м. Чернівці), доктор медичних наук, професор Віктор Корнійович Тащук представив доповідь «Органопротекція кардіологічного хворого в епоху COVID‑19».
Основними аспектами лікування хронічних коронарних синдромів є усунення гострого ішемічного болю (нітрати короткої дії); профілактика ішемічного болю та симптоматичне лікування (нітрати тривалої дії, антагоністи кальцію, метаболічні препарати, реваскуляризація тощо); вплив на прогноз (ацетилсаліцилова кислота, статини, інгібітори ангіотензинперетворювального ферменту, β-блокатори).
Із 2005 р. для означення сукупності факторів, які впливають на здоров’я протягом життя, застосовують термін «експосом». Експосом включає особливості харчування, клімат, уживання ліків, вплив токсичних речовин, а з кінця 2019 р. – й епідемію COVID‑19. Це необхідно враховувати при веденні пацієнтів, передусім кардіоваскулярного профілю.
Не слід вважати, що кардіоцитопротекція є виключно прерогативою пострадянського простору. Проблемам надмірного вивільнення вільних радикалів, пошкодження мітохондріальної ДНК та зменшення вмісту аденозинтрифосфату (АТФ) присвячена значна кількість робіт зарубіжних науковців (Vilahur G., 2015; Koller A., 2016). За відомим висловом L. Opie (1999), серце – це більше, ніж помпа. Це також орган, який потребує енергії, отриманої внаслідок метаболізму. Метаболічна хвороба – ішемія – в ідеалі має підлягати метаболічному лікуванню.
Навіть короткий епізод ішемії сповільнює відновлення запасів АТФ, тому протидія виснаженню цих запасів здатна захистити кардіоміоцити від загибелі внаслідок «енергетичного голоду». Говорячи про хронічні коронарні синдроми, ми завжди стикаємося з питанням гіпоксії – невідповідності енергопродукції в системі мітохондріального окисного фосфорилювання енергетичним потребам клітини. Вплинути на цю ланку патогенезу, запобігаючи гіпоксії, можна саме за допомогою метаболічної терапії.
Авторське дослідження «Смарт-ЕКГ» передбачало аналіз варіабельності серцевого ритму, фази реполяризації та деяких інших показників (нахил сегмента ST, форма зубця Т) на електрокардіограмі, в тому числі на тлі застосування різних препаратів. Було зроблено висновок, що Тіворель активує парасимпатичний контур у разі стабільної стенокардії, зменшуючи ризик несприятливих подій.
Без сумніву, NO, донатором якого виступає Тіворель, є ключовою молекулою в лікуванні гіпоксії, а отже, і пневмоній, спричинених новим коронавірусом. Судинні, імуномодулювальні, антиоксидантні та цитопротекторні властивості L‑карнітину й L‑аргініну обґрунтовують їх призначення при COVID‑19.
На завершення виступу професор В. К. Тащук нагадав про пандемію іспанського грипу, що мала місце в 1918-1919 рр., і наголосив, що ми не маємо часу чекати, потрібно діяти негайно.
.jpg) Виступ завідувача кафедри анестезіології та інтенсивної терапії Національної медичної академії ім. П. Л. Шупика (м. Київ), доктора медичних наук, професора Олега Анатолійовича Лоскутова стосувався нейроінвазії та неврологічних ускладнень COVID‑19.
Виступ завідувача кафедри анестезіології та інтенсивної терапії Національної медичної академії ім. П. Л. Шупика (м. Київ), доктора медичних наук, професора Олега Анатолійовича Лоскутова стосувався нейроінвазії та неврологічних ускладнень COVID‑19.
Типові клінічні ознаки COVID‑19 нагадують такі тяжкого гострого респіраторного синдрому (SARS), але в міру накопиченнях нових клінічних даних науковці знаходять дедалі більше відмінностей. Зокрема, порівняння тропності, кінетики реплікації та профілювання ушкодження клітин виявило, що SARS-CoV‑2 властива набагато вища тропність до нейронів, аніж SARS-CoV (Chu H. et al., 2020). COVID‑19 уражає не лише легені, але й серце та центральну нервову систему, що значною мірою відображається на клінічному перебігу захворювання. Патофізіологія неврологічних ускладнень COVID‑19 включає безпосереднє пошкодження рецепторів, цитокін-опосередковане ураження, вторинне пошкодження нервової системи внаслідок гіпоксії, ураження нейронів, зумовлене ретроградним транспортом вірусу вздовж нервових волокон. Уже через 3 дні після зараження M. Dube та співавт. (2020) виявляли вірусні антигени у зв’язаних із дендритами війках і клітинному тілі нюхових сенсорних нейронів епітелію порожнини носа. На думку авторів, нейроінвазія коронавірусів відбувається трансназальним шляхом. Згідно з результатами експерименту тих самих авторів, субепітеліальна ін’єкція вірусів у язик забезпечувала меншу інвазію вірусів у центральну нервову систему, ніж інтраназальний шлях уведення.
Відповідно до даних іноземних науковців, у 36,4% пацієнтів із COVID‑19 спостерігаються неврологічні прояви. У пацієнтів із тяжким перебігом частіше відзначаються цереброваскулярні порушення (5,4% проти 0,8% у осіб із легким перебігом), розлади свідомості (14,8% проти 2,4%), скелетно-м’язові симптоми (19,3% проти 4,8%). J. Helms і співавт. (2020) проаналізували підгрупу пацієнтів із тяжким перебігом COVID‑19 і з’ясували, що неврологічні симптоми (енцефалопатія, збудження, сплутаність свідомості, ураження кортикоспінального тракту) спостерігались у 84% хворих. Ризик тяжкого перебігу інфекції був у 2,5 раза вищим у пацієнтів з інсультом в анамнезі.
В опублікованій французькими науковцями послідовній серії клінічних випадків ГРДС, спричиненого SARS-CoV‑2, зміни свідомості задокументовано в ≥2/3 випадків. У 67% пацієнтів відзначалися кортикоспінальні симптоми, а у 20% – гіпоксична ішемічна енцефалопатія. Автори зауважили, що на тлі COVID‑19 навіть у молодих пацієнтів нерідко трапляється ішемічний інсульт, включаючи оклюзію великих судин.
Загалом неврологічні симптоми при COVID‑19 поділяють на три категорії: з боку центральної нервової системи (головний біль, запаморочення, порушення свідомості, нудота та блювання, атаксія, гострі цереброваскулярні захворювання, епілепсія), з боку периферичної нервової системи (гіпогевзія, гіпосмія, невралгія) та скелетно-м’язові симптоми.
Відмінною рисою енцефалопатії в цьому випадку є порушення уваги та збудження, що супроводжується сплутаністю свідомості, в’ялістю, делірієм або комою. Метаболічні й ендокринні порушення ще вираженіше підвищують ризик енцефалопатії. Спричиняти це неврологічне ускладнення можуть також сепсис і надмірна запальна реакція.
Відомо, що більшість вірусних реакцій зумовлюють цитокіновий шторм, призводячи до загибелі клітин через викид інтерферон-індукованого білка ІР‑10, ІЛ‑6, інтерферону-β. Оскільки провідну роль у розвитку запалення на тлі цитокінового шторму відіграють АФК, найважливішими лікарськими засобами в цьому аспекті виступають антиоксиданти, найперше ті, що здатні проникати в мітохондрії (Zhang Z. et al., 2016). Японські клінічні рекомендації з лікування ГРДС перелічують кілька унікальних медикаментів, які можуть бути застосовані в таких пацієнтів, у тому числі едаравон як поглинач вільних радикалів.
В експерименті S. Ikeda та співавт. (2013) було оцінено вплив едаравону на індукований фотохімічним способом інфаркт головного мозку. Автори з’ясували, що вміст вільних радикалів у ділянках, які оточують вогнище ішемії, поступово зростає, в тому числі після реперфузії. Едаравон зменшував площу інфаркту та сприяв функціональному відновленню геміпарезу при церебральному тромбозі в моделі на щурах. Підґрунтям такої дії є здатність едаравону чинити протекторний вплив на мозок, усуваючи вільні радикали та протидіючи окисним пошкодженням.
Едаравон інгібує цитокін-індуковану гіперпроникність легеневих мікросудинних ендотеліальних клітин, причому ця дія є вираженішою, ніж у дексаметазону. На тлі застосування едаравону індекс проникності знижувався на 45%, а дексаметазону – лише на 35% (Saitoa Y. et al., 2015).
У власному пілотному дослідженні було з’ясовано, що едаравон (Ксаврон, ТОВ «Юрія-Фарм») зменшує вираженість запалення та смертність у пацієнтів із коронавірусною інфекцією. У контрольній групі рівень прозапального ІЛ‑6 перевищував верхню межу норми на 1652,40%, а в групі Ксаврону – лише на 269,97%. Летальність у групі контролю становила 14,3%, а в групі Ксаврону – 0%.
На жаль, вірусні захворювання характеризуються не лише гострими неврологічними ускладненнями, а й відтермінованими наслідками. Дані наукової роботи працівників лабораторії нейроімунології (Канада) свідчать, що респіраторні патогени можуть зберігатися в центральній нервовій системі людини й, можливо, така персистентна інфекція може стати фактором або кофактором патогенезу довготривалих неврологічних наслідків у генетично схильних осіб (Desforges M. et al., 2014). Це обґрунтовує важливість своєчасного багатокомпонентного лікування.
.jpg) Доцент кафедри фтизіатрії, пульмонології та сімейної медицини Харківської медичної академії післядипломної освіти, доктор медичних наук Едуард Михайлович Ходош охарактеризував патогенетичну синдромну тактику ведення пацієнта з COVID‑19.
Доцент кафедри фтизіатрії, пульмонології та сімейної медицини Харківської медичної академії післядипломної освіти, доктор медичних наук Едуард Михайлович Ходош охарактеризував патогенетичну синдромну тактику ведення пацієнта з COVID‑19.
Основними ланками патогенезу коронавірусної пневмонії є пошкодження вірусом дрібних клітин бронхів та альвеол і потужна запальна відповідь, здатна уражати тканину легень. Як наслідок порушується стан сурфактанта, альвеоли та капіляри перестають забезпечувати повноцінне надходження кисню, через що розвивається ГРДС. Виникають поліорганна гіпоксія та синдром дисемінованого внутрішньосудинного згортання, а надалі – пневмофіброз.
Одна з головних причин ураження органів при COVID‑19 – гіпоксія. Її супроводжують біохімічні та морфологічні розлади: ослаблення аеробного гліколізу й активація анаеробного гліколізу, посилення окиснення жирних кислот у мітохондріях, накопичення недоокиснених продуктів, ацидоз (біохімічні порушення), порушення мікроциркуляції, набряки тканин, білкова та жирова дистрофія, неефективність дихання та кровопостачання, розвиток серцево-легеневої недостатності (морфологічні й функціональні).
Прозапальні цитокіни та макрофаги запускають процеси активації нейтрофілів і моноцитів, що призводить до зростання вмісту АФК приблизно вдесятеро, окисного пошкодження клітинних мембран, викиду лізосомальних протеаз. Таке патологічно активне запалення запускає хибне коло, ланками котрого є масивне пошкодження легеневих капілярів, утруднення мікроциркуляції, відкриття артеріовенозних шлюзів зі скидом крові справа наліво в обхід легеневих капілярів, що запускає першу фазу ГРДС із посиленням гіпоксії та подальшою активацією запальних процесів.
Основними індукторами мітохондріальної дисфункції й апоптозу виступають АФК, тому однією з найважливіших клінічних задач є вибір правильного антиоксиданту. Ефективність останніх залежить від здатності проникати та накопичуватися в зоні пошкодження без видалення сигнальних молекул. Отже, ключова вимога до антиоксидантів – жиророзчинність, тобто здатність проникати крізь мембрани клітин і мітохондрій, щоби блокувати сигнальні шляхи, котрими подається сигнал продукувати запальні цитокіни. Крім того, оптимальний антиоксидант має діяти синергічно з водорозчинними антиоксидантами (в цитозолі).
Характеристиками цитокінового шторму є не лише активне запалення, а й периферична інсулінорезистентність, ацидоз, анаеробний метаболізм, зменшення чи припинення обміну речовин у тканинах на кшталт гібернації, що спочатку має адаптивний характер, а згодом – патологічний. Загалом патогенез ГРДС певною мірою споріднений із таким ішемічних і постішемічних явищ.
Едаравон (Ксаврон) здатен «гасити» цитокінову пожежу. Цей препарат швидко нейтралізує широкий спектр вільних радикалів, гальмує перекисне окиснення ліпідів та активує власні механізми антиоксидантного захисту. Важливо, що едаравон потрапляє в біологічні мембрани шляхом пасивної дифузії та проникає крізь гематоенцефалічний бар’єр.
Окрім Ксаврону, компонентами патогенетичної терапії COVID‑19 можуть виступати Тівортін і Тіворель (ТОВ «Юрія-Фарм»). Аргінін, який є компонентом обох цих засобів, виступає субстратом для синтезу NO, таким чином сприяючи вазодилатації, а також має імуностимулювальний, мембраностабілізувальний, цитопротекторний та антиоксидантний вплив. Тіворель, окрім аргініну, містить левокарнітин, роль якого полягає в доставці жирних кислот до мітохондріального матриксу («карнітиновий човник»), гальмуванні апоптозу, антиоксидантній дії, кардіопротекції.
NO є природною молекулою метаболізму людини, що відіграє важливу роль у формуванні імунної відповіді на вплив патогенної флори. Дослідження in vitro показали, що NO гальмує реплікацію SARS-CoV і покращує виживаність інфікованих клітин. Це обґрунтовує доцільність призначення Тівортіну/Тіворелю при COVID‑19.
Ще одним патогенетичним засобом, який традиційно застосовується при пневмоніях, є Реосорбілакт (ТОВ «Юрія-Фарм»). Цей препарат потенціює дію вазопресорів, зменшуючи потребу в них; запобігає набряку легень за рахунок виведення рідини з інтерстиційного простору; відновлює мікроциркуляцію завдяки дезагрегантній дії та зменшенню в’язкості крові.
На завершення Е. М. Ходош представив клінічний випадок пацієнта з пневмонією, спричиненою SARS-CoV‑2, в якого призначене лікування (азитроміцин, гідроксихлорохін, Тіворель, Ксаврон, Реосорбілакт, еноксапарин) сприяло усуненню клінічних проявів хвороби та зменшенню потреби в кисні, а також іще кілька клінічних випадків, у яких лікування схожими схемами фармакотерапії забезпечувало значне покращення.
Обираючи тактику лікування COVID‑19, варто враховувати, що це захворювання може мати хвилеподібний перебіг. Перша хвиля характеризується досить легким перебігом, після чого приблизно у 80% пацієнтів відбуваються покращення й одужання. У 20% пацієнтів після першої хвилі може настати період тимчасового покращення, проте далі настає друга хвиля розвитку симптомів (так звана легенева фаза), перебіг якої є тяжчим. І саме в цей час на додаток до протокольної терапії доцільним є застосування засобів, дія котрих спрямована на комплексне пригнічення цитокінового шторму – препаратів Ксаврон, Тіворель і Реосорбілакт. Важливо призначити таке лікування на самому початку фази другої хвилі, що дасть можливість «зрізати» її подальше прогресування. Ця лікувальна стратегія дасть змогу полегшити перебіг захворювання, скоротити термін перебування пацієнтів у стаціонарі й уникнути тяжких ускладнень.
Підготувала Лариса Стрільчук
Медична газета «Здоров’я України 21 сторіччя» № 20 (489), 2020 р.


