29 жовтня, 2024
Концепція неврологічного чотирикутника та нові можливості для її реалізації*
 Глобальний тягар неврологічних розладів є значним і зростає, особливо в умовах обмежених ресурсів. Поточний підвищений інтерес до здоров’я мозку та його впливу на добробут населення й економічне зростання висвітлено в новому міжгалузевому глобальному плані дій Всесвітньої організації охорони здоров’я (ВООЗ) щодо епілепсії й інших неврологічних розладів на 2022-2031 рр. і дає можливість переосмислити надання неврологічних послуг.
Глобальний тягар неврологічних розладів є значним і зростає, особливо в умовах обмежених ресурсів. Поточний підвищений інтерес до здоров’я мозку та його впливу на добробут населення й економічне зростання висвітлено в новому міжгалузевому глобальному плані дій Всесвітньої організації охорони здоров’я (ВООЗ) щодо епілепсії й інших неврологічних розладів на 2022-2031 рр. і дає можливість переосмислити надання неврологічних послуг.
Глобальна ініціатива ВООЗ щодо покращення здоров’я мозку протягом усього життя
У зазначеному документі запропоновано прагматичні рішення для зміцнення неврологічного здоров’я населення з наголосом на побудові глобальної синергії та сприянні «неврологічній революції» на чотирьох ключових стовпах (векторах) – спостереження, профілактика, невідкладна допомога та реабілітація, що дістали назву «неврологічний чотирикутник» (рис. 1). Інноваційні стратегії для досягнення цієї трансформації включають визнання та сприяння цілісному, духовному та планетарному здоров’ю (рис. 2). Зазначені стратегії можна розгортати шляхом спільного проєктування й упровадження для створення справедливого й інклюзивного доступу до послуг для сприяння, захисту та відновлення неврологічного здоров’я в усіх групах людей протягом усього життя [1].
![Рис. 1. Неврологічний чотирикутник [1] ZU_18_2024_st20-21_pic1.png](/multimedia/userfiles/images/2024/ZU_18_2024/ZU_18_2024_st20-21_pic1.png)
Рис. 1. Неврологічний чотирикутник [1]
![Рис. 2. Взаємозв’язки між сферами здоров’я та добробуту [1] ZU_18_2024_st20-21_pic2.png](/multimedia/userfiles/images/2024/ZU_18_2024/ZU_18_2024_st20-21_pic2.png)
Рис. 2. Взаємозв’язки між сферами здоров’я та добробуту [1]
Збільшення тягаря неврологічних захворювань
Неврологічні розлади, включаючи всі хвороби головного мозку, спинного мозку, черепно-мозкових нервів, периферичних нервів і нервово-м’язової системи, є дуже поширеними: принаймні кожна 3-тя людина матиме неврологічний розлад у якийсь момент протягом життя. У період 1990-2016 рр. неврологічні розлади були основною причиною зростання кількості років життя з поправкою на інвалідність (disability-adjusted life years – DALYs) і другою за величиною причиною смерті в усьому світі, що становить 9 млн смертей на рік. У 2016 р. п’ятіркою головних неврологічних причин DALYs у всьому світі були інсульт (42,2%), головний біль (16,3%), деменція (10,4%), менінгіт (7,9%) та епілепсія (4,9%). Із 9 млн смертей у світі у 2016 р. трьома провідними неврологічними причинами серед 15 оцінених неврологічних розладів були інсульт (67,4%), хвороба Альцгеймера й інші пов’язані з нею деменції (20,3%) і менінгіт (3,7%). Спадкові нейрометаболічні хвороби охоплюють понад 1400 різних генетичних захворювань і разом становлять значний тягар із сукупною частотою від 1 на 800 до 1 на 2500 новонароджених [1].
Прямі та непрямі витрати на неврологічні хвороби
Інсульт «коштує» майже 900 млрд дол. США на рік у всьому світі. Деменція «коштувала» 1,3 трлн дол. США у 2019 р. Розлади сну та неспання, які вражають понад 20% населення, загалом призводять до економічних витрат у розмірі майже 700 млрд дол. США щорічно в Канаді, США, Великій Британії, Німеччині та Японії. У 2010 р. витрати на неврологічні розлади в країнах Європи оцінювали в 798 млрд євро.
Пріоритетні групи та популяції
Жінки становлять більшість осіб, які доглядають за пацієнтами з неврологічними розладами; саме на них припадає значне фінансове й емоційне навантаження. Тягар дитячих неврологічних розладів також потребує уваги через потенційний шкідливий вплив на розвиток мозку. Навантаження на дитину, батьків та опікунів і суспільство загалом з погляду DALYs і витрат залишається надзвичайно високим. Люди похилого віку також мають великий тягар неврологічних розладів (інсульт і нейродегенеративні хвороби). Крім того, особи похилого віку мають підвищений ризик щодо наявності супутніх двох або більше неврологічних захворювань, як-от інсульт/епілепсія/деменція, хвороба Паркінсона / деменція або інсульт/деменція, а також інші, як-от спондильоз, остеоартрит і доброякісна гіперплазія передміхурової залози [1].
Статистика вегетативної дисфункції
Із проблемою вегетативної дисфункції (ВД) стикається майже кожен лікар, адже симптоми ВД спостерігають у близько 80% дорослого населення світу, причому жінки – внаслідок психологічних, гормональних та інших чинників – хворіють у 3 рази частіше, ніж чоловіки. Максимальні прояви хвороби виявляють зазвичай у молодому віці (до 45 років) [2].
У Міжнародній класифікації хвороб 10-го перегляду ВД представлена в рубриці G 90.8 «Інші розлади вегетативної нервової системи» з такими характерними проявами, як напади головного болю, відчуття «порожньої» голови, неуважність, забудькуватість, гіперчутливість до змін погоди, коливання артеріального тиску, порушення сну, відчуття порушення в роботі серця.
Оцінювання функції вегетативної нервової системи
Є певні проби, які слід використовувати для того, щоб запідозрити та клінічно довести цей стан. Це відпочинок під час навантаження, тест холодного тиску, маневр Вальсальви, парадигми охолодження обличчя, тиск на очне яблуко.
Етіопатогенетичні чинники
В основі формування зазначеного синдрому, безумовно, лежить генетична конституційна особливість. Відіграють роль також екзогенні й ендогенні чинники (табл. 1). Патогенез ВД наведено в таблиці 2.
|
Таблиця 1. Етіологія ВД |
||
|
Спадковість |
Екзогенні чинники |
Ендогенні чинники |
|
◆ Спадково-конституційні особливості з формуванням синдрому дезадаптації |
◆ Порушення здорового способу життя ◆ Низька фізична активність ◆ Перевтома ◆ Тривала (більш ніж 3-6 годин) робота за комп’ютером ◆ Стрес ◆ Метеорологічні чинники ◆ Вживання алкоголю |
◆ Гормональна вікова перебудова (підлітки, вагітні, період клімаксу) ◆ Різноманітні хронічні хвороби |
|
Таблиця 2. Патогенез ВД |
|||
|
Вплив чинника |
|||
|
↓ |
|||
|
Порушення надсегментарних центрів на тканинному, клітинному та мембранному рівнях |
|||
|
↓ |
|||
|
Порушення злагодженої роботи симпатичної та парасимпатичної нервової системи |
|||
|
Порушення обміну речовин, стану гомеостазу |
Порушення іннервації внутрішніх органів і судин |
Порушення медіаторної ланки регуляції |
Підвищення та зниження чутливості периферичних і центральних рецепторів |
|
Клінічні прояви |
|||
Описують близько 150 синдромів, пов’язаних з ВД. Основні з них – нейроваскулярний синдром (головний біль, запаморочення, переднепритомний стан), прояви дезадаптації (порушення сну, метеочутливість, швидка стомлюваність у когнітивній, емоційній і фізичній сферах), кардіальний синдром (відчуття серцебиття, перебої ритму серця, коливання артеріального тиску), абдомінальний синдром (порушення функцій шлунково-кишкового тракту).
ВД при інфекційно-алергічних хворобах
Установлено, що багато вірусів, як-от ретровіруси (вірус імунодефіциту людини), віруси герпесу, ентеровіруси, ліccавіруси, флавівіруси, можуть зумовлювати ушкодження нервової системи. Зокрема, пряме вторгнення вірусів у центральну нервову систему, периферичну нервову систему й імуноопосередковані механізми вважають пусковими чинниками, що призводять до вегетативних розладів. Є повідомлення про розвиток ВД при синдромі Гієна – Барре, пов’язаного з COVID‑19, і гострої моторної аксональної нейропатії, що супроводжується симптомами дизавтономії. Синдром постуральної тахікардії також спостерігали як постінфекційне ускладнення COVID‑19. Нещодавно Американська вегетативна асоціація опублікувала розлогу статтю, в якій наголошується на важливості вегетативного функціонування та наводяться чіткі вказівки щодо ведення пацієнтів з інфекційно-алергічними хворобами [3].
ВД при розсіяному склерозі
ВД присутня в осіб з розсіяним склерозом (РС) починаючи з ранніх стадій хвороби. Під час перебігу РС серцево-судинна ВД спостерігається у близько ⅔ пацієнтів і є вираженішою на прогресивних стадіях РС. Серцево-судинна ВД може проявлятися як ортостатична непереносимість і призвести до падінь. Сечостатева дисфункція є одним з найпоширеніших симптомів РС і може проявлятися у вигляді сексуальної дисфункції, частого сечовипускання, нетримання чи затримки сечі. Порушення потовиділення при РС можуть призвести до перегріву та погіршити наявну неврологічну інвалідність. ВД при РС необхідно активно виявляти та лікувати. Ці симптоми можуть суттєво вплинути на якість життя хворих на РС поганою переносимістю вертикального положення, труднощами статевої функції та низькою витривалістю фізичної активності, особливо в теплих умовах [4].
ВД при легкій черепно-мозковій травмі
Дисфункція вегетативної нервової системи при легкій черепно-мозковій травмі (ЧМТ) може бути наслідком дифузного аксонального пошкодження, зниження церебрального кровотоку, погіршення стану після травми. Вищі центри головного мозку, включаючи префронтальну кору (передня поясна частина, острівець, орбітофронтальна та вентромедіальна кора) й лімбічні структури (мигдалеподібне тіло та гіпоталамус), структури в стовбурі мозку (періакведуктальна сіра речовина, nucleus ambiguus, medulla) утворюють центральну вегетативну мережу. Залежно від механізму пошкодження та наявності дифузного пошкодження аксонів можуть постраждати центри, відповідальні за контроль варіабельності серцевого ритму й інші вегетативні функції. Церебральний кровотік дедалі частіше досліджують після легкої ЧМТ з використанням різноманітних методів, включаючи транскраніальну доплерографію та магнітно-резонансну томографію з артеріальним спіновим маркуванням. Покращення у відновленні частоти серцевих скорочень, вимірювання парасимпатичної активності, яке спостерігають після 6-тижневої програми тренувань, втрачається лише після 4 тижнів детренованості. Показано, що в осіб з вищою частотою серцевих скорочень у стані спокою та меншим відсотком прогнозованого пікового споживання кисню відновлення частоти серцевих скорочень після фізичних навантажень відбувається повільніше, що є мірою здатності людини залучати серцевий вагусний тонус.
Вимірювання вегетативної функції, як-от варіабельність серцевого ритму та чутливість барорецепторів, є об’єктивними кількісними показниками, які можна використовувати для оцінки траєкторії відновлення після легкої ЧМТ. Сьогодні одужання переважно оцінюють за суб’єктивними показниками з використанням опитувальників щодо симптомів. Хоча об’єктивні показники відновлення продовжують досліджувати, є значні можливості для використання нових методів провокації вегетативної нервової системи для оцінки як відновлення через часові точки, так і основної патофізіології постійних симптомів. Потенціал оцінки цих показників у різних часових точках для інформування про повернення до спорту, на додаток до традиційних оцінок симптомів, становить особливий інтерес у цій галузі [5].
Слід зазначити, що ВД дуже часто є предиктором виникнення цереброваскулярних захворювань (рис. 3), тому важливо запобігти їх розвитку за появи перших симптомів.
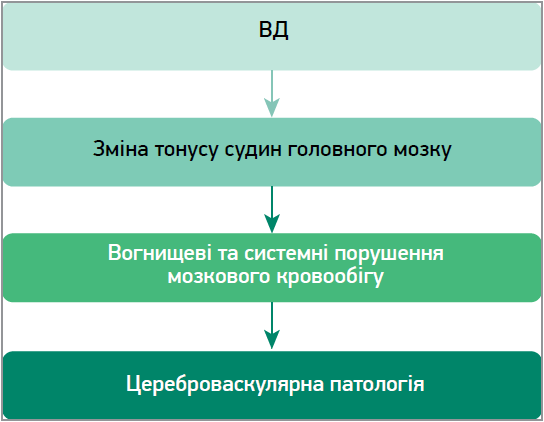
Рис. 3. ВД як предиктор розвитку цереброваскулярної хвороби
Лікування
Схему лікування ВД підбирають індивідуально, за результатами обстеження та специфіки симптоматики (табл. 3).
|
Таблиця 3. Схема лікування ВД |
|
|
Медикаментозне |
Немедикаментозне |
|
Седативні, вегетотропні тонізувальні препарати (адаптогени), блокатори β-адренорецепторів, антигіпертензивні препарати, антидепресанти, нейротропні препарати, венотоніки, вітамінотерапія |
Рефлексотерапія, масаж, психотерапія, лікувальна фізкультура, дозовані фізичні навантаження |
Містерія – революційна сила, що сприяє покращенню когнітивних функцій і зменшенню проявів вегетативних розладів
З огляду на компонентний склад Містерія як комплекс, який сприяє поліпшенню когнітивного стану і зменшенню вегетативних розладів, може бути рекомендована для профілактики цереброваскулярної патології, а також для реабілітації неврологічних хворих молодого віку (до 45 років). На нашу думку, ця дієтична добавка також може застосовуватися в разі стану фізіологічного зношування когнітивних функцій.
Комплекс Містерія у своєму складі поєднав компоненти преміум-якості: запатентовану форму цитиколіну Cognizin™ 250 мг, який схвалено в Європейському Союзі як дієтичну добавку та який довів свою ефективність у дослідженнях [6], стандартизований екстракт гінкго білоба 80 мг [7] та омега‑3 з олії водоростей (AvailOm® 50 High DHA Algae: докозагексаєнова кислота, ейкозапентаєнова кислота, L‑лізин та інші жирні кислоти – 200 мг) [8, 9].
Цитиколін Cognizin™ являє собою запатентовану японську субстанцію, яка, на відміну від інших добавок цитиколіну, спеціально вивчена в численних клінічних дослідженнях. Цитиколін Cognizin™ схвалений у країнах Європейського Союзу як дієтична добавка, що здатна покращувати концентрацію, увагу та запам’ятовування [6].
Екстракт гінкго білоба у складі комплексу має антиоксидантний, антигіпоксичний, гематореологічний, судинний, нейропротекторний ефекти. Вміст активних речовин та очищення від небажаних домішок суворо контролюється, завдяки чому досягається постійна концентрація активних речовин [7].
Омега‑3-поліненасичені жирні кислоти, зокрема докозагексаєнова кислота, у складі комплексу покращують когнітивні функції, настрій, увагу, забезпечуючи нормальну роботу мозку. Саме в комплексі Містерія омега‑3 перебуває в твердій формі, що має доведену біодоступність у 5 разів вищу, ніж рідкі форми омега‑3, і досягається вона в дуже короткий термін [9].
Вживання комплексу Містерія може бути рекомендоване як додаткове джерело есенціальних омега‑3-поліненасичених жирних кислот, холіну з цитиколіну та гінкго білоба для підтримки нормальної діяльності головного мозку, зокрема в людей з ВД та в період реабілітації після перенесених уражень головного мозку, а також для покращення когнітивних функцій.
Список літератури знаходиться в редакції.
* За матеріалами доповіді в рамках XVI Нейросимпозіуму (10-13 вересня 2024 року, м. Львів). – Прим. ред.
Медична газета «Здоров’я України 21 сторіччя» № 18 (579), 2024 р



 Негрич Т. І.
Негрич Т. І.