Метформин может оказывать долгосрочный защитный эффект в отношении нейродегенеративных заболеваний, таких как БА и болезнь Паркинсона (БП). К такому выводу пришли ученые после недавнего клинического исследования, представленного на ежегодном заседании Американской диабетической ассоциации (ADA). В рамках этого испытания было отобрано 6046 больных сахарным диабетом (СД) 2 типа, получавших инсулин (средний возраст – 63 года; >90% мужчин). Медиана наблюдения за больными составила 5,25 года. Критерием исключения служило наличие различной сопутствующей патологии (нейропатия, дефицит витамина B12, нейродегенеративные заболевания, когнитивные нарушения или отдаленные последствия патологии сосудов головного мозга, рак, почечная недостаточность в терминальной стадии и др.). Среди всех участников было диагностировано 334 случая деменции, 100 случаев БП и 71 случай БА, из них 19 – с когнитивными нарушениями.
Скорректированная по возрасту, полу, расовой принадлежности, функции почек, массе тела, а также другим критериям частота развития одного или нескольких нейродегенеративных заболеваний среди тех, кто никогда не использовал метформин, составила 2,08 случая на 100 пациенто-лет; среди тех, кто принимал препарат ≤1 года, – 2,47; ≤2 лет – 1,61; от 2 до 4 лет – 1,30; среди получавших терапию метформином на протяжении ≥4 лет – 0,49. На фоне его приема наблюдалось снижение частоты развития деменции (ОР для 2-4 лет – 0,567; ≥4 лет – 0,252), а также БП и БА (ОР для терапии ≥4 лет 0,038 и 0,229 соответственно). Результаты не изменились даже после того, как исследователи учли прием других препаратов для лечения СД.
Несмотря на положительные результаты, для окончательного подтверждения выявленной взаимосвязи необходимы дополнительные крупномасштабные испытания.
Shi Q. et al. Metformin Linked to Lower Neurodegenerative Disease Risk. Medscape, 11 Jun 2016.
Амиселимод сокращает количество патологических очагов при рассеянном склерозе
Новый пероральный модулятор сфингозин‑1-фосфатных рецепторов амиселимод в 2 различных дозировках показал эффективность в лечении пациентов с активным рецидивирующе-ремиттирующим рассеянным склерозом (РРРС). При этом препарат не вызывал серьезных побочных эффектов со стороны сердечно-сосудистой системы. Исследование II фазы MOMENTUM с участием 415 взрослых пациентов с РРРС продемонстрировало, что прием амиселимода в дозе 0,2 или 0,4 мг 1 р/сут ассоциировался со значительным сокращением очагов накопления в ЦНС контраста гадолиния на T1‑изображениях магнитно-резонансной томографии (МРТ) спустя 24 нед лечения.
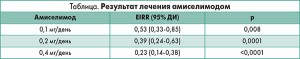
Участники исследования в возрасте 18-60 лет были рандомизированы в группы приема препарата в дозе 0,1 мг (n=105), 0,2 мг (n=103), 0,4 мг (n=104) или плацебо (n=103) 1 р/день на протяжении 24 нед. МРТ проводилась ежемесячно. Среднее количество очагов накопления гадолиния спустя 8-24 нед терапии достоверно не отличалось между группой приема 0,1 мг препарата и группой плацебо (2,0 vs 1,6 соответственно). Однако у пациентов, получавших 0,2 и 0,4 мг амиселимода, количество контрастируемых очагов сократилось до 0 (р=0,002 и p=0,0003 соответственно). Кроме того, на фоне активной терапии отмечалось дозозависимое снижение соотношения заболеваемости (estimated incidenсе rate ratio – EIRR), что отражено в таблице.
Спустя 24 нед лечения доля участников без очагов поражения увеличилась с 65 до 85% в группе 0,2 мг (р=0,0005) и с 67 до 91% в группе 0,4 мг (р<0,0001) и уменьшилась с 67 до 63% в группе плацебо. Количество очагов накопления в ЦНС контраста гадолиния на T2-изображениях МРТ также снизилось среди пациентов, получавших препарат в дозе 0,2 мг (EIRR 0,45; р=0,002) и 0,4 мг (EIRR 0,31; р<0,0001). Рецидив РРСС удалось предотвратить у 85 и 86% больных в группах амиселимода 0,2 и 0,4 мг соответственно и у 73% в группе плацебо (р=0,009 и р=0,002 соответственно). Нежелательные явления, связанные с лечением, возникали с одинаковой частотой во всех группах. Наиболее распространенными среди них оказались головная боль (у 10% участников в каждой группе активной терапии vs 4% пациентов в группе плацебо) и назофарингит. Не зафиксировано существенного влияния препарата на частоту сердечных сокращений или вероятность развития сердечно-сосудистых патологий (4-8%). В группах приема амиселимода 0,1 и 0,2 мг имели место эпизод атриовентрикулярной блокады 2 степени и случай неустойчивой желудочковой тахикардии, однако нарушения протекали бессимптомно и не были признаны клинически значимыми.
Полученные результаты предполагают использование амиселимода в качестве потенциальной терапии не только РРРС, но и других иммуноопосредованных воспалительных заболеваний, однако для окончательного подтверждения безопасности и эффективности препарата требуются испытания III фазы.
Kappos L., Arnold D. L. et al. Safety and efficacy of amiselimod in relapsing multiple sclerosis (MOMENTUM):
a randomised, double-blind, placebo-controlled phase 2 trial. The Lancet, Vol. 15, N11, p. 1148-1159, 16 Aug 2016.
Amiselimod May Decrease Lesions in Relapsing MS. Medscape, 15 Sep 2016.
 Спустя 24 нед лечения доля участников без очагов поражения увеличилась с 65 до 85% в группе 0,2 мг (р=0,0005) и с 67 до 91% в группе 0,4 мг (р<0,0001) и уменьшилась с 67 до 63% в группе плацебо. Количество очагов накопления в ЦНС контраста гадолиния на T2-изображениях МРТ также снизилось среди пациентов, получавших препарат в дозе 0,2 мг (EIRR 0,45; р=0,002) и 0,4 мг (EIRR 0,31; р<0,0001). Рецидив РРСС удалось предотвратить у 85 и 86% больных в группах амиселимода 0,2 и 0,4 мг соответственно и у 73% в группе плацебо (р=0,009 и р=0,002 соответственно). Нежелательные явления, связанные с лечением, возникали с одинаковой частотой во всех группах. Наиболее распространенными среди них оказались головная боль (у 10% участников в каждой группе активной терапии vs 4% пациентов в группе плацебо) и назофарингит. Не зафиксировано существенного влияния препарата на частоту сердечных сокращений или вероятность развития сердечно-сосудистых патологий (4-8%). В группах приема амиселимода 0,1 и 0,2 мг имели место эпизод атриовентрикулярной блокады 2 степени и случай неустойчивой желудочковой тахикардии, однако нарушения протекали бессимптомно и не были признаны клинически значимыми.
Полученные результаты предполагают использование амиселимода в качестве потенциальной терапии не только РРРС, но и других иммуноопосредованных воспалительных заболеваний, однако для окончательного подтверждения безопасности и эффективности препарата требуются испытания III фазы.
Kappos L., Arnold D. L. et al. Safety and efficacy of amiselimod in relapsing multiple sclerosis (MOMENTUM):
a randomised, double-blind, placebo-controlled phase 2 trial. The Lancet, Vol. 15, N11, p. 1148-1159, 16 Aug 2016.
Amiselimod May Decrease Lesions in Relapsing MS. Medscape, 15 Sep 2016.
Спустя 24 нед лечения доля участников без очагов поражения увеличилась с 65 до 85% в группе 0,2 мг (р=0,0005) и с 67 до 91% в группе 0,4 мг (р<0,0001) и уменьшилась с 67 до 63% в группе плацебо. Количество очагов накопления в ЦНС контраста гадолиния на T2-изображениях МРТ также снизилось среди пациентов, получавших препарат в дозе 0,2 мг (EIRR 0,45; р=0,002) и 0,4 мг (EIRR 0,31; р<0,0001). Рецидив РРСС удалось предотвратить у 85 и 86% больных в группах амиселимода 0,2 и 0,4 мг соответственно и у 73% в группе плацебо (р=0,009 и р=0,002 соответственно). Нежелательные явления, связанные с лечением, возникали с одинаковой частотой во всех группах. Наиболее распространенными среди них оказались головная боль (у 10% участников в каждой группе активной терапии vs 4% пациентов в группе плацебо) и назофарингит. Не зафиксировано существенного влияния препарата на частоту сердечных сокращений или вероятность развития сердечно-сосудистых патологий (4-8%). В группах приема амиселимода 0,1 и 0,2 мг имели место эпизод атриовентрикулярной блокады 2 степени и случай неустойчивой желудочковой тахикардии, однако нарушения протекали бессимптомно и не были признаны клинически значимыми.
Полученные результаты предполагают использование амиселимода в качестве потенциальной терапии не только РРРС, но и других иммуноопосредованных воспалительных заболеваний, однако для окончательного подтверждения безопасности и эффективности препарата требуются испытания III фазы.
Kappos L., Arnold D. L. et al. Safety and efficacy of amiselimod in relapsing multiple sclerosis (MOMENTUM):
a randomised, double-blind, placebo-controlled phase 2 trial. The Lancet, Vol. 15, N11, p. 1148-1159, 16 Aug 2016.
Amiselimod May Decrease Lesions in Relapsing MS. Medscape, 15 Sep 2016.


