17 липня, 2024
Гостра мієлоїдна лейкемія з IDH1-мутацією – що нового в лікуванні
За результатами дослідження AGILE
Івосиденіб – перший таргетний препарат, який був спеціально розроблений для лікування пацієнтів з гострою мієлоїдною лейкемією (ГМЛ) та IDH1-мутацією. Його застосування у комбінації з азацитидином є новим ефективним варіантом лікування зазначеної патології. У глобальному подвійному сліпому рандомізованому плацебо-контрольованому дослідженні ІІІ фази AGILE комбінація івосиденібу з азацитидином продемонструвала значні переваги порівняно з азацитидином і плацебо у пацієнтів з уперше діагностованою ГМЛ та IDH1-мутацією, які не були придатні для інтенсивної хіміотерапії.
ГМЛ – гетерогенний мієлоїдний рак, який переважно уражає людей похилого віку (медіана віку на момент встановлення діагнозу – 68 років) [1, 2]. Пацієнти літнього віку та ті, які не є кандидатами (непридатні) для проведення інтенсивної індукційної хіміотерапії, отримують менш агресивні режими лікування, такі як цитарабін у низьких дозах або гіпометилювальні агенти. Додавання венетоклаксу до азацитидину асоціюється зі статистично значущим покращенням загальної виживаності (ЗВ) у непридатних до інтенсивної хіміотерапії пацієнтів з ГМЛ і наявністю специфічних мутацій [3, 4]. Незважаючи на досягнутий прогрес, результати лікування зазначеної групи пацієнтів з ГМЛ залишаються незадовільними. Одним із потенційних шляхів покращення результатів терапії є застосування нових таргетних препаратів, спрямованих на молекулярні зміни, які відіграють ключову роль у лейкогенезі [4, 5].
Соматичні мутації в гені, що кодує ізоцитратдегідрогеназу 1 (IDH1), виявляють у 6-10% пацієнтів з ГМЛ [6-9]. Мутований IDH1 каталізує вироблення D-2-гідроксиглутарату, що призводить до порушення клітинного метаболізму й епігенетичної регуляції та сприяє онкогенезу [7, 10, 11]. Деякі дослідники припускають, що IDH1-мутація при ГМЛ асоціюється зі старшим віком і гіршим прогнозом, особливо в контексті нормального каріотипу [12-14].
Івосиденіб – перший у своєму класі потужний пероральний таргетований низькомолекулярний інгібітор мутованого IDH1 – продемонстрував клінічну активність як єдиний препарат у дослідженнях за участю пацієнтів з гематологічними та солідними пухлинами [15-18]. Дані дослідження Ib фази, в якому брали участь 23 пацієнти з нещодавно діагностованою ГМЛ та IDH1-мутацією, продемонстрували обнадійливу клінічну ефективність комбінованої терапії, що включала івосиденіб та азацитидин [19]. Монотерапія івосиденібом (500 мг 1 раз на добу) схвалена у США для дорослих із рецидивами або рефрактерною ГМЛ та IDH1-мутацією чи вперше діагностованою ГМЛ з IDH1-мутацією у віці 75 років і старше або з супутніми захворюваннями, що перешкоджають проведенню інтенсивної хіміотерапії [20]. У статті представлені результати дослідження ІІІ фази AGILE.
Методи
Дизайн дослідження та рандомізація
У глобальному подвійному сліпому рандомізованому плацебо-контрольованому дослідженні ІІІ фази оцінювали ефективність і безпеку комбінацій івосиденібу й азацитидину та плацебо й азацитидину у пацієнтів з уперше діагностованою ГМЛ та IDH1-мутацією, які були непридатні для інтенсивної індукційної хіміотерапії.
Івосиденіб (500 мг) або плацебо застосовували перорально 1 раз на день у поєднанні з азацитидином (75 мг/м2 площі поверхні тіла підшкірно або внутрішньовенно протягом 7 днів у 28-денних циклах).
Пацієнти були рандомізовані у співвідношенні 1:1 для отримання івосиденібу й азацитидину або плацебо й азацитидину з різними розмірами блоків і стратифіковані відповідно до географічного регіону та статусу захворювання (первинний або вторинний). Всі пацієнти мали отримувати лікування впродовж щонайменше шести циклів, за винятком випадків рецидиву, прогресування захворювання, неприйнятної токсичності або смерті.
Пацієнти
Критерії включення пацієнтів у дослідження передбачали вік ≥18 років і централізовано верифікований діагноз вперше виявленої ГМЛ з IDH1-мутацією. Додаткові критерії відбору включали відсутність в анамнезі терапії інгібіторами IDH1 або гіпометилювальними агентами з приводу мієлодиспластичного синдрому, оцінку загального стану за шкалою Східної кооперативної онкологічної групи (ECOG) в межах 0-2 балів (де вищий бал відповідає більшому ступеню функціональних обмежень за 5-бальною шкалою), а також задовільні показники функції печінки та нирок.
Непридатність до інтенсивної хіміотерапії визначалася віком 75 років і старше або наявністю принаймні одного з медичних станів: оцінка за шкалою ECOG 2 бали, тяжкі серцеві розлади (наприклад, застійна серцева недостатність, що призвела до лікування, фракція викиду лівого шлуночка ≤50% або хронічна стабільна стенокардія), тяжкі легеневі розлади (наприклад, дифузійна здатність легень ≤65% чи об’єм форсованого видиху за 1 с ≤65%), кліренс креатиніну менше 45 мл/хв або рівень білірубіну, що у понад 1,5 разу перевищує верхню межу норми.
Кінцеві точки й оцінки
Основною первинною кінцевою точкою дослідження була виживаність без подій, яка визначалася як проміжок часу від рандомізації до невдачі лікування (відсутність повної ремісії – ПР – на 24-му тижні), рецидиву після досягнення ремісії або смерті з будь-якої причини, залежно від того, яка подія настала раніше. Ефективність івосиденібу оцінювалася на основі відповіді на лікування, яка визначалася дослідниками відповідно до модифікованих критеріїв оцінки відповіді при ГМЛ, розроблених Міжнародною робочою групою та Європейською мережею з лікування лейкемії (European LeukemiaNet) [21, 22].
Вторинні кінцеві точки включали частоту досягнення ПР, ЗВ, частоту досягнення ПР або ПР із частковим гематологічним покращенням, частоту об’єктивної відповіді, профіль безпеки та якість життя, пов’язану зі здоров’ям. Об’єктивна відповідь визначалася як ПР, ПР з частковим гематологічним покращенням, ПР з неповним гематологічним покращенням (включаючи ПР із частковим відновленням рівня тромбоцитів), часткова ремісія та морфологічний стан без лейкемії. Оцінка відповіді базувалася на результатах вивчення показників кісткового мозку та/або периферичної крові, яке проводили дослідники. Також виконано аналіз безрецидивної виживаності і ЗВ у підгрупах пацієнтів.
Розподіл пацієнтів на групи цитогенетичного ризику здійснювали відповідно до клінічних рекомендацій Національної онкологічної мережі США (NCCN) щодо лікування ГМЛ [23, 24]. Профіль безпеки та небажані явища оцінювали за допомогою фізикального обстеження, визначення загального стану за шкалою ECOG, життєвих показників, електрокардіографії у 12 відведеннях, клінічних лабораторних досліджень (гематологічних, біохімічних і коагулологічних) та реєстрації небажаних явищ (відповідно до Загальних термінологічних критеріїв побічних явищ Національного інституту раку США, версія 4.03) [25]. Якість життя, пов’язану зі здоров’ям, оцінювали у 1-й та 15-й день 1-го циклу, 1-й та 15-й день 2-го циклу, далі – у 1-й день кожного непарного циклу, наприкінці лікування та під час подальшого спостереження за безпекою з використанням питальника якості життя Європейської організації з дослідження та лікування раку (EORTC QLQ-C30). Частота досягнення ПР з кліренсом IDH1-мутації порівнювалася між групами дослідження, а також проводилася оцінка початкових мутацій в інших генах.
Результати
Пацієнти
Пацієнтів включали у дослідження з березня 2018 по травень 2021 року. На момент припинення збору даних (18 березня 2021 року) з 295 пацієнтів, які пройшли скринінг, 146 були рандомізовані: 72 – у групу івосиденібу й азацитидину (медіана віку 76,0 року; діапазон 58,0-84,0) та 74 – у групу плацебо й азацитидину (медіана віку 75,5 року; діапазон 45,0-94,0).
Первинна кінцева точка
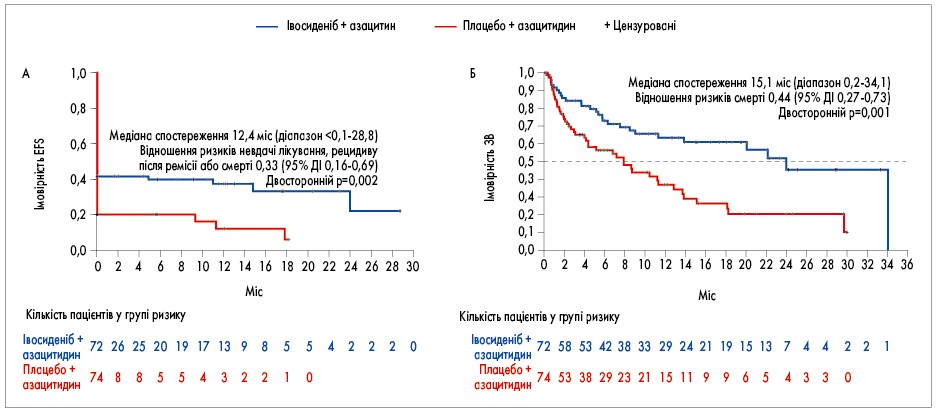
Медіана періоду спостереження становила 12,4 міс. Виживаність без подій була статистично значуще довшою у групі івосиденібу й азацитидину порівняно з групою плацебо та азацитидину (коефіцієнт ризику – КР– невдачі лікування, рецидиву після ПР або смерті 0,33; 95% довірчий інтервал – ДІ – 0,16-0,69; p=0,002; рис. А). Оскільки більше половини пацієнтів у кожній групі не досягли ПР на 24-му тижні, медіана виживаності без подій була однаковою в обох групах: 0,03 міс (95% ДІ 0,03-11,01) у групі івосиденібу й азацитидину та 0,03 міс (95% ДІ не оцінювався) у групі плацебо й азацитидину. Однак розрахункова ймовірність залишитися без подій через 6 та 12 міс становила 40 та 37% відповідно у групі івосиденібу й азацитидину порівняно з 20 та 12% відповідно у групі плацебо та азацитидину.
Рис. Виживаність без подій (А) і ЗВ (Б) у дослідженні AGILE
Вторинні кінцеві точки
У групі івосиденібу й азацитидину медіана ЗВ становила 24,0 міс (95% ДІ 11,3-34,1), а у групі плацебо й азацитидину – 7,9 міс (95% ДІ 4,1-11,3; КР смерті 0,44; 95% ДІ 0,27-0,73; p=0,001; рис. Б).
Якість життя, пов’язана зі здоров’ям
Початкові показники за питальником EORTC QLQ-C30 були доступні для 69 (96%) пацієнтів у групі івосиденібу й азацитидину та 66 (89%) пацієнтів у групі плацебо й азацитидину. Оцінка якості життя для групи плацебо й азацитидину після 19-го циклу лікування не проводилася через відсутність даних. Загальна прихильність до лікування перевищувала 70%. Результати продемонстрували перевагу комбінації івосиденібу й азацитидину за всіма субшкалами питальника EORTC QLQ-C30. Після початкового зниження показників в обох групах, що збігалося з часом до досягнення відповіді на лікування, якість життя, пов’язана зі здоров’ям, у пацієнтів, які отримували івосиденіб та азацитидин, повернулася до початкового рівня або перевищила його, тоді як у групі плацебо й азацитидину покращення порівняно з початковим рівнем не спостерігалося.
Безпека
Загалом 66 (93%) з 71 пацієнта, які отримували івосиденіб та азацитидин, і 69 (95%) із 73 пацієнтів, котрим вводили плацебо й азацитидин, мали небажані явища 3 ступеня або вище. Небажані явища 3 ступеня або вище, що виникли у більш ніж 15% пацієнтів в обох групах, включали фебрильну нейтропенію (28% при застосуванні івосиденібу й азацитидину та 34% – плацебо та азацитидину), анемію (25 і 26% відповідно), нейтропенію (27 та 16%), тромбоцитопенію (19 і 23%) та пневмонію (16 і 18%).
Висновки
У рандомізованому подвійному сліпому плацебо-контрольованому дослідженні III фази AGILE комбінація івосиденібу й азацитидину забезпечила статистично значуще покращення виживаності без подій, відповіді на терапію, ЗВ порівняно з плацебо та азацитидином у пацієнтів з уперше діагностованою ГМЛ та IDH1-мутацією, які не були кандидатами для проведення інтенсивної хіміотерапії. Ця клінічна ефективність підкріплюється прийнятними показниками якості життя, пов’язаної зі здоров’ям, збільшенням частоти досягнення незалежності від гемотрансфузій і профілем небажаних явищ, який відповідає очікуваному при лікуванні гострої лейкемії.
Список літератури знаходиться в редакції.
Реферативний огляд Montesinos P., Recher C., Vives S. et al. Ivosidenib and Azacitidine in IDH1-Mutated Acute Myeloid Leukemia. N Engl J Med. 2022 Apr 21; 386(16): 1519-1531.
DOI: 10.1056/NEJMoa2117344.
Підготувала Анна Сочнєва
Підготовлено на замовлення ТОВ «Серв’є Україна»
OncoHem-NonP-С1-2 (2023-2025, 2 years)-4
КОМЕНТАР ЕКСПЕРТА
 Про діагностику і таргетну терапію у пацієнтів з ГМЛ й IDH1-мутацією та використання таргетного препарату івосиденібу у комбінації з азацитидином, що є новим ефективним варіантом лікування зазначеної патології, розповів керівник Центру гематології, хіміотерапії гемобластозів та трансплантації кісткового мозку КЛ «Феофанія» ДУС, професор кафедри клінічної лабораторної діагностики Національного університету охорони здоров’я України імені П.Л. Шупика (м. Київ), доктор медичних наук Сергій Вікторович Клименко.
Про діагностику і таргетну терапію у пацієнтів з ГМЛ й IDH1-мутацією та використання таргетного препарату івосиденібу у комбінації з азацитидином, що є новим ефективним варіантом лікування зазначеної патології, розповів керівник Центру гематології, хіміотерапії гемобластозів та трансплантації кісткового мозку КЛ «Феофанія» ДУС, професор кафедри клінічної лабораторної діагностики Національного університету охорони здоров’я України імені П.Л. Шупика (м. Київ), доктор медичних наук Сергій Вікторович Клименко.
? Які мутації спостерігаються у пацієнтів з ГМЛ? Чи впливає це на прогноз?
– ГМЛ характеризується високим мутаційним навантаженням. Згідно з дослідженням V.V. Prassek (2018), середня кількість мутацій в одного пацієнта становила чотири. Частота мутацій була такою: TET2 – 42%, DNMT3A – 35%, NPM1 – 32%, SRSF2 – 25%, ASXL1 – 21%, RUNX1 – 19%, FLT3-ITD – 18%, NRAS – 17%, IDH2 – 15%, TP53 – 14%, FLT3-TKD – 12%, IDH1 – 9%. Автори дійшли висновку, що пацієнти з IDH1-мутаціями (9%) рідко досягали ПР, а ЗВ у цій підгрупі була значно коротшою, ніж у пацієнтів з IDH1 «дикого» типу.
Визначення мутацій у генах ізоцитратдегідрогенази було однією з найпомітніших знахідок у дослідженнях біології ГМЛ останніх десятиріч. Мутації IDH1/2 фіксують приблизно в 20% випадків ГМЛ, зокрема, за даними різних авторів, у 6-16% хворих на ГМЛ наявні мутації гена IDH1, а у 8-19% пацієнтів – IDH2.
? Коли саме варто робити тест на IDH1-мутацію? Які критерії є вирішальними?
– Визначення IDH1/2-позитивності стає важливим етапом діагностики ГМЛ. Мутації IDH1/2 вважають генетичною подією ранніх етапів лейкогенезу, тож більшість IDH1/2-позитивних випадків ГМЛ можна визначити вже під час первинної діагностики захворювання. Але мутація може набуватися й пізніше, тож при плануванні схеми лікування при рецидивній ГМЛ перевірка мутаційного статусу IDH1/2 вважається також доречною.
Пацієнти з ГМЛ та IDH-мутаціями, як правило, старшого віку (середній вік маніфестації хвороби – 67 років), мають більшу кількість тромбоцитів, вищий бластоз у кістковому мозку та периферичній крові, глибшу нейтропенію на момент встановлення діагнозу. Крім того, IDH-мутації здебільшого виявляють у групі середнього ризику, пацієнти частіше характеризуються нормальним каріотипом і мають підвищену частоту мутацій FLT3-ITD та NPM1. Тому треба звертати увагу на вік пацієнта та вищезазначені критерії.
? Чи впливає наявність IDH1-мутації на прогноз і вибір лікування?
– Незважаючи на чітке уявлення про особливості патогенезу IDH-позитивної ГМЛ, прогностичне значення IDH-мутацій залишається суперечливим. За даними окремих досліджень, IDH-мутації у поєднанні з NPM1-мутаціями і навіть з негативним молекулярним статусом FLT3-ITD були пов’язані зі сприятливішими результатами при ГМЛ у групі хворих проміжного ризику. Інші дослідники виявили гіршу ЗВ у хворих на ГМЛ з IDH-мутаціями, навіть у разі якщо ця аномалія була асоційована зі сприятливою щодо виживаності мутацією гена NPM1. Проте дані більшості досліджень свідчать радше про відсутність істотної прогностичної значущості IDH1/2-мутацій. У системі стратифікації ризику ELN (2022) не враховано мутаційний статус генів IDH при оцінці хворих на ГМЛ. Однак мутаційний статус генів IDH1/2 є важливим маркером предикції, оскільки визначає перспективи лікування хворих на ГМЛ таргетними препаратами – інгібіторами IDH.
? Чому важливо обирати саме таргетну терапію для пацієнтів з ГМЛ та IDH1-мутацією?
– Таргетна терапія, а саме препарат івосиденіб, який був схвалений Управлінням з контролю якості харчових продуктів і лікарських препаратів США, Європейським агентством з лікарських засобів і Міністерством охорони здоров’я України (наказ № 908 від 28.05.2024, реєстрацiйне посвiдчення № UA/20476/01/01) для лікування пацієнтів із вперше діагностованою і рецидивуючою/рефрактерною ГМЛ, є інгібітором мутованого ферменту IDH1. Мутований IDH1 перетворює альфа-кетоглутарат (α-KG) у 2-гідроксиглутарат (2-HG), що блокує диференціацію клітин і сприяє онкогенезу у гематологічних злоякісних пухлинах. У пацієнтів із гематологічними злоякісними пухлинами з IDH1-мутацією застосування багаторазового режиму дозування івосиденібу 500 мг на добу знижувало концентрацію 2-HG у плазмі крові до рівнів, наближених до тих, що спостерігалися у здорових осіб. У кістковому мозку пацієнтів із гематологічними злоякісними пухлинами середнє зниження концентрації 2-HG становило 93,1%.
Ефективність і безпека івосиденібу в комбінації з азацитидином доведена в рандомізованому багатоцентровому подвійному сліпому плацебо-контрольованому клінічному дослідженні AGILE (ClinicalTrials.gov, NCT03173248) за участю літніх пацієнтів з уперше діагностованою ГМЛ та середнім віком ≥75 років, не придатних до інтенсивної хіміотерапії. Медіана періоду спостереження становила 12,4 міс, а розрахункова ймовірність залишитися без подій через 6 та 12 міс – 40 та 37% відповідно у групі івосиденібу й азацитидину порівняно з 20 та 12% у групі плацебо й азацитидину. Досягнення глибокої відповіді із медіаною ЗВ 24 міс зафіксовано у 42% хворих. Тож використання інгібіторів IDH може значно покращити результати лікування ГМЛ і дозволить відійти від наявної парадигми мутаційно агностичної високотоксичної хіміотерапії хворих.
? Як вплине схвалення нової таргетної терапії івосиденібом на клінічну практику?
– З появою таргетної терапії IDH1-позитивної ГМЛ розшириться спектр терапевтичних можливостей для цієї складної категорії хворих. Сприятливий профіль токсичності івосиденібу уможливить проведення високоефективної терапії навіть пацієнтам літнього віку, обтяженим соматичної патологією. Пацієнтам, не придатним для інтенсивної хіміотерапії, прийом івосиденібу в комбінації з азацитидином істотно подовжить тривалість життя, надасть можливість досягти ремісії, оскільки інші опції у них можуть не бути використані через надмірну токсичність лікування. Для пацієнтів, придатних для інтенсивної хіміотерапії, івосиденіб може стати важливою складовою багатокомпонентної терапії, що підвищить частоту досягнення ремісії та збільшить шанси на одужання.
Тематичний номер «Онкологія. Гематологія. Хіміотерапія» № 3 (89) 2024 р.