4 грудня, 2024
Розширюємо можливості пацієнтів з алергійними захворюваннями. За матеріалами EAACI‑2024
 Весною 2024 р. у Валенсії (Іспанія) відбулась одна з найочікуваніших подій для європейської алергологічної спільноти – Конгрес Європейської академії алергології та клінічної імунології (European Academy of Allergy & Clinical Immunology, EAACI). Окрім обговорення новітніх підходів до діагностики, профілактики та лікування алергійних захворювань (АЗ) було розглянуто використання ІТ-технологій для вибору персоналізованого підходу до лікування та впровадження концепції One Health, що розглядає здоров’я людей із точки зору взаємозв’язку людей, тварин, рослин і довкілля, у контексті АЗ. Особливу увагу в рамках заходу було приділено очним симптомам алергії.
Весною 2024 р. у Валенсії (Іспанія) відбулась одна з найочікуваніших подій для європейської алергологічної спільноти – Конгрес Європейської академії алергології та клінічної імунології (European Academy of Allergy & Clinical Immunology, EAACI). Окрім обговорення новітніх підходів до діагностики, профілактики та лікування алергійних захворювань (АЗ) було розглянуто використання ІТ-технологій для вибору персоналізованого підходу до лікування та впровадження концепції One Health, що розглядає здоров’я людей із точки зору взаємозв’язку людей, тварин, рослин і довкілля, у контексті АЗ. Особливу увагу в рамках заходу було приділено очним симптомам алергії.

 Окремий блок виступів був присвячений проблемам алергійного ринокон’юнктивіту (АРК), зокрема його очним проявам, та якості життя (ЯЖ) пацієнтів з АЗ. Про розширення можливостей контролю алергійних проявів і поліпшення ЯЖ пацієнтів у своїй лекції розповів алерголог, пульмонолог, професор університету «Humanitas», директор Центру персоналізованої медицини, астми та алергії при дослідницькій лікарні «Humanitas» IRCCS (Мілан, Італія) Giorgio Walter Canonica.
Окремий блок виступів був присвячений проблемам алергійного ринокон’юнктивіту (АРК), зокрема його очним проявам, та якості життя (ЯЖ) пацієнтів з АЗ. Про розширення можливостей контролю алергійних проявів і поліпшення ЯЖ пацієнтів у своїй лекції розповів алерголог, пульмонолог, професор університету «Humanitas», директор Центру персоналізованої медицини, астми та алергії при дослідницькій лікарні «Humanitas» IRCCS (Мілан, Італія) Giorgio Walter Canonica.
Спікер передусім зазначив, що не кожен лікар усвідомлює масштаби тягаря алергійного риніту (АР). Так, у США на АР страждає до 30% населення, при цьому поширеність АР продовжує зростати в усьому світі, особливо в Океанії та Латинській Америці. Значущим є й економічний тягар АР, наприклад у США він дорівнює приблизно 11 млрд доларів на рік, і за останні 5 років ця сума подвоїлась. В Європейському союзі щорічні витрати на АР становлять від 30 до 50 млрд євро, що красномовно вказує на актуальність оптимізації менеджменту цього стану.
Для ефективного ведення пацієнта з АР треба пам’ятати, що це захворювання суттєво впливає на ЯЖ, бо пов’язане з відчуттям дискомфорту, соціальною ізоляцією та зниженням продуктивності праці. Понад 60% пацієнтів з АР повідомляють про порушення сну, 50% – мають проблеми через обмеження фізичної активності, 60% – стикаються з порушеннями настрою та зниженням результативності на роботі і під час навчання. Саме тому при веденні пацієнтів з АР необхідно використовувати спеціалізовані опитувальники для оцінки ЯЖ.
Варто зауважити, що зниження ЯЖ при АЗ пов’язане не лише із симптомами захворювання, але і з їх неадекватним лікуванням. Дані епідеміологічних досліджень показали, що 70% пацієнтів із симптомами АР не звертаються по медичну допомогу, а натомість використовують безрецептурні деконгестанти, які не впливають на причину захворювання, дають тимчасове полегшення і, з часом, зумовлюють розвиток медикаментозного риніту. Якщо ж пацієнти все-таки звертаються до лікаря і їм призначають H1-антигістамінні препарати (АГП) І покоління, це часто призводить до розчарування, адже надмірна седація – поширена побічна дія цих препаратів – інколи погіршує ЯЖ навіть сильніше, ніж власне симптоми алергії.
Порівняно з АГП І покоління АГП ІІ покоління є високоселективними щодо H1-рецепторів і не лише мають кращий профіль безпеки, а й позбавлені антихолінергічних ефектів або кардіотоксичності. Сучасні H1-АГП ІІ покоління чинять мінімальну седативну дію або взагалі не виявляють цього ефекту завдяки слабкому проникненню крізь гематоенцефалічний бар’єр. З цих причин їх сьогодні рекомендують як терапію першої лінії в пацієнтів з АР і кропив’янкою.
Нещодавнє міжнародне дослідження Delphi було проведено з метою оцінки експертами із 17 європейських і неєвропейських країн тягаря АР та кропив’янки, сучасних варіантів їх лікування і ролі біластину як АГП ІІ покоління (Church, 2023). У результаті понад 96% експертів дійшли одноголосного консенсусу щодо вираженого впливу АР та кропив’янки на популяційне здоров’я, ЯЖ і ключової ролі АГП ІІ покоління, і біластину зокрема, в ефективному контролі симптомів.
Біластин є потужним високоселективним пероральним АГП ІІ покоління, який тривало зв’язується з Н1-гістаміновими рецепторами, що забезпечує його подовжену тривалість дії. Він проникає в центральну нервову систему так само, як і плацебо, що дає підставу класифікувати його як АГП, що не проникає в мозок. Це обмежує можливість седації, погіршення когнітивних функцій або порушення здатності керувати автомобілем, а також потенціювання ефектів алкоголю. Після перорального прийому біластин швидко всмоктується зі шлунково-кишкового тракту завдяки активному механізму поглинання, що забезпечує швидший початок і більшу тривалість дії в порівнянні з фексофенадином, дезлоратадином і рупатадином. Біластин має низький потенціал міжлікарської взаємодії, оскільки не впливає значною мірою на ферментну систему CYP in vitro. Оскільки препарат практично не метаболізується, корекція дози пацієнтам із порушенням функції нирок і печінки, а також літнім пацієнтам не потрібна. Усе вищезазначене робить біластин ідеальним кандидатом для довготривалого контролю симптомів АР та кропив’янки.
 Тему вибору оптимального препарату для контролю симптомів АРК продовжив у своїй лекції кандидат наук, офтальмолог кліники «Сан Карлос» (м. Мадрид, Іспанія) Pedro Arriola Villalobos.
Тему вибору оптимального препарату для контролю симптомів АРК продовжив у своїй лекції кандидат наук, офтальмолог кліники «Сан Карлос» (м. Мадрид, Іспанія) Pedro Arriola Villalobos.
Більшість пацієнтів з АР, наголосив доповідач, мають очні симптоми, але лише 10% з них звертаються по медичну допомогу. Решта займається самолікуванням і використовує безрецептурні очні краплі, які не лише не впливають на причину симптомів, а й призводять до розвитку синдрому сухого ока (ССО).
Незважаючи на те що АРК і ССО є різними очними розладами, багато доказів свідчать про те, що їхні патофізіологічні механізми подібні, а нестабільність слізної плівки відіграє провідну роль в їхньому патогенезі (Montero-Iruzubieta, 2023). Фактично, зміни слізної плівки часто спостерігають у пацієнтів з АРК, а дисфункція епітеліального бар’єра характерна для кількох АЗ. Аналіз біомаркерів у слізній рідині і на поверхні ока нещодавно виявив, що прозапальні цитокіни, які зазвичай вважають специфічними для АРК, також надмірно експресують у пацієнтів із ССО. Цими цитокінами є інтерлейкін (IЛ)-4, IЛ‑5 та IЛ‑13 із запального шляху Th2 та IЛ‑1α, IЛ‑1β, IЛ‑17, фактор некрозу пухлини та інтерферон-гамма зі шляху Th1-Th7. Крім того, зміна рівнів муцинів (MUC1, MUC2, MUC4, MUC5 і MUC16) є поширеним відхиленням у слизовому шарі слізної плівки за обох станів.
Зміни, спричинені АРК, зумовлюють нестабільність слізної плівки та призводять до розвитку ССО. Алергени з протеолітичною активністю можуть руйнувати щільні з’єднання епітелію кон’юнктиви, дестабілізувати Е-кадгерин і проникати крізь епітелій. Крім того, потрапивши в підслизовий простір, алергени взаємодіють зі специфічними IgE, зв’язаними з високоафінними рецепторами IgE, розташованими на поверхні дендритних і кон’юнктивальних опасистих клітин. При IgE-опосередкованій Th1-алергійній реакції опасисті клітини дегранулюють, негайно вивільняючи гістамін та інші медіатори, що містяться в гранулах. Подальше вивільнення цитокінів призводить до запальної Тh2-відповіді, переважно при АРК, і до змішаних запальних відповідей Тh2 і Тh3 при тяжчих формах очних алергій (весняний та атопічний кератокон’юнктивіт). Th2-асоційовані цитокіни (IЛ‑4, IЛ‑5, IЛ‑13) і гістамін за умови надмірної експресії сприяють довгостроковій метаплазії епітелію кон’юнктиви, руйнуванню епітелію рогівки та стимуляції секреції келихоподібних клітин, що може змінити слізну плівку. Дисфункція епітеліального бар’єра при АРК також підтримує порочне коло алергічного запалення шляхом полегшення парацелюлярного транспорту алергенів, патогенів, забруднювальних речовин та інших шкідливих тригерів.
З огляду на все це, при виборі препарату для ефективного менеджменту очних симптомів алергії варто обирати засіб, який, з одного боку, стабілізує опасисті клітини, а з іншого – не містить консерванти, мікропластик та інші місцево-подразнювальні домішки. Біластин у формі розчину для очей у дозі 6 мг/мл відповідає всім вищезазначеним вимогам. Додатковими перевагами є також зручність застосування – 1 раз на добу, що значно поліпшує прихильність пацієнтів до лікування, і наявність у складі 0,1% гіалуронової кислоти, яка забезпечує додатковий комфорт у разі супутнього ССО.
Ефективність біластину у формі очних крапель порівнювали з розчинником (плацебо) в одноцентровому подвійному замаскованому рандомізованому дослідженні фази 2 (Gomes, 2023). Основною кінцевою точкою ефективності було зменшення свербежу очей. Модель Ora-CAC Conjunctival Allergen Challenge використовували для оцінки очних і назальних симптомів на початку дії (15 хв) і через 8 та 16 год після застосування крапель. Також оцінювали переносимість і безпеку препарату.
Офтальмологічні форми біластину 0,2%, 0,4% і 0,6% були достовірно ефективнішими (р>0,001) порівняно з плацебо в усуненні очного свербежу через 3; 5 і 7 хв після використання подразника на початку дії (15 хв) і через 8 год після застосування. Біластин 0,6% також був ефективним через 16 год після застосування. Відмінності в лікуванні біластином 0,6% були статистично значущими (р<0,001) порівняно з плацебо в усі моменти часу щодо сльозотечі, набряку повік і назальних симптомів. Побічних явищ не спостерігали. Отримані дані підтверджують належний профіль ефективності та безпеки, що робить біластин найбільш підходящим засобом для лікування очних симптомів при АРК.
 Фінальна частина блоку, яку презентував увазі присутніх алерголог, дерматолог, доктор медичних наук, професор, директор Інституту алергології Медичного університету «Charité» (м. Берлін, Німеччина), президент Європейської глобальної мережі з алергії та бронхіальної астми (Global Allergy and Asthma European Networ, GA²LEN) і голова Європейського центру алергологічних досліджень (European Centre for Allergy Research Foundation, ECARF) Torsten Zuberbier, стосувалася пацієнт-орієнтованого підходу в лікуванні хронічної кропив’янки (ХК) та ролі біластину в менеджменті цього захворювання. У той час як гостра кропив’янка здебільшого пов’язана з алергійною або псевдоалергійною реакцією на їжу, ліки або інфекції, ХК є складнішим захворюванням із різними додатковими етіопатологічними механізмами та провокувальними факторами.
Фінальна частина блоку, яку презентував увазі присутніх алерголог, дерматолог, доктор медичних наук, професор, директор Інституту алергології Медичного університету «Charité» (м. Берлін, Німеччина), президент Європейської глобальної мережі з алергії та бронхіальної астми (Global Allergy and Asthma European Networ, GA²LEN) і голова Європейського центру алергологічних досліджень (European Centre for Allergy Research Foundation, ECARF) Torsten Zuberbier, стосувалася пацієнт-орієнтованого підходу в лікуванні хронічної кропив’янки (ХК) та ролі біластину в менеджменті цього захворювання. У той час як гостра кропив’янка здебільшого пов’язана з алергійною або псевдоалергійною реакцією на їжу, ліки або інфекції, ХК є складнішим захворюванням із різними додатковими етіопатологічними механізмами та провокувальними факторами.
Хоча кропив’янка беззаперечно належить до шкірних захворювань, з’являється все більше доказів на користь того, що ХК є системним захворюванням із клінічними симптомами та ознаками, які переважно проявляються на шкірі (Darlenski R., 2014).
Оскільки це захворювання є системним, таким самим має бути його лікування.
Останнє оновлення та перегляд рекомендацій міжнародної Європейської академії алергології та клінічної імунології EAACI / GA2LEN / Європейського дерматологічного форуму (European Dermatology Forum – EDF) / Азіатсько-Тихоокеанської асоціації алергійної астми та клінічної імунології щодо визначення, класифікації, діагностики та лікування кропив’янки було опубліковано у 2022 р. (Zuberbier T., 2022). Його метою була допомога лікарям первинної ланки і фахівцям у лікуванні пацієнтів із кропив’янкою. Ці рекомендації обговорювалися на конференції Delphi за участю понад 250 спеціалістів, і їх схвалило понад 50 міжнародних товариств.
Поточна версія міжнародної настанови з менеджменту кропив’янки містить вичерпні та детальні вказівки щодо діагностики цієї патології. По-перше, у ній наголошується на тому, що діагностичне обстеження при хронічній спонтанній кропив’янці (ХСК) має кілька цілей, які разом називаються 7 Cs.
Діагностичні кроки передбачають:
- диференційний діагноз і підтвердження захворювання;
- пошук глибинних причин;
- визначення відповідних умов, які змінюють активність захворювання;
- виявлення супутніх захворювань;
- перевірку наслідків ХСК;
- оцінку предикторів захворювання та відповіді на лікування;
- моніторинг активності захворювання, впливу на ЯЖ та контролю.
З цією метою діагностичне обстеження має охоплювати ретельний збір анамнезу, фізикальне обстеження (у тому числі перегляд фотографій пухирів і/або ангіоневротичного набряку [АНН]), використання опитувальників, що містять показники результативності лікування, про які повідомляє пацієнт (PROM), і загальні тести (у тому числі аналіз крові з формулою та визначення рівня С-реактивного білка і/або швидкості осідання еритроцитів (ШОЕ) і загального рівня IgE та IgG до тиреоїдної пероксидази [TPO]). Останні 2 тести були додані на основі останніх доказів того, що ХСК може бути наслідком аутоалергійної або аутоімунно опосередкованої активації опасистих клітин шкіри, з IgE-аутоантитілами до власних антигенів при аутоалергійній ХСК та аутоантитілами IgG або IgM, спрямованими на активацію опасистих клітин, при аутоімунній ХСК. Визначення рівнів IgG до ТПО та загального IgE може допомогти внести більше ясності щодо того, чому в пацієнтів виникла ХСК.
Пацієнти з аутоімунною ХСК частіше мають низькі або дуже низькі рівні загального IgE та підвищені рівні IgG до ТПО. Високе співвідношення IgG до ТПО і загального IgE наразі є найкращим сурогатним маркером аутоімунної ХСК.
Потрібно також визначити індекс ХК у пацієнтів, які не реагують на H1-АГП, щоб з’ясувати, чи є в них антитіла проти IgE, FcεRI або анти-FcεRII або альтернативного фактора вивільнення гістаміну. Також повідомлялося, що ці біомаркери є прогностичними маркерами ефективності лікування омалізумабом або імуносупресантами, такими як циклоспорин. Крім того, як додаткова процедура для діагностики аутореактивної форми захворювання пропонується тест з аутологічною сироваткою, але його актуальність не дуже висока, оскільки омалізумаб діє незалежно від результатів цього тесту. На основі результатів, отриманих за допомогою базових тестів, даних анамнезу, фізичного огляду та PROM, за показаннями можна провести подальше діагностичне тестування.
Хоча запропонований діагностичний підхід забезпечує найоптимальніший менеджмент ХСК, у реальній клінічній практиці встановити причину чи тригери кропив’янки або ж усунути їх часто неможливо. Саме тому на перший план у лікуванні ХСК виходить патогенетичне лікування.
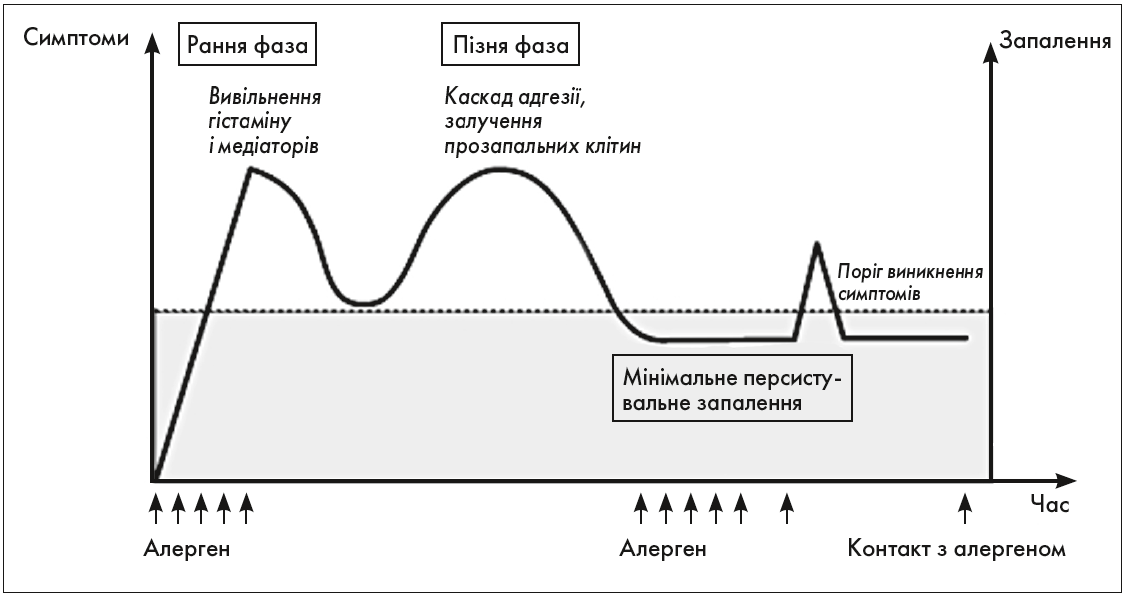
Одним із головних механізмів, що лежать в основі розвитку як ХСК, так і АР, є феномен мінімального персистувального запалення (МПЗ). Цей термін використовують для опису явища, за якого повторний вплив низьких рівнів алергену не зумовлює симптомів алергії, але спричинює підвищену чутливість до наступного впливу алергену, що відображено на рисунку (Canonica G.W., 2009). У слизовій оболонці носа МПЗ характеризується наявністю запальних клітин (еозинофілів, нейтрофілів) і підвищеною експресією ICAM‑1 на епітеліальних клітинах, які були виявлені у безсимптомних пацієнтів із сезонним та цілорічним АР протягом періодів без симптомів.
Рис. Парадигма мінімального персистувального запалення (Canonica G.W., 2009)
Саме вплив на МПЗ пояснює користь від лікування алергійного запалення навіть у безсимптомні періоди. Це обов’язково необхідно донести пацієнту, адже саме в цей період за рахунок МПЗ розвивається структурне ушкодження тканин, і відміна препаратів у такому разі створить порочне коло МПЗ та унеможливить контроль захворювання.
Якщо говорити про безпосередній вибір засобу для контролю симптомів ХСК, то як і при АР, препаратами вибору залишаються cучасні АГП ІІ покоління. Метою лікування ХСК є повний контроль захворювання і нормалізація ЯЖ. Менеджмент кропив’янки – це динамічний процес, який передбачає постійну оцінку контролю захворювання за допомогою PROM, зокрема тесту з оцінки контролю кропив’янки (UCT), і посилення або послаблення алгоритму лікування відповідно до перебігу захворювання. За неефективності первинного лікування треба підвищувати дозу АГП, а не додавати ще один лікарський засіб, оскільки доведено, що підвищення дози вчетверо є безпечнішим для пацієнта і не створює передумов для міжлікарських взаємодій. Важливо наголосити, що цей алгоритм є круговим, тобто його необхідно застосовувати як для ескалації, так і для деескалації терапії, таким чином, ми завжди застосовуємо найменшу ефективну дозу, яка забезпечує повний контроль симптомів.
Окрім того, якщо відомі тригерні фактори, що зумовлюють загострення ХСК, варто радити пацієнтам застосовувати подвійну дозу АГП (замість звичної щоденної) у день контакту з потенційним провокувальним фактором. Ідеальний АГП має ефективно усувати симптоми ХСК, діяти швидко і довго, найліпше – застосовуватися 1 раз на добу і не спричиняти небажаних ефектів, таких як сонливість. Усім цим вимогам в аспекті лікування пацієнтів із кропив’янкою відповідає біластин.
Він має швидший початок дії, ніж цетиризин, дезлоратадин і рупатадин. Через півтори години і АНН, і уртикарні висипання пригнічувалися на >70% в 11 з 12 осіб, що приймали біластин, порівняно з 3 з 11 осіб, що приймали цетиризин (p=003). У дослідженні Antonijoan та співавт. висипання починали зникати через годину при використанні біластину в дозі 20 мг і через 4 год після прийому дезлоратадину в дозі 5 мг або рупатадину в дозі 10 мг, тоді як для інгібування зони набряку та почервоніння біластин у дозі 20 мг починав діяти через 30 хв, а дезлоратадину і рупатадину було потрібно 4 год, щоб продемонструвати суттєву різницю проти плацебо. Біластин також достовірно зменшував свербіж, чого при застосуванні дезлоратадину чи рупатадину не спостерігали (Church, 2019).
Ефективність біластину в дорослих пацієнтів із кропив’янкою оцінювали в кількох рандомізованих контрольованих клінічних дослідженнях. У дослідженнях, проведених в Європі, зазвичай брали участь пацієнти віком 12-70 років, тоді як у дослідженнях в Японії – дорослі віком 18-74 роки. Біластин у дозі 20 мг 1 раз на добу був достовірно ефективніше за плацебо зменшував симптоми ХСК (оцінені за допомогою шкали загальної оцінки тяжкості кропив’янки, TSS) і був так само ефективним, як і левоцетиризин у дозі 5 мг 1 раз на добу. Біластин у дозі 20 мг 1 раз на добу також був значно ефективнішим за плацебо щодо контролю симптомів у пацієнтів із контактною холодовою кропив’янкою. Застосування біластину характеризувалося швидким початком дії з достовірним поліпшенням оцінки за TSS у пацієнтів із ХСК після одного дня лікування. Біластин у дозі 20 мг також забезпечував достовірне поліпшення індивідуальних симптомів, у тому числі АНН, висипу та свербежу (Church, 2019).
Окрім впливу на об’єктивні параметри було показано, що біластин у дозі 20 мг 1 раз на добу поліпшує ЯЖ в пацієнтів із ХСК. У найбільшому рандомізованому дослідженні середній загальний показник індексу ЯЖ через 4 тиж лікування значуще поліпшився порівняно з плацебо (-9,45 проти -5,93 відповідно; p<001).
Згідно з результатами досліджень біластин у дозі 20 мг добре переносився дорослими пацієнтами з кропив’янкою, при цьому загальна частота побічних ефектів була подібною до такої при застосуванні плацебо.
Однорічне непорівняльне дослідження за участю 198 дорослих із ХСК (n=56) або зі свербежем, пов’язаним з іншими шкірними захворюваннями (такими як екзема/дерматит, свербіж або шкірний свербіж), показало, що ефективність біластину 20 мг 1 раз на добу зберігалася і препарат добре переносився протягом тривалого періоду. TSS, показники висипань та свербежу, а також показник ЯЖ значно поліпшилися (p<001) порівняно з базовим рівнем із 2-го тиж і залишалися такими самими після цього. Побічні ефекти, пов’язані із застосуванням біластину (усі від легкого до помірного ступеня тяжкості), спостерігали у 2,5% пацієнтів протягом 1-річного періоду дослідження; сонливість була зареєстрована в 1% пацієнтів (Church, 2019).
Такі поширені АЗ, як АР та ХСК, асоційовані зі значущим тягарем для здоров’я пацієнтів і нерідко залишаються недооціненими як за своїм впливом на якість життя, так і за рівнем прихильності до лікування. Важливим аспектом ефективного контролю цих захворювань є застосування сучасних АГП ІІ покоління, зокрема біластину, у найменшій ефективній дозі, з можливістю збільшення або зниження дози залежно від ступеня контролю симптомів. Також необхідно забезпечити належний рівень комунікації з пацієнтом, пояснювати йому значення щоденного прийому АГП і важливість контролю МПЗ. Взаємна співпраця між пацієнтом і лікарем є запорукою досягнення стабільного контролю АЗ і поліпшення ЯЖ пацієнтів.
Підготувала Ганна Кирпач
Тематичний номер «Пульмонологія, Алергологія, Риноларингологія» № 3 (68) 2024 р.