21 квітня, 2024
Чому пацієнти з хронічною кропив’янкою часто залишаються недолікованими і як виправити ситуацію?
Результати онлайн-опитування DERMLINE
Хронічна кропив’янка (ХК) – це захворювання шкіри, яке характеризується повторюваною появою пухирів або уртикарних висипань з ангіоневротичним набряком (АНН) або без нього протягом понад 6 тиж [1, 2]. Це складно прогнозоване виснажливе захворювання виявляє виражений негативний вплив на якість життя пацієнтів [1]. ХК може знижувати продуктивність праці [3], порушувати сон і повсякденну активність [4], а також значуще підвищувати рівень тривоги та психологічного дистресу [5-7]. Крім того, непередбачуваний характер АНН, пов’язаного з ХК, який характеризується раптовим набряком дерми, підшкірної клітковини або підслизової оболонки, може супроводжуватися страхом пережити епізод, що загрожує життю [8]. Викликає тривогу й те, що АНН спостерігають приблизно в 40% пацієнтів із кропив’янкою [9], а поєднання АНН і пухирів – у 67% пацієнтів [8]. Незважаючи на те що настанови Європейської академії алергології та клінічної імунології (The European Academy of Allergy and Clinical Immunology – EAACI), Глобальної європейської спілки алергії та астми (Global Allergy and Asthma European Network – GA2LEN), Європейського дерматологічного форуму (The European Dermatology Forum – EDF) і Всесвітньої алергологічної організації (WAO) – EAACI/GA2LEN/EDF/WAO щодо лікування кропив’янки рекомендують використовувати специфічний алгоритм ескалації лікування до досягнення повного контролю симптомів, в умовах реальної клінічної практики значна частка пацієнтів із ХК залишаються недолікованими.
Результати всесвітнього обсерваційного дослідження ХК в умовах реальної клінічної практики AWARE показали, що перебіг хронічної спонтанної кропив’янки (ХСК) в пацієнтів, резистентних до H1-антигістамінних препаратів (Н1-АГП), характеризується поганим контролем захворювання, АНН, коморбідною хронічною індукованою кропив’янкою (ХІК), неповним виліковуванням, низькою якістю життя і значною залежністю від ресурсів охорони здоров’я [10]. Дійсно, численні глобальні звіти демонструють, що пацієнти з ХК недостатньо лікуються і не отримують рекомендованої терапії [4, 11, 12], таким чином наголошуючи на необхідності більшої обізнаності та дотримання міжнародних настанов.
Нещодавно проведене онлайн-опитування (DERMLINE) також оцінювало тягар ХК, однак із позиції окремого пацієнта, з метою висвітлення важливих незадоволених клінічних потреб у цієї категорії пацієнтів.
Матеріали та методи
Критеріями включення були діагностована ХК та наявність симптомів протягом 3 міс до початку дослідження. Різні групи дослідження охоплювали: демографічні дані; характеристики захворювання; аналіз симптомів залежно від ураженої ділянки тіла; вплив на повсякденне життя; емоційне навантаження; поточне і попереднє лікування; задоволеність медичним обслуговуванням і лікуванням; ступінь контролю захворювання, який визначався за допомогою контрольного тесту на кропив’янку (UCT). UCT ретроспективно оцінює контроль захворювання за попередні 4 тиж; якщо учасники мають оцінку ≥12 балів (діапазон 0-16), кропив’янка вважається контрольованою [13].
Результати
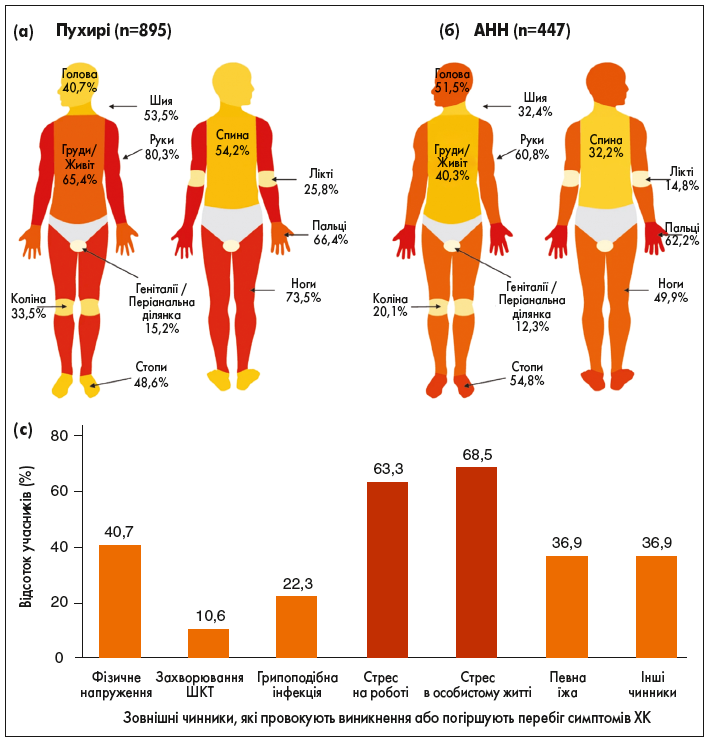
Загалом у дослідження було включено 1037 пацієнтів із діагностованою ХК; учасники заповнили онлайн-опитувальник. Середній вік (± стандартне відхилення [SD]) учасників становив 33,4±11,0 року (діапазон 18-67 років), більшість учасників були жінки (89,2%; 925/1037). Середня тривалість захворювання становила 10,0±9,3 року (n=1006), хоча 34,9% (351/1006) учасників повідомили про наявність симптомів ХК протягом >10 років (діапазон 1-53 роки). У середньому учасники мали симптоми кропив’янки протягом 3,0±4,3 року до встановлення діагнозу. Протягом 3 міс, що передували опитуванню, у 86,3% респондентів на різних ділянках тіла спостерігали пухирі, а в 43,1% – АНН. Середній бал UCT становив 7,9 (±3,9), причому 79,6% учасників мали оцінку за UCT <12, що вказує на недостатній контроль симптомів упродовж попередніх 4 тижнів. Частини тіла, які найчастіше вражалися пухирями або АНН, зображено на рисунку 1 (а, б). Більшість учасників опитування вважали, що їхні симптоми посилювалися під впливом зовнішніх чинників, повний список яких подано на рисунку 1, c. Основними тригерами були стрес через проблеми в особистому житті (68,5%) і стрес, пов’язаний із роботою (63,3%).
Рис. 1. Під час опитування учасників запитували: «На яких частинах вашого тіла переважно з’являються пухирі?» (n=895; а);
«На яких частинах тіла переважно виникає кропив’янка (АНН)?» (n=447; б);
«Який із наведених нижче зовнішніх чинників погіршує симптоми кропив’янки: фізичне напруження, захворювання шлунково-кишкового тракту (ШКТ), грипоподібна інфекція, стрес на роботі, стрес в особистому житті, певна їжа чи інші чинник?» (n=762; c). Відсотки для кожного запитання розраховували від загальної кількості респондентів
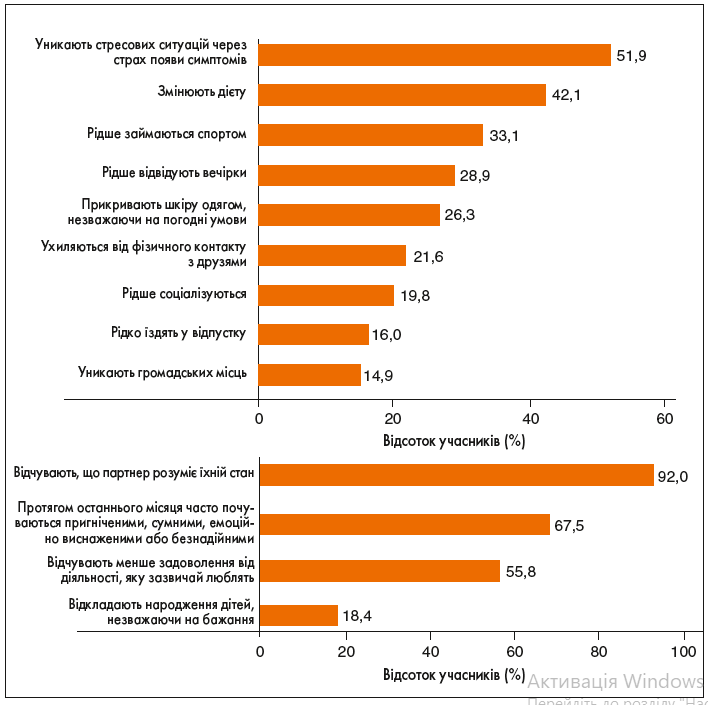
Під час оцінки впливу активності захворювання на повсякденне життя, результати якої наведено на рисунку 2 (а, б), було виявлено, що більшість учасників уникали стресових ситуацій через страх спровокувати симптоми захворювання, часто відчували депресію, смуток, емоційну втому або безнадійність протягом останнього місяця (67,5%) і відчували значно менше задоволення від діяльності, яку зазвичай любили (55,8%).
Рис. 2. Під час опитування учасників (n=1037) запитували про вплив кропив’янки на їхнє життя і про те, як вони змінили свій спосіб життя через захворювання (a), а також про вплив кропив’янки на їхні емоції та бажання (б)
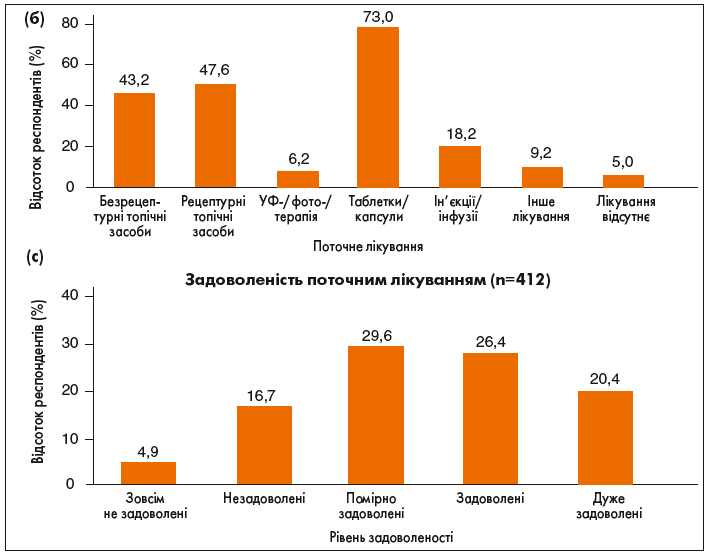
Препарати, які отримували учасники дослідження, і рівень задоволеності результатами терапії відображені на рисунку 3 (б, с).
Рис. 3. Учасники повідомили про своє поточне лікування, використовуючи попередньо сформульовані відповіді, наведені на графіку (б), і про задоволення поточним лікуванням, використовуючи попередньо визначені відповіді на графіку (n=412; c)
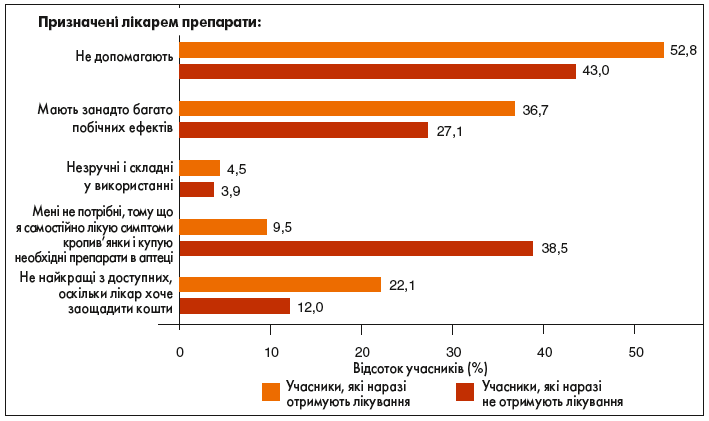
Загалом 22,6% учасників вважали, що їхнє попереднє лікування не допомогло, але теперішнє допомагає; 62,7% вказали, що попереднє лікування не допомогло і вони наразі взагалі не отримують жодних препаратів для контролю симптомів кропив’янки. Менше половини (48,8%) учасників були задоволені або дуже задоволені своїм лікуванням, а 52,8% учасників, які отримували лікування на момент опитування, вважали, що ліки їм не допомагають. Ці та інші параметри задоволеності лікуванням наведено на рисунку 4.
Рис. 4. Причини незадоволення пацієнтів ліками (пацієнти, які отримують лікування, n=211; пацієнти, які не отримують лікування, n=509)
Обговорення
Як зазначено в літературі, кропив’янка може виникати на будь-якій ділянці тіла [14, 15], але конкретної інформації про ділянки, на яких найчастіше виникають пухирі та АНН, опубліковано мало.
Згідно з результатами цього опитування, пухирями найчастіше вражалися руки, ноги, кисті/пальці та грудна клітка / живіт, тоді як АНН найчастіше виникав на кистях/пальцях, ногах, голові та руках. Багато з цих ділянок важко приховати одягом. Крім того, було встановлено, що пік активності захворювання припадає на найактивніший період життя людини (середній вік – 33,4 року), піковий час для народження дитини та високої продуктивності праці, що чинить значний вплив на якість життя [16].
Як і очікували, більшість учасників (73%) для контролю симптомів ХК, імовірно, приймали пероральні АГП (таблетки або капсули) першої лінії, хоча активна діюча речовина додатково не уточнювалася. 47,6% осіб використовували місцеві, а 43,2% – безрецептурні препарати. Це стало несподіванкою, оскільки не існує схвалених місцевих методів лікування ХК, хоча воно може передбачати застосування для усунення свербежу рецептурних топічних засобів, що містять, наприклад, кортикостероїди (КС), АГП, полідоканол, місцеві анестетики, ментол, камфору або водні розчини з цинком чи тальком [17].
Опитування також виявило, що багато осіб із ХК не лікувались у лікарів і намагалися впоратися зі своїм станом самостійно.
Учасники повідомили про високий тягар захворювання, причому багато хто вказав, що ХК суттєво вплинула на якість їхнього життя. Ці висновки узгоджуються з результатами попередніх досліджень, які показали, що пацієнти з ХК зазнають недооціненого емоційного та психологічного навантаження, що впливає на сон і повсякденну діяльність і обмежує їхню здатність працювати та спілкуватися [1, 3, 12, 18-20]. Більшість учасників зазначили, що поява або погіршення симптомів їхнього захворювання були спровоковані психологічними чинниками, такими як стрес на роботі чи в особистому житті. Дійсно, пацієнти з ХК продемонстрували значно вищий рівень стресу порівняно з контрольною групою [21], і було показано, що стрес загострює перебіг кропив’янки [22].
Отримані висновки підкреслюють актуальність менеджменту стресу і використання механізмів його подолання в лікуванні пацієнтів із ХК.
Частина учасників опитування підтвердили, що вони уникають стресових ситуацій через страх спровокувати симптоми ХК, тоді як інші повідомили, що обмежують свою соціальну діяльність і модифікують спосіб життя, у тому числі дієту. Усвідомлення пацієнтом потенційних чинників, здатних спровокувати симптоми ХК, розширюють можливості пацієнта і можуть допомогти в розробці індивідуальних стратегій лікування, тим самим полегшуючи симптоми ХК та поліпшуючи якість життя [23].
Це дослідження наголошує на високій вірогідності того, що пацієнт із ХК буде недостатньо задоволеним результатами лікування, і підтверджує потребу в більшій обізнаності щодо тягаря хвороби. Необхідно ретельно оцінити варіанти лікування і/або його ескалацію для досягнення контролю симптомів.
Однак інтерпретувати ці результати потрібно обережно, оскільки пацієнти можуть вважати, що їх лікування неефективне, якщо симптоми повністю не зникли протягом кількох тижнів терапії; вони можуть припинити прийом ліків через неефективність і/або неналежне виконання рекомендацій лікаря. Таким чином, лікар має обговорити з пацієнтом природу ХК, можливу подовжену тривалість захворювання та варіанти ескалації лікування.
Раніше повідомляли, що велика кількість пацієнтів не отримують лікування ХК в обсязі, рекомендованому міжнародними настановами, незважаючи на активність захворювання [10]. Це дослідження показало низький рівень успіху або розчарування лікуванням у реальних ситуаціях, оскільки більшість учасників вважали, що попередні терапевтичні методи не допомагали і такі пацієнти більше взагалі не отримували лікування.
Основні принципи лікування хронічної кропив’янки
Основною метою менеджменту пацієнтів із ХК є лікування захворювання до повного зникнення симптомів. Терапія має бути якомога більш ефективною і безпечною, що дає змогу досягти повного контролю захворювання та нормалізації якості життя.
Оптимальний терапевтичний підхід до лікування пацієнтів із ХК має охоплювати:
- пошук і, за можливості, усунення основних причин захворювання;
- уникнення впливу тригерних чинників;
- індукування толерантності;
- фармакологічне лікування для запобігання вивільненню медіаторів мастоцитів
- і/або дії останніх.
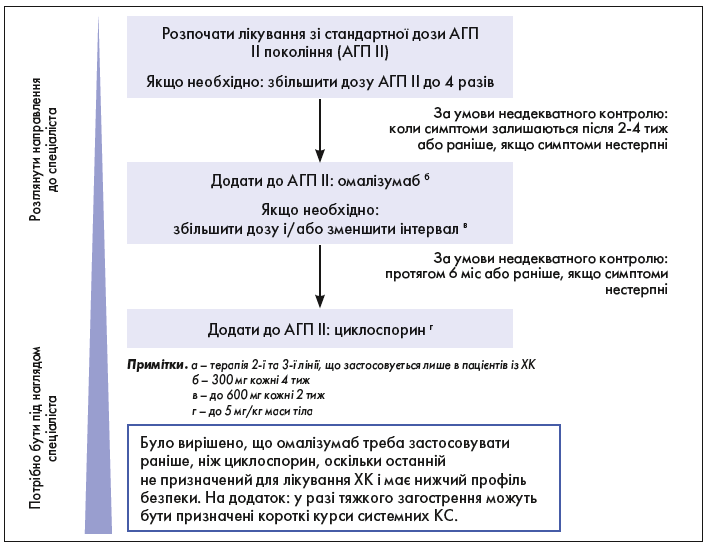
Під час ведення пацієнтів критично важливо використовувати методику «крок уверх – крок униз» з метою корекції алгоритму лікування відповідно до перебігу захворювання за принципом «оцінка, корекція, дія, повторна оцінка», що відображено на рисунку 5. Пацієнти потребують адекватного консультування щодо безперервного лікування і використання валідованих показників його ефективності.
Рис. 5. Алгоритм підходу до лікування та його ескалації в разі ХК
Загалом, основним завданням симптоматичної фармакотерапії в пацієнтів із ХК є усунення симптомів, допоки захворювання не перейде у фазу спонтанної ремісії. Для цього фармакологічне лікування має тривати доти, доки в ньому не зникне потреба.
Наприклад, для запобігання виникненню уртикарних висипань та АНН неседативні АГП ІІ покоління потрібно застосовувати щодня регулярно, а не за потреби. Доцільність застосування такої схеми лікування підтверджується профілем безпеки цієї групи лікарських засобів, результатами рандомізованих контрольованих досліджень і випробувань, проведених у реальних умовах [24, 25], а також їхнім механізмом дії, а саме зворотними агоністичними ефектами на H1-рецептор і стабілізацією неактивного стану останнього. Деякі пацієнти з ХК можуть мати користь від короткочасного профілактичного застосування АГП перед імовірним впливом відповідного тригерного чинника.
Результати досліджень демонструють, що деякі пацієнти з ХК, в яких спостерігають недостатню відповідь на лікування стандартними дозами АГП IІ покоління, можуть отримати користь від підвищення дози, і це є кращим варіантом, ніж комбінувати різні АГП IІ покоління. Відповідно, таким пацієнтам рекомендують збільшити дозу до 4 разів. Пацієнти мають бути поінформовані про те, що не рекомендується збільшувати дозу АГП ІІ покоління більш ніж учетверо, оскільки це донині не було досліджено. Поки не надходило повідомлень про серйозні побічні ефекти, пов’язані із застосуванням високих доз АГП та їх довгостроковим прийомом.
Вибір антигістамінного препарату
Під час вибору АГП необхідно мати на увазі, що АГП І покоління виявляють виражену антихолінергічну й седативну дію. Крім того, ця група препаратів має високий потенціал фармакокінетичних міжлікарських взаємодій (зокрема, з алкоголем і деякими лікарськими засобами, такими як аналгетики, снодійні, заспокійливі та антидепресанти). Також застосування АГП I покоління може порушувати фазу швидкого сну і впливати на навчання і продуктивність.
Відповідно до позиції GA2LEN [26] настійно рекомендується більше не застосовувати АГП I покоління для лікування симптомів алергії як у дорослих, так і в дітей. Цю думку поділяють рекомендації ВООЗ ARIA [27]. На основі переконливих доказів щодо потенційно серйозних побічних ефектів АГП I покоління (повідомляли і про смертельні випадки внаслідок передозування) останні не можна рутинно використовувати для лікування пацієнтів із ХК як засоби першої лінії.
Саме тому для менеджменту ХК треба призначати сучасні АГП IІ покоління, які чинять мінімальний седативний або неседативний ефект і не виявляють антихолінергічної активності [28]. Два представники АГП IІ покоління, а саме астемізол і терфенадин, продемонстрували кардіотоксичну дію в пацієнтів, які отримували інгібітори ізоформи цитохрому P450 (CYP) 3A4 (кетоконазол або еритроміцин). Саме тому астемізол і терфенадин більше не доступні в більшості країн і не рекомендуються до використання.
Ефективність і безпеку більшості, однак не всіх, АГП IІ покоління було досліджено серед пацієнтів із ХК. Отримані дані підтверджують доцільність застосування біластину, цетиризину, дезлоратадину, ебастину, фексофенадину, левоцетиризину, лоратадину та рупатадину.
У кількох дослідженнях було продемонстровано переваги застосування в пацієнтів із ХК вищих доз АГП IІ покоління [29-31]. Наявні дані підтверджують доцільність щоденного застосування доз, що в 4 рази перевищують стандартні дози для біластину, цетиризину, дезлоратадину, ебастину, фексофенадину, левоцетиризину і рупатадину [29, 30, 32-35].
Cьогодні відсутні добре розроблені клінічні дослідження, в яких порівнювали би ефективність і безпеку всіх сучасних АГП IІ покоління серед хворих на ХК. Саме тому варто обирати препарати, які відповідають вимогам ARIA і EACCI щодо сучасних АГП. Одним із таких засобів є оригінальний препарат біластину – Ніксар® виробництва компанії «Берлін Хемі».
Перевагами препарату є:
- належний профіль ефективності й безпеки, що було доведено низкою клінічних досліджень [36, 37];
- швидке настання ефекту та тривалий період дії – симптоми зникають уже через годину після прийому препарату Ніксар®, а ефект зберігається протягом 24 год;
- зручність використання – тривалий період дії дає можливість використовувати препарат лише 1 раз на добу, що підвищує прихильність пацієнтів до лікування [40];
- відсутність седативної дії та негативного впливу на когнітивні функції [41];
- безпечно застосовувати в дітей і пацієнтів літнього віку із супутньою патологією [37];
- відсутність впливу на здатність керування автотранспортом [42];
- відсутність впливу на психомоторні функції в разі одночасного прийому з алкоголем [43].
Ще однією важливою перевагою Ніксар® є його оригінальність. Обираючи препарат біластину, лікарю-практику необхідно розуміти, що згідно з рекомендаціями ЕМА (Європейського агентства з лікарських засобів) біоеквівалентність (біодоступність) генеричного препарату по відношенню до референтного має становити від -20% до +25% [38]. Різниця в біодоступності препарату на ±20% може супроводжуватися ризиком обмеженої ефективності терапії та підвищеним ризиком розвитку побічних реакцій [39]. На жаль, обираючи генеричний біластин, лікар чи пацієнт не можуть бути впевнені у відповідності препарату зазначеним вимогам, що може стати перешкодою на шляху досягнення контролю хвороби.
Доказова база ефективності біластину при хронічній кропив’янці
Проведені на сьогодні численні дослідження демонструють високий рівень ефективності та належну безпеку застосування біластину в лікуванні ХК. Так, у ході порівняльного дослідження M.K. Church (2011) було доведено, що біластин у дозі 20 мг демонструє швидший початок дії порівняно з цетиризином на прикладі гальмування появи пухирів (89±3 проти 44±14%; p=0,011) і висипань (85±4 проти 45±14%; p=0,016), індукованих гістаміном. Через 1,5 год основні симптоми кропив’янки в групі біластину були інгібовані на 70% (p=0,003).
Дослідження R. Antonijoan та співавт. (2017) було проведене з метою порівняння ефективності біластину, дезлоратадину і рупатадину в усуненні симптомів кропив’янки, індукованої підшкірним уведенням гістаміну здоровим добровольцям. На підставі результатів було встановлено, що біластин ліпше гальмував утворення нових пухирів, аніж дезлоратадин і рупатадин, у часовому діапазоні від 1 до 12 год (обидва р<0,001).
Необхідно також згадати результати відомих досліджень ефективності біластину при хронічній спонтанній кропив’янці (ХСК). Зокрема, дослідження Zuberbier та співавт. (2010; n=525), у рамках якого протягом 28 днів пацієнти отримували: біластин у дозі 20 мг на добу (n=173), левоцетиризин 5 мг на добу (n=165) або плацебо (n=184). У результаті в групі біластину відбулося поліпшення симптомів захворювання за даними загальної оцінки симптомів (TSS), дерматологічного опитувальника якості життя (DLQI), а також відомостей щодо загального дискомфорту і порушення сну в порівнянні з плацебо (p<0,001 для всіх). Біластин також продемонстрував безпеку і хорошу переносимість.
M. Hide та співавт. (2017) у своєму дослідженні вивчали ефективність і безпеку біластину в лікуванні ХСК. Учасників випробування (n=304) було рандомізовано на 3 групи: перша група (n=101) приймала біластин у дозі 20 мг, друга (n=100) – у дозі 10 мг, третя (n=103) отримувала плацебо. У результаті біластин у дозуванні 20 мг і 10 мг поліпшив TSS, оцінку висипань і свербежу і дані DLQI проти плацебо (p<0,001 для всіх), також препарат продемонстрував сприятливий профіль безпеки і хорошу переносимість. Автори дійшли висновку, що лікування ХСК біластином, навіть у невеликих дозах (10 мг), ефективніше, при цьому спостерігається ранній початок дії препарату.
Podder та співавт. у своєму дослідженні (2020) за участю 58 пацієнтів із ХСК помірного і тяжкого перебігу порівнювали ефективність і безпеку біластину в дозі 20 мг на добу (n=31) або левоцетиризину в дозі 5 мг на добу (n=27) впродовж 42 днів. Обидва АГП значно поліпшили, порівняно з вихідним рівнем, показники 7-денної оцінки активності кропив’янки (UAS7), дані DLQI та загальні симптоми, спричинені ХК, на 41-й день (p<0,001 для всіх). Показник UAS7 на 42-й день був значно нижчим у разі застосування біластину порівняно з левоцетиризином (p=0,03), натомість сонливість спостерігали частіше в групі левоцетиризину, ніж біластину (63 проти 12,9%; p=0,002).
На сьогодні є велика кількість досліджень, що демонструють безпеку використання біластину в умовах тривалого застосування чи збільшеного дозування. Наприклад, рандомізоване подвійне сліпе плацебо-контрольоване 12-тижневе дослідження K. Krause та співавт. (2013) демонструє ефективність і безпеку застосування біластину в більших дозах при холодовій кропив’янці. Двадцять пацієнтів із холодовою кропив’янкою отримували плацебо, біластин у дозах 20, 40 або 80 мг щоденно протягом 7 днів із подальшою 14-денною перервою. Біластин у дозі 20 мг виявився високоефективним (p<0,0001) засобом для зниження критичних температурних порогів. Збільшення дози до 80 мг ще більше (p<0,04) підвищило ефективність препарату. При цій дозі 19 із 20 (95%) пацієнтів відреагували на лікування. Автори дослідження зазначають, що всі дозування біластину пацієнти добре переносили, а випадків підвищеної седації в разі збільшення дози встановлено не було.
Отже, підвищення дози біластину забезпечує ще більшу його ефективність, але при цьому профіль безпеки препарату залишається незмінним.
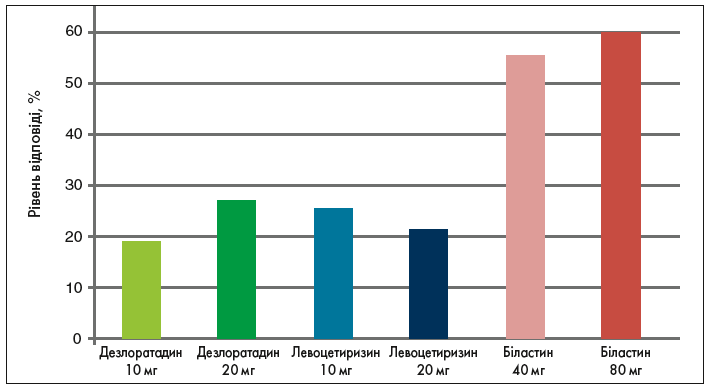
У дозах 40 і 80 мг препарат значуще поліпшував результати лікування пацієнтів із кропив’янкою. До того ж, оскільки біластин не проникає крізь гематоенцефалічний бар’єр, збільшення його дози в 4 рази під час лікування тяжкої ХК не призводитиме до появи сонливості. Вплив високих доз біластину досліджували в пацієнтів із ХСК та холодовою кропив’янкою в численних клінічних випробуваннях. Одне з найвідоміших із них – метааналіз M. Sanchez-Borges та співавт. (2014), у рамках якого аналізували дослідження, в яких для контролю симптомів ХК підвищували дозування неседативних АГП – таких як біластин, дезлоратадин, левоцетиризин. Виявилось, що підвищення стандартної добової дози для біластину вдвічі або навіть учетверо достовірно корелює з ефективністю, чого не можна сказати про 2 порівнюваних препарати. Застосування біластину в дозі 80 мг було ефективним у 60%, левоцетиризину – у 21,7% і дезлоратадину – у 27,1% випадків (рис. 6). Таке підвищення доз неседативних АГП, і біластину зокрема, не супроводжувалося розвитком небажаних явищ.
Рис. 6. Порівняльна ефективність підвищених доз неседативних АГП у пацієнтів із ХК (Sanchez-Borges М. та співавт., 2014)
Висновки
Таким чином, результати дослідження DERMLINE дали можливість отримати дані стосовно клінічного перебігу, порушення якості життя та ефективності лікування і задоволеності учасників опитування медичною допомогою у великій групі пацієнтів в умовах реальної практики, у тому числі в тих, хто зараз не перебуває під наглядом лікаря.
Отримані дані перегукуються з результатами попередніх досліджень і показують, що в значної частки пацієнтів із ХК (79,6% у дослідженні DERMLINE) не вдалося досягти належного контролю захворювання. Значуща частка учасників були незадоволені якістю свого життя, уникали соціалізації, часто відчували депресію, смуток, емоційну втому або безнадійність і отримували значно менше задоволення від діяльності, яку зазвичай любили. Більшість пацієнтів були незадоволені своїм лікуванням або взагалі його не отримували. Тобто, попри те що настанови EAACI/GA2LEN/EDF/WAO рекомендують використовувати специфічний алгоритм ескалації лікування до досягнення повного контролю симптомів ХК, в умовах реальної клінічної практики значна частка пацієнтів із ХК так і залишаються недолікованими.
Важливими складовими для досягнення цілей лікування є дотримання контактів із пацієнтом за схемою «лікар–пацієнт» і вибір зручної та ефективної схеми лікування. Варто обговорити з пацієнтом адекватні очікування від терапії, наголосити на необхідності регулярного прийому АГП з метою запобігання виникненню уртикарних висипань та АНН, а також розповісти про можливості посилення терапії в разі недостатнього контролю симптомів шляхом підвищення дози АГП, що вчетверо перевищують стандартні.
Препаратами першої лінії для контролю симптомів ХК, згідно із сучасними настановами, є АГП ІІ покоління. Одним із таких препаратів, доступних на ринку України, є біластин, оригінальний препарат якого Ніксар® підтвердив свою ефективність та безпеку в контрольованих клінічних дослідженнях. Зручність використання препарату Ніксар® забезпечується тривалою дією препарату, що дає можливість приймати його лише 1 раз на добу, підвищуючи тим самим прихильність пацієнтів до лікування.
Список літератури – у редакції.
За матеріалами: Wagner N., Zink A., Hell K. et al. Patients with Chronic Urticaria Remain Largely Undertreated: Results from the DERMLINE Online Survey. SpringerLinc. 2021. V.11, p. 1027-1039. https://link.springer.com/article/10.1007/s13555-021-00537-5
Підготувала Ганна Кирпач
Тематичний номер «Пульмонологія, Алергологія, Риноларингологія» № 1 (66) 2024 р.