13 березня, 2024
Ефективність застосування натурального комплексу на основі респіраторного пробіотика Lactobacillus helveticus MiMlh5 і гіалуронової кислоти при хронічному фарингіті та хронічному тонзиліті
 Хворі на хронічний фарингіт (ХФ) і хронічний тонзиліт (ХТ) складають вагому частку пацієнтів у щоденній практиці оториноларингологів та лікарів сімейної медицини в усьому світі. Симптоми ХФ і ХТ досить суттєво впливають на якість життя хворих (дискомфорт, відчуття стороннього тіла в глотці, сухий кашель від подразнення в горлі, неприємний запах із рота), змушують пацієнтів звертатися до спеціалістів у галузі патології верхніх дихальних шляхів, гастроентерологів, психотерапевтів, психологів.
Хворі на хронічний фарингіт (ХФ) і хронічний тонзиліт (ХТ) складають вагому частку пацієнтів у щоденній практиці оториноларингологів та лікарів сімейної медицини в усьому світі. Симптоми ХФ і ХТ досить суттєво впливають на якість життя хворих (дискомфорт, відчуття стороннього тіла в глотці, сухий кашель від подразнення в горлі, неприємний запах із рота), змушують пацієнтів звертатися до спеціалістів у галузі патології верхніх дихальних шляхів, гастроентерологів, психотерапевтів, психологів.
Слизова оболонка верхніх дихальних шляхів, зокрема ротоглотки, – перша лінія захисту організму проти різноманітних патогенних факторів зовнішнього середовища, як-от бактеріальні, вірусні, грибкові мікроорганізми, промислові та хімічні подразники. Різноманітні патологічні зміни й ушкодження слизової оболонки, супутні захворювання можуть сприяти її альтерації у результаті впливу вищезазначених чинників [1, 2].
ЛОР‑органи не є стерильними порожнинами, зокрема, в ротоглотці в нормі можуть існувати певні мікроорганізми (сапрофіти), які формують мікробіоценоз (автохтонну мікробіоту). За даними F. E. Dewhirst і співавт. (2010), порожнини рота та глотки – складні екосистеми, в яких можуть співіснувати >700 бактеріальних організмів [2]. Сапрофітні мікроорганізми утворюють на слизовій оболонці порожнини рота та глотки біоплівку з мікробних полісахаридів і муцину, а також продукують різні речовини (кислоти, спирти, лізоцим тощо), стимулюють продукцію секреторного імуноглобуліну, що обумовлює адекватну функцію місцевих імунних механізмів і протистоїть колонізації патогенними мікроорганізмами [1-3]. Склад мікробіоценозу глотки змінюється якісно та кількісно залежно від таких факторів, як вік пацієнта, наявність супутньої патології, умов зовнішнього середовища, харчування, шкідливих звичок, застосування лікарських засобів, рівня стресу тощо.
Дисбаланс у спільнотах резидентної мікрофлори (дисбактеріоз або дисбіоз) сприяє розвитку низки захворювань респіраторної, шлунково-кишкової, серцево-судинної, опорно-рухової та інших систем організму. Саме тому санація запалення в ротоглотці часто являє собою необхідний крок при лікуванні численних патологічних процесів.
Серед інших методів у лікуванні та профілактиці інфекційно-запальних захворювань ротоглотки перспективним є застосування пробіотичних засобів. Згідно з визначенням Всесвітньої організації охорони здоров’я, пробіотики – це живі мікроорганізми, які сприятливо впливають на здоров’я людини та мають здатність протидіяти інфекціям у різних ділянках тіла [4].
Останніми десятиріччями в експериментальних і клінічних випробуваннях продемонстровано, що пробіотики, зокрема при їхньому місцевому застосуванні, можуть бути ефективними як профілактичний і лікувальний засіб за інфекцій верхніх дихальних шляхів, отиту [5-7]. Властивості пробіотичних штамів дозволяють їм агрегувати та конкурувати з патогенами за поживні речовини, простір і прикріплення до клітин господаря. Отже, вони можуть безпосередньо протистояти патогенам, а також у такий спосіб надавати корисні ефекти без впливу безпосередньо на метаболізм хазяїна.
Як ад’ювантні засоби в лікуванні хворих з інфекційно-запальною патологією порожнин рота та ротоглотки вже досить тривалий час успішно застосовуються пробіотики, що містять Lactobacillus reuteri DSM 17938 та РТА 5289 [8], S. salivarius K12 [9].
Нещодавно в Україні представлено новий пробіотичний засіб для місцевого застосування Лактоангін відомого виробника пробіотиків Nutrilinea S.r.l. (Італія). 1 таблетка Лактоангіну містить Lactobacillus helveticus MiMlh5 (тіндалізована бактеріальна культура) – 3,78 мг, гіалуронат натрію – 43,20 мг (що відповідає 40 мг гіалуронової кислоти), сухоребрик лікарський (Sisymbrium officinale) – 30,00 мг.
Lactobacillus helveticus представляє одну з >80 видів молочнокислих бактерій, які належать до роду Lactobacillus, а саме до групи Lactobacillus delbrueckii. В дослідженнях на шарі клітин глотки людини FaDu in vitro вивчені характеристики функціональних та імуномодулювальних властивостей Lactobacillus helveticus MIMLh5 як перспективного фарингеального пробіотика [10-15].
У дослідженнях було доведено, що штам Lactobacillus helveticus MIMLh5 ефективно знижує індукцію інтерлейкіну‑6 (IL‑6), IL‑8 і фактора некрозу пухлини (залежно від дози). Також спостерігалася підвищена секреція IL‑6, γ-інтерферону (IFN‑γ), гранулоцито-макрофагального колонієстимулювального фактора (GM-CSF) за умов експерименту. Штам MIMLh5 збільшив співвідношення GM-CSF/G-CSF, що сумісно з перемиканням імунної відповіді на шлях Th1 [10].
Штам Lactobacillus helveticus MIMLh5 (як окремо, так і в комбінації з S. salivarius ST3) продемонстрував ефективну адгезію до епітеліальних клітин глотки, модуляцію вродженого імунітету хазяїна шляхом індукції потенційно захисних ефектів, антагонізм до S. pyogenes через виключення та конкуренцію за сайти адгезії на клітинах (72% зниження біолюмінесценції S. pyogenes C11LucFF) [10, 12].
Важливо зауважити безпеку застосування Lactobacillus helveticus, зокрема штаму MIMLh5, який використовується як закваска у виробництві сиру грана падано. Lactobacillus helveticus є «загалом визнаним безпечним» мікроорганізмом, який отримав статус «Кваліфікована презумпція безпеки» (QPS) від Європейського органу з безпеки харчових продуктів (EFSA) [16]. Статус QPS – це мітка оцінки безпеки EFSA на основі «сукупності знань» або «знайомості» мікроорганізму. Отже, Lactobacillus helveticus заслуговує на статус QPS, оскільки він має довгу історію очевидного безпечного використання в харчових продуктах і є чутливим до більшості антибіотиків [17]. Lactobacillus helveticus MiMlh5 також працює у своєму нежиттєздатному стані (парапробіотик), який є максимально безпечним, оскільки він не дозволяє мікроорганізму ні розмножуватися, ні передавати генетичний матеріал іншим бактеріям. Завдяки цьому Лактоангін зручний у застосуванні, адже не потребує зберігання в холодильній камері.
У клінічному дослідженні місцевого застосування пробіотичного засобу на основі штаму Lactobacillus helveticus MIMLh5 у пацієнтів із рецидивувальним ринофарингітом продемонстровано значне покращення стану хворих після 90-денного лікування. Як у дорослих пацієнтів, так і в дітей клінічна симптоматика оцінювалася балами (за SNOТ‑20 та візуальною аналоговою шкалою, ВАШ), які значно знижувалися після лікування порівняно з початковими значеннями. Показники CРБ, ШОЕ й АСЛO в крові також зменшилися, що свідчить про зменшення запалення. У групі дітей спостерігалося зменшення кількості навчальних днів, втрачених через ринофарингіт і відсутність патогенної мікрофлори, за даними бактеріологічного дослідження мазків із зіва в кінці дослідження [18].
До складу Лактоангіну, крім пробіотичного штаму MIMLh5, входить гіалуронат натрію, який створює стійку захисну плівку та має високу здатність до зв’язування води, що забезпечує зволожувальний ефект, сприяє регенерації, зменшує відчуття подразнення слизової оболонки глотки. Водночас гіалуронат натрію посилює антагонізм Lactobacillus helveticus MIMLh5 – зменшує адгезію S. pyogenes [12].
Третій компонент Лактоангіну (сухоребрик лікарський) – засіб, що діє на залози верхніх дихальних шляхів, збільшуючи кількість мокротиння і розріджуючи його, що полегшує відхаркування. У Франції сухоребрик називають травою співаків і рекомендують його педагогам, артистам та іншим особам, котрі за професією напружують голос, як засіб, що пом’якшує болісні відчуття й запальний стан верхніх дихальних шляхів, зменшує хриплість.
Отже, завдяки своєму комплексному складу Лактоангін забезпечує комбіновану антибактеріальну, протизапальну, імуномодулювальну, заспокійливу, пом’якшувальну та регенерувальну дію на слизову оболонку ЛОР‑органів.
Матеріали та методи
Мета клінічного дослідження – оцінка ефективності та безпеки застосування таблеток для розсмоктування Лактоангін у хворих на ХФ і ХТ.
Критерії включення:
• наявність суб’єктивних ознак ХФ або ХТ: прояви дискомфорту в горлі (першіння, відчуття сухості, печіння та стороннього тіла, стікання слизу задньою стінкою глотки), галітоз, сухий кашель;
• наявність об’єктивних ознак ХФ або ХТ: гіперемія, сухість та витончення слизової оболонки ротоглотки, слиз на задній стінці глотки, гіперемія піднебінних дужок, наявність казеозно-гнійного детриту в лакунах;
• чоловіки та жінки віком від 18 до 65 років;
• здатність до адекватної співпраці з лікарем у процесі дослідження.
Критерії виключення:
• тяжка супутня соматична патологія (в т. ч. цукровий діабет, імунодефіцитні стани);
• наявність симптомів гострого запалення в ротоглотці з місцевими та системними ознаками ГРЗ, регіонарним лімфаденітом;
• вагітність, лактація.
До випробування залучили 30 хворих (по 15 пацієнтів із ХФ і ХТ).
Клініко-демографічні дані пацієнтів, залучених до дослідження, наведено в таблиці 1.
|
Таблиця 1. Характеристика пацієнтів із ХФ і ХТ, залучених до дослідження |
||
|
Характеристика |
ХФ (n=15) |
ХТ (n=15) |
|
Кількість чоловіків / жінок |
6/9 |
7/8 |
|
Середній вік пацієнтів (роки) |
35,8±11,78 |
34,07±11,3 |
|
Тонзилектомія в анамнезі |
6 |
- |
|
Супутні захворювання* |
||
|
Стоматологічні захворювання |
5 |
6 |
|
Гастроезофагеальна |
5 |
3 |
|
Інші захворювання ШКТ |
5 |
4 |
|
Захворювання серцево- |
2 |
4 |
|
Захворювання опорно- |
2 |
4 |
|
Примітка: * у частки пацієнтів спостерігали |
||
Серед хворих на ХФ і ХТ часто спостерігалися супутні захворювання шлунково-кишкового тракту. Так, зокрема, >⅓ усіх пацієнтів, котрі брали участь у випробуванні, мала супутній діагноз – гастроезофагеальна рефлюксна хвороба. Відомо, що подразнення слизової глотки рефлюксатами (соляна кислота, пепсин) сприяє порушенню функції місцевого імунітету ВДШ і дисбіозу.
Пацієнти (відповідно до рекомендації виробника) повільно розсмоктували 1 таблетку Лактоангіну ввечері після вживання їжі та гігієни порожнини рота.
Тривалість спостереження для кожного хворого становила 30 діб. До початку застосування Лактоангіну та після його закінчення (30-й день) отримували мазок із ротоглотки пацієнтів для мікробіологічного дослідження, виконували якісне і кількісне дослідження мікрофлори з визначенням рівня колонізації, ідентифікацію за родом, а також видом бактерій.
Для визначення ефективності застосування Лактоангіну оцінювали вираженість об’єктивних і суб’єктивних клінічних ознак ХФ/ХТ на початку дослідження, а також на 10-й, 20-й та 30-й дні спостереження. Виокремлено основні скарги пацієнтів із ХФ і ХТ (суб’єктивні ознаки): дискомфорт у горлі (першіння, біль, відчуття сухості в глотці); відчуття стікання слизу задньою стінкою глотки; утворення «гнійних пробок» у лакунах мигдаликів, галітоз. Під час орофарингоскопії лікарем оцінювалися об’єктивні симптоми ХФ (гіперемія слизової оболонки ротоглотки, сухість, витончення слизової оболонки ротоглотки, слиз на задній стінці глотки) і ХТ (гіперемія піднебінних дужок, наявність казеозно-гнійного детриту в лакунах піднебінних мигдаликів). Ступінь вираженості кожного симптому визначали в балах за такою шкалою: 0 – відсутність ознаки; 1 – слабкий ступінь вираженості; 2 – помірний ступінь вираженості; 3 – значний ступінь вираженості.
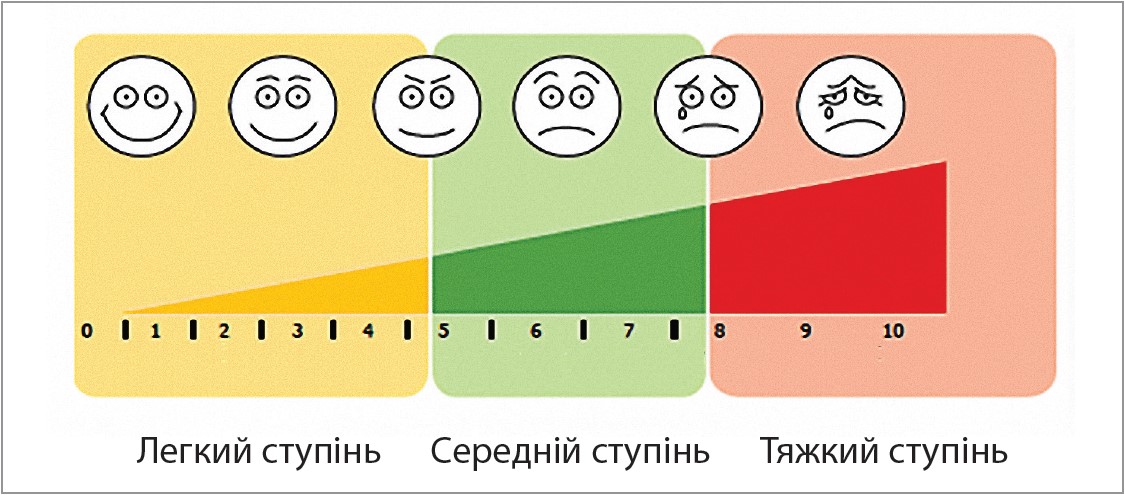
На початку та наприкінці дослідження пацієнтом виконувалася власна загальна оцінка ступеня тяжкості проявів ХФ/ХТ (фарингеальних симптомів) за шкалою ВАШ шляхом відповіді на таке запитання: «Наскільки симптоми, пов’язані з ХФ/ХТ, турбують Вас сьогодні?». Пацієнту пропонували зробити позначення на відрізку в 10 см, де 1 см відповідає 1 балу (рис. 1), при цьому варіант відповіді «не турбують взагалі» приймається за 0 балів, а відповідь «дуже сильно турбують», – за 10 балів.
Рис. 1. ВАШ для оцінки симптомів ХФ/ХТ
Після закінчення курсу лікування виконувалася оцінка ступеня поліпшення стану пацієнта за шкалою CGI-I (шкала глобального клінічного враження, підшкала оцінки ступеня поліпшення стану). Хворому пропонували порівняти свій стан до лікування і після, оцінити те, наскільки він змінився:
• виражено покращився;
• помітно покращився;
• дещо покращився;
• без змін;
• дещо погіршився;
• став помітно гірше;
• дуже сильно погіршився.
Із 7 можливих градацій позитивною відповіддю на лікування вважається відповідність категоріям «виражене поліпшення» або «помітне поліпшення». В іншому випадку відповідь на лікування розглядається як негативний результат.
Достовірність отриманих результатів оцінювали за допомогою парного t-критерію Стьюдента (р<0,05 вважалося статистично значущим).
Результати та обговорення
Оцінка ефективності лікування в групах дослідження за результатами шкал фарингеальних симптомів
Після початку застосування Лактоангіну серед хворих на ХФ і ХТ спостерігалося поступове зменшення вираженості суб’єктивних та об’єктивних ознак запальної патології ротоглотки.
На 1-й день дослідження всі пацієнти із ХФ і ХТ (30 хворих) повідомляли про наявність різноманітних проявів відчуття дискомфорту в глотці (табл. 2).
|
Таблиця 2. Суб’єктивні ознаки ХФ і ХТ |
||
|
Симптом |
Кількість осіб |
|
|
|
ХФ (n) |
ХТ (n) |
|
Першіння |
6 |
2 |
|
Відчуття сухості |
4 |
1 |
|
Відчуття печіння |
3 |
0 |
|
Відчуття стороннього тіла в горлі |
5 |
2 |
|
Відчуття стікання слизу задньою стінкою глотки |
7 |
1 |
|
Галітоз |
2 |
13 |
|
Сухий подразнювальний кашель |
4 |
1 |
|
Утворення «гнійних пробок» |
0 |
15 |
Оскільки кількість осіб із різними вищезазначеними симптомами не дозволяла виконати достовірну оцінку, пацієнтам запропонували оцінити перелічені суб’єктивні прояви як «дискомфорт у горлі». В дослідженні спостерігалося зменшення вираженості дискомфорту в горлі, причому різниця між показниками в 1-й та 30-й день спостереження була статистично достовірною (p<0,05). Також після курсу застосування Лактоангіну достовірно знизилася оцінка пацієнтами симптому «галітоз» (p<0,05) (табл. 3).
|
Таблиця 3. Вираженість суб’єктивних ознак ХФ і ХТ при застосуванні Лактоангіну |
|||||
|
Суб’єктивна ознака (симптом) |
Кількість хворих із ХФ/ХТ (n) |
Середнє значення вираженості симптому в балах |
Емпіричне значення критерію |
р |
|
|
день 1 |
день 30 |
||||
|
Дискомфорт у горлі |
15/15 |
1,767±0,568 |
1,233±0,679 |
2,57 |
0,016* |
|
Галітоз |
13/3 |
1,875±0,806 |
1±0,73 |
2,333 |
0,034* |
|
Утворення «гнійних пробок» |
15/0 |
2,308±1,109 |
1,385±0,961 |
2,009 |
0,068 |
Результати оцінки вираженості об’єктивних ознак ХФ і ХТ при застосуванні Лактоангіну наведено в таблиці 4.
|
Таблиця 4. Вираженість об’єктивних ознак ХФ і ХТ при застосуванні Лактоангіну |
|||||
|
Суб’єктивна ознака (симптом) |
Кількість хворих із ХФ/ХТ (n) |
Середнє значення вираженості симптому в балах |
Емпіричне значення критерію |
р |
|
|
День 1 |
День 30 |
||||
|
Гіперемія слизової ротоглотки |
15/0 |
1,533±0,516 |
1,2±0,676 |
1,323 |
0,207 |
|
Слиз на задній стінці глотки |
12/0 |
1,5±0,674 |
1±0,603 |
2,171 |
0,053 |
|
Застійна гіперемія піднебінних дужок |
0/15 |
1,867±0,64 |
1,267±0,458 |
2,201 |
0,045* |
|
Казеозно-гнійний вміст у лакунах |
0/15 |
2,133±0,64 |
1,667±0,816 |
3,5 |
0,004** |
|
Примітки: * p<0,05; ** p<0,01. |
|||||
Після курсу застосування Лактоангіну за орофарингоскопії спостерігалося зменшення ознак ХФ і ХТ, однак достовірними були зміни таких симптомів ХТ, як застійна гіперемія піднебінних дужок, казеозно-гнійний вміст у лакунах (p<0,05).
Отже, позитивну динаміку вищезазначених суб’єктивних та об’єктивних ознак ХФ і ХТ можна пов’язати зі сприятливим впливом Lactobacillus helveticus MiMlh5 на орофарингеальний мікробіоценоз та дією двох інших компонентів Лактоангіну (гіалуронату натрію, сухоребрика лікарського) на слизову оболонку ротоглотки, що зменшували прояви дискомфорту в глотці.
Оцінка ефективності лікування в групах дослідження за ВАШ
Для порівняння оцінки ВАШ (вираженість фарингеальних симптомів) у процесі дослідження використано t-критерій Стьюдента для залежних вибірок. Дані представлено в таблиці 5.
|
Таблиця 5. Динаміка ВАШ |
|||
|
День дослідження |
Середнє значення ВАШ у балах |
p (ХФ/ХТ) |
|
|
хворі на ХФ |
хворі на ХТ |
||
|
День 1 |
3,8±0,676 |
4±1 |
|
|
День 10 |
3,33±0,9 |
3,6±0,986 |
|
|
День 20 |
3±0,845 |
3,4±0,986 |
|
|
День 30 |
2,8±0,775 |
3,2±0,941 |
0,013*/0,075 |
|
Примітка: * p<0,05 (при порівнянні оцінки ВАШ |
|||
Відповідно до отриманих результатів виявлено зменшення середнього показника ВАШ у процесі спостереження серед пацієнтів із ХФ і ХТ. Однак достовірною була різниця у ВАШ до та після застосування Лактоангіну в групі пацієнтів із ХФ.
Оцінка ефективності лікування за шкалою CGI-I
Дані опитування пацієнтів груп дослідження за шкалою CGI-I (шкала глобального клінічного враження, підшкала оцінки ступеня поліпшення стану) фіксувалися на початку дослідження та на 30-й день спостереження.
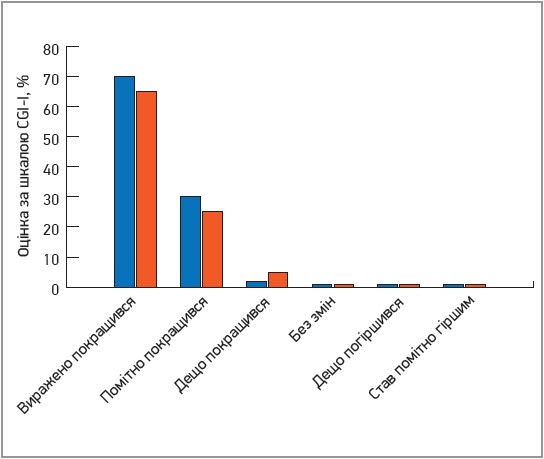
Загалом 15 пацієнтів із ХФ і 14 хворих із ХТ (96% від загальної кількості осіб у дослідженні) оцінили свій стан на 30-й день лікування як «виражено покращився» та «помітно покращився». Серед усіх пацієнтів оцінка «виражено покращився» була зафіксована 20 особами (66,7%). Один хворий на ХТ оцінив свій стан за шкалою CGI-I як «дещо покращився». Не було зареєстровано негативної відповіді на лікування. Отже, наведені дані шкали CGI-I підтверджують високу ефективність застосування Лактоангіну хворими на ХФ і ХТ (рис. 2).
Рис. 2. Оцінка ступеня поліпшення стану хворих на ХФ і ХТ за шкалою CGI-I
Результати мікробіологічних осліджень
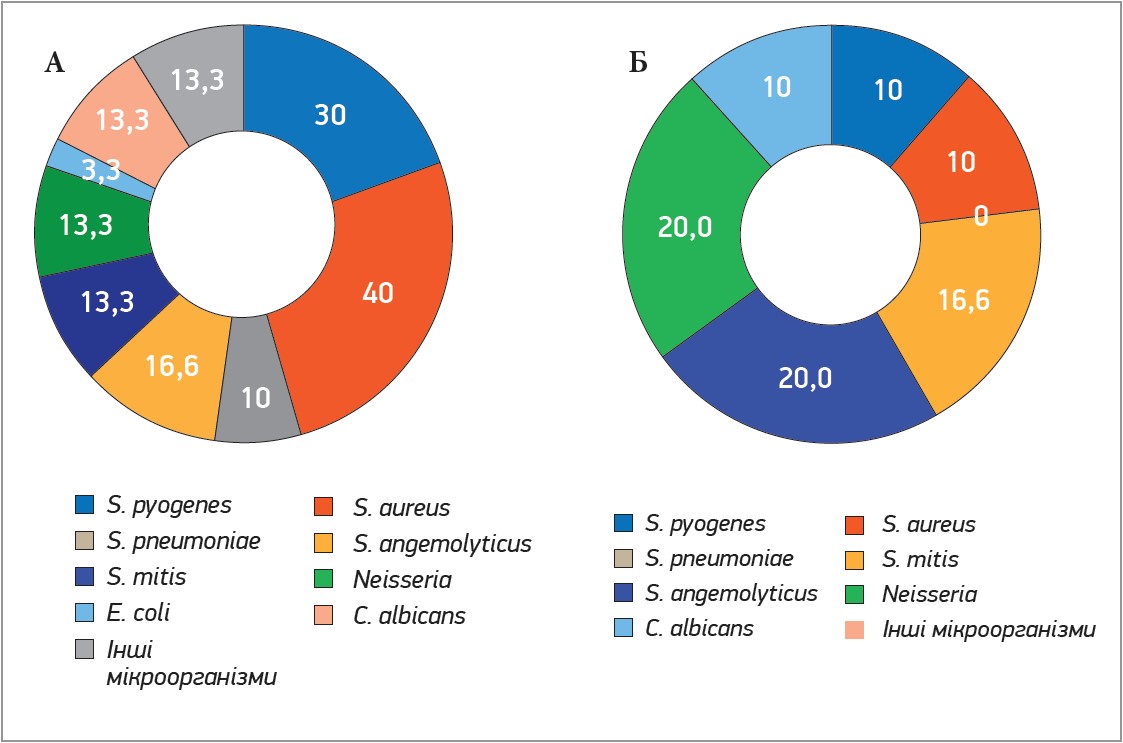
При мікробіологічному дослідженні мазків із ротоглотки на 1-й день спостереження в хворих на ХТ і ХФ виділено переважно грампозитивну мікрофлору (зокрема, S. aureus, S. pyogenes, S. pneumoniae в 30, 40 та 13,3% пацієнтів відповідно) в кількості 103-106 КУО/мл. У частки досліджуваних (5 хворих на ХФ і 7 хворих на ХТ) виявлено асоціації з 2-3 мікроорганізмів. У 4 пацієнтів висіяно C. albicans у кількості 102-104 КУО/мл, однак клінічних ознак орофарингеального кандидозу в них не спостерігалося. Розподіл мікроорганізмів у відсотковому еквіваленті до та після застосування Лактоангіну представлено в діаграмах (рис. 3).
Рис. 3. Якісний склад мікробіоценозу ротоглотки хворих на ХТ і ХФ до застосування Лактоангіну (А) та на 30-й день його застосування (Б)
Наприкінці спостереження в залучених до дослідження хворих на ХФ і ХТ спостерігалися позитивні зміни в якісному складі виділеної з ротоглотки мікрофлори. На 1-й день спостереження S. pneumoniae було знайдено в 3 пацієнтів, на 30-й день – у жодного. Також не висівалася E. coli, яку було виділено в 1 пацієнта із ХФ на початку дослідження. Зменшився відсоток хворих, у яких були висіяні S. pyogenes (із 30 до 10%), S. aureus (із 40 до 10%), C. albicans. Слід зазначити, що серед пацієнтів, у яких продовжували висіватися S. pyogenes і S. aureus, зменшилися показники мікробного обсіменіння до 102-103 КУО/мл.
Отже, відповідно до отриманих результатів мікробіологічних досліджень Lactobacillus helveticus MiMlh5 сприяє поступовому витісненню патогенних мікроорганізмів і відновленню резидентної мікрофлори ротоглотки.
У проведеному випробуванні спостерігався сприятливий профіль переносимості та безпеки досліджуваного засобу Лактоангін. Не було зареєстровано жодного випадку побічної дії серед пацієнтів із ХФ і ХТ.
Висновки
У дослідженні продемонстровано, що застосування Лактоангіну в пацієнтів із ХФ і ХТ може зумовлювати поступовий регрес об’єктивних і суб’єктивних клінічних проявів захворювання та сприяти покращенню якості їхнього життя. Згідно з результатами мікробіологічного дослідження, Lactobacillus helveticus MiMlh5 сприяв поступовому витісненню патогенних мікроорганізмів і відновленню резидентної мікрофлори ротоглотки в більшості хворих на ХТ і ХФ.
Список літератури знаходиться в редакції.
Медична газета «Здоров’я України 21 сторіччя» № 3 (564), 2024