3 листопада, 2025
Алергія і патологія ЛОР-органів: чи є взаємозв’язок?
Алергійні захворювання верхніх дихальних шляхів (ВДШ), зокрема алергійний риніт (АР), залишаються одними з найпоширеніших хронічних патологій як у дорослих, так і в дітей. За даними європейських епідеміологічних оглядів, АР вражає до 30% населення Європи (Greiner et al., 2011; Bousquet et al., 2008). В Україні тенденція аналогічна: усе більше пацієнтів звертаються зі скаргами на закладеність носа, чхання, ринорею, свербіж, а також супутні симптоми – головний біль, втомлюваність, кон’юнктивіт, порушення сну та зниження концентрації уваги. Найбільшу стурбованість зумовлює недооцінка ролі АР у розвитку коморбідних станів, зокрема риносинуситів, отитів та аденоїдитів. Часто такі стани розцінюють як ізольовані інфекційні процеси, хоча низка досліджень підтверджує, що саме алергійне запалення є тригером або сприяє хронізації перебігу цих патологій (Klimek et al., 2025; Mabry, 2003). У педіатричній практиці це питання набуває особливої ваги.
Алергійний риніт виступає незалежним фактором ризику виникнення ексудативного середнього отиту (ЕСО), особливо в дітей віком 4-8 років (Yang et al., 2016; Juszczak et al., 2020). При цій патології про алергійну компоненту нерідко забувають: батьки інтерпретують симптоми як часті застуди або затяжний нежить, а лікарі не враховують потенційну роль АР у патогенезі. При цьому ЕСО визнаний однією з головних причин тимчасової приглухуватості та затримки мовленнєвого розвитку в дітей (Brenner M.J., Boss E.F., 2010).
Відсутність своєчасної діагностики та належної фармакотерапії призводить до нераціонального використання антибіотиків, деконгестантів, інтраназальних кортикостероїдів, а в деяких випадках – до хірургічного втручання (наприклад, аденотомії чи тимпаностомії). Утім сучасні міжнародні рекомендації (ARIA, EPOS, EUFOREA) акцентують: у разі підозри на алергійний генез респіраторних симптомів першочергове значення мають пероральні антигістамінні препарати (АГП) ІІ покоління як безпечні, ефективні та добре переносимі засоби для стартової терапії (Bousquet et al., 2020; Hellings et al., 2019; Roberts et al., 2018; Fokkens W.J. et al., 2020).
З огляду на високий рівень коморбідності алергії та патології ЛОР-органів, медичні працівники мають бути добре обізнані щодо сучасних підходів до діагностики та лікування таких станів. Це допоможе не лише поліпшити якість життя пацієнтів, а й знизити частоту ускладнень, зменшити навантаження на систему охорони здоров’я та запобігти надмірному використанню антибіотиків і хірургічних утручань (Klimek et al., 2025; Mabry, 2003).
Алергійна компонента як складова патогенезу ЛОР-патології
Анатомо-фізіологічні основи концепції єдиних дихальних шляхів
Сучасна концепція «єдиних дихальних шляхів» (united airways) базується на анатомічній, гістологічній та імунологічній подібності верхніх і нижніх дихальних шляхів. Слизова оболонка носової порожнини, приносових пазух, глотки, гортані та бронхів характеризується однаковою будовою: вона вкрита війчастим псевдобагатошаровим циліндричним епітелієм із келихоподібними клітинами та має активну мукоциліарну систему (Klimek et al., 2025; Cingi et al., 2015).
Нещодавні результати свідчать, що до цієї системи треба віднести й середнє вухо разом з євстахієвою трубою (ЄТ). Слизова оболонка середнього вуха розвивається з тієї ж ектодерми, що й епітелій носа, і має подібну мікроскопічну будову – війчастий епітелій із мукоциліарною активністю (Hurst та Venge, 2000; Klimek et al., 2025). Ця спільність пояснює, чому середнє вухо так само зазнає впливу алергенів, як і решта респіраторного тракту.
ЄТ формує прямий анатомо-функціональний канал між носоглоткою і середнім вухом. Вона виконує декілька ключових функцій: вентиляційну (вирівнювання тиску), дренажну (виведення секрету), бар’єрну (захист від патогенів і запальних агентів) (Mabry, 2003; Klimek et al., 2025). При набряку, запаленні чи порушенні мукоциліарної функції – зокрема внаслідок АР – дренаж і вентиляція середнього вуха погіршуються, що створює умови для виникнення отитів або хронізації процесу.
Алергійне запалення в патології ЛОР-органів
Алергія відіграє важливу роль у розвитку захворювань ЛОР-органів. В основі лежать IgE-опосередковані реакції гіперчутливості та Th2-запалення, які запускають широкий спектр порушень із боку ВДШ. Найбільш показовим прикладом є АР, при якому вдихання аероалергенів (пилові кліщі, пилок, спори плісняви) спричиняє дегрануляцію опасистих клітин і накопичення еозинофілів у слизовій оболонці носа. Це проявляється класичними симптомами – ринореєю, чханням, свербежем і закладеністю носа (Varshney et al., 2015). Реакція супроводжується вивільненням прозапальних медіаторів, таких як гістамін і лейкотрієни, які посилюють місцеву запальну відповідь (Sigua et al., 2014; Grayson, 2017).
Ще одним із ключових механізмів алергійного запалення є залучення специфічних популяцій імунних клітин. Зокрема, встановлено, що в пацієнтів з атопією під час дії алергенів у носових тканинах і периферичній крові з’являються CD49d+-нейтрофіли, які, імовірно, беруть участь у регуляції місцевої алергійної відповіді (Grayson, 2017; Jha, 2022). Разом з еозинофілами та опасистими клітинами вони формують клітинну мережу, яка забезпечує запальний фон, характерний для більшості алергійних ЛОР-захворювань (Sigua et al., 2014).
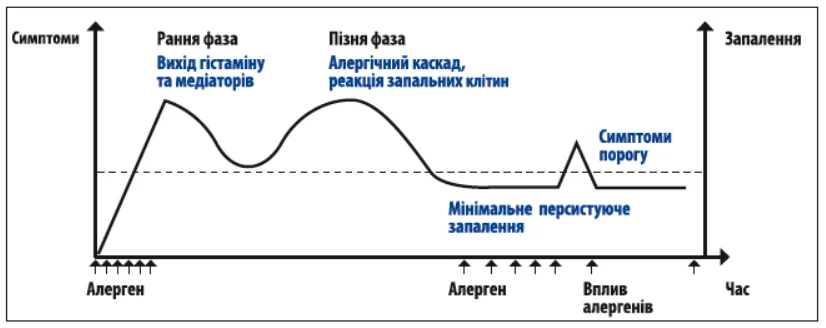
Алергійне запалення ВДШ, зокрема АР, часто є тригером або фоновим фактором розвитку інших ЛОР-патологій. Навіть після зникнення гострих симптомів у частини пацієнтів зберігається персистуюче запалення слизової, яке підтримується інфільтрацією еозинофілів та інших імунних клітин (рис.). Це «приховане» запалення може тривати тижнями або місяцями, зберігаючи гіперреактивність слизової і підвищуючи ризик загострень при повторному контакті з алергенами. Персистуюче запалення також сприяє ремоделюванню слизової, підвищенню чутливості до неспецифічних подразників та створює умови для формування коморбідних станів. Найбільш вивченими серед таких патологій вважають риносинусити, аденоїдити, середній отит (особливо ЕСО) та дисфункцію євстахієвої труби (ДЄТ) (Klimek et al., 2025; Mabry, 2003).
Рис. Етапи розвитку персистуючого запалення
АР і риносинусити
При АР набряк слизової оболонки носа, гіперсекреція та порушення мукоциліарного кліренсу створюють умови для порушення дренажу приносових пазух. Це підвищує ризик приєднання вторинної інфекції та розвитку гострого чи хронічного риносинуситу (Mabry, 2003). Оскільки остіомеатальний комплекс має анатомічно зумовлену схильність до обструкції, алергійне запалення часто сприяє хронізації процесу, особливо в дітей (Klimek et al., 2025).
У пацієнтів із хронічним риносинуситом із носовими поліпами виявлення еозинофільного слизу та ознак аспірин-чутливої астми вказує на виражену роль алергії в патогенезі захворювання. Запальна інфільтрація еозинофілами, підвищена експресія цитокінів і медіаторів зумовлюють ремоделювання тканин та утворення поліпів, що ускладнює лікування і сприяє хронізації процесу (Virkkula, 2018; Witterick, 2010).
АР і аденоїдит
Хронічний АР асоціюється зі стимуляцією лімфоїдної тканини носоглотки, що призводить до гіперплазії аденоїдів. У дітей це проявляється стійким утрудненням носового дихання, хропінням, порушенням сну й рецидивними отитами.
Дослідження свідчать, що в дітей з АР частота гіперплазії аденоїдів і пов’язаних із нею отитів вища, ніж у пацієнтів без атопії (Zhao et al., 2017; Juszczak et al., 2020).
АР, ДЄТ та ЕСО
Алергійне запалення нерідко поширюється і на суміжні структури – слухову трубу і середнє вухо. Під впливом алергенів виникає набряк слизової, посилюється продукування слизу та порушується мукоциліарний кліренс, що призводить до ДЄТ. Це створює умови для розвитку ЕСО та рецидивних епізодів гострого отиту (Ciprandi et al., 2020; Klimek et al., 2025). Своєю чергою, Th2-цитокіни – IL‑4, IL‑5 і IL‑13 – стимулюють утворення IgE, гіперплазію келихоподібних клітин і надмірне продукування слизу, що додатково погіршує вентиляцію в середньому вусі (Rizzi M. et al., 2019; Yang et al., 2017). У тяжких випадках можливий розвиток ЕСО, що свідчить про глибоке залучення до патологічного процесу еозинофілів (Klimek et al., 2025; Yang et al., 2017).
За даними EAACI (Klimek et al., 2025), АР є незалежним фактором ризику розвитку ЕСО. У пацієнтів з АР, особливо персистуючим, ризик розвитку ЕСО зростає у 2-4,5 раза (Yang et al., 2016; Hurst et al., 2000). У дітей з атопією частіше виявляють двобічний випіт (80% проти 56% у дітей без атопії) (Klimek et al., 2025). Це можна пояснити генералізованим алергійним запаленням слизової носоглотки та євстахієвих труб, яке має симетричний характер і призводить до двобічного порушення вентиляційної функції середнього вуха. Унаслідок цього накопичення ексудату відбувається одночасно з обох боків, що відрізняє алергійно зумовлений ЕСО від ізольованих випадків, пов’язаних з інфекціями чи локальними анатомічними чинниками.
Інші клінічні прояви
АР також може супроводжуватися синдромом постназального затікання, кашлем, ларингітом, хронічним фарингітом або навіть дисфонією внаслідок подразнення глотки та гортані. У цих випадках пацієнти часто помилково трактують симптоми як прояви «хронічної ангіни» або «залишкового вірусного процесу» (Mabry, 2003).
Таким чином, алергійне запалення в ЛОР-органах – це складний і багатофакторний процес, який охоплює IgE-опосередковані реакції, активацію опасистих клітин, еозинофілів, CD49d+-нейтрофілів та секрецію Th2-цитокінів. Ці механізми лежать в основі низки клінічних станів – від АР та отиту до алергійного ларингіту і хронічного риносинуситу – і обґрунтовують необхідність цілеспрямованої терапії, що враховує концепцію єдиних дихальних шляхів (Varshney et al., 2015; Sigua et al., 2014). У цьому контексті особливе значення мають сучасні неседативні АГП ІІ покоління, які не лише усувають симптоми алергії, а й модулюють основні ланки імунного запалення. Їх застосування є патогенетично обґрунтованим кроком у веденні пацієнтів із коморбідною ЛОР-патологією на тлі алергії.
Застосування сучасних неседативних АГП ІІ покоління при патології ЛОР-органів
З огляду на ключову роль гістаміну в ініціації та підтриманні запальної відповіді, блокування H1-гістамінорецепторів залишається базовим підходом у терапії алергійних захворювань. Однак сучасне уявлення про механізми дії АГП ІІ покоління значно виходить за межі класичного антагонізму. Згідно з Консенсусом CONGA (Consensus Group on New Generation Antihistamines, 2015), ці засоби не лише конкурентно блокують H1-рецептори, а й чинять низку додаткових протизапальних ефектів (Bousquet J. et al., 2015):
- Знижують експресію молекул адгезії (ICAM-1, VCAM-1) на ендотеліальних і епітеліальних клітинах, що перешкоджає міграції еозинофілів та інших запальних клітин у вогнище запалення.
- Пригнічують вивільнення цитокінів і хемокінів Th2-типу (IL-4, IL-5, IL-8), які підтримують еозинофільне запалення та продукування IgE.
- Зменшують дегрануляцію опасистих клітин і базофілів, знижуючи секрецію гістаміну, лейкотрієнів та інших медіаторів.
- Чинять стабілізувальний вплив на мембрани опасистих клітин, що додатково сприяє пригніченню запального каскаду.
У клінічній практиці саме ці фармакологічні властивості мають особливе значення для пацієнтів з алергією та супутніми ЛОР-захворюваннями. При АР, що супроводжується риносинуситом або отитом, призначення неседативного АГП сприяє не лише зменшенню закладеності носа та ринореї, а й поліпшенню дренажної функції, зменшенню набряку ЄТ та нормалізації вентиляції середнього вуха. Подібна дія є надзвичайно важливою для запобігання рецидивам ЕСО, особливо в дітей.
У дітей з атопією застосування одного із сучасних АГП ІІ покоління – левоцетиризину – асоціюється зі зниженням частоти епізодів ЕСО і поліпшенням вентиляційної функції ЄТ (Ertugay et al., 2013).
Водночас переваги сучасних АГП ІІ покоління – це не лише ефективність, а й профіль безпеки. Низька проникність крізь гематоенцефалічний бар’єр забезпечує відсутність седативного ефекту, що важливо для якості життя пацієнтів, у тому числі тих, хто навчається чи працює. Препарати цього класу також демонструють відсутність кардіотоксичності, не подовжують інтервал QT та не потребують корекції дози при супутній патології печінки чи нирок.
У пацієнтів із хронічною ЛОР-патологією, де алергія виступає фоновим або тригерним чинником, тривале застосування таких препаратів дає можливість контролювати перебіг захворювання, знижуючи ризик ускладнень і необхідність антибіотикотерапії.
Таким чином, застосування неседативних АГП ІІ покоління при ЛОР-патології за наявності алергійного фону є не лише симптоматичним, а й патогенетично обґрунтованим підходом. Така терапія відповідає сучасним принципам цілісного бачення захворювань дихальних шляхів і забезпечує кращий контроль стану пацієнтів як у педіатричній, так і в терапевтичній практиці.
Позиція міжнародних гайдлайнів щодо менеджменту алергійної компоненти при ЛОР-патології
Наявність алергійної компоненти при ЛОР-патології відображена в багатьох міжнародних настановах. Глобальні рекомендації підтримують активне виявлення АР у пацієнтів із ринітом, синуситом, отитами та іншими захворюваннями ВДШ, акцентуючи на значенні пероральних АГП ІІ покоління в менеджменті цих станів.
Детальний огляд рекомендацій подано в таблиці.
|
Таблиця. Міжнародні гайдлайни про алергійну складову при ЛОРпатології |
|
|
Назва настанови/рекомендації |
Основні постулати |
|
ARIA (Allergic Rhinitis and its Impact on Asthma), 2020 (Bousquet et al., 2020) |
• АГП ІІ покоління – препарати першої лінії для лікування АР. • Перевагу треба віддавати неседативним засобам із тривалою дією та низьким ризиком побічних ефектів. • Підкреслюється коморбідність АР з астмою, риносинуситом (РС), отитом та потреба в системному підході до лікування |
|
EPOS (European Position Paper on Rhinosinusitis and Nasal Polyps), 2020 (Fokkens et al., 2020) |
• АР визнано фактором ризику розвитку РС. • Рекомендовано застосування АГП навіть за відсутності сенсибілізації. • При ГПРС доцільне призначення пероральних АГП у перші 3 дні захворювання для полегшення симптомів і профілактики бактеріальних ускладнень |
|
EUFOREA (European Forum for Research and Education in Allergy and Airway Diseases) |
• Пропонує покрокову стратегію ведення пацієнтів з АР після підтвердження сенсибілізації та оцінки тяжкості. • Поетапна терапія: пероральні АГП ± інтраназальні стероїди ± імунотерапія. • Наголошує на необхідності контролю симптомів у пацієнтів із супутньою астмою, РС, отитом чи аденоїдитом |
Таким чином, усі провідні світові гайдлайни визнають:
- значущу роль АР у розвитку та перебігу ЛОР-патології;
- доцільність раннього призначення АГП, навіть за відсутності підтвердженої алергії, згідно з рекомендаціями EPOS;
- ефективність і безпеку сучасних АГП ІІ покоління, які забезпечують системний контроль алергійного запалення.
Вибір АГП ІІ покоління при ЛОР-патології
Серед інших АГП ІІ покоління левоцетиризин вирізняється збалансованим профілем ефективності, безпеки та переносимості, що робить його обґрунтованим вибором стартової терапії при ЛОР-патологіях, пов’язаних з алергійним запаленням. Як активний енантіомер цетиризину, він забезпечує більш виражену та тривалу блокаду H1-рецепторів у нижчій дозі, зменшуючи ризик побічних ефектів.
Його фармакокінетичні характеристики забезпечують швидкий початок дії – симптоматичне полегшення настає вже через 12 хв у 50% пацієнтів і протягом 30-60 хв – у 95%, що дає змогу швидко досягти терапевтичного ефекту. Прийом один раз на добу забезпечує високий комплаєнс, а відсутність седативного ефекту пояснюється мінімальним впливом препарату на центральну нервову систему, що підтверджено багаторічною клінічною практикою (Holgate et al., 2003).
Левоцетиризин виявляє не лише антигістамінну, а й мультиспрямовану активність (Walsh, 2009; Kang et al., 2010):
- антигістамінна дія – селективна блокада H1-рецепторів;
- антиалергійна дія – гальмування вивільнення медіаторів з опасистих клітин: гістаміну, триптази, лейкотрієну С4, простагландину D2;
- протизапальна дія – зниження продукування ключових цитокінів (IL-3, IL-4, IL-6, IL-13, TNF-α) і хемокінів (RANTES, IL-8), пригнічення хемотаксису і міграції лімфоцитів та еозинофілів у вогнище запалення.
Завдяки цьому препарат впливає на гістамінзалежну фазу алергійного запалення, зменшує судинну проникність, знижує вираженість місцевого набряку та запобігає хронізації запального процесу.
Висновки
Алергія, зокрема АР, є не лише самостійним хронічним захворюванням, а й ключовим фактором розвитку та підтримання патологічних процесів у ЛОР-органах. Завдяки концепції єдиних дихальних шляхів сьогодні стає очевидною роль алергійного запалення у формуванні риносинуситів, отитів, аденоїдиту, а також постназального затікання, ларингіту та інших станів.
Ігнорування цього взаємозв’язку призводить до хибної діагностики, нераціональної терапії, надмірного застосування антибіотиків і зайвих хірургічних утручань. Своєчасне виявлення алергійної природи симптомів і призначення сучасних неседативних АГП ІІ покоління, зокрема левоцетиризину, допомагає досягти контролю перебігу захворювань і зменшити ризик ускладнень.
Таким чином, міждисциплінарна обізнаність лікарів та орієнтування на міжнародні гайдлайни є ключовими передумовами для підвищення ефективності терапії пацієнтів з алергією та супутньою ЛОР-патологією.
Список літератури – у редакції.
Підготувала Ганна Кирпач
Тематичний номер «Пульмонологія. Алергологія. Риноларингологія» №3-4 (71-72), 2025 р.