28 липня, 2021
Профілактика інфекційних ускладнень при проведенні біопсії передміхурової залози та інших урологічних втручаннях
Оновлені рекомендації Європейської асоціації урології (ЄАУ) 2021
 У 2021 році експерти ЄАУ оновили рекомендації стосовно вибору методики й профілактики ускладнень при проведенні біопсії передміхурової залози (ПЗ). Дані нового метааналізу показали суттєве зменшення інфекційних ускладнень при біопсії ПЗ трансперинеальним доступом порівняно із трансректальним. Відповідно до результатів 7 рандомізованих клінічних досліджень за участю 1786 чоловіків, найбільш ефективною профілактикою інфекційних ускладнень при цьому втручанні є попередня обробка прямої кишки розчином повідон-йоду (рівень доказовості 1а).
У 2021 році експерти ЄАУ оновили рекомендації стосовно вибору методики й профілактики ускладнень при проведенні біопсії передміхурової залози (ПЗ). Дані нового метааналізу показали суттєве зменшення інфекційних ускладнень при біопсії ПЗ трансперинеальним доступом порівняно із трансректальним. Відповідно до результатів 7 рандомізованих клінічних досліджень за участю 1786 чоловіків, найбільш ефективною профілактикою інфекційних ускладнень при цьому втручанні є попередня обробка прямої кишки розчином повідон-йоду (рівень доказовості 1а).
Ключові слова: біопсія передміхурової залози, урологічні інфекції, повідон-йод, антибіотикопрофілактика.
Загальні принципи
Застосування заходів асептики
Існує комплекс заходів, призначених для зниження ризику післяопераційної ранової інфекції (ПРІ), більшість із яких давно застосовують під час рутинного хірургічного втручання. Зведені дані про ефективність цих заходів, доведену у рандомізованих контрольованих дослідженнях (РКД), представлені у систематичних оглядах, які проводить Кокранівська група з питань ран (http://wounds.cochrane.org/news/reviews).
Хірурги-урологи та заклади, у яких вони працюють, мають перевіряти асептичність навколишнього середовища і підтримувати її, у такий спосіб знижуючи ризик розмноження патогенів в організмі пацієнта (мікробіому) або інфікування його ззовні (нозокоміальної/внутрішньолікарняної інфекції). Для цього слід забезпечити правильне миття та стерилізацію інструментів, часте та ретельне прибирання операційних та післяопераційних палат і належну дезінфекцію кожного забрудненого осередку. Хірургічна бригада має належно готуватися до оперативного втручання: проводити ефективне миття рук (Tanner et al., 2016), одягати спеціальний захисний одяг та підтримувати асептику. За потреби цих заходів продовжують дотримуватись у післяопераційних і загальних палатах.
Пацієнтам рекомендовано приймати перед операцією душ, при цьому не доведено ефективність від використання хлоргексидинового мила (Webster et al., 2015). Отримано дані низької достовірності про те, що будь-яку епіляцію краще виконувати шляхом зрізання волосся, а не гоління, і проводити її безпосередньо перед здійсненням хірургічного надрізу (Tanner et al., 2011). Не слід виконувати механічне очищення кишок: за даними оглядів встановлено, що воно більше шкідливе, ніж корисне (Arnold et al., 2015; Guenaga et al., 2011). Деякі малодостовірні дані свідчать, що використання препаратів для обробки шкіри, які містять спирт або хлоргексидин, ефективніше запобігають ПРІ, ніж йодовмісні розчини (Dumville et al., 2015). У відповідному дослідженні не встановлено, що клейкі поліетиленові стрічки для операційного поля знижують ризик ПРІ (Webster et al., 2015).
Виявлення бактеріурії перед урологічними втручаннями
Дослідження на наявність бактеріурії, які проводять перед діагностичними та терапевтичними процедурами, спрямовані на зниження ризику інфекційних ускладнень шляхом усунення виявленої перед операцією бактеріурії та оптимізації антимікробної профілактики під час процедури. За даними систематичного огляду 18 досліджень, було виявлено, що для діагностики бактеріурії у дорослих пацієнтів перед урологічними втручаннями не прийнятний жоден із сучасних методів, крім посіву сечі (Bonkat et al., 2017).
Вибір препарату для перипроцедурної анибіотикопрофілактики
Урологи повинні бути поінформованими стосовно типу та різновиду місцевої патогенної мікрофлори, характерної для кожного виду процедур, профілі її чутливості до антибіотиків та вірулентності, щоб розробити місцеві письмові настанови. Відповідні вказівки слід укладати на підставі систематичного огляду літератури, і вони мають містити п’ять методик, визначених ECDC [ECDC, 2013]. Оптимальний препарат для профілактики не має збігатися із препаратом, рекомендованим для лікування інфекції. Якщо рівень інфікування шкірної рани низький або рана не інфікована, для захисту від можливих уропатогенів слід застосовувати аміноглікозид (гентаміцин), за умови показника швидкості клубочкової фільтрації >20 мл/хв; альтернативою є цефалоспорини 2-го покоління. Слід також ознайомитися з останніми результатами посівів сечі пацієнта, зокрема для виявлення мультирезистентних мікроорганізмів, визначити, чи є у нього медикаментозна алергія, чи була в анамнезі діарея, викликана C. difficile, чи приймав він останнім часом антибіотики, чи мав симптомну інфекцію та який у нього сироватковий рівень креатиніну. Комісія експертів вирішила не рекомендувати конкретних препаратів для певних процедур у зв’язку зі значними відмінностями в поширеності та сприйнятливості збудників у Європі й в усьому світі та неоднаковою наявністю антибіотиків.
Конкретні процедури та проблема отриманих даних
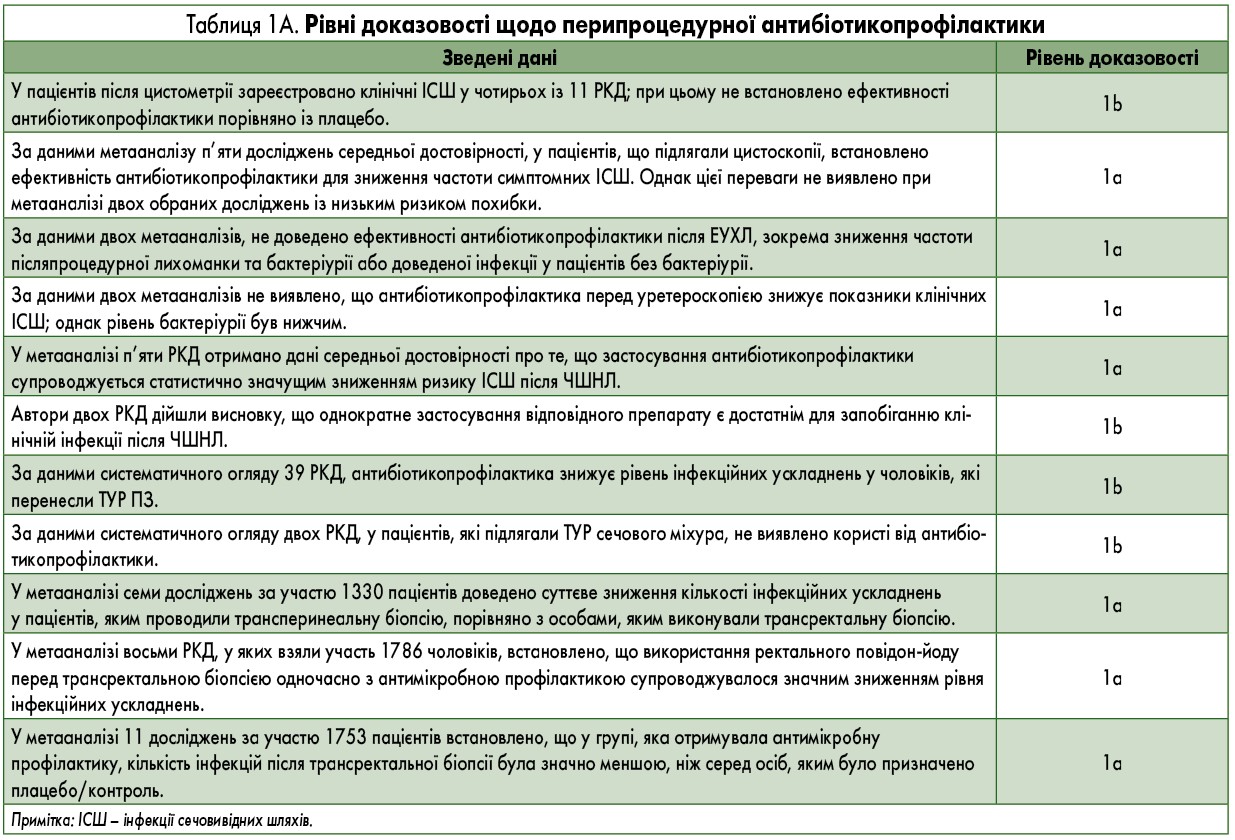
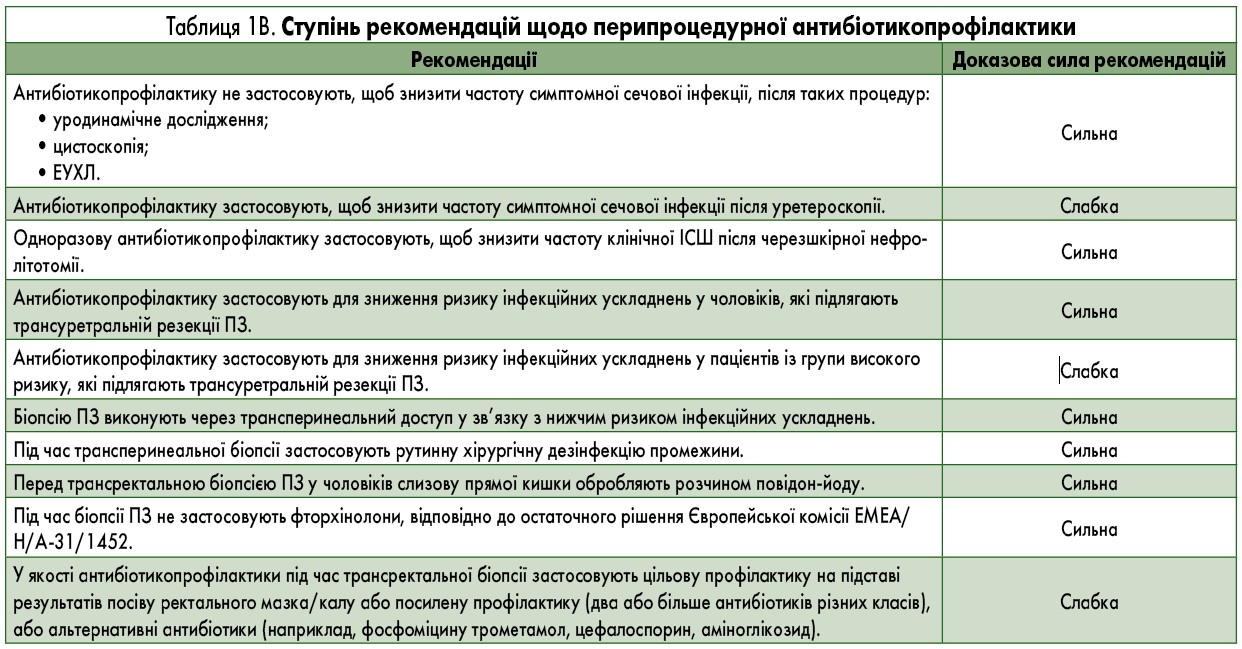
Під час огляду літератури, проведеного з 1980 року по лютий 2017 року, до якого ввійшли РКД, систематичні огляди та метааналізи, досліджено користь та шкоду від застосування антибіотикопрофілактики перед певними урологічними процедурами. На підставі отриманих даних комісія експертів визначила рівень доказовості та силу рекомендацій щодо проведення антибіотикопрофілактики при уродинамічних дослідженнях, цистоскопії, видаленні каменів (екстракорпоральної ударно-хвильової літотрипсії [ЕУХЛ], уретероскопії та черезшкірної нефролітотомії [ЧШНЛ]), біопсії простати, трансуретральній резекції (ТУР) ПЗ та ТУР сечового міхура (табл. 1 А, В).
Біопсія передміхурової залози
На підставі результатів 7 рандомізованих досліджень за участю 1330 пацієнтів було доведено, що інфекційні ускладнення виникали значно частіше при проведенні біопсії ПЗ трансректальним доступом порівняно із трансперинеальним (RR 1,81; 95% СІ 1,09-3,00) (Pradere B. et al., 2020). Крім того, у популяційному дослідженні вчених із Великобританії (n=73 630) доведено, що частота повторних випадків розвитку сепсису була меншою при проведенні біопсії ПЗ трансперинеальним доступом порівняно із трансректальним: 1,0% проти 1,4% відповідно (Berry B. et al., 2020). Таким чином, наявні докази свідчать про необхідність відмови від трансректального доступу на користь трансперинеального. На сьогодні не опубліковано результатів жодного рандомізованого клінічного дослідження, у якому б оцінювали різні схеми антибіотикопрофілактики для трансперинеальної біопсії ПЗ.
У метааналізі 8 РКД, у яких взяли участь 1786 чоловіків, доведено, що попередня обробка прямої кишки розчином повідон-йоду одночасно із антимікробною профілактикою супроводжувалося значним зниженням частоти інфекційних ускладнень (RR 0,55; 95% СІ 0,41-0,72) (Pradere B. et al., 2020). За даними одиночного сліпого РКД не встановлено ефективності від дезінфекції шкіри промежини (Taher et al., 2015), але виявлено, що препарат повідон-йоду краще застосовувати перед біопсією, ніж після неї (Yu et al., 2014).
У метааналізі 4 РКД, до яких був залучений 671 чоловік, оцінювали ефективність промивання прямої кишки дезінфекційними розчинами перед трансректальною біопсією. При цьому не зареєстровано істотної користі у вигляді зниження показника інфекційних ускладнень (RR 0,96; 95% СІ 0,64-1,54) (Pradere et al., 2020).
За даними метааналізу 26 РКД за участю 3857 пацієнтів не доведено, що при перипростатичному введенні місцевого анестетика виникає більше інфекційних ускладнень, ніж за відсутності цього втручання (RR 1,07; 95% СІ 0,77-1,48) (Pradere B. et al., 2020). У метааналізі 9 РКД із залученням 2230 пацієнтів виявлено, що частота інфекційних ускладнень при розширеній рамковій біопсії зіставна з аналогічним показником при стандартній рамковій біопсії (RR 0,80; 95% СІ 0,53-1,22) (Pradere B. et al., 2020). За результатами додаткових метааналізів, не виявлено різниці за частотою інфекційних ускладнень у групах, де використовували різний тип голки (одно- чи багаторазову), зріз голки (коаксіальний чи некоаксіальний), розмір голки (великий чи малий) та кількість ін’єкцій для перипростатичної блокади нервів (стандартну чи збільшену) (Pradere B. et al., 2020).
За даними метааналізу 11 досліджень за участю 1753 пацієнтів, які перенесли трансректальну біопсію ПЗ, серед осіб, які отримували антимікробну профілактику, виявлено суттєве зниження частоти інфекцій, ніж у групі плацебо/контролю (RR 0,56; 95% СІ 0,40-0,77) (Pilatz et al., 2020).
Для антибіотикопрофілактики під час цієї процедури зазвичай використовують фторхінолони; однак надмірне та неправильне використання цих антибіотиків призвело до підвищеної резистентності до цієї групи препаратів. Крім того, Європейська комісія запровадила жорсткі нормативні умови щодо використання фторхінолонів, тому сьогодні ці препарати не показані для періопераційної антибіотикопрофілактики, зокрема перед біопсією ПЗ (European Medicines Agency, 2019).
За даними систематичного огляду та метааналізу методів антибіотикопрофілактики, які застосовують для запобігання інфекційним ускладненням після біопсії ПЗ, встановлено, що у країнах, де дозволена антибіотикопрофілактика фторхінолонами, її проводять у формі мінімум одного повноденного застосування (табл. 2). У разі стійкості до фторхінолонів рекомендують цільову або посилену профілактику (комбінацію двох або більше антибіотиків різних класів) (Pilatz et al., 2020). У країнах, де тимчасово заборонена профілактика фторхінолонами, можна застосовувати цефалоспорини або аміноглікозиди.
У метааналізі 3 РКД встановлено, що фосфоміцину трометамол ефективніший, ніж фторхінолони (RR 0,49; 95% СІ 0,27-0,87) (Pilatz et al., 2020), але водночас у нерандомізованих його випробуваннях зареєстровано інфекційні ускладнення. Тому, перш ніж призначати цей препарат рутинно, перед усіма процедурами, слід критично оцінити можливі наслідки (Carignan et al., 2019). Ще одним варіантом профілактики є посилена терапія нефторхінолоновими антибіотиками, хоча на сьогодні не відомо жодної стандартної їх комбінації. Зрештою, можна застосовувати цільову профілактику на підставі даних посіву ректальних мазків/калу, враховуючи, що для нефторхінолонових препаратів відсутні дані РКД.
На рисунку наведено алгоритм біопсії ПЗ для зниження ризику інфекційних ускладнень.
Як зазначено раніше, комісія експертів вирішила не рекомендувати конкретних препаратів для антибіотикопрофілактики при проведенні певних урологічних втручань. Перелічені нижче препарати є лише можливими варіантами. Лікарям-урологам слід підбирати конкретний антимікробний засіб на підставі знань про поширеність місцевих збудників для кожного типу процедур, їх профілі чутливості до антибіотиків та вірулентності.

 Рис. Алгоритм проведення біопсії ПЗ для зниження ризику інфекційних ускладнень*
Рис. Алгоритм проведення біопсії ПЗ для зниження ризику інфекційних ускладнень*
Примітки: 1 – РКД не проводились, але втручання обґрунтоване; 2 – слід зібрати дані про місцеву протимікробну стійкість; 3 – заборонено Європейською комісією через побічні ефекти; 4 – суперечить принципам належного застосування антимікробних препаратів; 5 – фосфоміцину трометамол (3 РКД), цефалоспорини (2 РКД), аміноглікозиди (2 РКД); 6 – за даними лише одного РКД, у якому порівнювали цільову та посилену профілактику; 7 – первинно запроваджена як схема альтернативної антибіотикопрофілактики у разі стійкості до фторхінолонів; 8 – різні схеми: фторхінолон + аміноглікозид (3 РКД); і фторхінолон + цефалоспорин (1 РКД); 9 – значно поступається цільовій та посиленій профілактиці.
Ступені доказовості за даними робочої групи, що розробила шкалу GRADE (Шкала ступенів рекомендацій, оцінювань, прогнозування і оцінок): висока достовірність – (⊕⊕⊕⊕) висока впевненість у тому, що реальний ефект відповідатиме прогнозованому; середня достовірність – (⊕⊕⊕O) помірна впевненість у прогнозі ефекту: реальний ефект, імовірніше за все, буде близьким до прогнозованого, але існує ймовірність суттєво іншого ефекту; низька достовірність – (⊕⊕OO) ефект важко передбачити, реальний ефект може суттєво відрізнятися від прогнозованого; дуже низька достовірність – (⊕OOO) ефект дуже важко передбачити, реальний ефект, імовірно, буде суттєво відрізнятися від прогнозованого.
* Рисунок взято зі статті Pilatz et al. з дозволу видавництва Elsevier.
Довідка від редакції
На вітчизняному ринку повідон-йод представлений високоякісними препаратами – Бетайод-Здоров’я розчин нашкірний 50, 100 і 1000 мл, а також Бетайод-Здоров’я у вигляді мазі 20 мг у тубі. Дані препарати широко застосовуються для ефективної профілактики та лікування інфекцій при проведенні хірургічних процедур, у тому числі біопсії передміхурової залози та інших урологічних втручань.
Група компаній «Здоров’я» – один із визнаних лідерів українського фармацевтичного ринку. Його місія – забезпечення населення якісними, доступними та ефективними лікарськими препаратами.
Нині до цієї групи компаній входять ТОВ «Фармацевтична компанія «Здоров’я», ТОВ «Дослідний завод «ГНЦЛС», ТОВ «ХФП «Здоров’я Народу», ТОВ «Фармекс Груп». Варто відзначити високу якість продуктів бренда «Здоров’я», яку гарантує дотримання суворих вимог GMP. На сьогодні групою компаній «Здоров’я» на фармацевтичний ринок України виведено близько 700 найменувань лікарських засобів, серед яких 101 препарат входить до переліку життєво необхідних і 15 є оригінальними брендами.
Тематичний номер «Урологія. Нефрологія. Андрологія» № 2 (23), 2021 р.