24 грудня, 2017
Нобелевская премия в области физиологии и медицины присуждена за исследование циркадных ритмов
 Ключевым, четвертым, лауреатом этой премии является одна маленькая муха.
Ключевым, четвертым, лауреатом этой премии является одна маленькая муха.
Дж. Холл
Нобелевской премии 2017 г. в области физиологии и медицины удостоены американские генетики Джеффри Холл, Майкл Росбаш и Майкл Янг за открытия так называемых клеточных часов – молекулярных механизмов, регулирующих циркадные ритмы организма.
Все живые организмы на Земле, включая людей, адаптированы к вращению нашей планеты благодаря внутренним биологическим часам, которые помогают им подстраиваться под разные фазы суточного цикла. Открытия нынешних лауреатов Нобелевской премии объясняют, как устроены суточные ритмы и каким образом они влияют на состояние организма.
Используя в качестве модельного организма плодовых мушек дрозофил (Drosophila melanogaster), ученые определили ген, который контролирует нормальный ежедневный биологический ритм. Они показали, что этот ген кодирует белок, который накапливается в клетке в течение ночи, а затем деградирует в течение дня. Впоследствии они идентифицировали дополнительные белковые компоненты, принимающие участие в этом процессе, и показали, что принципы функционирования биологических часов одинаковы в клетках всех многоклеточных организмов, включая людей. Эти механизмы отвечают за адаптацию физиологических процессов к разным фазам дня, регулируют такие важные функции, как поведение, уровни гормонов, сон, температуру тела и обмен веществ. Ученые также исследовали, как несоответствие между нашей внешней средой обитания и внутренними биологическими часами сказывается на биологических процессах в организме, например, когда во время путешествия человек переживает смену нескольких часовых поясов. Кроме того, получены доказательства, что хроническое несоответствие между современным образом жизни и внутренними циркадными ритмами человека повышает риск развития различных заболеваний.
 В течение многих лет механизмы циркадных ритмов оставались одним из наиболее загадочных биологических феноменов. В 1984 г. Дж. Холл и М. Росбаш, работая в тесном сотрудничестве в Университете Брандейса (г. Бостон), а также М. Янг в Университете Рокфеллера (г. Нью-Йорк) выделили специфический ген period, отвечающий за циркадные ритмы. Затем Дж. Холл и М. Росбаш обнаружили, что белок PER, кодируемый этим геном, накапливается в течение ночи и деградирует в течение дня. Таким образом, уровни этого белка колеблются в течение 24-часового цикла, синхронно с циркадным ритмом.
В течение многих лет механизмы циркадных ритмов оставались одним из наиболее загадочных биологических феноменов. В 1984 г. Дж. Холл и М. Росбаш, работая в тесном сотрудничестве в Университете Брандейса (г. Бостон), а также М. Янг в Университете Рокфеллера (г. Нью-Йорк) выделили специфический ген period, отвечающий за циркадные ритмы. Затем Дж. Холл и М. Росбаш обнаружили, что белок PER, кодируемый этим геном, накапливается в течение ночи и деградирует в течение дня. Таким образом, уровни этого белка колеблются в течение 24-часового цикла, синхронно с циркадным ритмом.
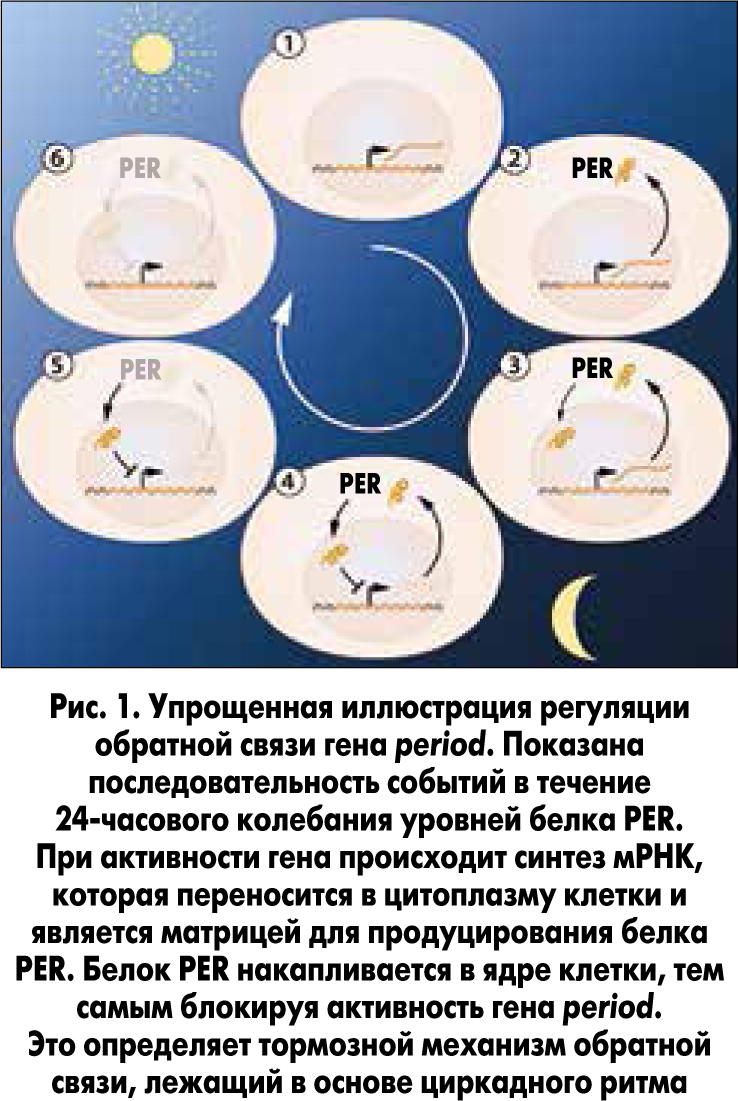
Следующая цель исследователей заключалась в том, чтобы понять, каким образом возникают и поддерживаются циркадные колебания уровней белка PER. Ученые высказали гипотезу о том, что белок PER обладает свойством препятствовать собственному синтезу с помощью ингибирующего механизма обратной связи, регулируя темсамым собственный уровень в непрерывном циклическом ритме (рис. 1).
Однако в этой модели отсутствовали некоторые составляющие. Чтобы блокировать активность гена, белок PER, продуцируемый в цитоплазме, должен достичь клеточного ядра, которое содержит генетический материал. Дж. Холл и М. Росбаш показали, что белок PER действительно ночью накапливается в клеточном ядре, но нужно было еще выяснить, каким образом он в него попадает.
В 1994 г. М. Янг обнаружил еще один ген синхронизации, кодирующий белок TIM, необходимый для нормального циркадного ритма. Он показал, что когда белок TIM связывается с PER, они оба приобретают способность войти в ядро клетки и блокировать активность гена period, чтобы замкнуть ингибирующую петлю обратной связи (рис. 2).
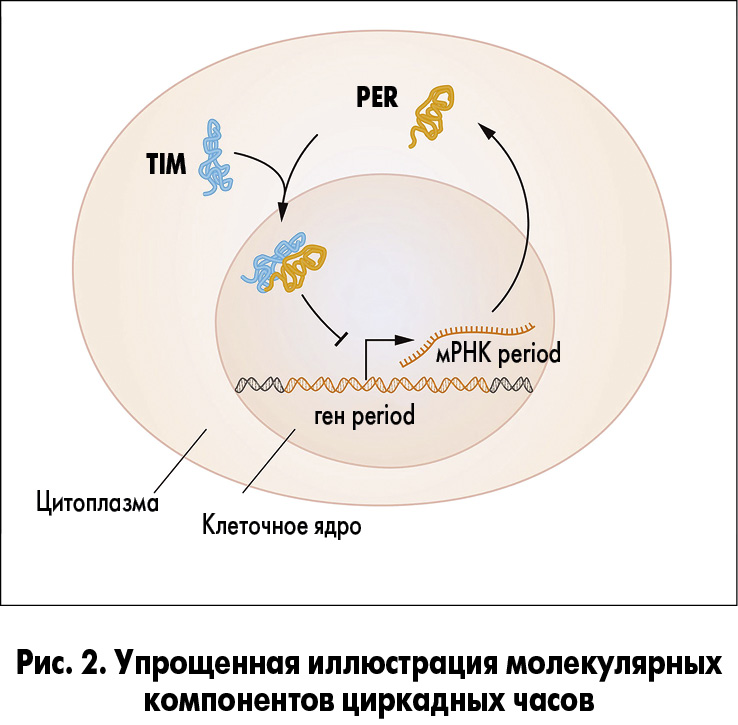 Такой механизм регулятивной обратной связи объяснил, как возникают колебания уровней клеточного белка PER, но оставался нерешенным вопрос о том, что контролирует частоту колебаний. М. Янг идентифицировал еще один ген, кодирующий белок DBT, который задерживал накопление белка PER. Это обеспечило понимание того, как регулируется колебание, чтобы соответствовать 24-часовому циклу.
Такой механизм регулятивной обратной связи объяснил, как возникают колебания уровней клеточного белка PER, но оставался нерешенным вопрос о том, что контролирует частоту колебаний. М. Янг идентифицировал еще один ген, кодирующий белок DBT, который задерживал накопление белка PER. Это обеспечило понимание того, как регулируется колебание, чтобы соответствовать 24-часовому циклу.
Открытия нобелевских лауреатов 2017 г. позволили установить ключевые механизмы биологических часов. Позже были выявлены и другие молекулярные компоненты, объясняющие их стабильность и функционирование. В частности, ученые обнаружили дополнительные белки, необходимые для активации гена period, а также механизм, посредством которого свет может синхронизировать циркадные ритмы.
Биологические часы задействованы во многих аспектах физиологии человека. Все многоклеточные организмы, включая людей, имеют аналогичный механизм контроля циркадных ритмов. Большая часть наших генов регулируется биологическими часами – и, следовательно, тщательно откалиброванный циркадный ритм адаптирует все физиологические процессы к разным фазам суточного цикла. Сегодня «циркадная» биология представляет собой обширную и динамично развивающуюся область исследований, достижения которой непосредственно связаны с нашим здоровьем и благополучием.
Примечательно, что не только нынешние лауреаты, но и большинство ученых, удостоенных Нобелевской премии в области физиологии и медицины, являются генетиками – в общей сложности 48 человек! С момента основания в 1901 г. и до сегодняшнего времени Нобелевской премии в области физиологии и медицины удостоены 214 ученых, из них всего 12 женщин. Дважды в истории эта премия была присуждена супругам: Герти и Карл Кори, а также Мэй-Бритт и Эдвард Мозер получили Нобелевскую премию в области физиологии и медицины, соответственно, в 1947 и 2014 г.
Вручение Нобелевской премии проводится в Стокгольме в день памяти Альфреда Нобеля – 10 декабря. Согласно традиции, на праздничном банкете первый тост в честь основателя премии провозглашает король Швеции Карл XVI Густав. Торжества в честь нобелевских лауреатов обычно завершаются 13 декабря, в один из крупнейших шведских праздников – День святой Люсии.
О лауреатах
 Джеффри Коннор Холл (Jeffrey Connor Hall) – американский генетик, родился 3 мая 1945 года в г. Нью-Йорк. В 1963 г. поступил в Амхерстский колледж в Массачусетсе, планируя получить медицинское образование, позже заинтересовался генетикой. Начав с исследования классической и молекулярной генетики дрозофилы, ученый постепенно перешел к нейрогенетике, исследуя генетические основы полового поведения и биологических ритмов этих насекомых, а также их взаимодействие.
Джеффри Коннор Холл (Jeffrey Connor Hall) – американский генетик, родился 3 мая 1945 года в г. Нью-Йорк. В 1963 г. поступил в Амхерстский колледж в Массачусетсе, планируя получить медицинское образование, позже заинтересовался генетикой. Начав с исследования классической и молекулярной генетики дрозофилы, ученый постепенно перешел к нейрогенетике, исследуя генетические основы полового поведения и биологических ритмов этих насекомых, а также их взаимодействие.
В 1971 г. Дж. Холл получил докторскую степень в Вашингтонском университете (г. Сиэтл), а с 1971 по 1973 г. работал в Калифорнийском технологическом институте (г. Пасадина). Начиная с 1974 г. и по сегодняшний день работает в Брандейском университете (г. Уолтем); с 2002 г. параллельно сотрудничает с Университетом штата Мэн.
В 1984 г. Дж. Холл с коллегами выделили так называемый ген периода (period), мутации в котором приводили к нарушению циркадных ритмов у дрозофил. Ген кодировал неизвестный на то время белок. Изучая его взаимодействие с другими белками, Дж. Холл совместно с М. Росбашем обнаружили, что кодируемый этим геном белок PER накапливается в течение ночи и деградирует в течение дня. Таким образом, уровень белка PER колеблется в течение суток синхронно с циркадным ритмом. Ученые обосновали, что с помощью ингибирующей петли обратной связи белок может препятствовать собственному синтезу и тем самым регулировать собственный уровень в непрерывном циклическом ритме.
«У нас была большая взаимная поддержка и много общих интересов – даже в те далекие времена, когда мы еще не занимались исследованием циркадного ритма», – рассказал Дж. Холл о своем сотрудничестве с М. Росбашем в интервью Нобелевскому сайту. «Ключевым, четвертым, лауреатом этой премии, как мы иногда говорим, является одна маленькая муха», – заявил он, подразумевая дрозофилу. Ведь именно на модели этой мухи были сделаны все открытия.
 Майкл Моррис Росбаш (Michael Morris Rosbash) родился 7 марта 1944 года в г. Канзас-Сити в семье еврейских беженцев из нацистской Германии, прибывших в США в 1938 г. Его отец Альфред Росбаш был кантором синагоги, мать Хильде Росбаш занималась научными исследованиями в области клинической цитопатологии. Еще будучи школьником, будущий нобелевский лаурет посещал лекции по биологии в Калифорнийском технологическом институте и работал в лаборатории Нормана Дэвидсона. Окончил Калифорнийский технологический институт со специализацией по химии в 1965 г., а в 1970 г. – отделение биофизики Массачусетского технологического института. После трехлетней постдокторантуры по генетике в Эдинбургском университете в 1974 г. был принят на работу в Брандейский университет, где работает до сих пор. Его жена, ученый-генетик Надя Абович (Nadja Abovich), также является соавтором некоторых его работ.
Майкл Моррис Росбаш (Michael Morris Rosbash) родился 7 марта 1944 года в г. Канзас-Сити в семье еврейских беженцев из нацистской Германии, прибывших в США в 1938 г. Его отец Альфред Росбаш был кантором синагоги, мать Хильде Росбаш занималась научными исследованиями в области клинической цитопатологии. Еще будучи школьником, будущий нобелевский лаурет посещал лекции по биологии в Калифорнийском технологическом институте и работал в лаборатории Нормана Дэвидсона. Окончил Калифорнийский технологический институт со специализацией по химии в 1965 г., а в 1970 г. – отделение биофизики Массачусетского технологического института. После трехлетней постдокторантуры по генетике в Эдинбургском университете в 1974 г. был принят на работу в Брандейский университет, где работает до сих пор. Его жена, ученый-генетик Надя Абович (Nadja Abovich), также является соавтором некоторых его работ.
C Дж. Холлом его связывает многолетнее партнерство: «Мы всегда были очень хорошими друзьями, прежде чем начали работать вместе. Кроме того, у нас были похожие навыки».
 Майкл Уоррен Янг (Michael Warren Young) родился 28 марта 1949 года в г. Майами (США). Получил докторскую степень в Техасском университете в г. Остин в 1975 г. В период с 1975 по 1977 г. был докторантом в Стэнфордском университете в г. Пало-Альто. С 1978 г. работает на факультете Рокфеллеровского университета в Нью-Йорке.
Майкл Уоррен Янг (Michael Warren Young) родился 28 марта 1949 года в г. Майами (США). Получил докторскую степень в Техасском университете в г. Остин в 1975 г. В период с 1975 по 1977 г. был докторантом в Стэнфордском университете в г. Пало-Альто. С 1978 г. работает на факультете Рокфеллеровского университета в Нью-Йорке.
Более 30 лет своей научной деятельности М. Янг посвятил исследованиям генетически контролируемых закономерностей сна и дневной деятельности у дрозофилы. На протяжении работы в Рокфеллеровском университете он и его лаборатория внесли значительный вклад в хронобиологию, определив основные гены, связанные с регулированием клеточных часов, ответственных за циркадные ритмы. М. Янг раскрыл функцию гена period, необходимого для нормального функционирования цикла сна плодовых мушек. Лаборатории М. Янга также приписывают открытие двух других генов, отвечающих за синтез необходимых для циркадного ритма белков – генов timeless и doubletime.
В интервью Нобелевскому сайту М. Янг рассказал, почему занялся изучением циркадных ритмов: «Я просто подумал, что это потрясающая научная проблема и, может быть, самая сложная вещь, которую я мог бы попытаться решить, потому что она связана с поведением. Можно исследовать и научно обосновать довольно сложное поведение, которое мы все демонстрируем и которое наиболее отчетливо представлено циклами сна. Нам невероятно повезло – удалось найти гены, которые объясняют, как работает циркадный ритм. Большинство открытий были сделаны независимо, но нам втроем приходилось иногда сотрудничать, хотя мы работали над немного разными проблемами. В то же время решения этих научных проблем складываются вместе подобно кусочкам пазла, создавая единую картину».
Литература
- Zehring W.A., Wheeler D.A., Reddy P., Konopka R.J., Kyriacou C.P., Rosbash M., Hall J.C. (1984). P-element transformation with period locus DNA restores rhythmicity to mutant, arrhythmic Drosophila melanogaster. Cell 39, 369-376.
- Bargiello T.A., Jackson F.R., Young M.W. (1984). Restoration of circadian behavioural rhythms by gene transfer in Drosophila. Nature 312, 752-754.
- Siwicki K.K., Eastman C., Petersen G., Rosbash M., Hall J.C. (1988). Antibodies to the period gene product of Drosophila reveal diverse tissue distribution and rhythmic changes in the visual system. Neuron 1, 141-150.
- Hardin P.E., Hall J.C., Rosbash M. (1990). Feedback of the Drosophila period gene product on circadian cycling of its messenger RNA levels. Nature 343, 536-540.
- Liu X., Zwiebel L.J., Hinton D., Benzer S., Hall J.C., Rosbash M. (1992). The period gene encodes a predominantly nuclear protein in adult Drosophila. J Neurosci 12, 2735-2744.
- Vosshall L.B., Price J.L., Sehgal A., Saez L., Young M.W. (1994). Block in nuclear localization of period protein by a second clock mutation, timeless. Science 263, 1606-1609.
- Price J.L., Blau J., Rothenfluh A., Abodeely M., Kloss B., Young M.W. (1998). Double-time is a novel Drosophila clock gene that regulates PERIOD protein accumulation. Cell 94, 83-95.
Подготовила Катерина Котенко
Тематичний номер «Онкологія» № 5 (51), грудень 2017 р.


