26 грудня, 2017
Грип та його ускладнення: у фокусі – патогенез
Продовження. Початок у № 3 (40), 2017 р., стор. 12-14.
 Патогенетична терапія геморагічного набряку легень має істотні особливості і, на жаль, об’єктивні обмеження. На початковій фазі набряку відбувається нагромадження рідини й розширення простору в альвеолярно-капілярній мембрані (АКМ), що відразу ж призводить до порушення дифузії кисню крізь цей бар’єр, водночас рівень дифузії вуглекислого газу залишається практично незмінним (його дифузійна здатність у 20-25 разів вища, ніж у кисню) [6, 18-20]. При подальшому прогресуванні набряку порушується дифузія вуглекислого газу. На початковому етапі набряк іще не виходить за межі інтерстицію та базальної мембрани альвеолоцитів і, по суті, ще є інтерстиціальним. На цьому етапі рідина не пропотіває в альвеоли, але рівень гіпоксії однаково зростає і може проявлятися посиленням ознак гострої дихальної недостатності у вигляді тривоги, відчуття нестачі повітря, швидко наростаючої задишки з ціанозом, хоча фізикальна картина в легенях мізерна й проявляється у вигляді жорсткого дихання і сухих хрипів, а також незначним дифузним аускультативним послабленням дихання.
Патогенетична терапія геморагічного набряку легень має істотні особливості і, на жаль, об’єктивні обмеження. На початковій фазі набряку відбувається нагромадження рідини й розширення простору в альвеолярно-капілярній мембрані (АКМ), що відразу ж призводить до порушення дифузії кисню крізь цей бар’єр, водночас рівень дифузії вуглекислого газу залишається практично незмінним (його дифузійна здатність у 20-25 разів вища, ніж у кисню) [6, 18-20]. При подальшому прогресуванні набряку порушується дифузія вуглекислого газу. На початковому етапі набряк іще не виходить за межі інтерстицію та базальної мембрани альвеолоцитів і, по суті, ще є інтерстиціальним. На цьому етапі рідина не пропотіває в альвеоли, але рівень гіпоксії однаково зростає і може проявлятися посиленням ознак гострої дихальної недостатності у вигляді тривоги, відчуття нестачі повітря, швидко наростаючої задишки з ціанозом, хоча фізикальна картина в легенях мізерна й проявляється у вигляді жорсткого дихання і сухих хрипів, а також незначним дифузним аускультативним послабленням дихання.
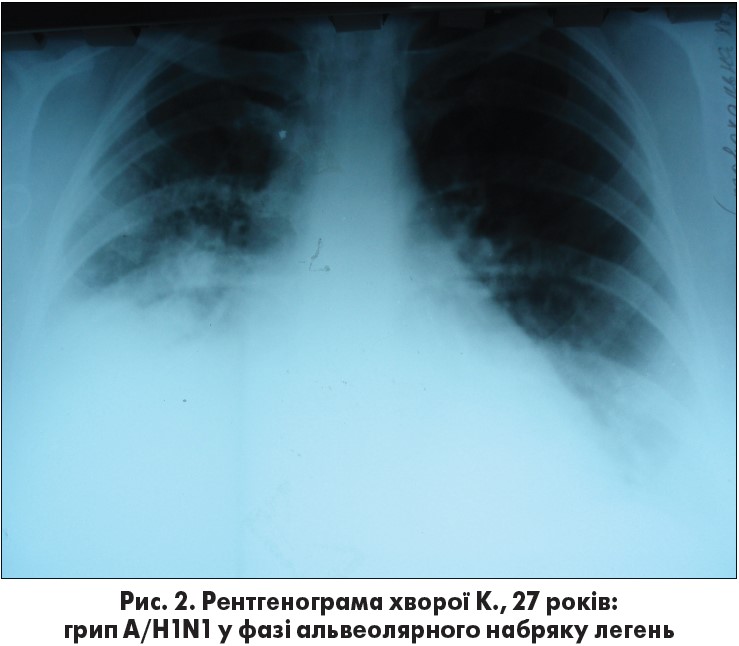
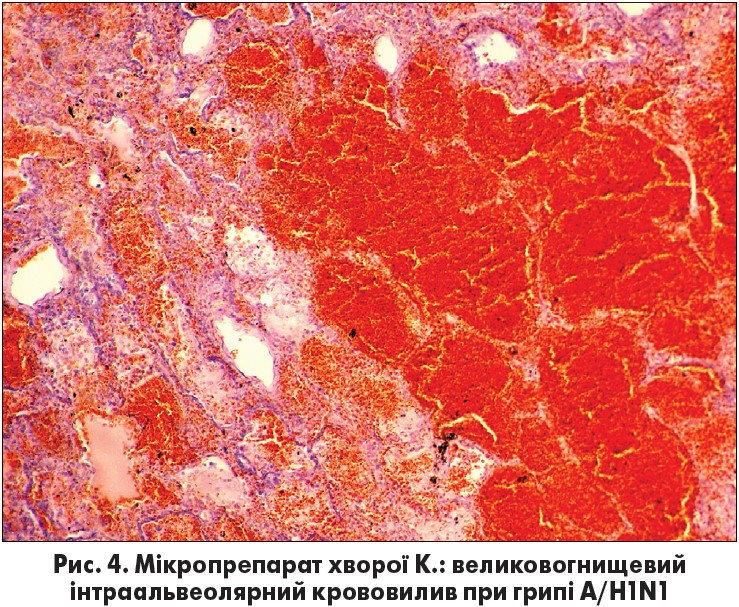
При рентгенологічному обстеженні у фазі інтерстиціального набряку легень можна виявити лише неістотне посилення легеневого малюнка. Наступним етапом є пропотівання рідини й проникнення формених елементів крові в альвеоли. З цієї миті набряк стає альвеолярним, а отже, практично некерованим, з усіма властивими йому клінічними ознаками (рис. 2-4). Досвід показує, що саме момент переходу від інтерстиціального в альвеолярний набряк є критичним для хворих із геморагічним набряком легень при грипі. Розвиток альвеолярного набряку легень часто відбувається лавиноподібно, і терапія нерідко вже виявляється малоефективною.
Тому вкрай важлива саме рання діагностика початку геморагічного набряку легень при грипі. Незважаючи на те що клінічно геморагічний набряк легень проявляється скупо, саме клінічні симптоми, особливо їх динаміка, здатні вказати на розвиток набряку легень. Одним із таких симптомів є прогресуюча задишка. Це фактично єдиний суб’єктивний і об’єктивний критерій, що сигналізує про необхідність початку проведення протинабрякової терапії. Цей момент не можна пропустити у жодному разі, оскільки лише на стадії інтерстиціального геморагічного набряку легень іще можна отримати помітний ефект від патогенетичної терапії. У разі розвитку альвеолярного набряку можливий несприятливий прогноз для життя хворого. У зв’язку з цим саме на стадії інтерстиціального набряку слід провести всі можливі заходи інтенсивної терапії.
Насамперед необхідно скорегувати підвищену проникність капілярної ланки мікроциркуляції. На цьому етапі єдиними ефективними препаратами, незважаючи на тривалі дискусії про доцільність їх призначення, є глюкокортикоїди, здатні блокувати провідні патогенетичні шляхи геморагічного набряку при грипі. Глюкокортикоїди справляють потужну протинабрякову дію (найефективніший – дексаметазон), мембраностабілізуючий (стабілізація клітинних мембран капілярних ендотеліоцитів, базальних мембран капілярів та альвеолоцитів), імуносупресивний (блокування аутоімунних реакцій), антитоксичний, замісний і антистресовий ефект, а також сприяють репарації, стимулюючи клітинний геном. Досвід показує, що добова доза глюкокортикоїдів має бути доволі високою (в перерахунку на преднізолон близько 300 мг), і вводять їх при цьому стані тільки внутрішньовенно, хоча ефективними можуть бути й нижчі дози. На ранніх етапах терапії перевагу слід віддавати дексаметазону, зважаючи на те, що він забезпечує найбільш виражений протинабряковий ефект серед усіх глюкокортикоїдів. Таку інтенсивну терапію призначають за життєвими показаннями, і триває вона, як правило, не більш як 3-5 діб. Така схема призначення практично не може сприяти розвитку імунодефіциту з наступними бактерійними ускладненнями [4, 6, 20, 21].
Питання про ефективність глюкокортикоїдів при геморагічному набряку легень на сьогодні залишається дискусійним. Так, на превеликий жаль, неврахування факту розвитку у хворих на тяжкий грип не вірусної пневмонії, а токсичного геморагічного набряку легень призвело до того, що в адаптованій клінічній настанові «Грип та гострі респіраторні інфекції» (2014) введено заборону призначати кортикостероїди. Є лише єдина поправка: «Застосування кортикостероїдів у малих дозах можна розглядати у пацієнтів із септичним шоком, які потребують судинозвужувальних препаратів, і з підозрою на наднирникову недостатність» [12]. Натомість призначення кортикостероїдів за життєвими показаннями і з урахуванням механізмів їхньої фармакологічної дії дає хворому шанс на виживання та одужання.
Наразі не розроблено лікарських засобів та методів для ефективної терапії при ушкодженні легеневих капілярів [20]. Хворим із геморагічним набряком легень призначається патогенетичне лікування з паралельним забезпеченням транспорту й дифузії кисню та вуглекислого газу в системі АКМ, про що йтиметься далі.
Особливістю проведення протинабрякової терапії при грипозному геморагічному набряку легень є її обмеженість, яка тісно пов’язана з об’ємом парентерально введеної з метою дезінтоксикації рідини. Звісно, що при тяжких чи навіть неускладнених формах грипу парентерально вводять не більш ніж 300-400 мл рідини, переважно розчини дрібномолекулярних декстранів. При проведенні протинабрякової терапії перевагу віддають таким дрібномолекулярним нативним колоїдам, як 10-20% розчин альбуміну. Кристалоїдні розчини вводити не рекомендовано внаслідок їхньої здатності швидко проникати в тканини, у результаті чого може виникнути набряк або ж посилитися вже наявний.
Одночасно вживають заходів для «розвантаження» малого кола кровообігу. За допомогою елементарних прийомів можна досягти позитивного ефекту, до яких, зокрема, належать напівсидяче положення зі спущеними ногами, а також такі відволікаючі процедури, як гарячі ножні ванни, накладання венозних джгутів на нижні кінцівки.
Застосування гангліоблокаторів для «безкровного кровопускання» з метою зниження тиску в малому колі кровообігу й депонування крові на периферії практично неможливе через небезпеку системного зниження артеріального тиску і порушення тканинної перфузії легень, які вже й так страждають від гіпоксії. Це ж стосується і звичайного кровопускання, оскільки ефективною при набряку легень може бути евакуація не менш як 500 мл крові [1, 6, 20]. Для розвантаження малого кола кровообігу можна застосовувати 2,4% розчин теофіліну по 10 мл внутрішньовенно, попередньо розвівши його в 10-20 мл ізотонічного розчину натрію хлориду. Для корекції небажаного позитивного хронотропного ефекту останнього допустиме застосування 0,06% корглікону внутрішньовенно не більш ніж 0,5 мл в окремому шприці (також розведений в ізотонічному розчині).
Як ефективний протинабряковий засіб застосовують фуросемід у разовій дозі 60-120 мг, і надалі у разі необхідності його використовують під контролем показників гемодинаміки та з оцінкою ефективності терапії. Проте не всі автори погоджуються, що фуросемід забезпечує ефективну протинабрякову дію, хоча й відзначають позитивний вплив останнього на оксигенацію [6, 20].
Слід зауважити, що застосування осмотичних діуретиків при грипозному набряку легень досить небезпечне. Адже сечовина вільно проникає в інтерстиціальний простір, посилюючи набряк тканини, а у разі застосування манітолу необхідно враховувати можливість виникнення різкого підвищення внутрішньосудинного об’єму крові, що також може призвести до посилення набряку. Тому найбезпечнішим засобом, щоправда, вже онкотичної протинабрякової терапії, є застосування 20% розчину альбуміну. Водночас у разі прогресування набряку легень і його переходу в альвеолярну фазу можливе застосування й осмотичних діуретиків, але за життєвими показаннями. На думку низки авторів [6, 20], при набряку легень перевагу слід віддавати сечовині, яку вводять у вигляді 30% розчину в дозі 1,0-1,5 г/кг зі швидкістю 30-60 крапель на хвилину. Проте з огляду на зазначену вище інформацію, така перевага доволі сумнівна.
Для корекції гіпоксичних розладів при інтерстиціальному набряку легень застосовують кисневу терапію – від інгаляційної до екстракорпоральної. Механізм дії інгаляційної оксигенотерапії полягає у збільшенні парціального тиску кисню у вдихуваній хворим газовій суміші (повітряно-кисневій). Застосування чистого кисню можливе тільки на короткий період, оскільки як сильний окислювач він додатково може призвести до пошкодження АКМ. Найбільш оптимальними й безпечними вважають повітряно-кисневі суміші з умістом кисню не більш ніж 60% (зазвичай 40-50%) зі швидкістю введення по носових катетерах 4-6 л/хв [6].
У разі виникнення загрози розвитку альвеолярного набряку легень і швидко прогресуючої дихальної недостатності, що супроводжується вираженою гіпоксією, хворого необхідно перевести на штучну вентиляцію легень (ШВЛ), особливістю якої є наявність спеціальних режимів, – з постійним позитивним тиском у процесі ШВЛ або підвищеним тиском при видиху. Використовують також високочастотні режими ШВЛ і осциляторну модуляцію дихання [20].
Такі режими, з одного боку, запобігають розвитку альвеолярної фази набряку легень і зприяють зменшенню інтерстиціального набряку, а другого – здатні підвищити понижену оксигенацію крові за рахунок посилення дифузії газів крізь АКМ. Переведення хворого на ШВЛ має бути мотивоване й показане пацієнтам за наявності зниження сатурації артеріальної крові киснем. Основна мета оксигенотерапії полягає у підтримці рівня насичення крові киснем не менш ніж 90% [20].
При вираженому пошкодженні АКМ жодні варіанти ШВЛ, навіть із високим умістом кисню у вдихуваній суміші, не забезпечать належного насичення крові киснем та ефективне виведення вуглекислого газу. У такому разі єдиним методом забезпечення оксигенації крові залишається екстракорпоральна мембранна оксигенація (ЕКМО). Фактично це апарат «штучних легень». Розробку й практичне використання таких апаратів розпочали ще в 1970-ті роки. Звісно, що зараз вони більш ефективні й доступні для практичного застосування. Водночас усе ще залишаються дорогими, відтак – їх використання обмежене. Та й їхня ефективність залишається недостатньою. Проте саме розробка ефективних апаратів для ЕКМО наразі є фактично єдиним реальним і перспективним засобом для хворих з ушкодженням АКМ легень. Альвеолярно-капілярний сектор легень має надзвичайно високий регенераторний потенціал [6, 18-20], тому ефективна тимчасова «заміна» його основних функцій ЕКМО за відсутності наступного ушкодження робить можливим швидке відновлення пошкоджених тканин цього життєво важливого органа.
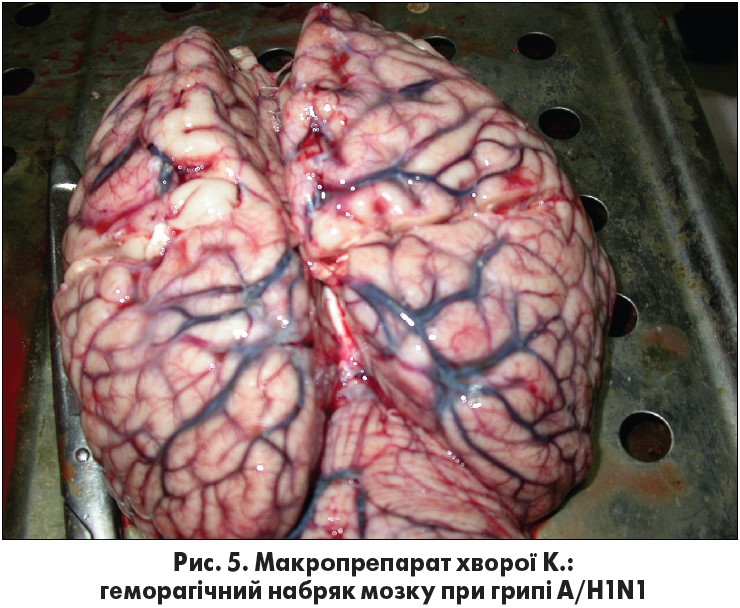
Нерідко тяжкі форми грипу ускладнюються геморагічним набряком мозку та його оболонок [4, 6, 20] (рис. 5), який зазвичай помилково трактують як «грипозний менінгоенцефаліт». Набряк мозку й оболонок при грипі може бути не лише наслідком ураження власне мікросудин, а й зумовлений значною гіпоксією, спричиненою легеневою патологією. Клінічна картина набряку мозку та його оболонок при грипі досить
інформативна, що дає змогу рано розпізнати таке ускладнення і вдатися до протинабрякової терапії. З огляду на особливості патогенезу цього набряку, який виникає внаслідок ушкодження мікросудин, і його геморагічну природу необхідно знову повернутися до глюкокортикоїдної терапії, передусім – до дексаметазону. В іншому протинабрякова терапія кардинально не відрізняється від тактики, засобів і методів, використовуваних у патогенетичній терапії набряку мозку та його оболонок при менінгоенцефаліті. На жаль, первинне ураження центральної нервової системи (ЦНС) при грипі нерідко призводить до несприятливих наслідків. Однією з основних причин цього є низька ефективність антивірусної терапії, зумовлена об’єктивними викладеними раніше поясненнями.
У разі комбінованого первинного ураження легень і ЦНС у хворого на грип (ураховуючи їхні патогенетичні особливості), навіть незважаючи на проведення інтенсивної терапії, прогноз для життя у такого пацієнта завжди залишається сумнівним.
На практиці лікарі нерідко зловживають антибіотиками. Необхідно пам’ятати, що ці препарати мають чіткі клінічні показання до застосування: 1) украй тяжкий ступінь грипу (гіпертоксична форма); 2) грип у дітей віком до 2 років, вагітних, різко ослаблених хворих, осіб похилого і старечого віку; 3) бактерійні ускладнення; 4) супутні хронічні захворювання, які можуть загостритися під впливом грипу. У решті випадків антибіотики протипоказані, адже підсилюють алергізацію організму, пригнічують утворення протигрипозних антитіл, збільшують частоту виникнення різних ускладнень [17].
Ефективність антибіотиків пеніцилінового ряду та цефалоспоринів істотно обмежує широке розповсюдження штамів бактерій, які продукують пеніцилінази, цефалоспоринази й хромосомні бета-лактамази. Тому при тяжких бактерійних ускладненнях грипу слід застосовувати цефалоспорини III-IV покоління, комбінації цефалоспоринів чи пеніцилінів з інгібіторами бета-лактамаз, аміноглікозидами III покоління, а також макроліди III покоління (не поєднувати з пеніцилінами й цефалоспоринами – антагонізм). Препаратами вибору можуть бути «респіраторні» фторхінолони III-IV покоління, які мають високу антибактерійну активність і широкий спектр дії, зокрема на полірезистентні грамнегативні та грампозитивні бактерії. Високоефективними, у тому числі при нозокоміальних інфекціях, є оксазолідинони (в Україні зареєстрований лінезолід), які цілком позбавлені перехресних реакцій з іншими антибіотиками, однак діють тільки на грампозитивні бактерії, анаеробні бактероїди й клостридії. Засобами резерву залишаються карбапенеми (тієнаміцини), які мають найширший спектр дії.
З метою первинної специфічної профілактики (насамперед осіб категорії ризику) наразі проводиться прискорена розробка і реєстрація специфічних вакцин на основі виділеного штаму збудника.
Грипозні вакцини виготовляють з актуальних штамів вірусу грипу людини, які щороку рекомендує ВООЗ для використання в майбутньому епідемічному сезоні на підставі аналізу епідемічної ситуації. Ці рекомендації розробляють, спираючись на дані епіднагляду за ситуацією із грипом, який здійснюють через всесвітню мережу у 110 лабораторіях 83 країн світу.
Щеплення проти грипу захищає від захворювання близько 80% здорових дітей і дорослих. У старих людей захист дещо слабший, але вакцинація однаково істотно зменшує ступінь тяжкості грипу, знижує частоту ускладнень і летальних наслідків.
Нині для профілактики грипу застосовують переважно інактивовані грипозні вакцини – препарати, що містять антигени вірусів грипу актуальних штамів, які циркулюють саме у цей час і спричиняють епідемію. Вони належать до трьох серотипів вірусу грипу: A/H1N1, A/H3N2 і В. Вірус грипу вирощують у курячих ембріонах, інактивують і ретельно очищають від білків та інших баластних компонентів курячого ембріона.
Застосовують три види інактивованих грипозних вакцин: цільновіріонні, спліт- і субодиничні вакцини.
Цільновіріонна вакцина містить інактивовані високоочищені незруйновані (цілісні) віріони вірусу грипу.
Спліт-вакцина містить зруйновані інактивовані віріони вірусу грипу; до її складу входять усі віріонні білки вірусу, не тільки поверхневі, а й внутрішні антигени. Завдяки високому очищенню в ній немає вірусних ліпідів і білків курячого ембріона.
Субодинична вакцина включає лише два поверхневих вірусних білки – гемаглютиніну й нейрамінідази, найважливіших для індукції імунної відповіді проти грипу. Решта білків віріона й курячого ембріона видаляється при очищенні.
З перерахованих вакцин цільновіріонна вакцина дещо реактогенніша, особливо для маленьких дітей; субодиничні вакцини найменш реактогенні.
Щеплення проти грипу здатне індукувати захисний рівень протигрипозних сироваткових антитіл у більшості вакцинованих – від дітей 6-місячного віку до старшого віку осіб, і приводити до утворення секреторних антитіл у носоглотці. З огляду на слабку реактогенність спліт- і субодиничної вакцин, їх доцільно застосовувати для осіб різного віку, починаючи з 6 міс, а також для людей із хронічними захворюваннями легень, серця та іншими патологічними станами.
Розвиток імунітету починається з другої доби після вакцинації, досягає максимуму на 15-30-ту добу після щеплення і триває всього лише 6-12 міс, що вимагає щорічного введення вакцини. Профілактична ефективність щеплення – 70-90%.
Протипоказаннями до вакцинації від грипу є:
- наявність гострого захворювання або загострення хронічного захворювання в день вакцинації;
- алергія на білок курячих яєць;
- алергічні реакції на інші компоненти препарату;
- тяжкі алергічні реакції на попереднє щеплення конкретним препаратом.
Сьогодні альтернативи вакцинації немає. Відтак необхідно провести щеплення від сезонного грипу передусім представників так званої групи ризику (медпрацівників, вагітних, дітей, осіб, які мають хронічні недуги), а також усіх охочих.
На жаль, мінливість вірусу грипу призводить до швидкого старіння вакцин – саме тому відбуваються сезонні епідемії. Науковці припускають, що поява нових форм A/H1N1 нівелює ефект від вакцинації, що може стати причиною постійної циркуляції в популяції цього штаму вірусу.
Первинна неспецифічна профілактика спрямована на запобігання потраплянню вірусу в організм, а також на посилення неспецифічної імунної відповіді для уникнення розвитку захворювання.
Найбільш простим і ефективним способом профілактики грипу є так зване соціальне дистанціювання, тобто перебування якнайдалі від людей, які можуть бути інфіковані. Якщо інфекція розповсюджується у суспільстві, необхідно уникати великих зібрань, скупчень людей на роботі і, якщо можливо, залишатися вдома.
Водночас ВООЗ не рекомендує обмежувати переміщення людей, а також організовувати карантинний контроль у пунктах прибуття, зокрема в аеропортах. Такі заходи є неефективними й економічно недоцільними.
Рекомендується ретельно й доволі часто мити руки з милом або дезінфікуючими розчинами на спиртовій основі. Експерти ВООЗ підтверджують, що часте миття рук здатне запобігти вірусним інфекціям, у тому числі грипу. За результатами одного з досліджень, невеликі крапельки, що містять вірус, можуть затримуватися на поверхні різних предметів, і вірус передаватиметься через пальці в ніс або в очі. Засоби, у вигляді гелю або піни, що містять алкоголь, добре знищують віруси та бактерії на поверхні предметів.
Література
1. Андрейчин М.А. Проблема грипу А/H1N1: історія і сучасність / М.А. Андрейчин, В.С. Копча // Інфекційні хвороби. – 2009. – № 4. – С. 5-19.
2. Гострі респіраторні вірусні інфекції: навч. посіб. / [М.А. Андрейчин, В.П. Малий, Л.Я. Ковальчук та ін.]; за ред. М.А. Андрейчина, В.П. Малого. – Тернопіль: ТДМУ, 2011. – 304 с.
3. Возіанова Ж.І. Інфекційні і паразитарні хвороби: У 3-х т. / Ж.І. Возіанова. – К.: Здоров’я, 2001. – Т. 1. – 856 с.
4. Фролов А.Ф., Шабловская Е.А., Шевченко Л.Ф. и др. Грипп. – К.: Здоров’я, 1985. – 128 с.
5. Букринская А.Г. Молекулярные основы патогенности вирусов / А.Г. Букринская, В.М. Жданов. – М.: Мед., 1991. – 256 с.
6. Бондаренко А.М. Грип А/H1N1 – реалії та «особливості» / А.М. Бондаренко // Інфекційні хвороби. – 2009. – № 4. – C. 96-102.
7. Deadly new flu virus in US and Mexico may go pandemic, April 24, 2009. – Режим доступу: http://www.newscientist.com/article/dn17025-deadly-new-flu-virus-in-us-and-mexico-may-go-pandemic.html.
8. Strong interferon-inducing capacity of a highly virulent variant of influenza A virus strain PR8 with deletions in the NS1 gene / [G. Kochs, L. Martinez-Sobrido, S. Lienenklaus et al.] // J. Gen. Virol. – 2009. – Vol. 197. – P. 2661-2672.
9. Дашо М.Б. Грип А: перебіг, типові й нетипові ускладнення / М.Б. Дашо, О.Б. Надрага, С.А. Лишенюк // Інфекційні хвороби. – 2010. – № 3 – Т. 61. – С. 38-42.
10. WHO Global influenza Surveillance Network. – 2009. – Режим доступу: http://www.who.int/ csr/disease/influenza/surveillance/en/.
11. Antiviral drugs and pandemic (H1N1). – 2009. – Режим доступу: http://www.who.int/csr/disease/ swineflu/frequently_asked_questions/ swineflu_faq_antivirals/en/index.html.
12. Наказ МОЗ України від 16.07.2014 № 499 «Про затвердження та впровадження медико-технологічних документів зі стандартизації медичної допомоги при грипі та гострих респіраторних інфекціях». – Режим доступу: http://www.moz.gov.ua/ua/portal/dn_20140716_0499.html.
13. Предотвращение тяжелых случаев гриппа H1N1 – основа новых рекомендаций ВОЗ. – Режим доступа: http://www.roche.ru/content/ ru/publication-newwho.html 24.11.2009.
14. Тамифлю. – 2009. – Режим доступа: http://medi.ru/doc/22301.htm.
15. Taubenberger J.K. Diskovery and characterization of the 1918 pandemic influenza virus in historical context / J.K. Taubenberger, J.V. Hultin, D.M. Morens // Antivir. Ther. – 2007. – Vol. 12. – P. 581-591.
16. Lung Pathology in Fatal Novel Human Influenza A (H1N1) Infection / [T. Mauad, L.A. Hajjar, G.D. Callegari et al.] // Am. J. Respir. Crit. Care Med. – 2009. – Vol. 142. – P. 1982-1991.
17. Інфекційні хвороби в загальній практиці та сімейній медицині / За ред. М.А. Андрейчина. – Тернопіль: Укрмедкнига, 2007. – 500 с.
18. Гистология, цитология и эмбриология / [Ю.И. Афанасьев, Н.А. Юрина, Е.Ф. Котовский и др.]: Под ред. Ю.И. Афанасьева, Н.А. Юриной. – 5-е изд. перераб. и доп. – М.: Медицина, 2002. – 744 с.
19. Хэм А. Гистология. В 5-ти т., Т. 4 / А. Хэм, Д. Кормак. – М.: Мир, 1983. – 245 с.
20. Сепсис и полиорганная недостаточность / В.Ф. Саенко, В.И. Десятирик, Т.А. Перцева, В.В. Шаповалюк. – Кривой Рог: Минерал, 2005. – 466 с.
21. Патент 63098. Україна, МПК A61К 31/573 (2006.01). Спосіб лікування грипозного геморагічного набряку легень / А.М. Бондаренко, М.А. Андрейчин, В.С. Копча. – № u 201102908; Заявлено 12.03.2011; Опубл. 26.09.2011, Бюл. № 18.