9 травня, 2018
Инновационное лечение остеоартроза: обзор современных данных
Болезни, связанные с поражением хрящевой ткани сустава, в частности остеоартроз (ОА), являются важнейшей проблемой здравоохранения, особенно в странах с высокой продолжительностью жизни.
 Зведующий кафедрой внутренней медицины № 3 Национального медицинского университета им. А.А. Богомольца (г. Киев), доктор медицинских наук, профессор Олег Борисович Яременко в рамках научно-практической конференции «Родственные группы системных болезней соединительной ткани: определение статуса и менеджмент на основе международных стандартов» (22-23 марта, г. Киев) выступил с докладом, посвященным перспективам современных методов лечения ОА, в частности тканевой инженерии.
Зведующий кафедрой внутренней медицины № 3 Национального медицинского университета им. А.А. Богомольца (г. Киев), доктор медицинских наук, профессор Олег Борисович Яременко в рамках научно-практической конференции «Родственные группы системных болезней соединительной ткани: определение статуса и менеджмент на основе международных стандартов» (22-23 марта, г. Киев) выступил с докладом, посвященным перспективам современных методов лечения ОА, в частности тканевой инженерии.
Проблемы, связанные с ведением больных ОА, сохраняют сегодня свою актуальность, и в значительной степени они обусловлены тем, что лечение ОА, как правило, начинается на поздних стадиях развития заболевания, когда повреждения хряща уже значительны. Между тем полноценная регенерация суставного хряща, который не кровоснабжается и имеет низкий уровень метаболизма, возможна лишь при небольших по площади повреждениях (K. Gronning et al., 2016).
В настоящее время проводятся многочисленные исследования по разработке новых подходов к восстановлению поврежденных хрящевых тканей, в том числе основанных на применении технологий тканевой инженерии и регенеративной медицины. Тканевая инженерия – подход, при котором используются фундаментальные структурно-функциональные взаимодействия в нормальных и патологически измененных тканях при создании биологических заместителей для восстановления или улучшения функционирования тканей.
Клеточно- и тканеинженерные конструкции
На сегодняшний день суставные хрящи пытаются восстанавливать с помощью двух технологий тканевой инженерии: клеточно- и тканеинженерных конструкций (КИК и ТИК). Оба подхода имеют целью замещение разрушенных фрагментов хрящей нормальной полноценной тканью. Для создания КИК хрящевой ткани клетки предварительно культивируют in vitro на трехмерном биодеградируемом матриксе. Затем в сустав имплантируют смесь, содержащую биостимулирующий матрикс, в котором, как в сеточке, находятся хондроциты либо мультипотентные мезенхимальные стромальные клетки, а также биоактивные молекулы (факторы роста, цитокины). Биополимерный матрикс «отвечает» за доставку компонентов смеси к хрящам, а содержащиеся в КИК клетки оказывают регенерирующее действие, тем самым восстанавливая функции сустава (V.I. Sevastyanov, 2014). К клеткам КИК предъявляются наиболее высокие требования, а именно: простота получения, способность к быстрому культивированию и размножению в достаточном количестве.
В свою очередь, ТИК «выращивают» из КИК в специальных биореакторах, обеспечивающих необходимые условия для пролиферации и дифференциации клеточных элементов. Для стимуляции дифференцировки и роста хондроцитов применяют различные методы воздействия на культуру клеток: механическая и ультразвуковая стимуляция способствуют увеличению синтеза гликозаминогликанов, в то время как электрическая приводит к увеличению синтеза внутриклеточного матрикса (H. Yu et al., 2016).
Для культивирования часто используют соматические стволовые клетки взрослого организма, которые представляют собой недифференцированные клетки, находящиеся в составе дифференцированной ткани. В достаточно большом количестве они содержатся в костном мозге, сетчатке глаза, роговице, пульпе зуба, печени, коже и поджелудочной железе. Чаще всего используют клетки, полученные путем пункции костного мозга.
Однако источником стромальных стволовых клеток могут быть и другие ткани. В настоящее время разработана методика выделения фибробластоподобных клеток из гетерогенной популяции клеток жировой ткани (Р. Zuk et al., 2001).
Если говорить о факторах роста, то наиболее изученным и активным является так называемый трансформирующий фактор роста-β (TGF-β). В наибольшей концентрации он содержится в костном матриксе, где стимулирует пролиферацию клеток соединительной ткани и их дозревание. При применении в высоких концентрациях может проявляться побочное действие TGF-β: гипертрофия хондроцитов и оссификация хряща. Кроме того, к недостаткам метода следует отнести его высокую стоимость.
Известно, что тромбоциты содержат факторы роста и вещества, которые являются потенциальными хондропротекторами. Следовательно, обогащенную тромбоцитами плазму можно с успехом использовать для стимуляции регенеративных процессов в суставных хрящах. При этом хорошего терапевтического эффекта можно добиться лишь с помощью плазмы, содержащей не менее 1 млн тромбоцитов в 1 мкл. Главным действующим веществом в данном случае являются именно факторы роста, в том числе TGF-β, который в большом количестве содержится в концентрате тромбоцитов. Однако, как свидетельствуют данные литературы, этот метод лечения наиболее эффективен у молодых пациентов с незначительными дегенеративными изменениями суставов.
Межклеточный матрикс представляет собой полимер с трехмерной структурой, который обеспечивает организацию и удержание клеток, создавая условия для их роста. Матрикс чаще всего формируют из коллагена или гиалуроната (коллагеновые волокна покрывают фибронектином).
Неомыляемые соединения масел сои и авокадо (препарат Пиаскледин®)
В многочисленных экспериментах in vitro и in vivo была продемонстрирована способность препарата Пиаскледин снижать уровень маркеров деградации хряща и оказывать стимулирующее действие на хрящевую ткань. Пиаскледин оказывает ингибирующее действие на коллагеназу и простагландины 2 типа, уменьшает синтез фибронектина, что, в свою очередь, способствует естественному восстановлению конструкции хряща. Кроме того, он снижает выработку металлопротеиназ, ингибирует интерлейкины‑1β, -6, -8, а также оказывает стимулирующее действие на синтез коллагена ІІ в хондроцитах. В условиях клиники было продемонстрировано, что на фоне приема Пиаскледина происходит повышение уровня TGF-β (как TGF-β1, так и TGF-β2) в синовиальной жидкости коленных суставов. Данный эффект наиболее выражен на 1-2-м месяце лечения. Таким образом, представлялось вполне вероятным, что использование Пиаскледина отдельно или в комбинации с TGF-β1 будет способствовать дифференциации стволовых клеток в культуральной среде.
Чтобы проверить данную гипотезу, в недавнем исследовании сравнивали влияние TGF-β, препарата Пиаскледин и их комбинации на хондрогенную дифференцировку стволовых клеток в фибриновых и фибрин-альгинатных каркасах (B. Hashemibeni et al., 2018).
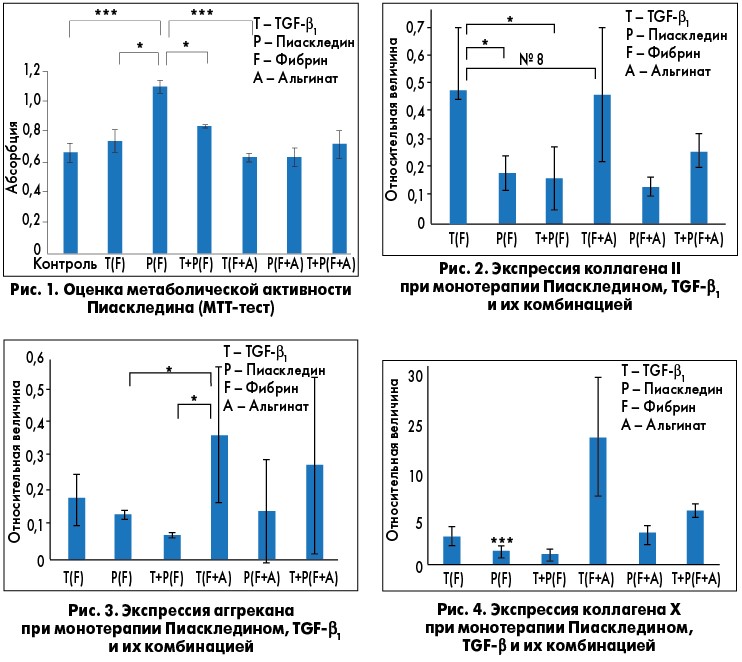
Установлено, что Пиаскледин более выражено увеличивает выживаемость и пролиферацию дифференцированных клеток в каркасе фибрина по сравнению с TGF-β и комбинацией Пиаскледин + TGF-β. Комбинация Пиаскледина и TGF-β значительнее увеличивала пролиферацию стволовых клеток в фибриновом каркасе, чем только TGF-β или только Пиаскледин в фибрин-альгинатном каркасе (рис. 1). Кроме того, при лечении Пиаскледином, в том числе в комбинации с TGF-β, отмечался достоверно более низкий уровень в хрящевой ткани коллагена Х, ответственного за побочное действие TGF-β (оссификация хряща и других мягких тканей) по сравнению с монотерапией TGF-β. Авторы исследования также отмечают, что и Пиаскледин, и TGF-β значительно повышали уровень аггрекана – протеогликана, участвующего в сохранении гидратированности хрящевой ткани. Протеогликаны, в частности аггрекан, являются основными компонентами матрикса суставного хряща, поэтому данные о возможности влияния на их концентрацию в хрящевой ткани немаловажны. По результатам полимеразно-цепной реакции установлены значительные различия в экспрессии коллагена ІІ, X и аггрекана между группами (рис. 2-4), и на основании этих данных можно сделать вывод, что Пиаскледин по ряду биостимулирующих эффектов не уступает TGF-β1, а по некоторым – превосходит его.
Эти результаты позволяют лучше понять данные клинических исследований с применением Пиаскледина, прежде всего проспективного рандомизированного двойного слепого плацебо-контролируемого исследования ERADIAS, в котором изучали влияние препарата на прогрессирование ОА тазобедренного сустава. Было показано, что в группе пациентов, получавших Пиаскледин, доля пациентов с прогрессированием ОА была меньшей (на 20%), чем в группе плацебо (E. Maheu et al., 2014). Профессор О.Б. Яременко в ходе выступления привел данные собственного исследования, которые перекликаются с результатами исследований с применением Пиаскледина. Согласно этим данным прием Пиаскледина сопровождается 5-кратным снижением уровня маркера деградации коллагена, что сопровождается соответствующими клиническими изменениями.
Таким образом, развитие инновационных методов терапии ОА позволяет надеяться на то, что в ближайшие годы эндопротезирование суставов будет не единственным методом радикального лечения этого инвалидизирующего заболевания. В настоящее время задача врачей – диагностировать ОА на более ранних стадиях и своевременно назначать терапию, способствующую активации процесса регенерации хрящевой ткани. Одним из таких терапевтических методов является применение Пиаскледина, обладающего доказанной клинической эффективностью и потенциальными хондропротективными свойствами.
Подготовила Александра Демецкая
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 2 (56) Квітень 2018 р.