9 травня, 2018
Позиції EULAR щодо застосування протиревматичних препаратів перед вагітністю, під час вагітності та в період лактації
Вступ
Завдяки новим ефективним методам лікування та зниженню частоти віддаленої інвалідизації більшість жінок із ревматичними захворюваннями (РЗ) отримали можливість планувати вагітність, хоча неабиякий ризик несприятливих наслідків зберігається як для матері, так і для плода, особливо при РЗ із поліорганною патологією. Фармакотерапія РЗ під час вагітності може знадобитися для контролю прогресування останніх, оскільки РЗ самі по собі можуть бути загрозою для здоров’я плода та сприятливого родорозрішення.
Ризик, пов’язаний із запальним РЗ у матері, яка не отримала лікування протягом 9 міс вагітності, має бути зіставлений із ризиком потенційної шкоди, спричиненої впливом лікарського засобу на плід.
Корекція терапії в пацієнток, що планують вагітність, спрямована на використання препаратів, які, з одного боку, забезпечували б контроль захворювання в матері, а з іншого – були б безпечними для плода. Однак цим вимогам відповідає лише обмежена кількість протиревматичних засобів та імунодепресантів.
При швидко зростаючій кількості препаратів, доступних для лікування РЗ, відомостей про їхню безпеку у вагітних мало. У 2006 році був опублікований, а в 2008-му – оновлений консенсусний документ про використання протиревматичних препаратів під час вагітності та лактації з урахуванням даних про нові імунодепресанти.
Європейська протиревматична ліга (European League Against Rheumatism – EULAR) визнала своєчасним аналіз нових доступних даних із літературних джерел і декількох баз даних, для того щоб досягти експертного консенсусу щодо безпеки їх застосування до планованої вагітності, а також під час вагітності та лактації. Результатом цього аналізу став новий консенсус EULAR, опублікований у лютому 2016 року.
Дискусія
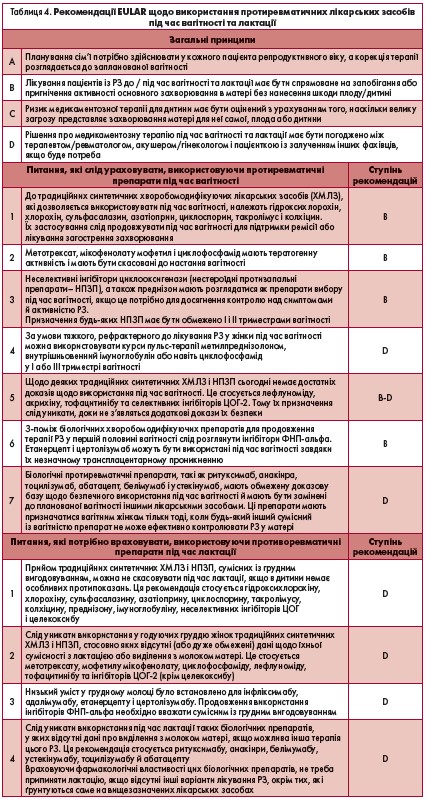 Дані літературних джерел і реєстрів показують, що значна частина лікарських засобів може бути призначена вагітним і годуючим жінкам із РЗ без відчутної шкоди для плода. Систематичні огляди останнього десятиліття надають докази безпеки застосування під час вагітності й лактації для глюкокортикостероїдів, сульфасалазину, протималярійних препаратів, азатіоприну, колхіцину, циклоспорину, такролімусу та імуноглобуліну для внутрішньовенного введення (табл. 4).
Дані літературних джерел і реєстрів показують, що значна частина лікарських засобів може бути призначена вагітним і годуючим жінкам із РЗ без відчутної шкоди для плода. Систематичні огляди останнього десятиліття надають докази безпеки застосування під час вагітності й лактації для глюкокортикостероїдів, сульфасалазину, протималярійних препаратів, азатіоприну, колхіцину, циклоспорину, такролімусу та імуноглобуліну для внутрішньовенного введення (табл. 4).
Наводимо найважливіші зміни в консенсусних рекомендаціях:
1. Систематичні кількісні огляди і регістри підтримують можливість використання антитіл або антагоністів рецепторів до ФНП-альфа в першій половині вагітності. Одне дослідження, опубліковане після завершеного аналізу методом дельфійського експертного оцінювання, показало невелике збільшення кількості вроджених дефектів у І триместрі на тлі лікування за допомогою анти-ФНП-альфа без формування будь-яких вад розвитку. З огляду на відсутність контрольованих досліджень, клінічна значущість цього висновку ще не ясна.
2. Існують відмінності в трансплацентарному перенесенні хворобомодифікуючих біологічних препаратів, що пов’язані зі структурою їхньої молекули і періодом напіввиведення, які мають враховуватися при виборі оптимального препарату для жінок фертильного віку. Наприклад, інфліксимаб і адалімумаб мають бути відмінені на 20-му, а етанерцепт – на 30-32-му тиж вагітності. Безпека використанні цертолізумабу протягом усієї вагітності потребує детальнішого підтвердження за допомогою систематичних кількісних оглядів і метааналізів.
3. для багатьох хворобомодифікуючих біологічних препаратів (цертолізумабу, голімумабу, абатацепту, тоцилізумабу, ритуксимабу, белімумабу й анакінри) не вистачає свідоцтв, які б доводили безпеку для плода/новонароджених. Проте дані вже наявних кількісних систематичних оглядів і реєстрів не вказують на наявність будь-якої шкоди від використання цих препаратів до зачаття або в І триместрі вагітності.
4. Систематичні кількісні огляди й регістри показали, що циклофосфамід, метотрексат і мікофенолату мофетил характеризуються вираженим тератогенним ефектом і мусять бути скасовані перед запланованою вагітністю. Щодо інших іммуносупресантів, то причиною припинення їх застосування перед вагітністю або на її ранніх термінах є відсутність достатніх доказів безпеки цих засобів для плода.
Оскільки в 30-50% випадків вагітність не є запланованою, основне питання полягає в тому, як протікатиме вагітність у жінок, які отримують терапію потенційно тератогенними препаратами.
Дехто з пацієнток вирішують негайно перервати вагітність, тоді як інші розглядають можливість її збереження. Підтвердження факту вагітності гінекологом і визначення точного терміну вагітності абсолютно необхідно для індивідуальної оцінки ризику.
Детальне ультразвукове дослідження (УЗД) плода має бути проведено всім пацієнткам, в яких передбачається незапланована вагітність на тлі прийому потенційно тератогенного препарату.
Макроскопічні аномалії можуть бути оцінені досвідченими фахівцями в галузі репродуктивної медицини в кінці І триместру, а УЗД слід повторювати на більш пізніх стадіях ІІ триместру вагітності.
Інші пренатальні тести, такі як амніоцентез або біопсія ворсин хоріона, зазвичай не показані для підтвердження тератогенного впливу лікарських засобів, але можуть бути рекомендовані для пацієнток із високим ризиком хромосомних аберацій або будь-яких аномалій розвитку, підтверджених УЗД.
Експерти робочої групи досягли високого ступеня узгодженості позицій (90-100%) щодо сумісності протиревматичних препаратів із вагітністю. Набагато менше узгодженості досягнуто з приводу використання кожного з препаратів у клінічній практиці. У позиціях акцент робиться на вроджених вадах розвитку, тоді як у рекомендаціях із клінічного застосування викладено інші критерії, у тому числі особистий досвід лікаря з використання певного медикаментозного препарату, фармакологічні властивості лікарських засобів, національні вподобання, доступність медикаментів у деяких країнах і юридичні проблеми, що виникають під час застосування деяких лікарських засобів (страхове відшкодування, відшкодування витрат).
Позиції щодо грудного вигодовування обмежені оцінкою сумісності препаратів із лактацією, але в них відсутні докладні рекомендації стосовно короткострокового припинення грудного вигодовування або відмови від вигодовування в дні прийому медикаментів, здатних чинити несприятливий вплив на дитину. Як наслідок, спостерігалася доволі велика гетерогенність думок експертів щодо грудного вигодовування в реальній клінічній практиці. Це відбивається в тенденції до перешкоджання пролонгації грудного вигодовування, хоча гнучкий графік годувань міг би дати можливість більшості жінок годувати груддю. Матері, що годують немовлят, можуть дотримуватися альтернативної точкі зору і радше годувати груддю, ніж приймати лікарські засоби для активного лікування свого захворювання.
Проаналізувавши результати досліджень цих проблем, можна погодитися з тим, що саме фармакологічні властивості лікарських засобів могли б слугувати базою для прийняття рішення про дозвіл грудного вигодовування навіть у разі недостатньої доказової бази.
Неіонізовані та ліпофільні агенти з низькою молекулярною масою наймовірніше виділяються з грудним молоком. Навпаки, препарати з високим ступенем зв’язування з білками й високою молекулярною масою навряд чи можуть проникати в грудне молоко, і, таким чином, для них характерний низький ризик побічних ефектів, пов’язаних із грудним вигодовуванням. Останнє особливо важливо для немовлят з екстремально низькою і дуже низькою вагою при народженні, які могли б отримати максимальну користь від грудного вигодовування, проте не існує жодних досліджень по цій підгрупі пацієнтів з оцінкою ризиків, які можуть виникати при контакті з лікарськими засобами в грудному молоці.
Дослідження, спрямовані на оцінку довгострокового впливу лікарських засобів, що вводяться під час вагітності та/або грудного вигодовування, на здоров’я і розвиток дітей, нечисленні й часто низькоякісні.
Дані, доступні для азатіоприну, циклоспорину та дексаметазону, не вказують на імуносупресію в дітей або не викликають особливого занепокоєння щодо їхнього фізичного або неврологічного розвитку. Навпаки, біологічні препарати зі значним трансплацентарним перенесенням, що створюють високі концентрації в сироватці крові дитини у разі призначення після 30-го тиж вагітності, здатні збільшити ризик післяпологової інфекції. Діти, що піддавалися впливу біологічних препаратів тільки до 22-го тиж вагітності, можуть отримувати щеплення відповідно до стандартних протоколів і календаря вакцинації, в тому числі живими вакцинами.
Діти, що піддавалися впливу біологічних препаратів наприкінці ІІ і в ІІІ триместрах вагітності, можуть бути включені в програми вакцинації, але вони не мусять отримувати живі вакцини в перші 6 міс життя. Вимірювання концентрації біологічного препарату в крові може стати підґрунтям для вирішення, чи використовувати живу вакцину, чи ні.
Сильними сторонами цього аналізу, що став базою для консенсусу EULAR, є: включення великих баз даних, кількісні систематичні огляди й регістри, включення дотепер неопублікованих даних та їх оцінка різними фахівцями. Обмеженнями є велика варіабельність якості клінічних звітів у літературних джерелах і в реєстрах.
У лікарських засобів, що призначаються під час вагітності з різними цілями і за різними показаннями, є безліч побічних ефектів. Нозологічна форма, активність захворювання під час вагітності, інтенсивність системного запалення й залучення різних органів і систем, а також коморбідні стани і супутня лікарська терапія можуть сприяти високій гетерогенності отриманих даних.
У разі використання комбінації імунодепресантів і цитотоксичних препаратів побічні ефекти лікарської терапії вагітності неможливо оцінити окремо для кожного з цих класів медикаментів.
Одночасне використання метотрексату з недавно схваленими біологічними хворобомодифікуючими препаратами протягом І триместру незапланованої вагітності призводило до збільшення частоти самовільного переривання вагітності та вроджених вад розвитку.
У дослідженнях без ретельно підібраних груп контролю, що не піддавалися впливу, важко відокремити побічні ефекти лікарських засобів від інших чинників, зазначених вище.
У більшості досліджень контрольні групи були відсутні, а про частоту вроджених вад розвитку майже завжди судять після народження дитини, без урахування даних про викидні або переривання вагітності. Таким чином, дані про частоту вроджених вад розвитку найкраще брати з досліджень, які включають здорових вагітних жінок, а також із групи порівняння жінок з одним і тим самим захворюванням, які не приймали розглянутий препарат.
У цілому лікування РЗ у жінок під час вагітності та лактації є серйозною проблемою, оскільки необхідно враховувати вплив лікарських засобів на організми матері та дитини.
Рішення з приводу терапії РЗ під час вагітності та годування груддю часто пов’язане з медичними та юридичними проблемами. Загальна обережне ставлення до застосування будь-яких лікарських засобів під час вагітності та лактації призводить до відмови від необхідної терапії, найчастіше при істотному ризику для матері й плода. Тому оновлення знань і поширення нових ідей, що стосуються лікарської терапії РЗ під час вагітності й лактації, мають велике значення для оптимізації рутинної клінічної практики.
Консенсус EULAR, який базується на результатах систематичних кількісних оглядів і доступних реєстрів, є першим кроком у цьому напрямі, подальше поширення нових відомостей серед медичної спільноти має здійснюватися завдяки конгресам, конференціям, семінарам і навчальних курсам.
Поширення інформації має відбуватися за допомогою національних товариств фахівців із ревматології, внутрішньої медицини, гінекології та акушерства, сімейної медицини, педіатрії та фармакології, а також національних інформаційних служб із тератологіі. Розміщення нових відомостей на доступних веб-сайтах зможе залучити більшу аудиторію фахівців різного профілю, яким доводиться мати справу з лікуванням вагітних із РЗ. В ідеалі про нові ідеї слід повідомляти пацієнткам також через національні асоціації хворих.
Оскільки є значний пробіл у доступних друкованих матеріалах і освітніх ресурсах, які могли б задовольнити потребу пацієнток в ознайомленні з новими підходами до лікування РЗ, розробка адаптованих інформаційних матеріалів, заснованих на фактичних даних доказової медицини про використання лікарських засобів в період вагітності й лактації, допоможе жінкам приймати обґрунтовані та виважені рішення.
Підготував Олександр Збрицький
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 2 (56) Квітень 2018 р.


