9 травня, 2018
Недифференцированное заболевание соединительной ткани
Диагностическая неопределенность – нередкое для ревматологии явление. В других областях медицины также встречаются пациенты с клинически необъяснимыми симптомами. Некоторым из этих пациентов в конечном итоге может быть поставлен точный диагноз, у других же заболевания не могут идентифицировать на протяжении многих лет.
 Ярким примером является история Сюзанны Кахалан, журналистки газеты «Нью-Йорк пост». Ее болезнь с самого начала выглядела странно: считалось, что у девушки развивается психическое заболевание. Однако результаты нейропсихологического исследования помогли установить наличие новой формы аутоиммунного энцефалита – анти-NMDA-болезни (антитела IgG к N-метил-D-аспартатному рецептору). Другой пример – пирофосфатная артропатия, которую долгие годы – до открытия Маккарти пирофосфатных кристаллов – называли псевдоподагрой. Рассмотрим с этих позиций следующие вопросы:
Ярким примером является история Сюзанны Кахалан, журналистки газеты «Нью-Йорк пост». Ее болезнь с самого начала выглядела странно: считалось, что у девушки развивается психическое заболевание. Однако результаты нейропсихологического исследования помогли установить наличие новой формы аутоиммунного энцефалита – анти-NMDA-болезни (антитела IgG к N-метил-D-аспартатному рецептору). Другой пример – пирофосфатная артропатия, которую долгие годы – до открытия Маккарти пирофосфатных кристаллов – называли псевдоподагрой. Рассмотрим с этих позиций следующие вопросы:
- Насколько оправдан диагноз «недифференцированное заболевание соединительной ткани (НЗСТ)»?
- Свидетельствует ли он о недостаточной компетенции врача или является вынужденным в условиях недостаточной определенности симптомов?
- Как долго мы можем вести пациента с таким диагнозом? Какова должна быть лечебная тактика?
Около 25% больных с симптомами ЗСТ окончательный диагноз не может быть установлен при первичном обращении. Кроме того, у большинства этих пациентов диагноз не устанавливается в течение 5-10 лет наблюдения [1]. Каковы правильные диагнозы для этих пациентов? Почему это имеет значение?
Установление окончательного диагноза подразумевает определенность или уверенность в патогенезе, прогнозе, терапевтических последствиях и результатах лечения. В случае отсутствия такой уверенности преждевременная интерпретация симптомов в пользу той или иной нозологии может ограничивать клиническое мышление врача и приводить к ошибочной лечебной тактике, нанесению вреда, а иногда и к неблагоприятным юридическим последствиям. В условиях диагностической неопределенности мы выносим этим пациентам диагноз «недифференцированное системное ревматическое заболевание» или НЗСТ. Эксперты Американского колледжа ревматологов (ACR) и Европейской противоревматической лиги (EULAR) советуют: если вы точно не уверены в диагнозе конкретного пациента, вы не должны ставить окончательный диагноз без достаточных для этого оснований [16].
В условиях работы многопрофильной больницы врач-ревматолог почти всегда участвует в консилиумах по разбору тяжелых диагностически неопределенных пациентов. При этом перед ним часто возникает следующий вопрос: «Кому можно ставить диагноз НЗСТ – всем диагностически неясным пациентам или тяжелым пациентам с непонятной сыпью, температурой, повышенной скоростью оседания эритроцитов (СОЭ) или повышенным уровнем С-реактивного белка (СРБ)?».
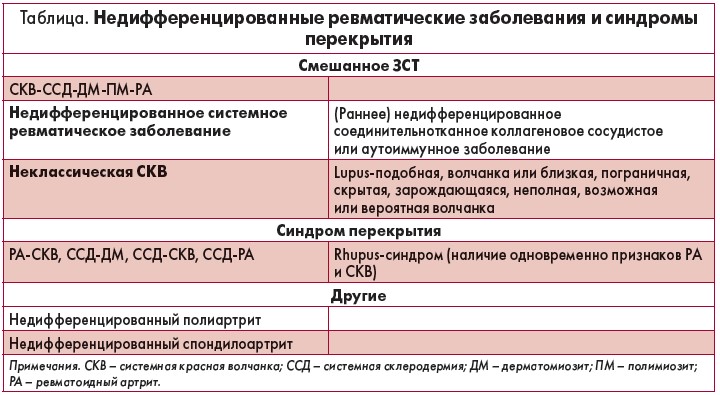
Эксперты ACR и EULAR разработали диагностические критерии, призванные помочь врачам в классификации и диагностике пациентов с ревматическими заболеваниями. Расстройства, обычно считающиеся недифференцированными системными ревматическими заболеваниями и/или синдромами перекрытия, представлены в таблице.
Диагностические критерии ACR/EULAR для НЗСТ:
- Феномен Рейно (ФР).
- Ранний воспалительный полиартрит, который не соответствует критериям ACR для диагностики РА.
- Неспецифическая сыпь, напоминающая кожные поражения, обнаруженные при определенных ревматических заболеваниях.
- Интерстициальное заболевание легких (ИБЛ) и/или неспецифическая интерстициальная пневмония.
- Неспецифические клинические или серологические аномалии, не соответствующие установленным классификационным или диагностическим критериям для конкретного ревматического заболевания.
Феномен Рейно является ранним симптомом системного ЗСТ у 10% больных. Самый простой метод диагностики данного феномена – проведение капилляроскопии ногтей с помощью офтальмоскопа с иммерсионным маслом. У пациентов с ФР необходимо тщательно собирать анамнез, а также проводить целенаправленный осмотр таких больных на выявление других возможных признаков НЗСТ. Кроме того, рекомендуется проводить исследование крови на антинуклеарные антитела (АНА) и криоглобулины [2]. M. Meli и соавт. [3] приводят в своей работе данные, которые показывают частоту развития и перехода ФР в системную патологию соединительной ткани и РА. Так, при обследовании 1024 пациентов с ФР у трети из них была выявлена патологическая картина в виде наличия гигантских капилляров, нерегулярной архитектуры капилляров без каких-либо серологических или клинических признаков ЗСТ, однако через 6,5 года наблюдения у 109 пациентов развилось ЗСТ. Таким образом, ФР является одним из значимых прогностических маркеров развития данного заболевания и его наличие у конкретного пациента требует внимательного динамического наблюдения для отслеживания развития других симптомов.
Полиартрит, или диффузные мигрирующие артралгии, – следующий клинический сценарий развития НЗСТ согласно критериям ACR/EULAR. Для него характерны наличие утренней скованности, ускорение СОЭ, позитивные АНА или ревматоидный фактор и достаточно хороший ответ на противовоспалительную терапию. В этом случае важно как можно раньше выделить из этой группы пациентов с ранним РА, которым могла бы быть назначена терапия базисными противовоспалительными препаратами. Доказано, что необратимые изменения могут произойти в течение первых 6 мес возникновения РА и что существует узкое окно возможностей, позволяющее оптимально применить эффективную базисную терапию. В проспективном исследовании [4] продолжительностью менее 2 лет с участием 346 пациентов с артритом, которые не соответствовали классификационным критериям для любого конкретного типа артрита, было показано, что серологическое тестирование на антитела к циклическому цитруллинированному пептиду (анти-CCP) является ценным при прогнозировании прогрессирования в РА.
Кожные поражения НЗСТ не определены. Интересным фактом является сочетание кожных проявлений при НЗСТ и обнаружение антитиреоидных антител. Явления дерматита более распространены у пациентов с антитиреоидными антителами, чем у пациентов без таких аутоантител. В исследовании [5] с участием 526 пациентов с НЗСТ и антитиреоидными антителами у 47 больных наблюдался дерматит, который проявлялся эритематозными пятнами либо папулами. Кожные поражения чаще всего встречались на нижних конечностях, но наблюдались и на верхних конечностях и спине. При биопсии кожи у 15 из 47 пациентов были выявлены лимфоцитарный дерматит, поверхностные периваскулярные инфильтраты мононуклеарных воспалительных клеток, пятнистый дермальный муцин и лимфоцитарная васкулопатия.
Неспецифическая интерстициальная пневмония – ИБЛ, также известна как идиопатическая интерстициальная пневмония – может возникать в начале или после развития других системных симптомов. Гистологическая картина ИБЛ часто встречается в образцах биопсии легких у пациентов со многими ревматическими и системными заболеваниями, включая СКВ, синдром Шегрена, системный склероз и ДМ [6]. Однако у пациентов с положительными серологическими реакциями, свидетельствующими в пользу системной патологии (антисинтетаза, антитела к Scl‑70, SSA или CCP) был отмечен более благоприятный прогноз и ответ на терапию нестероидными противовоспалительными препаратами, чем для интерстициальной пневмонии, не связанной с ревматическим заболеванием [7]. В связи с этим Европейское респираторное общество / Американское торакальное общество предложили для таких случаев термин «интерстициальная пневмония с аутоиммунными особенностями» [8].
К настоящему времени накоплены достаточно обширные данные в отношении дальнейшего развития и трансформации НСЗТ, в какие заболевания и через какой промежуток времени. В исследовании, которое проводилось в Северной Америке, с участием 143 пациентов, наблюдавшихся на протяжении 10 лет, определенное ревматическое заболевание возникло в 29% случаев (СКВ – у 13% пациентов, системный склероз – у 15%, РА – у 3%, смешанное ЗСТ – у 3%); полная ремиссия развилась у 6% участников [9]. В исследовании венгерских ученых [10] у 665 пациентов в течение 5 лет эволюция до четко определенного аутоиммунного синдрома отмечена у 35% обследуемых (28 случаев СКВ, 26 – смешанного ЗСТ, 19 – ССД, 45 – синдрома Шегрена, 3 – ДМ/ПМ, 87 – РА и 22 – системного васкулита). 65% случаев оставались в категории НЗСТ, полная ремиссия развилась у 12% больных. В другом многоцентровом исследовании оценивалась когорта из 213 пациентов с симптомами НЗСТ на протяжении 1 года, которые затем наблюдались еще в течение 5 лет. Прогрессирование в РА или СКВ составляло 20 и 13% соответственно [11]. Авторы еще одной публикации [12] сообщают о результатах, полученных в исследовании 98 пациентов с НЗСТ, наблюдавшихся в течение 11 лет. Ученые установили, что у 62% больных оставалась НЗСТ, 24% участников вступили в ремиссию, а у 14% – развились определенные ревматические заболевания. Цитопения, наличие титра АНА >1:640, антител к центромеру и аномальная капилляроскопия ногтей были предикторами развития конкретного заболевания.
Таким образом, общий портрет пациента с НЗСТ выглядит следующим образом. Чаще всего это – женщины в возрасте 18-60 лет, с наличием субфебрилитета, кожными изменениями, поражением суставов и мышц в виде артралгий, артрита, миалгий, миозита, ФР, изменениями со стороны легких, анемией (панцитопенией), лимфаденопатией, повышенными СОЭ и СРБ и наличием иммунологических феноменов, которые могут включать АНА, антитела к dsDNA, Sm, RNP, центромеру, Ro/SSA, La/SSB, Jo‑1, Scl‑70 и PM1; ревматоидный фактор; анти-CCP.
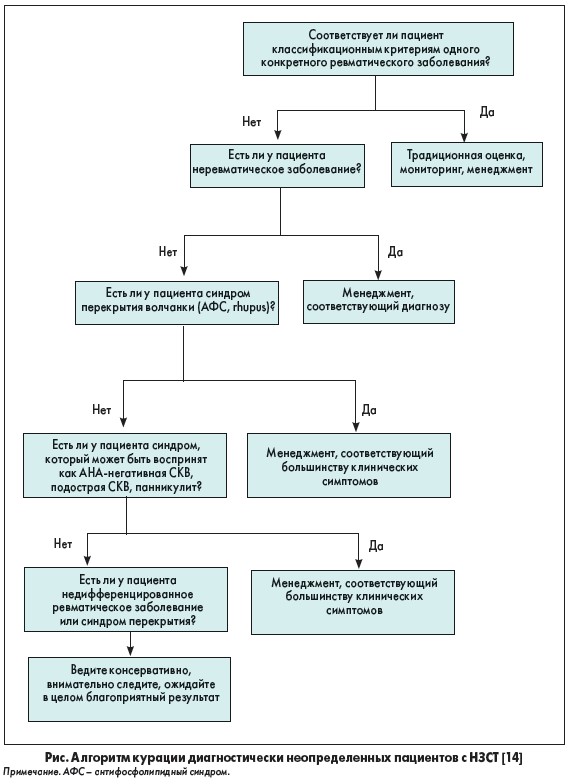 Эксперты сходятся во мнении, что следует избегать диагностических ярлыков, если они не подтверждаются установленными критериями [14]. Клиницисты должны проявлять терпение и выдержку при неопределенности, а также помогать пациентам психологически принимать эту ситуацию. В таких случаях следует занимать выжидательную позицию, осуществляя ведение пациентов в соответствии с основными клиническими синдромами (например, артрит, интерстициальная пневмония, ФР). Вместе с тем следует осуществлять мониторинг клинических симптомов и периодически пересматривать свое видение проблемы. Конкретный диагноз может быть поставлен только когда пациент будет соответствовать классификационным критериям. На рисунке представлен алгоритм курации таких диагностически неопределенных пациентов с НЗСТ [14].
Эксперты сходятся во мнении, что следует избегать диагностических ярлыков, если они не подтверждаются установленными критериями [14]. Клиницисты должны проявлять терпение и выдержку при неопределенности, а также помогать пациентам психологически принимать эту ситуацию. В таких случаях следует занимать выжидательную позицию, осуществляя ведение пациентов в соответствии с основными клиническими синдромами (например, артрит, интерстициальная пневмония, ФР). Вместе с тем следует осуществлять мониторинг клинических симптомов и периодически пересматривать свое видение проблемы. Конкретный диагноз может быть поставлен только когда пациент будет соответствовать классификационным критериям. На рисунке представлен алгоритм курации таких диагностически неопределенных пациентов с НЗСТ [14].
? Каковы же подходы к терапии у пациентов с НЗСТ и значит ли диагностическая неопределенность, что мы можем откладывать начало терапии?
Безусловно, нет. Пациентам следует назначать терапию в соответствии с превалирующими клиническими симптомами. Базовой терапией НЗСТ являются глюкокортикоиды, доза которых зависит от выраженности клинической симптоматики и активности заболевания. В случае наличия кожных и суставных изменений необходимо рассмотреть вопрос о назначении метотрексата в стандартных дозах 15-25 мг в неделю. При наличии ИБЛ принимается решение о назначении циклофосфана или азатиоприна. ФР также требует медикаментозной коррекции согласно действующим стандартам лечения данной патологии. Интересны также данные, полученные при изучении роли витамина D в комплексной терапии НЗСТ за счет его влияния на регуляцию соотношения Treg/Т [15].
В заключение хотелось бы отметить, что в ситуации с курацией пациентов с НЗСТ неопределенность может быть неприятной, но неоправданные действия – действительно опасными. Не следует опасаться термина «недифференцированное заболевание». Этот термин свидетельствует не о врачебной некомпетенции, а об осторожности специалиста, принявшего выжидательную тактику, его информированности о возможном развитии клинических сценариев разными путями. Такой подход способствует исключению врачебных ошибок и выбору оптимального лечения для конкретной ситуации. Такую тактику врача-клинициста лучше всего передают слова Вольтера: «Неопределенность – неудобная позиция. Но определенность – абсурдная».
Литература
1. Cervera R., Khamashta M.A., Hughes G.R. Overlap syndromes. Ann. Rheum. Dis. 1990 Nov; 49 (11): 947-948.
2. Kallenberg C.G. Early detection of connective tissue disease in patients with Raynaud’s phenomenon. Rheum. Dis. Clin. North Am. 1990; 16 (1): 11.
3. Meli M., Gitzelmann G., Koppensteiner R., Amann-Vesti B.R. Predictive value of nailfold capillaroscopy in patients with Raynaud’s phenomenon. Clin. Rheumatol. 2006; 25 (2): 153.
4. van Gaalen F.A., Linn-Rasker S.P., van Venrooij W.J., et al. Autoantibodies to cyclic citrullinated peptides predict progression to rheumatoid arthritis in patients with undifferentiated arthritis: a prospective cohort study. Arthritis. Rheum. 2004; 50 (3): 709.
5. Cheng W., Gilliam A.C., Castrovinci A., et al. Anti-thyroid autoantibody-associated interface dermatitis in individuals with undifferentiated connective tissue disease – an unrecognized subset of autoimmune disease? J. Rheumatol. 2007; 34 (1): 81.
6. de Lauretis A., Veeraraghavan S., Renzoni E. Review series: Aspects of interstitial lung disease: connective tissue disease-associated interstitial lung disease: how does it differ from IPF? How should the clinical approach differ? Chron. Respir. Dis. 2011; 8 (1): 53-82.
7. Fischer A., West S.G., Swigris J.J., et al. Connective tissue disease-associated interstitial lung disease: a call for clarification. Chest, 2010; 138 (2): 251.
8. Fischer A., Antoniou K.M., Brown K.K., et al. «ERS/ATS Task Force on Undifferentiated Forms of CTD-ILD».
9. An official European Respiratory Society / American Thoracic Society research statement: interstitial pneumonia with autoimmune features. Eur. Respir. J. 2015 Oct; 46 (4): 976-87. Epub 2015 Jul 9.
10. Williams H.J., Alarcon G.S., Joks R., et al. Early undifferentiated connective tissue disease (CTD). VI. An inception cohort after 10 years: disease remissions and changes in diagnoses in well established and undifferentiated CTD. J. Rheumatol. 1999; 26 (4): 816.
11. Bodolay E., Csiki Z., Szekanecz Z., et al. Five-year follow-up of 665 Hungarian patients with undifferentiated connective tissue disease (UCTD). Clin. Exp. Rheumatol. 2003; 21 (3): 313.
12. Alarcоn G.S., Willkens R.F., Ward J.R., et al. Early undifferentiated connective tissue disease. IV. Musculoskeletal manifestations in a large cohort of patients with undifferentiated connective tissue diseases compared with cohorts of patients with well-established connective tissue diseases: followup analyses in patients with unexplained polyarthritis and patients with rheumatoid arthritis at baseline. Arthritis. Rheum. 1996; 39 (3): 403.
13. Garcіa-Gonzаlez M., Rodrіguez-Lozano B., Bustabad S., et al. Undifferentiated connective tissue disease: predictors of evolution into definite disease. Clin. Exp. Rheumatol. 2017; 35 (5): 739. Epub 2017 Aug 2.
14. Panush R.S., Greer J.M., Morshedian K.K. What is lupus? What is not lupus? Rheum. Dis. Clin. North Am. 1993; 19 (1): 223.
15. Zold E., Szodoray P., Nakken B., et al. Аlfacalcidol treatment restores derailed immune-regulation in patients with undifferentiated connective tissue disease. Autoimmun. Rev. 2011 Jan; 10 (3): 155-62. Epub 2010 Sep 22.
16. Kelly A., Panush R.S. Diagnostic uncertainty and epistemologic humility. Clin. Rheumatol. 2017; 36 (6): 1211. Epub 2017 Apr 22.
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 2 (56) Квітень 2018 р.