8 жовтня, 2018
Запальні й дегенеративні захворювання скронево-нижньощелепного суглоба
 Донедавна різні пацієнти, звернувшись за медичною допомогою, зазвичай проходили однакові діагностичні процедури й отримували подібне лікування. За цього підходу одному хворому могло пощастити з результатом терапії, натомість іншому – ні. Останні досягнення в розумінні природи хвороб та біології організму людини дозволяють принципово змінити майбутнє медицини.
Донедавна різні пацієнти, звернувшись за медичною допомогою, зазвичай проходили однакові діагностичні процедури й отримували подібне лікування. За цього підходу одному хворому могло пощастити з результатом терапії, натомість іншому – ні. Останні досягнення в розумінні природи хвороб та біології організму людини дозволяють принципово змінити майбутнє медицини.
Нині вважають, що лікування буде підбиратися індивідуально для кожного конкретного пацієнта, ґрунтуючись на його генетичних даних. Наразі проводяться різноманітні дослідження з вивчення індивідуальних особливостей болю з метою надання персоніфікованої терапії. Наприклад, у дослідженні OPPERA (Orofacial Pain: Prospective Evaluation and Risk Assessment) беруть участь пацієнти з дисфункцією скронево-нижньощелепного суглоба (СНЩС), частина з яких страждає від супутніх захворювань, що супроводжуються появою болю (Wilentz J. B. і співавт., 2017).
Невипадково саме ця патологія потрапила в поле зору вчених, адже скронево-нижньощелепні розлади займають особливе місце в клінічній практиці у зв’язку зі складністю клінічної картини, що нерідко нагадує таку при хворобах, які перебувають у межах компетенції лікарів різних спеціальностей: стоматологів, отоларингологів, невропатологів, психіатрів, ревматологів та ін. За даними статистики, захворювання СНЩС на різних стадіях зустрічається у 25-65% населення земної кулі (Wilentz J. B. і співавт., 2017).
Лікувальні процедури та діагностика захворювань СНЩС розроблені як усереднені з позицій так званого шаблонного пацієнта. Перехід до прецизійної (від англ. precise – точна) медицини передбачає залучення спеціалізованої багатопрофільної команди, до складу якої входили б ортопеди, ревматологи, фізіотерапевти, психіатри.
СНЩС – типовий та унікальний
На перший погляд, СНЩС – це простий суглоб, який утворюється двома кістковими поверхнями (голівкою нижньої щелепи, скроневою кісткою), має фіброзну капсулу та суглобовий диск. Останній, як і диски в багатьох інших суглобах, є двошаровою структурою, що складається зі щільної волокнистої сполучної тканини. Диск СНЩС, як і інші його «колеги», згладжує нерівності кісткових поверхонь, що зчленовуються, робить їх конгруентними, амортизує поштовхи і струси під час руху.
Значну роль у гарному функціонуванні будь-якого суглоба відіграє синовіальна рідина. Саме вона забезпечує вільне ковзання суглобових поверхонь, сприяє живленню безсудинних шарів суглобового диска та суглобових поверхонь, а також виведенню чужорідних клітин і речовин, які проникають із крові при ушкодженнях суглобової капсули.
Будова суглобових поверхонь СНЩС також досить типова: вони вкриті сполучнотканинним хрящем, а синовіальна мембрана, яка вистилає порожнину суглоба, контактує із внутрішньосуглобовою рідиною. Живлення хряща СНЩС теж здійснюється згідно з класичними канонами: з капілярів синовіальної оболонки та субхондральної кістки шляхом дифузії до нього з двох боків надходять поживні речовини.
При кожному руховому акті нижньої щелепи хрящова тканина, немов губка, стискається, а при розслабленні – розправляється. Завдяки цим особливостям синовіальна рідина постійно циркулює із суглобової сумки всередину хряща і назад. Хрящ у СНЩС має типові властивості, притаманні хрящовій тканині організму людини; для його адекватного функціонування необхідні такі речовини, як глюкозаміноглікани та хондроїтинсульфат.
При цьому СНЩС має деякі особливості, що виокремлюють його серед усіх інших кісткових зчленувань. СНЩС є одним з найбільш активно працюючих шарнірних суглобів, який забезпечує плавні рухи щелепи вгору-вниз і з боку в бік та надає людині можливість виконувати унікальні функції: розмовляти, співати, їсти, позіхати та ін. Саме цей суглоб працює набагато більше, адже рухи у СНЩС можуть здійснюватися під час функціонального спокою інших суглобів. Таким чином, на СНЩС припадає велике фізичне навантаження, під час якого можуть страждати як його суглобові поверхні, диск, так і хрящова тканина.
Дисфункція СНЩС
Для опису широкого спектра симптомів, які з’являються при порушенні нормальної функції СНЩС, використовують термін «дисфункція», або «порушення». Дисфункція СНЩС може виникати з різних причин. СНЩС уражається при дегенеративних захворюваннях суглобів (остеоартрозі, остеоартриті), системних артритах. Перебіг ревматоїдного або псоріатичного артриту також може супроводжуватись ураженням СНЩС: у 67-71% пацієнтів з ревматоїдним артритом діагностують патологію не лише великих суглобів, а й СНЩС. Також відомі інші захворювання СНЩС: кондилізи, або ідіопатична кондилярна резорбція, остеохондрит та остеонекроз, новоутворення і синовіальний хондроматоз.
Клініка
Клінічно ураження СНЩС незалежно від етіологічних факторів майже завжди маніфестує болем різного ступеня інтенсивності. У разі гострого процесу біль має колючий, ріжучий характер, він перешкоджає відкриванню рота, розмові, унеможливлює прийом їжі. Біль переслідує хворих під час жування, розмови та в спокої. Дуже часто мають місце головній біль і невелике локальне підвищення температури тіла.
Необхідно підкреслити, що в деяких випадках ураження СНЩС може маскуватися під інші захворювання, наприклад мігрень, неврит. При поширенні запального процесу відбувається звуження слухових каналів, що клінічно проявляється зниженням гостроти слуху, оталгією. Також гостра дисфункція СНЩС може маніфестувати міалгією жувальних м’язів, болями в шиї, артралгіями.
За умов тривалого перебігу запального процесу, обмеження кількісного складу ексудату в порожнині СНЩС, можливої появи проліферативних ускладнень внутрішньосуглобові структури починають неадекватно впливати одна на одну. Усі ці зміни спричиняють звуження суглобової щілини, зближення сусідніх кістково-суглобових поверхонь, що призводить до появи специфічного хрускотіння, клацання, яке лякає багатьох пацієнтів.
Крім того, тривала бездіяльність СНЩС через значні больові відчуття зумовлює відповідну реакцію – скутість рухів лицьових м’язів і суглобових ділянок, а також погіршення слухових якостей. Різноманіття клінічної картини спонукає хворих звертатися до лікарів різних спеціальностей, у тому числі до стоматологів й отоларингологів.
Ураження СНЩС при супутніх захворюваннях суглобів
Слід розуміти, що дисфункція СНЩС може виникати при різноманітних супутніх захворюваннях суглобів, наприклад при ревматоїдному артриті. У цих хворих труднощі при відкриванні рота зумовлені не тільки болем, а й фіброзними спайками, м’язовою контрактурою, запаленням, дегенерацією СНЩС.
При ревматоїдному ґенезі ураження СНЩС на рентгенограмах виявлюсь досить типові зміни: кортикальні ерозії, звуження міжсуглобової щілини, анкілоз. Але, за статистичними даними, значуща різниця між утрудненням відкривання рота в пацієнтів з ревматоїдним артритом та в загальній популяції відсутня, тому ця знахідка сама по собі не дає достатніх підстав для остаточного підтвердження ревматоїдного ґенезу ураження.
Дисфункція СНЩС спостерігається в 90% пацієнтів із псоріатичним артритом, а також у 29% у хворих на псоріаз. Доведено, що наявність псоріатичного ураження великих суглобів не асоціюється зі збільшенням ризику дисфункції СНЩС, але при ураженні останнього перебіг захворювання погіршується, клінічні ознаки ураження скронево-нижньощелепної ділянки посилюються.
У деяких випадках може розвиватись однобічне ураження. До клінічних особливостей псоріатичного ураження СНЩС можна віднести наявність крепітації чи інших суглобних звуків, біль при відкриванні рота та жуванні, ранкову скутість; атрофію м’язів. За умови прогресування захворювання біль змінюється обмеженням руху через розвиток фіброзу.
Відносно невелика кількість (приблизно 22%) хворих на анкілозивний спондиліт мають рентгенологічні ознаки ураження СНЩС. При цьому такі пацієнти майже не скаржиться на біль і не мають специфічних симптомів, що виникають при ураженні скронево-нижньощелепної ділянки. Найпоширенішими клінічними ознаками дисфункції СНЩС в осіб з анкілозивним спондилітом є крепітація, атрофія жувальних м’язів, обмеження рухів у суглобах (обмежене відкривання рота).
Відомі випадки виникнення дисфункції СНЩС при системній склеродермії. При прогресуванні захворювання з’являється значне обмеження рухів щелепи, що дуже важко піддається лікуванню. З урахуванням цього в будь-якого пацієнта із системною склеродермією рекомендується регулярно аналізувати стан СНЩС при динамічному рентгенографічному дослідженні з метою підбору ефективного лікування та попередження виникнення ускладнень.
У літературі описано декілька випадків септичного артриту СНЩС без очевидного джерела інфекції. Щоб уникнути серйозних проблем, необхідно враховувати ймовірність розвитку септичного артриту СНЩС у пацієнтів з болем у скронево-нижньощелепній ділянці, тризмом і набряком.
Діагностика
Нині за підозри на дисфункцію СНЩС в діагностичному пошуку використовують різноманітні сучасні інструментальні методи. Ультразвукове дослідження високої якості дозволяє виявити зміни внутрішньо- і навколосуглобових м’яких тканин. У ході артросонографії можна виявити ознаки ексудативного або проліферативного синовіїту суглобів, синовіальні кісти й ерозивні дефекти кісткової і суглобової поверхонь, визначити дегенеративні зміни суглобів і м’яких тканин (остеофіти, бурсит, навколосуглобову осифікацію, ушкодження капсульно-зв’язкового апарату).
Традиційне рентгенологічне дослідження суглобів (панорамна й оглядова рентгенографія, ортопантомографія), яке широко застосовується в повсякденній практиці, також має велике значення. Воно дозволяє отримати певні уявлення про стан кісткових структур, що формують СНЩС, рентгенівської суглобової щілини, внутрішньосуглобових поверхонь. Упровадження комп’ютерної томографії (КТ) дозволило отримати зображення СНЩС у різних площинах та візуалізувати кісткові елементи суглоба більш детальною, але цей метод дослідження не може визначити стан некісткових структур СНЩС.
Повноцінним методом діагностики ушкоджень СНЩС є магнітно-резонансна томографія (МРТ), яка дозволяє констатувати анатомічні зміни м’якотканинних та фіброзних структур. Проведення МРТ СНЩС є запорукою комплексної оцінки стану синовіальної оболонки, суглобового диска, внутрішньосуглобових зв’язок, біламінарної зони та виявлення ексудативно-проліферативних, дегенеративно-дистрофічних і деструктивних змін у хрящових та фіброзних структурах суглоба.
Найперспективнішим у діагностиці функціональних порушень зубощелепного апарату на сьогодні вважається функціональний метод – аксіографія (графічний запис траєкторії руху суглобової головки та диска СНЩС при різноманітних рухах нижньої щелепи), що дозволяє провести поглиблений аналіз клінічної ситуації.
Використовуючи спеціальне програмне забезпечення, можна додатково обстежити особливості рухів нижньої щелепи для визначення можливих функціональних порушень. Результати аналізу подають у вигляді проекції траєкторії руху нижньої щелепи на три взаємно перпендикулярні площини.
Одночасно особливості руху кондиляра при переміщенні щелепи вздовж горизонтальної осі (право-ліво) подаються у вигляді зміни просторового положення кінематичної осі. Ці дані дають змогу не тільки виявити наявні функціональні порушення (обмеженість, дискоординація рухів, надлишкова рухомість щелепи), а й визначити причини їх виникнення (артрогенні, міогенні чи оклюзійні дефекти).
Лікування
Метою лікування дисфункції СНЩС може бути досягнення знеболення, припинення патологічних структурних змін, відновлення/покращення функції суглоба та відтермінування проведення артропластики. На сьогодні вважається, що порушення оклюзії є важливим і провідним етіологічним чинником у розвитку суглобових дисфункцій. Відтак, завжди пропонується нормалізувати оклюзію, наразі це ключовий момент у комплексному лікуванні дисфункції СНЩС та подальшому адекватному протезуванні.
Проте кілька тривалих досліджень виявили слабкий зв’язок між порушеннями оклюзії та дисфункціями СНЩС. Автори цих досліджень вважають, що власне дисфункції як первинний чинник можуть зумовлювати різноманітні порушення оклюзійних взаємовідносин зубів, тому саме комплексний підхід є запорукою успішного лікування.
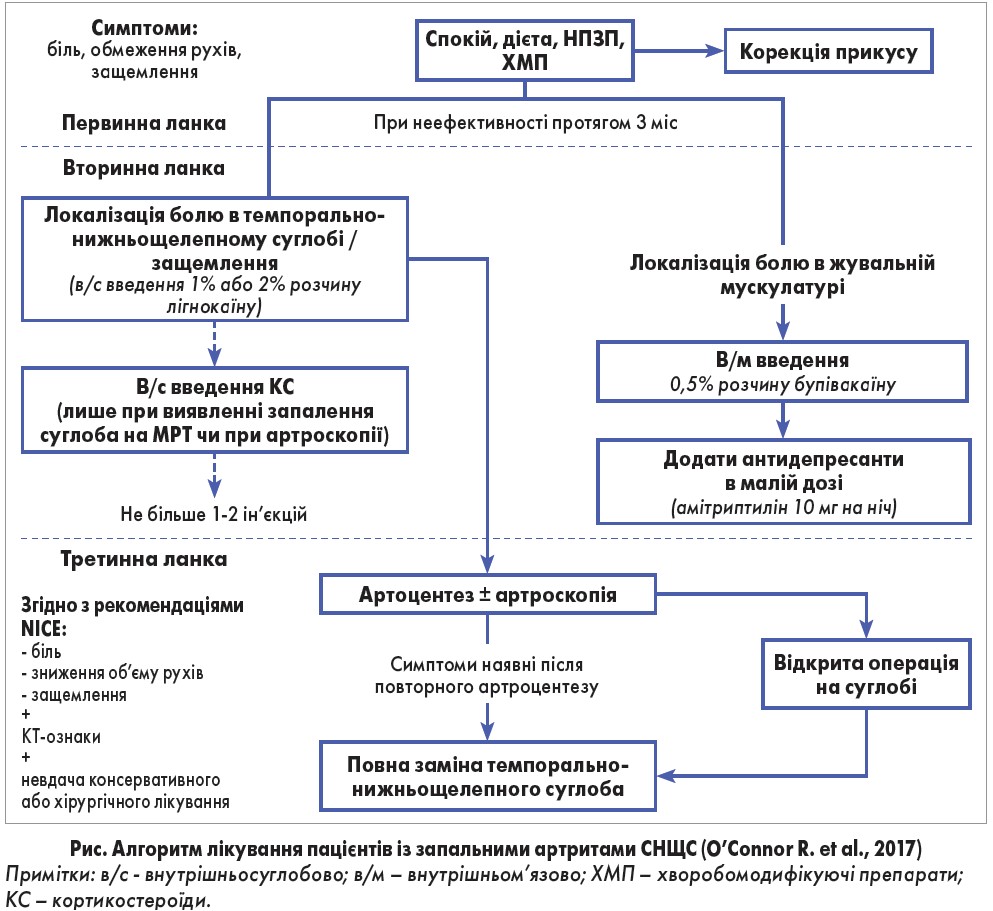 Слід зауважити, що за невизначеної етіології ураження СНЩС терапія переважно носить симптоматичний характер, що в більшості випадків може призвести до прогресування захворювання. Зменшити темпи запального ураження СНЩС при ревматоїдному чи псоріатичному ґенезі захворювання можна шляхом призначення метотрексату, імунобіологічної терапії; при остеоартриті доцільно використовувати хворобомодифікуючі препарати (ХМП). Нещодавно R. O’Connor і співавт. (2017) запропонували алгоритм лікування пацієнтів із запальними ураженнями СНЩС, що передбачає декілька етапів (рис.).
Слід зауважити, що за невизначеної етіології ураження СНЩС терапія переважно носить симптоматичний характер, що в більшості випадків може призвести до прогресування захворювання. Зменшити темпи запального ураження СНЩС при ревматоїдному чи псоріатичному ґенезі захворювання можна шляхом призначення метотрексату, імунобіологічної терапії; при остеоартриті доцільно використовувати хворобомодифікуючі препарати (ХМП). Нещодавно R. O’Connor і співавт. (2017) запропонували алгоритм лікування пацієнтів із запальними ураженнями СНЩС, що передбачає декілька етапів (рис.).
Відповідно до цього алгоритму на першому етапі надання допомоги пацієнтам із дисфункцією СНЩС призначають
нестероїдні протизапальні препарати (НПЗП), які мають переваги щодо усунення запалення. Однак є потреба в проведенні подальших досліджень щодо вивчення безпеки тривалого використання НПЗП та їх переваг у контролі болю, запалення, а також порівняльної оцінки профілю ефективності та можливих негативних побічних дій.
Внутрішньосуглобове введення кортикостероїдів (КС) є мінімально інвазивною терапією. У пацієнтів з ревматоїдним артритом СНЩС така терапія має наслідком зменшення болю в 75,6% випадків у порівнянні з використанням гіалуронової кислоти (19,6%) та плацебо (17,8%). Утім, застосування КС можливе тільки при виявленні ознак запалення під час МРТ або артроскопії; крім цього, максимальна кількість зазначених втручань становить лише 1-2 ін’єкції. Необхідно акцентувати, що ні НПЗП, ні КС не забезпечують повного відновлення суглоба / суглобових поверхонь.
Автори наведеного алгоритму підкреслюють, що перша лінія терапії остеоартриту СНЩС має бути неінвазивною та передбачати застосування ХМП – глюкозаміну та хондроїтину, а ін’єкції гіалуронової кислоти слід зарезервувати для пацієнтів, які не користуються консервативними методами, а процедуру артропластики (заміну диска та суглобів) призначати лише тоді, коли консервативні заходи є неефективними.
.Переконливо доведено, що неінвазивне консервативне лікування є досить ефективним і має бути наріжним каменем ведення пацієнтів з остеоартритом СНЩС. Цей підхід передбачає призначення хондропротекторів – глюкозаміну та хондроїтину. Встановлена хондропротекторна дія комбінованого прийому хондроїтинсульфату та глюкозаміну, що асоціюється зі зниженням рівнів запальних медіаторів (інтерлейкіну‑1 та фактора некрозу пухлини) у сироватці крові, а також зі зменшенням концентрації біомаркерів запалення хряща (матриксної металопротеїнази‑3, С-телопептидного типу колагену ІІ типу і RANKL κB / остеопротегеріну).
Показано, що терапія хондроїтинсульфатом і глюкозаміном сприяє покращенню мікроархітектоніки кістки. Хондроїтинсульфат та глюкозамін можуть бути корисними при необхідності контролю катаболічних ефектів запального стресу. Комбінований прийом хондроїтинсульфату та глюкозаміну забезпечує симптоммодифікуючий та структурно-модифікуючий ефекти; поєднане призначення цих компонентів характеризується високим рівнем безпеки.
В одному дослідженні (Haghighat A. et al., 2013) встановлено, що в пацієнтів з дегенеративними порушеннями СНЩС за рівнем ефективності та безпеки глюкозамін перевершує такий НПЗП, як ібупрофен). Глюкозамін як хондропротектор гальмує катаболічні механізми дегенеративних процесів у суглобах. Крім того, вважається, що глюкозаміну сульфат може пригнічувати прозапальні цитокіни.
Дослідження A. Haghighat і співавт. показало, що в порівнянні із загальновизнаним НПЗП ібупрофеном глюкозаміну сульфат може бути використаний як більш ефективний та безпечний терапевтичний засіб для лікування пацієнтів із дегенеративними порушеннями СНЩС.
Метааналіз отриманих даних дозволив зробити висновок, що глюкозамін і хондроїтинсульфат можуть зменшити сумарне проміжне звуження суглобової щілини після 2-3 років безперервного застосування. Нині майже в усіх настановах містяться рекомендації щодо застосування ХМП з метою запобігання розвитку та прогресуванню денегенеративних змін у хрящі.
Підкреслюється також доцільність призначення тривалих курсів лікування хондропротекторами. Наприклад, доцільно розпочинати лікування з прийому комплексу Терафлекс Адванс (компанія Bayer, Німеччина), що містить хондроїтинсульфат, глюкозамін та ібупрофен, в режимі по 2 капсули тричі на добу, поки є гострий біль. Далі слід приймати Терафлекс, до складу якого входять хондроїтинсульфат та глюкозамін, по 3 капсули на добу. Загальна тривалість терапії Терафлексом має становити 3-6 місяців і більше. Таким чином, саме хондроїтинсульфат і глюкозамін (Терафлекс) можуть сприяти відновленню структури хряща, зменшенню болю та поліпшенню функції при дисфункції СНЩС, спричиненій остеоартрозом.
Медична газета «Здоров’я України 21 сторіччя» № 17 (438), вересень 2018 р.


