29 грудня, 2018
Поддерживающая терапия вортиоксетином в течение года при большом депрессивном расстройстве: эффективность и переносимость по данным анализа пяти исследований
Несмотря на успехи психофармакологии второй половины ХХ века, результаты и сроки лечения большого депрессивного расстройства (БДР) не всегда удовлетворяют пациентов и клиницистов. Поэтому продолжаются разработка и клинические исследования перспективных антидепрессантов. Вортиоксетин стал одним из ярких представителей последнего поколения препаратов мультимодального действия. Метаанализ результатов рандомизированных контролируемых исследований кратковременной терапии при БДР подтвердил краткосрочную и противорецидивную эффективность вортиоксетина (M.E. Thase et al., 2016). Логическим продолжением стали долгосрочные исследования поддерживающей терапии. В 2017 г. в журнале Европейской коллегии нейропсихофармакологов были опубликованы результаты апостериорного анализа данных пяти открытых исследований длительной (до 52 нед) терапии БДР (E. Vieta, H. Loft, I. Florea. European Neuropsychopharmacol. 2017; 27: 877-884), проливающие свет на важные аспекты эффективности и безопасности поддерживающей терапии вортиоксетином.
По данным Всемирной организации здравоохранения (2014), БДР поражает 350 млн жителей планеты. Данное психическое расстройство ассоциируется со значительными социальными и экономическими потерями (W.W. Ishak et al., 2014; J.-P. Lepine & M. Briley, 2011). Согласно результатам исследования глобального бремени заболеваний 2013 года, БДР уступило первенство лишь боли в спине по количеству лет, прожитых с инвалидностью, во всем мире (Global Burden of Disease Study Collaborators, 2015). У каждого четвертого человека, восстановившегося после большого депрессивного эпизода (БДЭ), в течение первого года происходит рецидив (D.A. Solomon et al., 2000). Его вероятность пропорциональна количеству предыдущих эпизодов депрессии, выраженности симптомов и длительности текущего БДЭ. Для предотвращения рецидива лицам с БДР, которые ответили на начальную терапию, необходима длительная терапия (как минимум в течение 6-9 мес). Более длительное профилактическое лечение рекомендуется пациентам с высоким риском развития рецидива, хотя доказательная база в поддержку длительности терапии более 9 мес ограничена (M. Bauer et al., 2015).
Вортиоксетин – антидепрессант мультимодального действия, одобренный в 2013 г. в США и Европейском Союзе, а впоследствии также и в других странах для лечения взрослых с БДР. Механизм действия вортиоксетина сочетает два фармакологических эффекта: прямую модуляцию активности рецепторов и ингибирование транспортера серотонина (5-HT). В дополнение к ингибированию транспортера 5-HT вортиоксетин является антагонистом рецепторов 5-HT3, 5-HT7 и 5-HT1D, частичным агонистом рецепторов 5-HT1B, а также агонистом рецепторов 5-HT1A (B. Bang-Andersen et al., 2011; A. Mork et al., 2012; L. Westrich et al., 2012).
Вортиоксетин эффективен при кратковременной терапии БДР в диапазоне доз 5-20 мг/сут (M. Thase et al., 2016). Также вортиоксетин продемонстрировал способность эффективно предотвращать рецидивы. В исследовании профилактики рецидива наблюдались статистически значимые преимущества вортиоксетина по сравнению с плацебо в отношении времени до рецидивирования БДР в течение первых 24 нед двойного слепого периода; доля пациентов группы вортиоксетина, у которых произошел рецидив, была достоверно меньше (отношение рисков 2,01; р=0,0035), что означает снижение риска в 2 раза на фоне приема вортиоксетина по сравнению с плацебо (J.P. Boulenger et al., 2012).
В ходе объединенного анализа безопасности и переносимости вортиоксетина при краткосрочной терапии было обнаружено, что побочные эффекты, которые обычно испытывают пациенты при приеме большинства антидепрессантов (такие как головная боль, сухость во рту, головокружение, запор, инсомния и дневная сонливость, истощение сил, потливость), при приеме вортиоксетина наблюдались с такой же частотой, как в группе плацебо (D.S. Baldwin et al., 2016). Побочными эффектами, возникающими у ≥5% пациентов с частотой в 2 раза выше, чем в группах плацебо, были тошнота и рвота. Низкая частота потенциально клинически значимых изменений массы тела (увеличение или уменьшение) и сексуальной дисфункции, возникавших менее чем у 2% участников любой из групп вортиоксетина, подчеркивает благоприятный профиль безопасности терапии. Анализ безопасности позволил вычислить индекс потенциального вреда при лечении вортиоксетином – среднее число пациентов, которым следует назначить препарат, чтобы у одного дополнительного больного развился неблагоприятный исход: от 24 (при дозе 15 мг/сут) до 126 (при дозе 5 мг/сут).
Результаты пяти открытых исследований, в рамках которых терапия была продлена до 52 нед (M.Y. Alam et al., 2014; D.S. Baldwin et al., 2012; G. Filippov & P. Christen, 2013; I. Florea et al., 2012; P.L. Jacobsen et al., 2014), подтвердили удержание эффекта, достигнутого во время краткосрочной терапии. В отдельных исследованиях было обнаружено, что у пациентов, завершивших 6-8-недельный курс терапии вортиоксетином, продолжалось улучшение симптомов депрессии и тревоги при продленном приеме вортиоксетина, независимо от предыдущей терапии. Уровни терапевтического ответа и достижения ремиссии также существенно повысились в ходе исследований с продлением терапии до 52 нед.
С целью более детального изучения эффективности, безопасности и переносимости вортиоксетина у пациентов, длительно получавших терапевтические дозы препарата (5-20 мг/сут), были проанализированы данные пяти вышеупомянутых долгосрочных открытых исследований (E. Vieta, H. Loft, I. Florea, 2017). Анализ был спланирован с целью оценить, продолжалось ли улучшение симптомов депрессии и тревоги после краткосрочной (от 6 до 8 нед) терапии вортиоксетином в терапевтических дозах 5-20 мг/сут и влияют ли на эффективность долгосрочной терапии такие факторы риска, как тяжесть симптомов, длительность текущего БДЭ или количество перенесенных БДЭ.
Материалы и методы
Были проанализированы данные пяти долгосрочных открытых исследований продления терапии с гибким дозированием вортиоксетина, в которые включали пациентов 18-75 лет с БДР, завершивших участие в одном из восьми краткосрочных стартовых исследований (M.Y. Alam et al., 2014; D.S. Baldwin et al., 2012; G. Filippov & P. Christens, 2013; I. Florea et al., 2012; P.L. Jacobsen et al., 2014). Семь стартовых исследований имели длительность 8 нед, а в одном исследовании (NCT00761306) продолжительность терапии составляла 6 нед. Исследования проводились в Азии, Австралии, Европе, Северной Америке (США и Канада) и Южной Африке.
Протокол продленных исследований предусматривал обследования пациентов на 1-й, 2-й и 4-й неделях, затем каждые 4 нед до 28-й недели, а в дальнейшем – каждые 8 нед до 52-й недели. Наблюдение для оценки безопасности продолжалось 4 нед после завершения продленных исследований или после преждевременной отмены препарата. В данном анализе исходная точка I определяется как начало активной терапии в стартовых исследованиях, а исходная точка II – как начало активного лечения в продленных исследованиях.
Безопасность и переносимость оценивали по частоте, характеру и тяжести побочных эффектов, которые возникали после исходной точки II и в течение 30 дней после получения последней дозы исследуемого препарата. Во время каждого визита исследователь задавал пациенту вопрос о любых возникавших явлениях. Пациенты также могли сообщать о них в другое время в ходе исследования. Побочные эффекты, которые продолжались после завершения стартовых исследований и наблюдались на момент подписания информированного согласия в исходной точке ІІ, расценивались как сопутствующие медицинские состояния и в дальнейшем регистрировались как новые побочные явления, если они ухудшались или осложнялись.
Долгосрочную эффективность вортиоксетина оценивали по средним общим баллам рейтинговой шкалы депрессии Монтгомери – Асберг (MADRS), рейтинговой шкалы тревоги Гамильтона (HAM-A) и шкалы общего клинического впечатления о тяжести заболевания (CGI-S), которые подсчитывали в исходных точках І и ІІ, а также по окончании продленных исследований. Ремиссия определялась как общий балл по MADRS ≤10, а терапевтический ответ – как улучшение общего балла по MADRS на ≥50% от исходной точки І к окончанию поддерживающей терапии.
Подгрупповые анализы для сравнения общих оценок по MADRS проводились в следующих категориях:
- по полу (женщины по сравнению с мужчинами);
- по возрасту (<55 по сравнению с ≥55 лет);
- по тяжести симптомов тревоги в исходной точке І (общий балл по HAM-A <20 по сравнению с ≥20);
- по тяжести симптомов депрессии в исходной точке І (общий балл по MADRS <30 по сравнению с ≥30);
- по статусу терапевтического ответа после острой фазы терапии (<50% по сравнению с улучшением на ≥50% общих оценок по MADRS от исходной точки І к окончанию стартового исследования);
- по длительности текущего БДЭ к моменту исходной точки І (<6 по сравнению с ≥6 мес), а также по количеству перенесенных БДЭ к моменту исходной точки І (<3 по сравнению с ≥3).
В анализы включали всех пациентов, которые приняли хотя бы одну дозу вортиоксетина в ходе исследования продленной терапии после завершения участия в стартовом исследовании и для которых была доступна хотя бы одна валидная оценка общего балла по шкале MADRS после исходной точки ІІ. Описательная статистика представлена для оценок по MADRS, HAM-A и CGI-S, для терапевтического ответа и ремиссии по критериям MADRS, а также для безопасности и переносимости. Актуальные средние значения для всех непрерывных переменных в конце 52-й недели лечения получены посредством методов анализа наблюдавшихся случаев и переноса данных последнего наблюдения вперед (LOCF). В данном апостериорном анализе обобщенные данные анализировали как общую группу вортиоксетина без разделения по дозам, поскольку дизайн исследований предусматривал гибкое дозирование.
Результаты
После исключения из 2592 пациентов (общее число в пяти исследованиях продленной терапии) тех, кто ранее принимал плацебо (n=700), дулоксетин (n=326), венлафаксин (n=24) или вортиоксетин в субтерапевтических дозах (1 и 2,5 мг/сут; n=311), остался 1231 пациент, ранее принимавший вортиоксетин в дозе 5-20 мг/сут. Это соответствует 888,8 пациенто-года терапии вортиоксетином с медианой длительности 51,7 нед. Из 1231 включенного пациента 1230 были включены в анализы эффективности, 706 (57%) завершили 52-недельный протокол исследований продленной терапии, 525 (43%) выбыли досрочно.
Безопасность и переносимость. Из 1230 пациентов, включенных в данный анализ, 96 выбыли из-за побочных эффектов в ходе 52-недельных исследований продленной терапии. Побочными эффектами, связанными с лечением, которые наиболее часто приводили к ее отмене, были тошнота (n=18; 1,5%) и рвота (n=9; 0,7%). Частота выбывания в связи с побочными эффектами была дозозависимой: 0,9% пациентов, принимавших вортиоксетин в дозе 5-10 мг/сут, и 2,0% участников группы с дозировкой 15-20 мг/сут прекратили лечение в связи с тошнотой; 0,3 и 1,1% пациентов соответственно прекратили лечение из-за рвоты. Всего 204 (16,6%) пациента жаловались на тошноту в ходе исследований продленной терапии; ее встречаемость составила 13,3% в группе с дозировкой 5-10 мг/сут и 24,2% в группе с дозировкой 15-20 мг/сут. В большинстве (96%) случаев тошнота была легкой или умеренной степени тяжести. Из 204 пациентов, которые испытывали тошноту в ходе исследований продленной терапии, 96 также жаловались на нее во время участия в стартовых исследованиях; у большинства из них (79%) тяжесть тошноты была такой же или меньшей, чем в стартовых исследованиях.
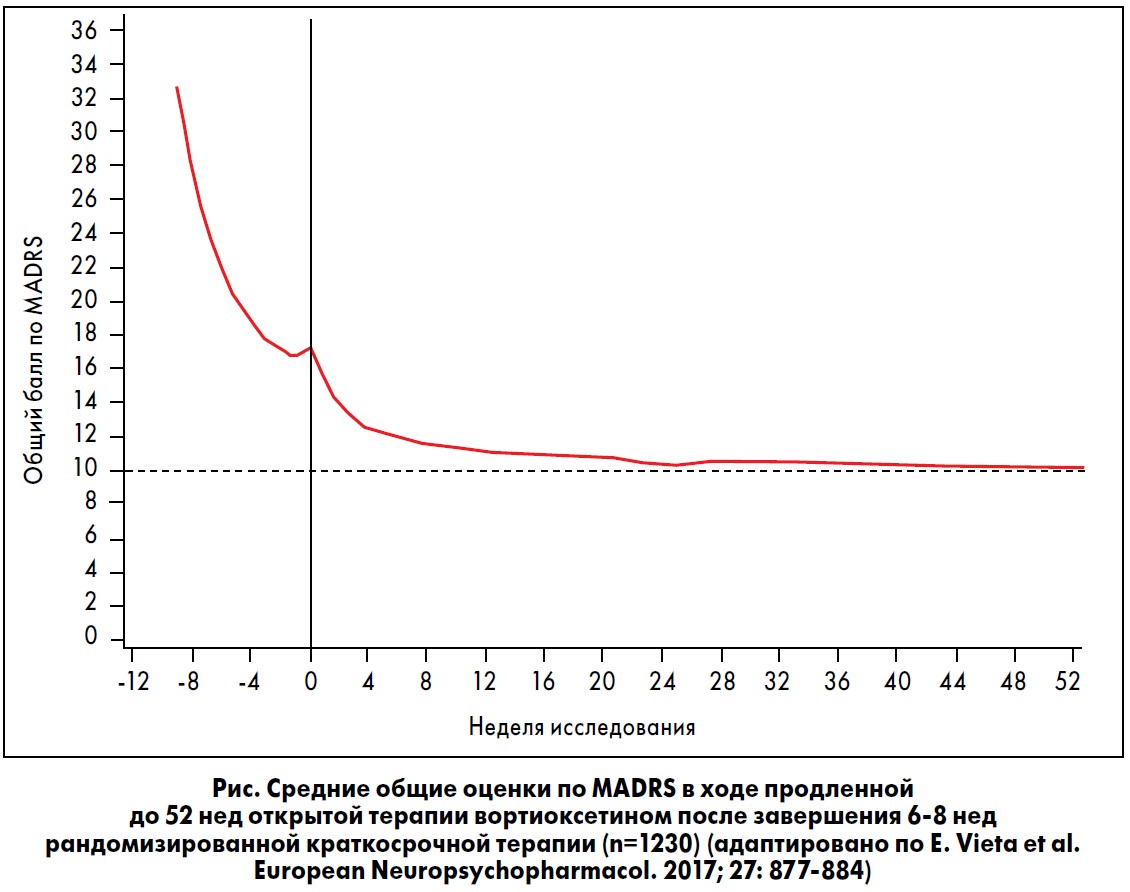
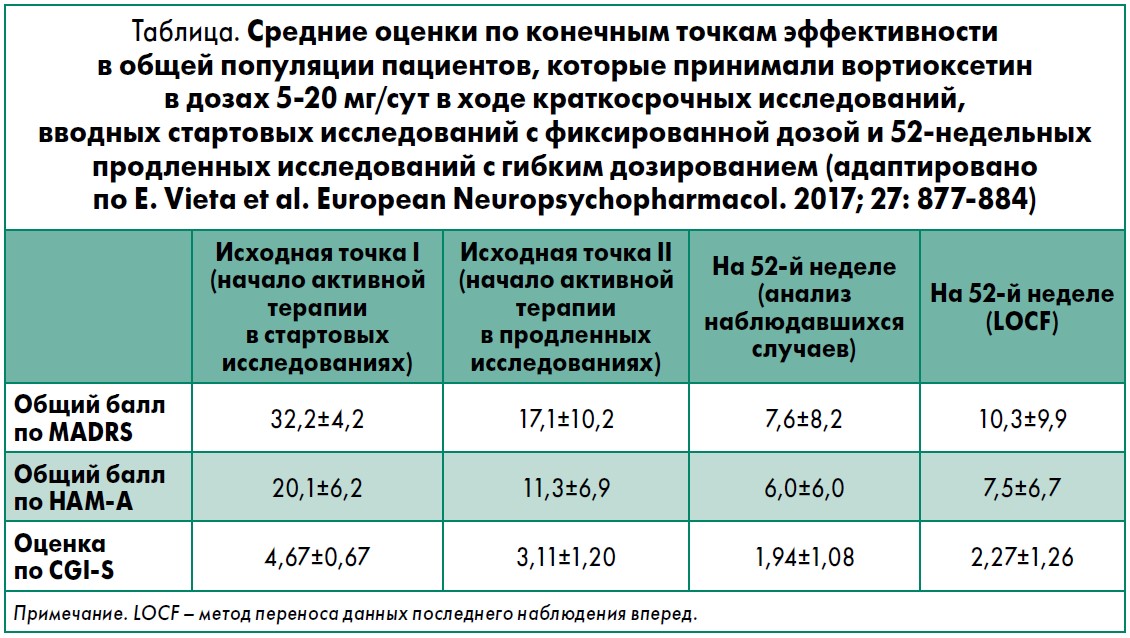
Эффективность. Поддерживающая терапия вортиоксетином ассоциировалась с продолжающимся улучшением симптомов депрессии в соответствии с общими оценками по шкале MADRS (рис., табл.). Наиболее выраженное улучшение наблюдалось в первые 4 нед исследований продленной терапии. Симптомы тревоги, оцениваемые по шкале HAM-A, и общее клиническое впечатление о тяжести заболевания, оцениваемое по CGI-S, также улучшились в результате длительной поддерживающей терапии (табл.).
Доля пациентов, которые ответили на терапию по критериям шкалы MADRS, выросла с 47,8% (588/1230) в исходной точке II до 85,8% (606/706) на 52-й неделе (по данным анализа наблюдавшихся случаев). Всего 310 пациентов, ответивших на терапию, выбыли досрочно из исследований продленной терапии; таким образом, уровень терапевтического ответа составил 75,4% (n=916/1215 по данным анализа LOCF). Процент пациентов, которые достигли ремиссии, вырос с 29,6% (364/1230) в исходной точке II до 71,7% (506/706) на 52-й неделе (по данным анализа наблюдавшихся случаев). За вычетом 232 пациентов, которые вошли в ремиссию, но досрочно выбыли из исследования, уровень достижения ремиссии составил 60,7% (n=738/1215 по данным анализа LOCF). Из 364 пациентов, которые находились в ремиссии в исходной точке II, 66 (18,1%) утратили ремиссию (общая оценка по MADRS >15), а у 29 (8,0%) был зафиксирован рецидив (общая оценка по MADRS ≥22) в ходе долгосрочной терапии.
Во всех выделенных подгруппах наблюдалось продолжающееся улучшение симптомов депрессии в соответствии с общими оценками по шкале MADRS в ходе поддерживающей терапии вортиоксетином в дозах 5-20 мг/сут. Ни пол, ни возраст не влияли на клинические исходы; не отмечено различий между средними общими оценками по MADRS у мужчин (n=384) и женщин (n=846) ни в одной из точек в ходе длительной терапии вортиоксетином (по данным LOCF), как и у пациентов моложе 55 лет (n=948) и ≥55 лет (n=282) (по данным LOCF).
Средние общие оценки по MADRS на 52-й неделе были схожими в подгруппах пациентов, которые в исходной точке I имели оценки по HAM-A <20 (n=613) или ≥20 (n=617). У пациентов со средним общим баллом по HAM-A <20 в исходной точке I средняя общая оценка по MADRS улучшилась на 6,8 балла за 52 нед участия в исследовании продленной терапии (по данным анализа LOCF). У пациентов со средним общим баллом по HAM-A ≥20 в исходной точке I было достигнуто улучшение на 7,0 балла по MADRS в результате длительной терапии вортиоксетином.
У пациентов, у которых в исходной точке I отмечалась умеренная депрессия (средний общий балл по MADRS <30, n=353), средний общий балл по MADRS улучшился на 5,4 в результате длительной терапии вортиоксетином. У пациентов с исходно тяжелой депрессией (средний общий балл по MADRS ≥30, n=877) средний общий балл по MADRS в результате продленной терапии улучшился на 7,4 (по данным анализа LOCF).
Продленная терапия вортиоксетином поддерживала результаты, достигнутые в острую фазу терапии, у пациентов, ответивших на лечение (n=643): средний общий балл по MADRS улучшился на 3,3. Улучшение было более выраженным у больных, которые не ответили на краткосрочную терапию вортиоксетином (n=606). В этой подгруппе средний общий балл по MADRS улучшился на 10,5 (по данным анализа LOCF).
Вортиоксетин улучшал симптомы депрессии в ходе длительной терапии независимо от длительности текущего БДЭ на момент исходной точки I или количества перенесенных ранее БДЭ. На 52-й неделе средняя общая оценка по MADRS у пациентов, у которых текущий БДЭ длился <6 мес (n=660), улучшилась на 6,3 балла, а у больных с длительностью текущего БДЭ ≥6 мес (n=568) – на 7,6 балла (по данным анализа LOCF). Не наблюдалось различий между пациентами, которые перенесли <3 БДЭ (n=722) и ≥3 БДЭ (n=508): улучшение по MADRS в ходе длительной терапии вортиоксетином составило 7,1 и 6,5 балла соответственно (по данным анализа LOCF).
Обсуждение
Анализируя результаты, авторы исследования ставят на первое место данные о переносимости вортиоксетина, так как переносимость важна для поддержания приверженности пациентов к длительному лечению антидепрессантами. Данные этого апостериорного анализа долгосрочной терапии в отношении переносимости вортиоксетина авторы сопоставляют с ранее опубликованными данными D.S. Baldwin и соавт. (2016). Они обращают внимание на то, что в предыдущем анализе популяция больных была более разнородной: в него включали и тех пациентов, которых переводили на вортиоксетин для участия в исследованиях продленной терапии после того, как они принимали плацебо, дулоксетин или венлафаксин в рамках исследований краткосрочного лечения. Интересно отметить, что частота некоторых побочных эффектов, связанных с терапией, встречавшихся в ≥5% случаев у участников краткосрочных исследований (таких как сухость во рту, головокружение и инсомния), не достигла 5% порога в ходе 52-недельных исследований, хотя частота этих побочных эффектов в стартовых исследованиях была сопоставима с уровнем в группах плацебо (D.S. Baldwin et al., 2016).
В данном анализе частота случаев тошноты была дозозависимой, но этот побочный эффект редко приводил к преждевременной отмене в ходе поддерживающего лечения. В работе D.S. Baldwin и соавт. дополнительно анализировались долгосрочные данные о безопасности без учета данных за первые 8 нед открытых исследований. В результате этого анализа не было обнаружено каких-либо новых побочных эффектов за период продленной терапии вортиоксетином по сравнению с краткосрочной терапией. Кроме того, анализ показал, что побочные эффекты возникали менее чем у 10% пациентов после исключения данных о первых 8 нед и что большинство побочных эффектов, возникавших в ходе продленной терапии, были транзиторными (D.S. Baldwin et al., 2016).
Частота отмены препарата из-за любых побочных эффектов в ходе продленной терапии была низкой (7,8%), случаев сексуальной дисфункции не наблюдалось. Общая частота прекращения лечения (43%) не была неожиданной для открытого испытания продолжительностью 1 год. Для сравнения: по данным исследований сопоставимой длительности, уровни отмены составляли 26% для эсциталопрама (A. Wade et al., 2006), 59% для вилазодона (D.S. Robinson et al., 2011) и 59% для дулоксетина (D.L. Dunner et al., 2008). В целом результаты анализа E. Vieta и соавт. подтвердили хорошую долгосрочную переносимость вортиоксетина.
Данный апостериорный анализ также обнаружил, что продолжение лечения вортиоксетином способствует поддержанию результата, достигнутого во время краткосрочной терапии, или обеспечивает дальнейшее улучшение симптомов депрессии и тревоги. Средние общие оценки по MADRS, HAM-A и CGI-S улучшились за 52 нед терапии вортиоксетином в дозах 5-20 мг/сут в общей популяции исследования, причем возраст и пол не влияли на эффективность. Более того, участники с высоким риском рецидива (оценка по MADRS >30, по HAM-A ≥20, длительность текущего БДЭ ≥6 мес в исходной точке I и/или ≥3 перенесенных БДЭ в анамнезе) отвечали на поддерживающее лечение вортиоксетином так же хорошо, как и пациенты с низким риском. Улучшение по выбранным критериям отмечалось как у пациентов, ответивших на краткосрочную терапию вортиоксетином (по шкале MADRS), так и у не достигших лечебного эффекта. Доля больных, у которых была достигнута ремиссия или ответивших на лечение, также увеличилась в ходе долгосрочной терапии вортиоксетином. Среди пациентов, которые вошли в ремиссию при краткосрочной терапии, только у 8% произошел рецидив в ходе поддерживающей фазы лечения. По данным 24-недельного исследования профилактики рецидивирования, среди больных, которые вошли в ремиссию в фазе краткосрочной терапии (n=396), рецидив наступил у 13% рандомизированных к продолжению приема вортиоксетина (5 или 10 мг/сут) и у 26% рандомизированных к приему плацебо (J.P. Boulenger et al., 2012).
Важным отличием работы E. Vieta и соавт. от упомянутого исследования профилактики рецидивирования было то, что в данном анализе дозу вортиоксетина разрешалось повышать до 20 мг/сут, тогда как в исследовании J.P. Boulenger и соавт. максимальная доза составляла 10 мг/сут. Это указывает на то, что и в поддерживающую фазу после достижения ремиссии может понадобиться коррекция дозы. В целом анализ эффективности показал, что длительная терапия БДР вортиоксетином приносит пользу пациентам, которые начали принимать этот препарат в краткосрочной фазе лечения.
Выводы
Ценность данного апостериорного анализа заключается в получении данных о профиле ответа на вортиоксетин в терапевтических дозах у пациентов с БДР, которых продолжали лечить до 60 нед. Показано, что длительная терапия вортиоксетином в дозах до 20 мг/сут способствует поддержанию результата, достигнутого в фазу краткосрочного лечения, и приводит к дальнейшему его улучшению. Этот эффект стабилен и не зависит от пола, возраста, исходной тяжести симптомов депрессии и тревоги, числа ранее перенесенных БДЭ или длительности текущего эпизода. Кроме того, пациенты хорошо переносили длительную терапию вортиоксетином.
По материалам Vieta E., Loft H., Florea I.
Effectiveness of long-term vortioxetine treatment of patients with major depressive disorder. European Neuropsychopharmacol. 2017;
27: 877-884.
Подготовил Дмитрий Молчанов