29 грудня, 2018
Нейропротекторная терапия острых неврологических состояний: «интуитивный» метод лечения или научно обоснованный подход?
В последние годы нейропротекторная терапия все шире применяется не только в лечении хронических заболеваний нервной системы, но и при острых состояниях, что обусловлено получением многочисленных доказательств о целесообразности такого подхода.
Мы попросили одних из ведущих украинских специалистов прокомментировать возможности применения нейропротекторной терапии при инсультах и черепно-мозговых травмах (ЧМТ) в свете последних данных доказательной медицины.
? Эффективна ли нейропротекция при ЧМТ?
.jpg) На этот вопрос отвечает профессор кафедры анестезиологии и интенсивной терапии Национального медицинского университета им. А.А. Богомольца (г. Киев), президент Ассоциации анестезиологов Украины, доктор медицинских наук Сергей Александрович Дубров.
На этот вопрос отвечает профессор кафедры анестезиологии и интенсивной терапии Национального медицинского университета им. А.А. Богомольца (г. Киев), президент Ассоциации анестезиологов Украины, доктор медицинских наук Сергей Александрович Дубров.
Травматическое повреждение головного мозга (ТПГМ) – глобальная проблема, частота которой возрастает год от года. Всемирная организация здравоохранения прогнозирует, что к 2020 году ТПГМ займет третье место среди всех причин смертности. В то же время единые стандарты лечения пациентов с подтвержденными улучшениями клинических исходов на сегодня не разработаны. Нет эффективной специфической лекарственной терапии, которая была бы официально одобрена для лечения ТПГМ.
К вмешательствам с доказанной эффективностью, которые снижают риск смерти и достоверно улучшают результаты лечения, относятся:
- поддержание перфузии головного мозга;
- нормовентиляция;
- адекватная оксигенация;
- предупреждение гипоксемии, артериальной гипотензии и внутричерепной гипертензии.
Выживание нейронов зависит от поддержания церебрального кровотока. Церебральное перфузионное давление определяется как разница между средним артериальным давлением и внутричерепным давлением (ВЧД) и в норме составляет >50 мм рт. ст. Поэтому основным условием терапии пациентов с ЧМТ должно быть поддержание среднего артериального давления в оптимальном диапазоне 100-110 мм рт. ст. на фоне мониторинга ВЧД (оптимальные значения – 10-15 мм рт. ст.).
К важнейшим составляющим терапии относятся обеспечение адекватной оксигенации крови, управляемая аналгезия и седация по необходимости, профилактика венозных тромбоэмболий, адекватная нутритивная поддержка, поддержание нормогликемии (4,4-6,6 ммоль/л – допустимый уровень глюкозы крови, который не требует фармакологической коррекции до 10 ммоль/л).
Возможность улучшения ранних и отдаленных исходов ЧМТ путем применения нейропротекторов имеет сторонников, но и остается предметом дискуссий в связи с противоречивыми клиническими данными. Многие перспективные молекулы с нейропротективными свойствами не имеют доказательной базы или не подтвердили эффективность в клинических исследованиях.
Цитиколин (цитидин‑5’-дифосфохолин) – метаболический предшественник фосфолипидного компонента клеточных мембран и нейромедиатора ацетилхолина со множественными молекулярными механизмами нейропротекции. Цитиколин стабилизирует клеточные мембраны, нейтрализует свободные радикалы и процессы перекисного окисления мембранных липидов, активирует работу ионных насосов, подавляет избыточную продукцию глутамата и ингибирует глутамат-индуцированный апоптоз (R.M. Adibhatla, 2001; J.J. Secades, 2002; O. Hurtado, 2005).
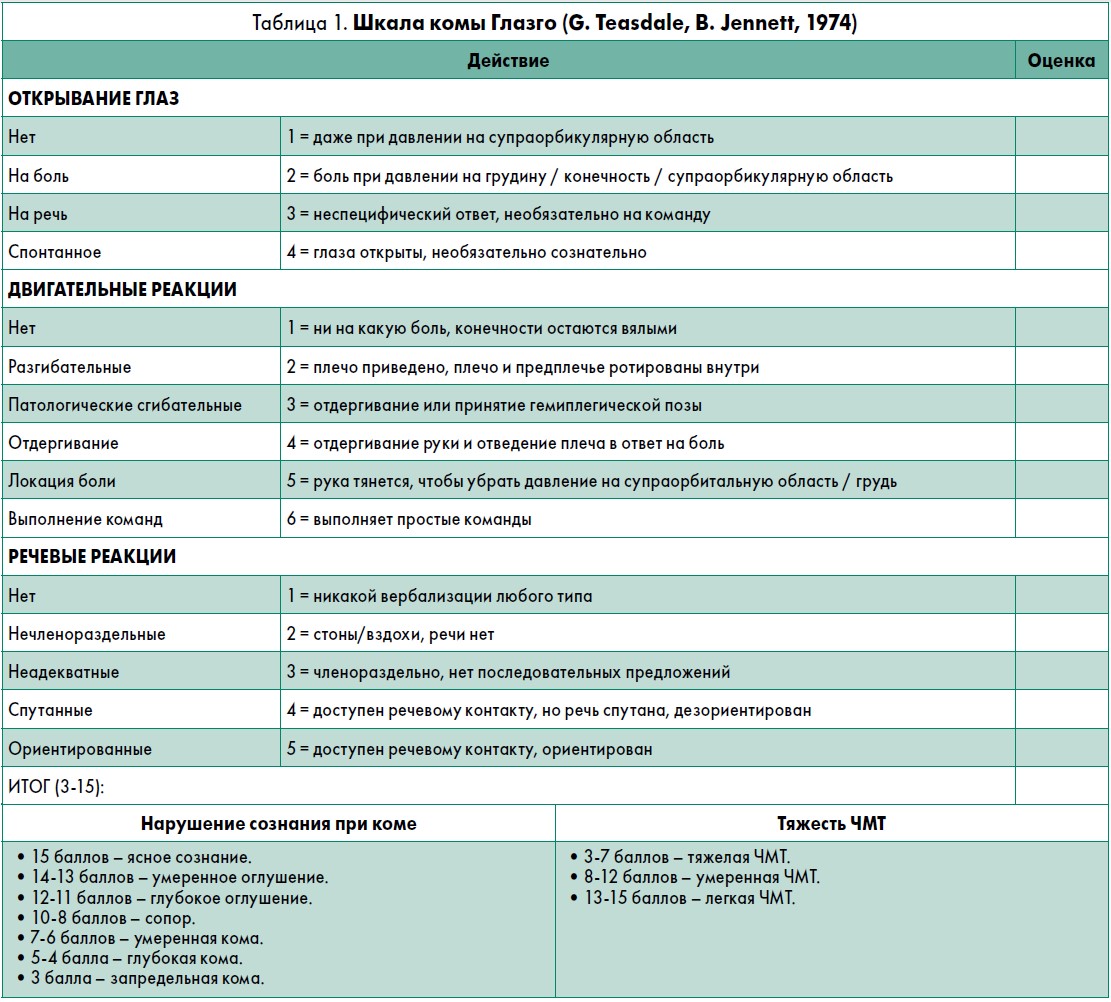
Цитиколин в качестве нейропротектора при ЧМТ изучен в ряде исследований. F. Salehpour и соавт. (2015) оценивали эффекты цитиколина у 40 пострадавших с диффузным аксональным повреждением и оценкой по шкале комы Глазго (ШКГ) <8 баллов (табл. 1). Отмечено достоверное снижение уровня малонового диальдегида – маркера оксидативного стресса – у пациентов, которым вводили цитиколин по 500 мг 4 р/сут, по сравнению с контрольной группой.
В двойном слепом рандомизированном исследовании G. Shokouhi и соавт. (2014) изучались эффекты цитиколина в отношении уровня сознания, сывороточных концентраций фетуина-А и матриксного Gla-протеина (MGP) – маркеров воспаления и вторичной васкулярной кальцификации – у 58 пациентов с тяжелой ЧМТ и оценкой по ШКГ ≤8. Цитиколин применяли внутривенно по 500 мг каждые 6 ч в течение 15 дней. Оценки по ШКГ улучшились у всех пациентов, но без статистически достоверных различий между группами цитиколина и контроля. В то же время уровни фетуина-А и MGP достоверно повысились в группе цитиколина, что указывает на его церебропротекторный эффект путем предотвращения вторичных повреждений в результате воспаления и васкулярной кальцификации после ЧМТ.
В систематический обзор опубликованных исследований с применением цитиколина в острой фазе ЧМТ (J.J. Secades, 2014) включено 12 контролируемых исследований с участием в общей сложности 2706 пациентов. Цитиколин применяли по 250-6000 мг/сут внутрь, внутримышечно или внутривенно, с длительностью курса от 7 до 90 дней. По результатам метаанализа на модели случайных эффектов отношение шансов (ОШ) составило 1,815 (95% доверительный интервал (ДИ) от 1,302 до 2,530) в пользу цитиколина по отношению к таким клиническим исходам, как независимость от посторонней помощи и оценка по ШКГ. Также в кумулятивном метаанализе показано, что эффект цитиколина со временем «размывался» на фоне повышения стандартов оказания помощи пациентам с ЧМТ. Это объясняет, почему положительные эффекты нейропротекции у пациентов с ЧМТ так трудно выявить и оценить.
В рамках проекта по оптимизации раннего оказания помощи пациентам с ЧМТ в 14 австрийских клиниках нейротравмы проведен ретроспективный анализ результатов лечения 67 пациентов Wiener Neustadt Hospital, которым назначали цитиколин, и 67 пациентов с подобными характеристиками из других клиник, которые не получали нейропротективную терапию. Анализ показал достоверное снижение смертности в отделении интенсивной терапии (5 против 24%; p<0,01), общей госпитальной смертности (9 против 24%; p=0,035) и 6-месячной смертности (13 против 28%; p=0,031) в группе пациентов, в комплексном лечении которых применяли цитиколин. Несмотря на ограничения, присущие ретроспективному подгрупповому анализу, это исследование демонстрирует возможную корреляцию между ранним и последовательным применением цитиколина и положительными исходами у пациентов с ЧМТ (H. Trimmel et al., 2018).
Профессор представил анализ данных собственного опыта применения цитиколина (Цераксона). В анализ включены данные 15 пациентов, из которых контрольную (ретроспективную) группу составляли 8 человек, не получающие фармакологической нейропротекции.
Пациенты исследуемой (проспективной) группы (n=7) получали Цераксон® внутривенно капельно в течение 60 мин в дозе 1000 мг 2 р/сут в интервале с 3-го по 10-й день.
Критериями включения в анализ были: возраст 18-45 лет, мужской пол, изолированная тяжелая ЧМТ в сочетании с ушибом головного мозга тяжелой степени и субдуральной гематомой (80-200 мл); отсутствие выраженной артериальной гипотензии и потребности в применении вазопрессоров с момента травмы до включения в исследование; стабильная гемодинамика (без вазопрессоров); уровень сознания по ШКГ 5-8 балов (кома І-ІІ стадии) и отсутствие хронической сопутствующей патологии.
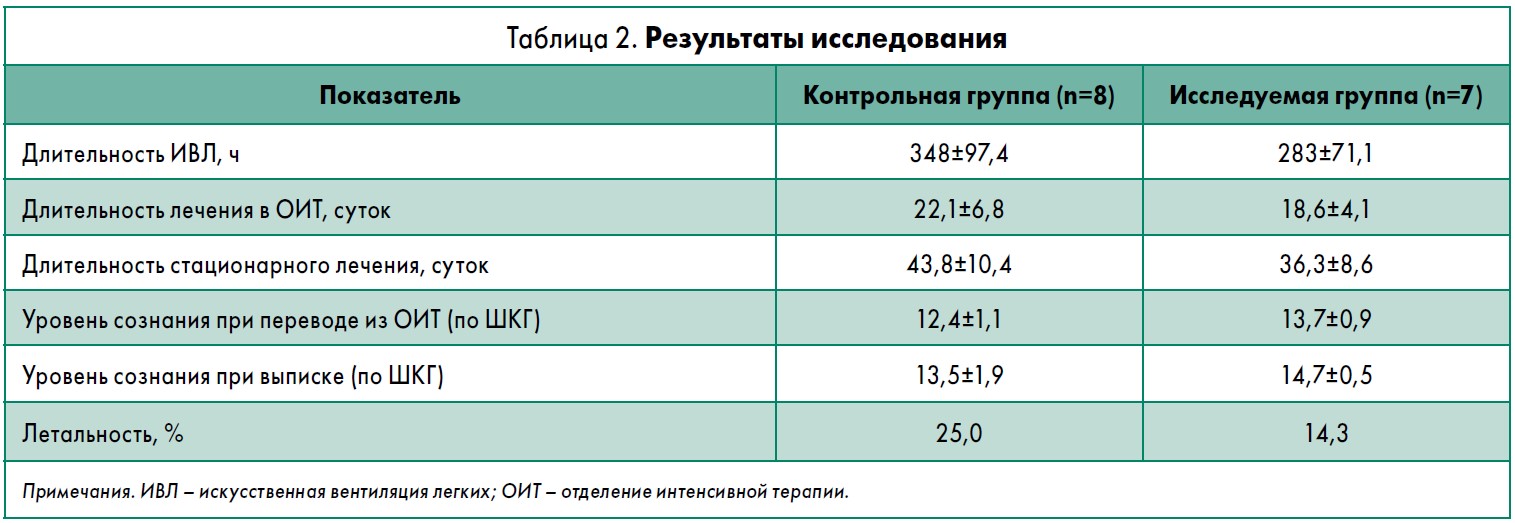
Полученные результаты продемонстрировали положительный эффект Цераксона® в терапии ЧМТ, что выражалось в снижении летальности (14,3 против 25,0% в контрольной группе), улучшении по ШКГ как при переводе из отделения интенсивной терапии, так и при выписке, уменьшении длительности стационарного лечения и времени пребывания на искусственной вентиляции легких (табл. 2).
Хотя роль нейропротекторов остается неопределенной, результаты исследований с использованием оригинального цитиколина (Цераксона) являются обнадеживающими.
Еще одной широко распространенной проблемой в неотложной неврологии являются инсульты. Для этой патологии также важно инициировать нейропротекторную терапию как можно раньше – в острую и подострую фазы инсульта – и проводить длительно с целью улучшения функционирования пациентов и повышения качества их жизни.
 О роли нейропротекторного лечения с применением цитиколина в оптимизации ведения пациентов в острой и подострой стадиях инсульта, а также в восстановительном периоде рассказывает член-корреспондент НАМН Украины, заведующая кафедрой нервных болезней и нейрохирургии ГУ «Днепропетровская медицинская академия МЗ Украины», доктор медицинских наук, профессор Людмила Антоновна Дзяк.
О роли нейропротекторного лечения с применением цитиколина в оптимизации ведения пациентов в острой и подострой стадиях инсульта, а также в восстановительном периоде рассказывает член-корреспондент НАМН Украины, заведующая кафедрой нервных болезней и нейрохирургии ГУ «Днепропетровская медицинская академия МЗ Украины», доктор медицинских наук, профессор Людмила Антоновна Дзяк.
Нейропротекция при острых нарушениях мозгового кровообращения
Повреждение клеточных мембран всегда сопровождает церебральную ишемию при острых нарушениях мозгового кровообращения. Отсюда идея терапевтического применения прекурсора фосфатидилхолина для защиты нервных клеток при остром инсульте. Мультимодальные эффекты цитиколина находят точки приложения на разных этапах ишемического каскада.
В клинических исследованиях продемонстрированы положительные эффекты от применения цитиколина в острую и подострую фазы ишемического инсульта. В 2016 году группа испанских авторов (J. Secades, J. Castillo, J. Alvarez-Sabin и др.) обновила систематический обзор результатов рандомизированных плацебо-контролируемых исследований (РКИ) цитиколина при инсульте. Изучался вопрос: улучшает ли исходы острого ишемического инсульта назначение цитиколина в первые 14 дней? В обзор и метаанализ включили данные 10 РКИ. Применение цитиколина ассоциировалось с достоверным повышением уровня самостоятельности пациентов, независимо от методов оценки (ОШ 1,56; 95% ДИ 1,12-2,16 в модели случайных эффектов; ОШ 1,20; 95% ДИ 1,06-1,36 в модели фиксированных эффектов). После проведения кумулятивного метаанализа и с учетом результатов, полученных в подгруппе пациентов, которые не получали лечения методом тромболизиса (ОШ 1,63; 95% ДИ 1,18-2,24 в модели случайных эффектов; ОШ 1,42; 95% ДИ 1,22-1,66 в модели фиксированных эффектов), подтвердилась гипотеза испанских исследователей о «растворении» эффекта цитиколина в эффектах других вмешательств при инсульте. Когда эффекты проанализировали у пациентов, которые не получали тромболизис, но получали максимальную дозу цитиколина, начиная с первых суток после появления симптомов инсульта, гетерогенность результатов отсутствовала и размер эффекта имел ОШ 1,27 (95% ДИ 1,05-1,53). Авторы заключили, что данный метаанализ подтверждает положительный эффект цитиколина в отношении функциональных исходов ишемического инсульта, хотя при использовании на фоне золотого стандарта – тромболизиса – эффект нейропротекции ограничен.
Нейропротекция в постинсультном периоде
Кроме нейропротекторных эффектов, в острую фазу ишемии цитиколин приносит долгосрочную пользу в восстановительном периоде, усиливая процессы регенерации и облегчая реабилитацию пациентов. Эти эффекты объясняются влиянием цитиколина на апоптоз, ангиогенез, нейрогенез, глиагенез, синаптогенез в головном мозге. В ряде экспериментальных исследований цитиколин продемонстрировал способность стимулировать клеточную пролиферацию, васкуляризацию (M. Gutierrez-Fernandez, 2012) и образование новых синаптических связей нейронов (O. Hurtado, 2007), что сопровождалось ускоренным восстановлением двигательных и когнитивных функций лабораторных животных после моделирования инсульта.
Кокрановский метаанализ 12 РКИ по применению цитиколина у больных с сосудистыми когнитивными нарушениями (всего 942 пациента) подтвердил улучшение памяти и поведения, а также достоверное повышение оценок по шкале общего клинического впечатления лицами, ухаживающими за пациентами (M. Fioravanti, 2005).
 В рамках открытого рандомизированного исследования J. Alvarez-Sabin и соавт. (2013) проверяли гипотезу о влиянии цитиколина на когнитивные функции и исходы после перенесенного ишемического инсульта. Пациенты получали цитиколин по 1000 мг/сут в течение 12 мес дополнительно к стандартной терапии или только стандартную терапию. На фоне терапии цитиколином через 6 и 12 мес отмечались статистически достоверно лучшие исходы в отношении внимания, исполнительных функций и ориентации. Также пациенты, которые получали цитиколин, демонстрировали тенденцию к лучшим функциональным исходам, определяемым по модифицированной шкале Рэнкина (mRS). Так, оценку по mRS ≤2 на шестом месяце получили 50,6% пациентов группы цитиколина против 44,2% в контрольной группе, а через 12 мес этот показатель составлял 57,3 и 48,7% соответственно. Таким образом, улучшение когнитивных функций под влиянием цитиколина действительно коррелирует с улучшением общих функциональных исходов, то есть способности пациентов к самообслуживанию.
В рамках открытого рандомизированного исследования J. Alvarez-Sabin и соавт. (2013) проверяли гипотезу о влиянии цитиколина на когнитивные функции и исходы после перенесенного ишемического инсульта. Пациенты получали цитиколин по 1000 мг/сут в течение 12 мес дополнительно к стандартной терапии или только стандартную терапию. На фоне терапии цитиколином через 6 и 12 мес отмечались статистически достоверно лучшие исходы в отношении внимания, исполнительных функций и ориентации. Также пациенты, которые получали цитиколин, демонстрировали тенденцию к лучшим функциональным исходам, определяемым по модифицированной шкале Рэнкина (mRS). Так, оценку по mRS ≤2 на шестом месяце получили 50,6% пациентов группы цитиколина против 44,2% в контрольной группе, а через 12 мес этот показатель составлял 57,3 и 48,7% соответственно. Таким образом, улучшение когнитивных функций под влиянием цитиколина действительно коррелирует с улучшением общих функциональных исходов, то есть способности пациентов к самообслуживанию.
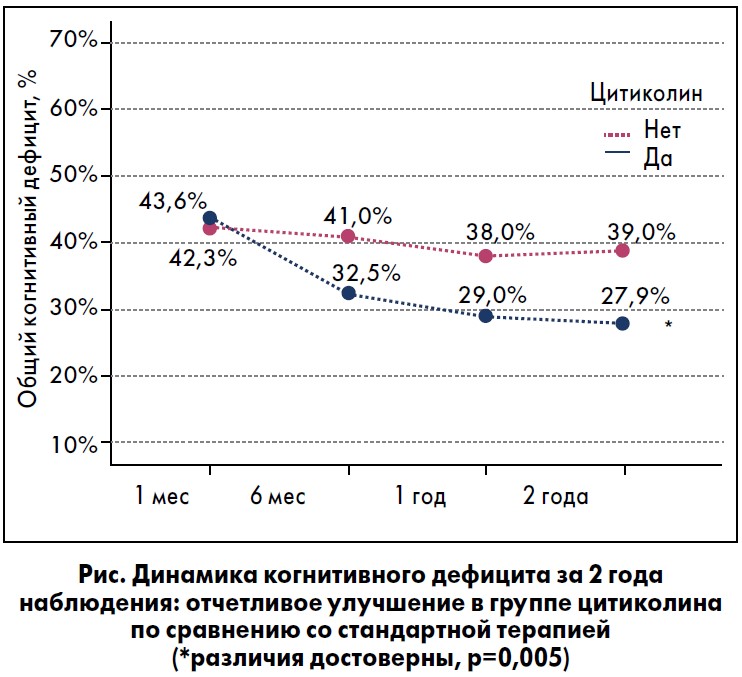
Также заслуживают внимания результаты продленного наблюдения 163 постинсультных пациентов, которые получали терапию цитиколином или только стандартную терапию (J. Alvarez-Sabin et al., 2016). Повторные нейропсихологические тесты через 1 и 6 мес, 1 и 2 года после сосудистой катастрофы показали достоверное замедление темпов снижения когнитивных функций при использовании цитиколина (рис.). Терапия цитиколином ассоциировалась с улучшением качества жизни пациентов разных возрастных групп согласно оценкам по Европейскому опроснику EuroQoL‑5D.
Подводя итог, следует отметить, что цитиколин (Цераксон®) является одним из немногих нейропротекторов, который в контролируемых исследованиях продемонстрировал клинически значимые эффекты предотвращения нейрональных потерь в остром периоде инсульта, а также в качестве стимулятора репарации в восстановительном периоде.
Данные исследований и метаанализов свидетельствуют и о перспективах оригинального цитиколина (Цераксона®) в сфере лечения пациентов с ЧМТ и инсультами. Таким образом, наблюдается все более явный переход нейропротекторной терапии из разряда «интуитивной» в категорию «основанной на доказательствах».
Подготовил Дмитрий Молчанов
Статья печатается при содействии ООО «Такеда Украина».
UA/CITI/1118/0034