16 лютого, 2019
Целевые специфические антидоты для новых оральных антикоагулянтов
В современной практической медицине антикоагулянтная терапия играет важную роль в лечении и профилактике тромбоэмболических осложнений, которые включают в себя тромбоз глубоких вен и тромбоэмболию легочных артерий.
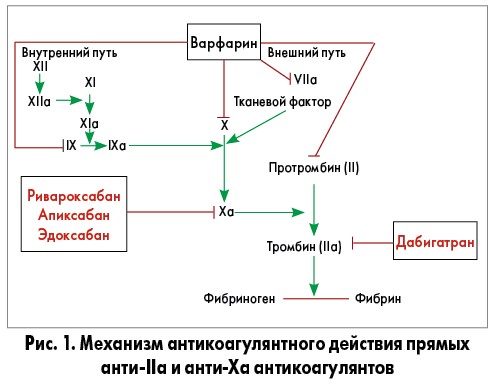 Еще совсем недавно лидирующую позицию среди пероральных антикоагулянтов занимал антагонист витамина К лекарственный препарат (ЛП) варфарин. Хотя эффективность варфарина доказана в многочисленных международных исследованиях, тем не менее особенности фармакокинетики и фармакодинамики этого ЛП очень существенно осложняют его практическое применение [1, 2]. За последние 10 лет на фармацевтическом рынке появились новые пероральные антикоагулянты (НОАК), представляющие собой ингибиторы фактора IIa (дабигатран этексилат) и фактора Xа (ривароксабан, апиксабан, эдоксабан) (рис. 1.).
Еще совсем недавно лидирующую позицию среди пероральных антикоагулянтов занимал антагонист витамина К лекарственный препарат (ЛП) варфарин. Хотя эффективность варфарина доказана в многочисленных международных исследованиях, тем не менее особенности фармакокинетики и фармакодинамики этого ЛП очень существенно осложняют его практическое применение [1, 2]. За последние 10 лет на фармацевтическом рынке появились новые пероральные антикоагулянты (НОАК), представляющие собой ингибиторы фактора IIa (дабигатран этексилат) и фактора Xа (ривароксабан, апиксабан, эдоксабан) (рис. 1.).
Безопасность применения НОАК во многом определяется наличием антидотов, способных быстро и эффективно устранить возникшие геморрагические осложнения. К тому же одним из требований Управления по контролю за качеством продуктов питания и лекарственных средств США (FDA) при регистрации новых препаратов с антикоагулянтным действием является существование антидота. Это положение стало дополнительным стимулом у компаний – производителей НОАК разработать и внедрить в практику антидоты для этих лекарственных препаратов.
I. Идаруцизумаб
НОАК дабигатран этексилат
Дабигатран является первым прямым антикоагулянтом, одобренным FDA в 2008 г. на основе исследования Randomized Evaluation of Long-Term Anticoagulant Therapy (RE-LY), в котором дабигатран сравнивали с варфарином [3]. Механизм действия дабигатрана заключается в конкурентном связывании с активным центром тромбина, что предотвращает переход растворимого фибриногена в нерастворимый фибрин. Дабигатран способен ингибировать как свободный тромбин, так и связанный с фибриновым сгустком. Биодоступность после его перорального введения составляет 6-7% и не зависит от дозы пролекарства дабигатрана этексилата [4]. В некоторых исследованиях продемонстрировано, что концентрация дабигатарана в плазме увеличивается дозозависимым образом. Пиковая концентрация (Cmax) достигается через 1,5-2 ч после введения, среднее время полужизни составляет 12-14 ч, до 80% выводится через почки [5, 6]. В зависимости от клинического диагноза рекомендуемая доза дабигатрана этексилата может составлять 150, 220 или 300 мг/сут.
Идаруцизумаб – антидот для дабигатрана
Идаруцизумаб представляет собой Fab (участок связывания антигена, fragment antigen binding) гуманизированных моноклональных антител, обладающий очень высокой аффинностью к дабигатрану, нейтрализует его антикоагулянтный эффект и не влияет на каскад коагуляции. В 2015 г. идаруцизумаб был представлен в соответствии со схемой ускоренной регистрации в FDA и Европейском агентстве лекарственных средств (EMA) для применения у пациентов, которым требуется срочное купирование действия дабигатрана, и получил одобрение FDA 16 октября 2015 г. [7].
Получение идаруцизумаба
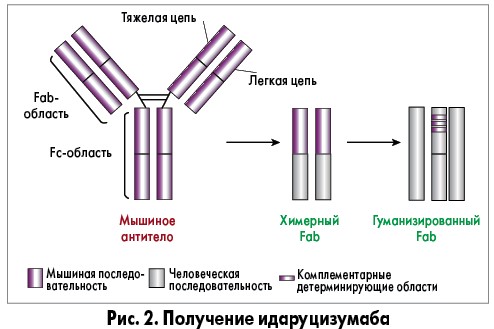 Первым шагом в создании идаруцизумаба является иммунизация мышей гаптенами, полученными из дабигатрана, которые связаны с белками-носителями для выработки антител против дабигатрана [8]. После этого последовательности мышиного белка заменяются последовательностями человека сначала в константной области, в результате чего образуется химерный Fab, а затем в вариабельной области (гуманизированный Fab) посредством специальной технологии (рис. 2). Затем дабигатрансвязывающие гуманизированные Fab экспрессируют в клеточные линии млекопитающих с использованием рекомбинантной ДНК (клетки яичника китайского хомячка). Применение гуманизированных Fab вместо интактных антител приводит к их более короткому периоду полужизни и уменьшению побочных иммунологических реакций.
Первым шагом в создании идаруцизумаба является иммунизация мышей гаптенами, полученными из дабигатрана, которые связаны с белками-носителями для выработки антител против дабигатрана [8]. После этого последовательности мышиного белка заменяются последовательностями человека сначала в константной области, в результате чего образуется химерный Fab, а затем в вариабельной области (гуманизированный Fab) посредством специальной технологии (рис. 2). Затем дабигатрансвязывающие гуманизированные Fab экспрессируют в клеточные линии млекопитающих с использованием рекомбинантной ДНК (клетки яичника китайского хомячка). Применение гуманизированных Fab вместо интактных антител приводит к их более короткому периоду полужизни и уменьшению побочных иммунологических реакций.
Механизм действия идаруцизумаба
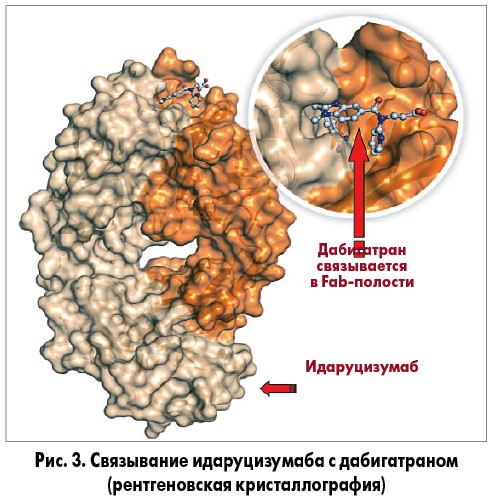 Идаруцизумаб связывает дабигатран с аффинностью в 350 раз выше, чем дабигатран связывается с тромбином (значения аффинности связывания [KD] (соответственно 2 пмоль/л и 0,7 нмоль/л) (рис. 3). Антидот связывает свободный и связанный с тромбином дабигатран, а также активные метаболиты дабигатрана, которыми являются ацилглюкорониды с образованием стехиометрических комплексов в соотношении 1:1 [9]. Как только произошло образование комплексов, антикоагулянтное действие дабигатрана нейтрализуется. Идаруцизумаб не связывается с факторами свертывания и не влияет на функцию тромбоцитов [10, 11]. Непосредственно антидот и его комплексы выводятся через почки. У пациентов с сохраненной функцией почек время полужизни идаруцизумаба после внутривенного введения составляет 45 минут (увеличивается у пациентов с нарушенной функцией почек).
Идаруцизумаб связывает дабигатран с аффинностью в 350 раз выше, чем дабигатран связывается с тромбином (значения аффинности связывания [KD] (соответственно 2 пмоль/л и 0,7 нмоль/л) (рис. 3). Антидот связывает свободный и связанный с тромбином дабигатран, а также активные метаболиты дабигатрана, которыми являются ацилглюкорониды с образованием стехиометрических комплексов в соотношении 1:1 [9]. Как только произошло образование комплексов, антикоагулянтное действие дабигатрана нейтрализуется. Идаруцизумаб не связывается с факторами свертывания и не влияет на функцию тромбоцитов [10, 11]. Непосредственно антидот и его комплексы выводятся через почки. У пациентов с сохраненной функцией почек время полужизни идаруцизумаба после внутривенного введения составляет 45 минут (увеличивается у пациентов с нарушенной функцией почек).
Лекарственный препарат идаруцизумаб доступен в виде готового к использованию раствора в упаковке, сожержащей 2 стеклянных флакона по 50 мл каждый с 2,5 г идаруцизумаба в каждом флаконе. Идаруцизумаб вводят внутривенно в виде 2 последовательных инфузий в течение 5-10 минут каждая или в виде 2 последовательных болюсных инъекций.
Показанием к применению идаруцизумаба является необходимость быстрой отмены антикоагулянтного эффекта в следующих случаях:
- для проведения неотложной хирургической операции / экстренных манипуляций;
- при возникновении угрозы жизни или при неконтролированном кровотечении.
 Следует рассмотреть целесообразность приема второй дозы 5 г идаруцизумаба в таких ситуациях:
Следует рассмотреть целесообразность приема второй дозы 5 г идаруцизумаба в таких ситуациях:
- Рецидив клинически значимого кровотечения вместе с пролонгированным временем свертывания.
- Если возможный рецидив кровотечения представляет угрозу для жизни и наблюдается пролонгированное время свертывания.
- Пациент нуждается в проведении втрой неотложной хирургической операции / экстренной манипуляции и имеет пролонгированное время свертывания.
Соответствующими параметрами коагуляции при введении идаруцизумаба являются:
- АЧТВ (активированное частичное тромбопластиновое время);
- dТВ (тромбиновое время с разведением);
- ECT (экариновое время).
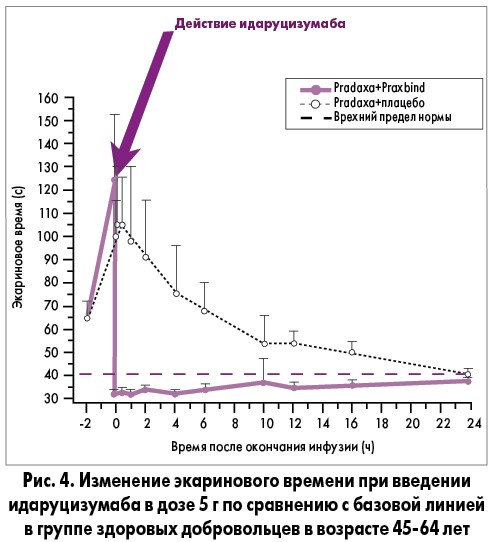
Пример изменения экаринового времени от базовой линии в группе здоровых добровольцев представлен на рис. 4.
II. Андексанет альфа
НОАК ривароксабан
Ривароксабан является НОАК, одобренным FDA в 2008 г. по результатам клинического исследования ROCKET AF [12]. Ривароксабан представляет собой производное оксазолидинона и является селективным прямым ингибитором фактора Xa (обладает селективностью в 1000 раз больше для фактора Xa, чем для других сериновых протеаз), который способен связываться конкурентно и обратимо как со свободным фактором Ха, так и фактором Ха, связанным с протромбиназным комплексом [13, 14]. Активированный фактор Xa играет важную роль в каскаде коагуляции, так как он объединяет внутренние и внешние пути коагуляции и влияет на скорость образования тромбина. Ривароксабан быстро абсорбируется, обладает высокой биодоступностью (60-80%) и достигает пика концентрации в плазме примерно через 2,5-4 ч после перорального приема [15]. Примерно 30% ривароксабана эксретируется с мочой. Метаболизм этого ЛП происходит при участии изофермента CYP 3A4 [16]. Период полужизни ривароксабана составляет около 5-9 ч у пациентов с нормальной функцией почек и печени [17]. Более высокий уровень ривароксабана может определяться у пациентов с нарушением почечной и печеночной функций, т. к. одна треть препарата выводится почками и около двух третей метаболизируется в печени.
Андексанет альфа – антидот для ривароксабана и апиксабана
Андексанет альфа представляет собой рекомбинантный модифицированный человеческий фактор Xa. Андексанет альфа утвежден FDA в мае 2018 г. и предназначен для пациентов, получающих ривароксабан или апиксабан для отмены антикоагуляционного эффекта из-за опасного для жизни или неконтролируемого кровотечения. Андексанет альфа – это молекула, которая высокоаффинно связывает прямые ингибиторы фактора Xa и дозозависимо блокирует их действие [18].
Основные замены в модифицированном факторе Xa (рис. 5):
1. В положении 419 каталитического центра аминокислота серин заменена на аланин. В связи с этим молекула теряет каталитическую активность при расщеплении протромбина.
2. Удален участок, содержащий GLA-домены. Без этого домена модифицированный фактор Xa не может связываться с мембраной, встраиваться в протромбиновый комплекс и оказывать прокоагулянтное действие.
3. Белок модифицирован для снижения иммуногенности.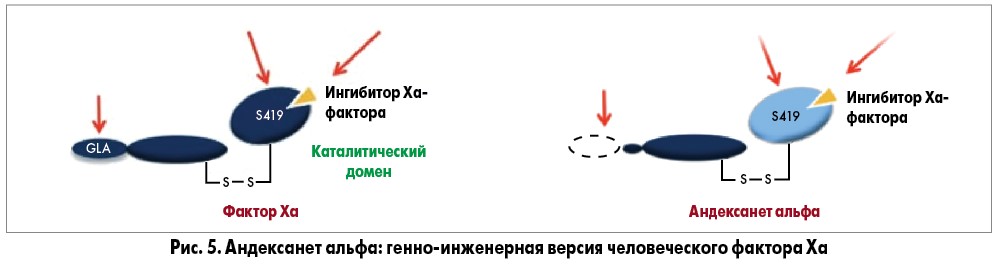
В серии экспериментов in vitro и in vivo было показано, что андексанет альфа быстро и дозозависимо инактивирует ингибиторы фактора Xa, что было подтверждено коагулогическими тестами [19-21].
Дозирование андексанета альфа
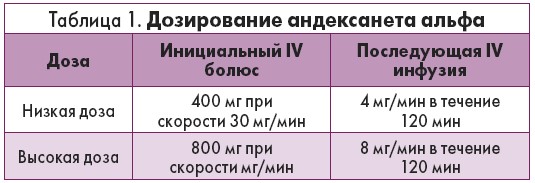 Существует два режима дозирования. Введение андексанета альфа в виде внутривенного (IV) болюса со скоростью 30 мг/мин с последующей непрерывной инфузией в течение 120 мин (табл. 1).
Существует два режима дозирования. Введение андексанета альфа в виде внутривенного (IV) болюса со скоростью 30 мг/мин с последующей непрерывной инфузией в течение 120 мин (табл. 1).
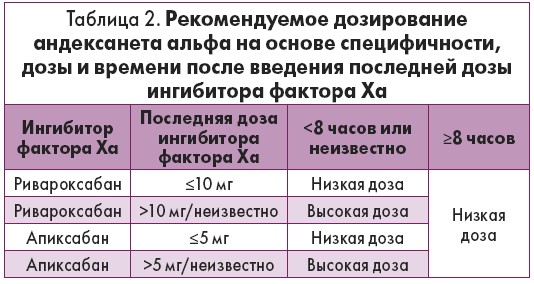
Рекомендуемое дозирование андексанета альфа на основе специфичности, дозы и времени после введения последней дозы ингибитора фактора Xa представлено в таблице 2.
III. Цирапарантаг
 Цирапарантаг – небольшая водорастворимая молекула с молекулярной массой 512 Da, которая изначально была синтезирована в качестве антидота к гепарину. Связывается с нефракционированными, низкомолекулярными гепаринами и пероральными антикоагулянтами прямого действия, такими как дабигатран, ривароксабан и апиксабан [22-24]. Цирапарантаг инактивирует антикоагулянты посредством нековалентного связывания водорода, который блокирует связь с целевыми сайтами факторов IIa, Xa и гепаринов (рис. 6).
Цирапарантаг – небольшая водорастворимая молекула с молекулярной массой 512 Da, которая изначально была синтезирована в качестве антидота к гепарину. Связывается с нефракционированными, низкомолекулярными гепаринами и пероральными антикоагулянтами прямого действия, такими как дабигатран, ривароксабан и апиксабан [22-24]. Цирапарантаг инактивирует антикоагулянты посредством нековалентного связывания водорода, который блокирует связь с целевыми сайтами факторов IIa, Xa и гепаринов (рис. 6).
Антидот не связывается с белками плазмы, в том числе с альбумином. Кроме того, было показано, что препарат не взаимодействует с основными сердечно-сосудистыми, противоэпилептическими и обезболивающими лекарственными препаратами. Сейчас заканчивается III фаза клинических испытаний цирапарантага [25].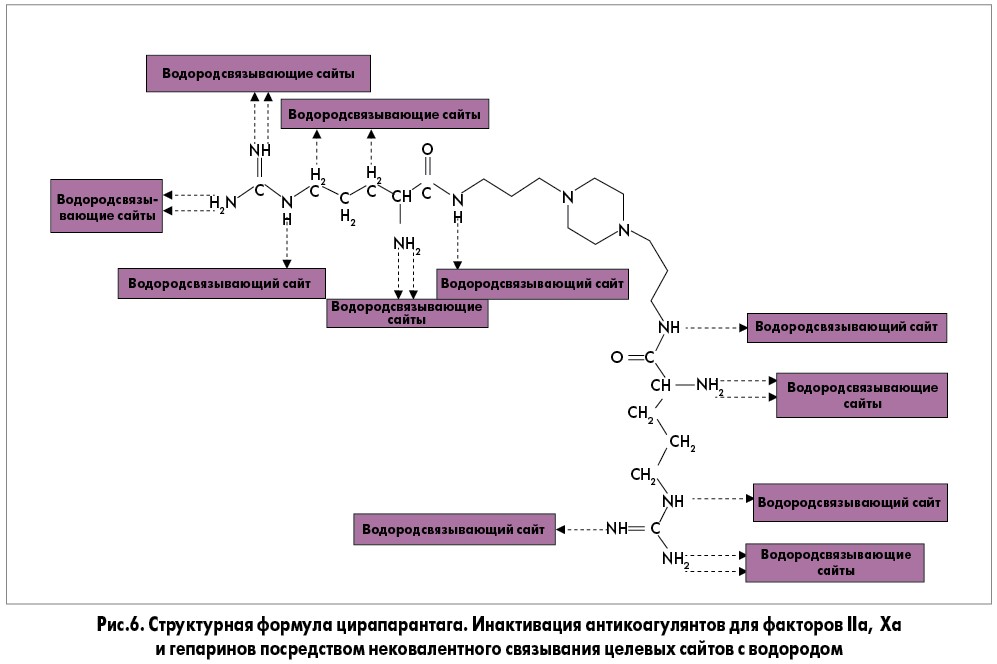
Заключение
На сегодняшний день НОАК заняли определенное место в клинической практике в качестве лекарственных препаратов для профилактики и лечения тромбоэмболических осложнений. Безопасность применения НОАК определяется наличием антидотов, способных быстро и эффективно устранять возникающие геморрагические осложнения. Утвержденными FDA антидотами являются идаруцизумаб для дабигатрана (зарегистрирован в Украине) и андексанет альфа для ривароксабана или апиксабана. Лекарственный препарат цирапарантаг (REP977) как инактиватор антикоагулянтов для факторов IIa, Xa и гепаринов находится в стадии клинических исследований.
Список литературы находится в редакции.
Медична газета «Здоров’я України 21 сторіччя» № 21 (442), листопад 2018 р.


