22 квітня, 2019
Как повлиять на системное воспаление при аллергическом рините? Роль блокаторов Н1-гистаминовых рецепторов
Аллергический ринит (АР) представляет собой IgE-опосредованный иммунный ответ, характеризующийся развитием воспалительного процесса в слизистой оболочке носа [1].
В настоящее время АР рассматривается как наиболее распространенное клиническое проявление аллергии, отмечающееся у 20-30% людей в общей мировой популяции [1, 2]. АР также является фактором риска развития бронхиальной астмы (БА): с течением времени она может сформироваться более чем у 25% пациентов с персистирующим АР (ПАР) [3].
В реализации иммунного ответа на воздействие антигена участвуют сразу несколько типов клеток и медиаторов. Сразу же после воздействия антигена, в ранней фазе аллергического воспаления, отмечается немедленное высвобождение мастоцитами биологически активных веществ, в том числе гистамина. Высвобождаемые медиаторы создают специфическое воспалительное окружение, которое способствует экспрессии и активации определенных молекул клеточной адгезии (CAM) [4, 5]. Активация CAM в свою очередь способствует миграции в слизистую оболочку носа провоспалительных клеток, таких как эозинофилы и нейтрофилы [5, 6]. Поздняя фаза иммунного ответа характеризуется высвобождением различных цитокинов, хемокинов и других медиаторов, преимущественно продуцируемых Т‑хелперами 2 типа (Th2) и гранулоцитами [5, 6].
Молекула адгезии сосудистого эндотелия 1 типа (VCAM‑1) и молекула межклеточной адгезии 1 типа (ICAM‑1) принадлежат к семейству иммуноглобулинов. Обе эти молекулы экспрессируются преимущественно на эндотелиальных клетках [7, 8]. Провоспалительные цитокины, такие как интерлейкин‑1 и фактор некроза опухоли (TNF), усиливают экспрессию обеих CAM, в то время как Th2-цитокины значимо повышают экспрессию VCAM‑1 [9]. ICAM‑1 и VCAM‑1 участвуют в трансэндотелиальной миграции и адгезии лейкоцитов (в том числе эозинофилов [6, 10]), способствуя поддержанию позднего иммунного ответа в слизистой оболочке носа.
E‑селектин – CAM, экспрессирующаяся на эндотелиальных клетках и опосредующая быструю низкоаффинную адгезию лейкоцитов к эндотелиальным клеткам. Уровень E‑селектина выше во время ранней стадии воспаления в сосудистом эндотелии [8, 9]. Он играет важную роль в процессе инициации и формирования аллергического воспаления.
! Антигистаминные препараты (АГП) – лекарственные средства первого выбора при всех формах АР [1]. Основной эффект этих препаратов связан с блокадой H1-гистаминовых рецепторов, опосредующей их противоаллергическое действие. Дальнейшие исследования выявили, что АГП также обладают противовоспалительным эффектом: они уменьшают количество мигрирующих в ткани воспалительных клеток и снижают экспрессию CAM [11-15].
Цель этого исследования состояла в анализе изменений CAM у пациентов с ПАР в условиях непрерывного естественного воздействия аллергенов на фоне лечения АГП второго поколения левоцетиризином и дезлоратадином на протяжении 1 мес.
Материалы и методы
Пациенты и клиническая оценка
В рамках данного исследования был выполнен анализ результатов первоначального рандомизированного контролируемого исследования, в которое были включены пациенты с ПАР и здоровые добровольцы [16]. В экспериментальную группу были включены 79 пациентов с ПАР (средний возраст – 30,44±9,9 года, соотношение числа мужчин и женщин – 1:1), а в контрольную группу – 30 здоровых добровольцев (средний возраст – 28,92±8,91 года, соотношение количества мужчин и женщин – 1:1).
Диагноз АР был установлен в соответствии с международными рекомендациями на основании данных анамнеза и результатов кожных прик-тестов (КПТ) [1]. Степень тяжести АР определяли по выраженности нескольких специфических симптомов: ринорея, заложенность носа, чихание, зуд в носу и глазах. Степень тяжести симптоматики оценивалась ретроспективно (за 12 ч, предшествовавших оценке) по шкале от 0 до 3 баллов (0 – симптом отсутствует, 1 – легкий, 2 – умеренно выраженный, 3 – тяжелый). Общая оценка симптомов (ООС) была рассчитана путем сложения показателей оценки каждого симптома. ООС <6 баллов свидетельствовала о наличии легкого АР, тогда как ООС >6 баллов отражала среднетяжелое и тяжелое течение заболевания.
После исходного обследования пациенты были рандомизированы на две группы: первая группа включала 39 участников, получавших левоцетиризин в дозе 5 мг/сут, вторая – 40 пациентов, принимавших дезлоратадин в дозе 5 мг/сут. Рекомендованная длительность лечения составляла 4 нед.
Кожные прик-тесты
В соответствии с международными рекомендациями диагностика аллергии проводилась путем выполнения КПТ [17]. Панель аллергенов включала клещи домашней пыли (Derm. pteronyssinus и Derm. farinae), пыльцу трав (смесь аллергенов), пыльцу злаковых, пыльцу березы, эпителий котов и собак, аллергены Alternaria alternata и аллергены сорных трав (Artemisia vulgaris и Ambrosia elatior).
Измерение фракции выдыхаемого оксида азота
Измерение фракции выдыхаемого оксида азота (FeNO) проводилось в соответствии с международными рекомендациями [18] до лечения АГП и через 1 мес после него.
Биологическая оценка
Все биологические показатели определялись до начала лечения АГП и через 1 мес после него. Общее содержание IgE в плазме крови определялось с использованием электрохемилюминесцентного анализа; нормальным считалось значение <100 МЕ/мл. Количество эозинофилов в периферической крови подсчитывали вручную в мазке на стекле; нормальным считалось значение 2-4%. Уровни ICAM‑1, VCAM‑1 и E‑селектина в плазме крови определяли методом иммуноферментного анализа.
Результаты
Оценка до лечения
У 56 (70,9%) пациентов имело место среднетяжелое и тяжелое течение АР. Изначальная ООС подтверждала тяжесть АР: медиана – 8 (5-11). У 41 пациента (51,9%) имела место множественная сенсибилизация – как к бытовым, так и к внешним аллергенам. Исходная ООС не коррелировала с длительностью АР, но была достоверно большей у пациентов с сенсибилизацией к пыльце или с множественной сенсибилизацией (p=0,01).
У пациентов с АР плазменные уровни ICAM‑1 и VCAM‑1 достоверно превышали таковые у здоровых добровольцев (p<0,001 и p<0,001 соответственно). Уровень E‑селектина был аналогичен у здоровых добровольцев и у пациентов с АР.
Степень тяжести АР, выражавшаяся в высоком значении ООС, коррелировала с уровнем Е‑селектина в плазме крови (R=0,996; p<0,001), но не с базальными уровнями ICAM‑1 (R=-0,051; p=0,657) или VCAM‑1 (R=-0,056; p=0,622). Отсутствовала корреляция между плазменным уровнем CAM и возрастом/полом пациентов, а также типом сенсибилизации (p>0,05). Отмечалась положительная корреляция между базальными значениями ICAM‑1 и Е‑селектина (R=0,353; p=0,001).
Общее содержание IgE и количество эозинофилов в крови были достоверно повышены исходно, без различий между группами (p=0,408 и p=0,838 соответственно). Начальное значение количества эозинофилов в периферической крови выражено коррелировало с общим уровнем IgE (R=0,853; p<0,001). Не отмечалось какой-либо корреляции между базальными уровнями эозинофилов или общими уровнями IgE и концентрациями ICAM‑1, VCAM‑1 и E‑селектина (p>0,05).
Значение FeNO было повышено у пациентов с АР (медиана – 27 (18-46) в сравнении со стандартизированным пороговым значением, равным 25 ppb (1 ppb = 1 часть газа на 109 частей выдыхаемой воздушной смеси. – Прим. ред.) (p<0,001). Между группами не отмечались различия в изначальных значениях FeNO и не было выявлено их корреляции с тяжестью симптомов АР, типом сенсибилизации или исходными значениями CAM (p>0,05).
Оценка через 1 мес
АГП достоверно ослабили все симптомы АР спустя 1 мес терапии. ООС значимо снизилась после лечения (медиана – 8 баллов (5-11) в сравнении с медианой 0 (0-4); p=0,01), при этом не наблюдалось различий между исследуемыми препаратами (p=0,571).
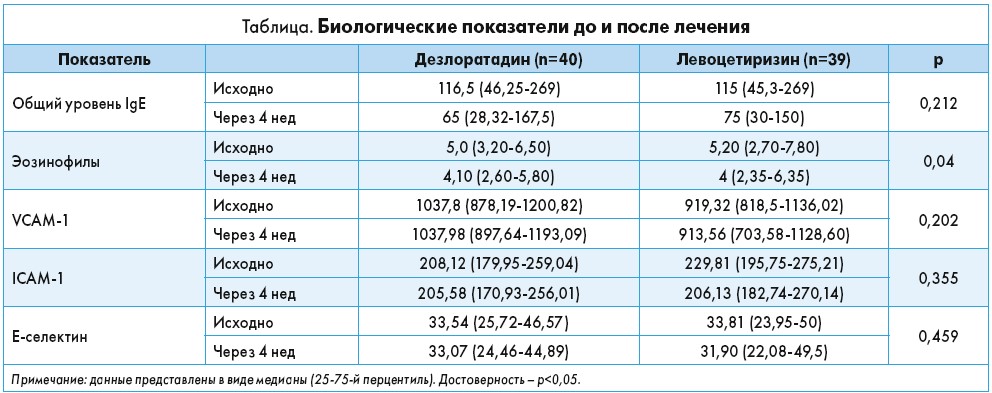
Оценка, проведенная через 1 мес терапии АГП, выявила значимое снижение уровня IgE в плазме крови (p<0,001), особенно у пациентов с моносенсибилизацией к бытовым или внешним аллергенам (p=0,05). При этом на снижение общего уровня IgE не влияли тип лечения, возраст и пол пациента, а также характеристики места его проживания и длительность АР (p>0,05) (табл.). Общий уровень IgE достоверно снизился у пациентов со среднетяжелым и тяжелым течением АР в сравнении с пациентами с легким АР (p=0,05).
После лечения отмечалось значимое снижение количества эозинофилов в периферической крови (p=0,04), особенно у пациентов с моносенсибилизацией к бытовым аллергенам или смешанной сенсибилизацией (p=0,002). Снижение количества эозинофилов также было статистически значимым у пациентов с тяжелыми формами АР (p=0,04). На уменьшение количества эозинофилов в крови не влияли такие факторы, как тип лечения, пол, возраст и условия проживания пациента, а также длительность АР (p>0,05).
Спустя 4 нед лечения АГП достоверно снизились плазменные уровни ICAM‑1 (p=0,049) и E‑селектина (p=0,002), но не VCAM‑1 (p=0,310) в сравнении с исходными значениями. Применение левоцетиризина и дезлоратадина приводило к снижению уровней молекул адгезии в плазме крови (табл.).
Отмечалось значимое снижение уровней CAM у пациентов со среднетяжелым и тяжелым АР в сравнении с пациентами с легким течением АР (VCAM‑1: p=0,037; ICAM‑1: p=0,001; E‑селектин: p=0,002). Возраст и пол пациентов, а также тип сенсибилизации не влияли на снижение уровней CAM. Уменьшение ООС положительно коррелировало со снижением уровня ICAM‑1 (R=0,238; p=0,035), но не с изменениями VCAM‑1 и E‑селектина. Снижение уровня ICAM‑1 положительно коррелировало с изменениями уровней E‑селектина (R=0,504; p<0,001) и VCAM‑1 (R=0,711; p<0,001).
Обсуждение
АР характеризуется развитием аллергического воспаления слизистой оболочки носа. Воздействие аллергенов опосредует высвобождение из мастоцитов медиаторов (особенно гистамина), которые ответственны за развитие характерных симптомов АР (чихание, зуд в носу и ринорея) [19]. Однако эти же медиаторы также стимулируют инфильтрацию слизистой оболочки носа воспалительными клетками, в том числе эозинофилами [20]. Хронический воспалительный ответ с эозинофильной инфильтрацией слизистой оболочки носа представляет собой характерный тип аллергического воспаления [1, 19]. Эти клетки продолжают продуцировать цитокины, хемокины и другие воспалительные медиаторы, которые приводят к сохранению симптомов, а также к структурным изменениям и повреждению ткани. Таким образом, прогрессирование и персистирование АР начинают в большей мере зависеть от медиаторов, которые стимулируют инфильтрацию слизистой оболочки носа такими клетками, как эозинофилы и Т‑хелперы [21]. АР является фактором риска развития БА и может возникать до или после ее дебюта. При этом именно аллергическое воспаление является ключевым в патогенезе обоих заболеваний и прогрессировании АР в БА [5, 19].
Эозинофилы мигрируют в зону воспаления ввиду высокой экспрессии молекул адгезии на поверхности эндотелиальных клеток [22]. Роль молекул адгезии в патогенезе аллергических заболеваний изучалась во многих исследованиях [10, 23-29]. Большинство из них продемонстрировали увеличение уровней ICAM‑1 и VCAM‑1 в смывах со слизистой оболочки носа, ее биоптатах и в сыворотке крови, взятой у пациентов с АР, в сравнении со здоровыми лицами после проведения провокационных аллергопроб или в условиях естественного воздействия аллергенов [10, 23, 24, 26-28]. В данном исследовании плазменные уровни ICAM‑1 и VCAM‑1 были достоверно повышены у пациентов с ПАР в сравнении со здоровыми добровольцами (p<0,001 и p<0,001 соответственно). Эти результаты подтверждают ранее опубликованные данные, отражая наличие системного воспаления у пациентов с ПАР.
Gorska-Ciebiada и соавт. [27] показали, что значения ICAM‑1 достоверно ниже у пациентов с легкими формами АР, чем у пациентов со среднетяжелым и тяжелым его течением [27]. Корреляции между ICAM‑1 и VCAM‑1 и тяжестью АР или типом сенсибилизации не отмечалось. Другое исследование показало, что уровни VCAM‑1 и ICAM‑1 возрастают во время сезона палинации и снижаются вне его [26]. Большинство пациентов в данном исследовании имели полисенсибилизацию как к бытовым, так и к внешним аллергенам, которая может объяснять высокий уровень CAM в сыворотке крови ввиду их непрерывной продукции.
Центральная роль в патогенезе всех аллергических заболеваний отводится IgE. IgE повышается после сенсибилизации к аллергенам и связывается с мастоцитами через специфические рецепторы, но растворимая фракция IgE остается в сыворотке крови и может быть определена лабораторно. В различных клинических исследованиях уровень IgE не коррелировал со значениями ICAM‑1 или TNF, которые были выше у лиц с БА, чем с АР [29]. В нашем исследовании отмечалась значимая корреляция между уровнями эозинофилов и общего IgE (p<0,001), но значения общего IgE не коррелировали с другими маркерами воспаления, такими как CAM или FeNO. Хотя CAM вовлечены в процесс миграции эозинофилов в участок воспаления, в нашем исследовании сывороточные значения количества эозинофилов не коррелировали с уровнями ICAM‑1 и VCAM‑1.
В нашей группе пациентов уровень FeNO был повышен у пациентов с АР и не коррелировал ни с одним исследуемым маркером. Не отмечалось корреляции между начальным уровнем FeNO и степенью тяжести симптомов АР, типом сенсибилизации или исходными значениями CAM (p>0,05). Однако это отсутствие корреляций не может исключить возможный минимальный воспалительный процесс в слизистой оболочке как носа, так и нижних дыхательных путей.
! В этом исследовании нами было установлено, что левоцетиризин и дезлоратадин ослабляли выраженность назальных симптомов АР, значительно снижая показатель ООС через 1 мес лечения, что согласуется с ранее опубликованными данными [2, 19, 38]. При этом не наблюдалось различий между исследуемыми препаратами в отношении степени снижения ООС (p=0,571). Через 4 нед лечения блокаторы Н1-гистаминовых рецепторов достоверно снизили плазменные уровни ICAM‑1 (p=0,049) и Е‑селектина (p=0,002), но не VCAM‑1 (p=0,310), в сравнении с их исходными значениями.
В нашем исследовании мы также отметили значимое снижение уровней CAM у пациентов со среднетяжелым и тяжелым АР в сравнении с легкой формой заболевания (VCAM‑1: p=0,037; ICAM‑1: p=0,001; E‑селектин: p=0,002). При этом на снижение уровней CAM на фоне терапии АГП не влияли такие факторы, как возраст, пол пациента и тип сенсибилизации.
В исследованиях in vitro было продемонстрировано, что не все АГП второго поколения способны оказывать противовоспалительный эффект. Так, цетиризин не влиял на уровни Е‑селектина, ICAM‑1 и VCAM‑1 в исследованиях in vitro, хотя авторы отмечали недостаточную экспрессию ICAM‑1 в эпителиальных клетках пациентов с АР, получавших лечение цетиризином [11]. У лоратадина наблюдалось влияние на VCAM‑1, но не на ICAM‑1 у пациентов с моносенсибилизацией к аллергенам клещей домашней пыли [12]. Исследования in vitro выявили, что левоцетиризин ингибировал ICAM‑1 [15], снижал активность P‑селектинов [41] и экспрессию VCAM‑1 [42]. Также имеются данные исследований in vivo, которые выявили наличие у АГП противовоспалительного эффекта. Левоцетиризин и дезлоратадин снижали уровень ICAM‑1 и количество эозинофилов в слизистой оболочке носа [44]. В настоящем исследовании уровень VCAM‑1 не снижался на фоне применения АГП, снижались только уровни ICAM‑1 и E‑селектина. Вероятно, экспрессия ICAM‑1 и E‑селектина (маркеров начального аллергического ответа) связана с высвобождением гистамина из мастоцитов, тогда как за экспрессию VCAM‑1, возможно, ответственны другие цитокины и хемокины.
! Выполненная через 1 мес оценка выявила значимое снижение плазменного уровня IgE (p<0,001) на фоне лечения АГП, особенно у пациентов с моносенсибилизацией к бытовым или внешним аллергенам (p=0,05). Уровень общего IgE значимо снизился у пациентов со среднетяжелым и тяжелым АР в сравнении с легким течением заболевания (p=0,05). Также после лечения АГП достоверно снизилось количество эозинофилов в периферической крови (p=0,04).
В целом результаты данного исследования подчеркивают противовоспалительный эффект АГП второго поколения, продемонстрированный на основании снижения плазменных уровней CAM у пациентов с ПАР.
Выводы
Пациенты с ПАР имеют высокие сывороточные уровни ICAM‑1 и VCAM‑1. У пациентов с ПАР повышен уровень FeNO как маркера субклинического воспаления. АГП значимо ослабляют симптомы АР и снижают уровень маркеров воспаления через 1 мес лечения.
Список литературы находится в редакции.
Статья печатается в сокращении.
Muntean I.A. et al. How Could We Influence Systemic Inflammation in Allergic Rhinitis? The Role of H1 Antihistamines. Oxid Med Cell Longev. 2018 Jun 12; 2018:3718437. doi: 10.1155/2018/3718437.
Перевела с англ. Елена Зотова
Медична газета «Здоров’я України 21 сторіччя» № 6 (451), березень 2019 р