24 травня, 2019
Подагра: мультидисциплінарний підхід і ранній початок терапії – запорука успіху лікування
 Подагра – системне захворювання, основним етіологічним фактором якого є порушення пуринового обміну з розвитком гіперурикемії (ГУ; збільшення вмісту сечової кислоти (СК) у сироватці крові вище рівня сатурації) з подальшим відкладенням у тканинах моноурату натрію та розвитком запального процесу.
Подагра – системне захворювання, основним етіологічним фактором якого є порушення пуринового обміну з розвитком гіперурикемії (ГУ; збільшення вмісту сечової кислоти (СК) у сироватці крові вище рівня сатурації) з подальшим відкладенням у тканинах моноурату натрію та розвитком запального процесу.
Захворювання відоме протягом століть і є принципово виліковним, утім, на жаль, і сьогодні значна кількість пацієнтів отримує неадекватне лікування або не дотримується наданих рекомендацій, що призводить до тривалої ГУ, формування хронічної подагри та розвитку низки ускладнень.
Одним із найчастіших клінічних проявів подагри є розвиток суглобового синдрому у вигляді гострого або хронічного запального артриту, що відноситься до кристал-індукованих (мікрокристалічних) артропатій і характеризується запаленням у місцях відкладення кристалів моноурату натрію (в суглобових та/або навколосуглобових тканинах). Іншим поширеним клінічним проявом є формування уратної нефропатії, сечокам’яної хвороби (СКХ). Прогресування ураження нирок часто є фактором, що визначає якість і тривалість життя пацієнта.
Коморбідність при подагрі та гіперурікемії
На сучасному етапі дані багатьох міжнародних досліджень вказують на наявність значної кількості коморбідних станів у пацієнтів із ГУ та подагрою (артеріальна гіпертензія (АГ), ішемічна хвороба серця (ІХС), метаболічний синдром (МС), ожиріння, дисліпідемія та ін.). Тривають інтенсивні наукові клінічні й експериментальні дослідження, які мають на меті встановити причинно-наслідковий зв’язок між зазначеними станами та захворюваннями і порушенням обміну СК. На практиці визначити, що є первинним – порушення обміну СК чи розвиток коморбідного стану, – часто буває складно і навіть неможливо. Кожного пацієнта з ГУ чи подагрою слід розглядати як пацієнта підвищеного ризику розвитку атеросклерозу, дисліпідемії, серцево-судинних захворювань (ССЗ), тому ведення такого хворого обов’язково має здійснювати мультидисциплінарна команда спеціалістів, яких залучає лікар первинної ланки для персоніфікованого вирішення наявних у цього хворого проблем.
Діагностика
Золотим стандартом діагностики подагри є дослідження синовіальної рідини або аспірація вмісту тофусу для ідентифікації кристалів моноурату натрію методом поляризаційної мікроскопії. Голкоподібні кристали моноурату натрію виявляються під час гострої атаки, а також у період між нападами у хворих із ГУ, переважно в суглобах, що раніше були уражені (Zhang W. et al., 2006). Проте така процедура не є рутинною у вітчизняній клінічній практиці, водночас стан ГУ не є достовірним діагностичним критерієм, оскільки не завжди виявляється в момент гострого нападу подагри. Тоді захворювання діагностують на основі типової клінічної картини: швидкий розвиток інтенсивного больового синдрому (протягом 24 год), зазвичай у межах одного суглоба.
Ведення пацієнтів
Метою є максимально швидке й безпечне зниження інтенсивності больового синдрому та відновлення функціональної здатності ураженого суглоба при гострому подагричному артриті, а також профілактика хронічного артриту, розвитку ускладнень і коморбідних станів та захворювань.
! Після встановлення діагнозу подагри першочерговим завданням лікаря є проведення консультування і навчання пацієнта. Відомо, що навчання пацієнтів підвищує ефективність лікування, прихильність до гіпоурикемічної терапії та збільшує кількість хворих, у яких досягнуто цільовий рівень СК за 12 міс.
Навчання пацієнтів має включати:
- роз’яснення природи захворювання, індивідуальних факторів ризику, тригерів і можливих наслідків та ускладнень;
- роз’яснення важливості тривалого (постійного) прийому гіпоурикемічної терапії;
- рекомендації щодо корекції способу життя (нормалізація маси тіла, низькопуринова дієта, фізичні навантаження);
- самодопомога – розпізнавання ранніх ознак загострення артриту для самостійного початку його лікування якомога раніше від появи симптомів;
- інформування про можливі побічні дії медикаментозної терапії.
Хоча встановлено лише незначний вплив корекції способу життя на рівень СК, більшість експертів наголошує на абсолютній необхідності мотивації пацієнтів до виконання рекомендацій зі здорового харчування, фізичної активності, припинення куріння і помірного вживання алкоголю для зниження серцево-судинного ризику, захворюваності і смертності від ССЗ серед цих хворих.
План ведення хворого на подагру обов’язково повинен передбачати проведення скринінгу коморбідних станів і захворювань, як-от цукровий діабет, АГ, хронічна хвороба нирок (ХХН), ІХС, ожиріння, дисліпідемія, депресія.
Лікування гострого подагричного артриту
Для лікування гострого нападу подагри застосовують нестероїдні протизапальні препарати (НПЗП), колхіцин і глюкокортикоїди (ГК) локально та системно. Експертні групи EULAR, ACR, NHS наголошують на важливості обов’язкової оцінки коморбідних станів і медикаментозної терапії, яку приймають хворі на подагру з приводу іншої патології, для правильного вибору найбільш безпечного алгоритму лікування гострого подагричного артриту. Варто пам’ятати, що колхіцин протипоказаний при вираженому порушенні функції нирок (швидкість клубочкової фільтрації (ШКФ) <30 мл/хв/1,73 м2); не слід призначати препарат на тлі прийому інших інгібіторів CYP3A4.
Лікування нападу необхідно починати якомога раніше (протягом перших 12-24 год від появи симптомів). Пацієнт може розпочати лікування гострого подагричного артриту самостійно (використовуючи рекомендації лікаря, надані заздалегідь при встановленні діагнозу). Медикаментозна терапія гострого нападу подагри включає НПЗП та/або колхіцин, ГК. Серед додаткових заходів можливе використання локальних аплікацій із льодом і розвантаження ураженого суглоба (ліжковий режим, підняте положення кінцівки).
Нестероїдні протизапальні препарати
За відсутності протипоказань НПЗП є препаратами першої лінії і засобами вибору у випадку гострого нападу подагри. Вибір препарату, режим дозування та тривалість терапії визначаються з урахуванням активності запального процесу, а також супутньої патології в кожного конкретного пацієнта. При подагричному нападі доцільно застосовувати НПЗП у максимальних терапевтичних дозах для швидкої ліквідації болю та запалення (іноді доводиться навіть перевищувати рекомендовані дози).
Слід також враховувати фармакодинамічні особливості НПЗП, що є доволі різними. Так, метамізол і парацетамол, хоча й належать до НПЗП, але протизапальної активності не виявляють. Тому при лікуванні подагричного артриту, де протизапальна дія є найважливішою, використання метамізолу та парацетамолу недоцільне.
Режим дозування і тривалість терапії гострого нападу подагри мають бути обрані таким чином, щоб максимально знизити інтенсивність запальної реакції. Згідно з клінічним досвідом, досягнення цієї мети відбувається протягом 7-10 днів, до того ж високі дози протизапальних препаратів використовуються переважно на початку терапії з поступовим їх зниженням у міру покращення перебігу симптомів захворювання.
Важливо відмітити, що лікування загострення подагричного артриту має проводитися на фоні безперервного прийому препаратів, що знижують рівень СК (гіпоурикемічної терапії). Якщо пацієнт раніше не приймав гіпоурикемічну терапію, необхідно обговорити з ним можливість початку такого лікування вже під час першої атаки артриту (рекомендації EULAR, 2016).
Наявність значної кількості супутніх захворювань у пацієнтів із подагрою диктує необхідність враховувати ці коморбідні стани, а також ефекти вже призначених ліків при виборі медикаментозної терапії гострого артриту.
Гіпоурикемічна терапія
Гіпоурикемічна терапія ефективно запобігає рецидивам подагричного артриту та розвитку ускладнень, пов’язаних із неконтрольованою ГУ.
Метою терапії є досягнення цільових рівнів СК <360 мкмоль/л у всіх пацієнтів і <300 мкмоль/л у разі важкого перебігу подагри (наявні тофуси, поліартритичне ураження, часті загострення, ХХН).
Значення зниження сироваткового рівня СК до цільового полягає в профілактиці виникнення гострих нападів, ураження нирок і розвитку тофусів, зменшенні ризику МС, ССЗ та їх ускладнень.
Сучасні рекомендації наголошують на необхідності активної тактики щодо призначення гіпоурикемічної терапії: слід обговорити з пацієнтом можливість і необхідність призначення такого лікування щонайменше на 6 міс уже під час першої атаки артриту, відразу після встановлення діагнозу. Особливо це стосується пацієнтів молодого віку (до 40 років) із рівнем СК >480мкмоль/л, наявними коморбідними захворюваннями (СКХ, ІХС, серцева недостатність, АГ). Подібна тактика має на меті максимально зменшити імовірність ураження нирок, розвитку хронічної тофусної подагри та серцево-судинний ризик у хворих на подагру.
Обов’язковим є призначення гіпоурикемічної терапії хворим, які мають ≥2 загострення за рік, тофуси (виявлені клінічними або рентгенологічними методами), уратну артропатію, нефролітіаз (у тому числі в анамнезі).
Найоптимальнішим режимом гіпоурикемічної терапії прийнято вважати термін 2-4 тиж після зникнення симптомів загострення з призначенням препаратів у низьких дозах із поступовим їх підвищенням протягом декількох тижнів – місяців, однак сучасні рекомендації (EULAR, 2016) наголошують на можливості і більш раннього початку такої терапії (під час гострого нападу (ACR, 2012). Протягом усього періоду підбору дози препаратів необхідний ретельний моніторинг – визначення рівнів СК, контроль ниркової функції, а також можливого розвитку небажаних побічних явищ. Доза препарату підбирається для досягнення цільового сироваткового рівня СК 6 мг/дл (359 мкмоль/л), що доведено асоціюється зі зниженням ризику розвитку повторних нападів і виникнення тофусів. Досягнення нижчого рівня СК – 5 мг/дл (300 мкмоль/л) – сприяє кращому контролю захворювання і рекомендується для більш швидкого усунення депозитів моноурату натрію в тканинах. Зазначена терапія проводиться протягом тривалого періоду і не є обмеженою часовими проміжками. Її ефективність визначається за досягненням цільового рівня СК у сироватці крові, зменшенням частоти гострих нападів подагри, розсмоктуванням тофусів і відсутністю прогресування уролітіазу, що, своєю чергою, зменшує загальний серцево-судинний ризик, показники смертності від ССЗ і покращує якість життя пацієнтів.
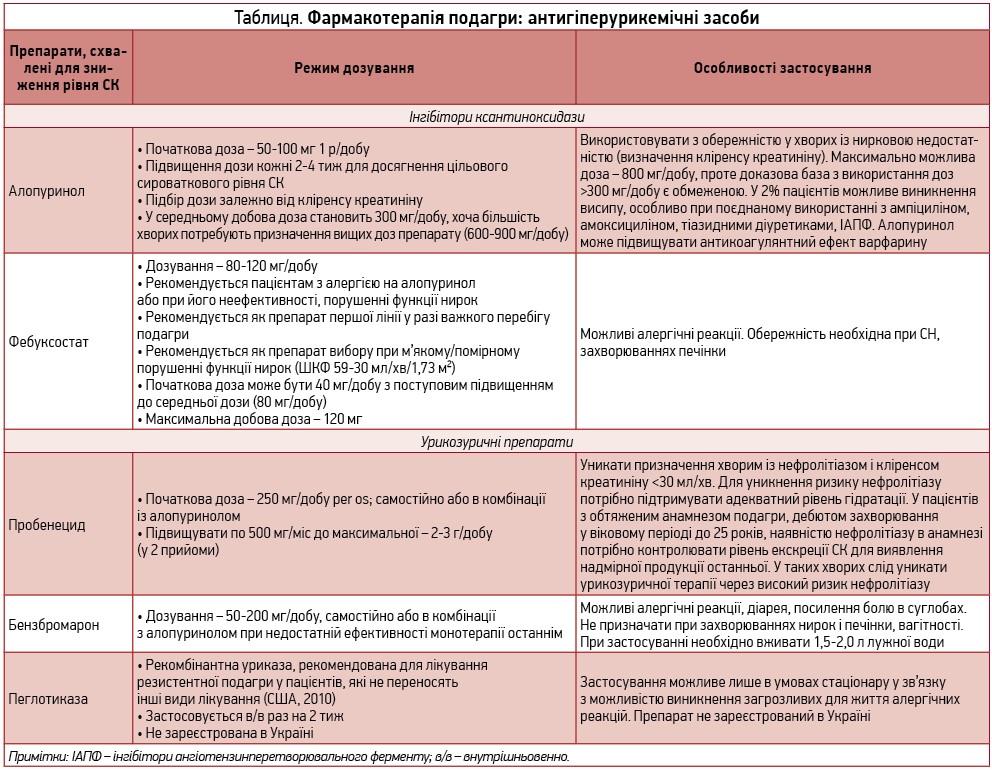
На сьогодні для зниження сироваткового рівня СК схвалені три групи препаратів: інгібітори ксантиноксидази, урикозуричні та уриказні агенти (табл.). Слід зазначити, що найчастіше як антигіперурикемічні засоби використовуються алопуринол і фебуксостат (Аденурик). Відповідно до сучасних рекомендацій ACR, обидва препарати відносять до терапії першої лінії, згідно з настановами з лікування подагри Європейської протиревматичної ліги (EULAR, 2016), фебуксостат (Аденурик) є препаратом першої лінії для лікування важкої подагри та в усіх випадках неефективності/непереносимості алопуринолу.
Інгібітори ксантиноксидази блокують синтез СК та використовуються в разі її надмірої продукції. При застосуванні алопуринолу в середній дозі (300 мг/добу) досягнення цільових рівнів СК, за даними низки досліджень, відбувається лише в 30-50% хворих з нормальною функцією нирок; збільшення дози до 600-800 мг/добу підвищує ефективність лікування: цільовий рівень СК у середньому досягається в 75-80% пацієнтів, однак зростає й кількість небажаних явищ. Абсолютно необхідно дотримуватися правил зменшення дози алопуринолу при різних ступенях зниження ШКФ. Найчастіше при ШКФ 60-90 мл/хв/1,73 м2 добова доза алопуринолу не перевищує 300 мг, при ШКФ <60мл/хв/1,73 м2 – 100 мг, що в значної кількості пацієнтів не дозволяє досягти цільових рівнів СК і вимагає перегляду фармакотерапії з подальшим призначенням фебуксостату. Порівняно з алопуринолом (300 мг/добу) фебуксостат (Аденурик) 80-120 мг/добу в низці рандомізованих клінічних досліджень показав значно більшу ефективність.
Слід пам’ятати про необхідність моніторингу небажаних явищ при застосуванні алопуринолу (диспептичні прояви, шкірні висипи, підвищення рівнів печінкових трансаміназ), а також про можливість розвитку (в незначної кількості пацієнтів) потенційно летального ускладнення – важкого алергічного ураження шкіри (SCARs), що є реакцією гіперчутливості, індукованою Т‑цитотоксичною відповіддю, і реалізується ураженням шкіри (синдром Стівенса-Джонсона, епідермальний некроліз), системними проявами, еозинофілією, високим рівнем оксипуринолу, метаболіту алопуринолу, в сироватці крові. Факторами ризику розвитку SCARs є порушення функції нирок, зростання концентрації оксипуринолу, перевищення рекомендованих доз алопуринолу при ХХН. Смертність у разі виникнення SCARs сягає 25-30%. За статистичними даними, у Європейському регіоні алопуринол є найчастішою причиною розвитку синдрому Стівенса-Джонсона й епідермального некролізу. Встановлено, що ризик виникнення тяжких алергічних реакцій може бути пов’язаний із генетичними особливостями (наявність гаплотипу HLA-B5801 в осіб, які не належать до монголоїдної раси), досліджується доцільність визначення цього генетичного фактора у хворих на подагру перед призначенням лікування алопуринолом.
Фебуксостат (Аденурик) – сучасний високоефективний антигіперурикемічний препарат, селективний інгібітор ксантиноксидази з подвійним шляхом виведення з організму (нирки/печінка – практично 50/50), тому має переваги при лікуванні хворих із супутньою ХХН.
У рекомендаціях ACR (2102) алопуринол і фебуксостат (Аденурик) рекомендовані як препарати першої лінії для застосування в усіх хворих на подагру з метою досягнення цільових рівнів СК та попередження розвитку ускладнень ГУ; фебуксостат є більш ефективним у пацієнтів зі зниженою ШКФ. У згадуваних вище настановах EULAR з лікування подагри (2016) рекомендується розпочинати терапію з алопуринолу і лише після визначення недостатньої ефективності або непереносимості цього препарату переводити пацієнта на прийом фебуксостату. Разом із тим в обговоренні експерти EULAR вказують, що ця рекомендація базується не на дослідженнях з ефективності і безпеки фебуксостату, а на міркуваннях вартості лікування (в більшості європейських країн лікування алопуринолом значно дешевше порівняно із застосуванням фебуксостату). Водночас наголошується, що фебуксостат довів більшу ефективність порівняно з алопуринолом як в осіб зі збереженою функцією нирок, так і в пацієнтів зі зниженою ШКФ; також він більш безпечний щодо виникнення SCARs.
Враховуючи більшу ефективність, фебуксостат також є препаратом вибору при лікуванні тяжкої подагри. Застосування препарату загалом є безпечним, реакції гіперчутливості виникають рідко. Фебуксостат може застосовуватися при виникненні алергічних реакцій, в тому числі SCARs, на прийом алопуринолу.
При відміні медикаментозної терапії рівень СК повертається до вихідного протягом 3-4 днів, тому гіпоурикемічну терапію потрібно проводити пожиттєво під ретельним контролем можливих ускладнень.
Відміна урикозуричних препаратів після тривалого підтримання цільового рівня СК призводить до рецидиву подагри в 40% пацієнтів протягом 5 років. Тому після встановлення діагнозу подагри контроль рівня СК у сироватці крові має бути регулярним, а застосування медикаментозної терапії для досягнення безпечного цільового рівня – пожиттєвим.
Урикозуричні препарати (пробенецид, бензбромарон) блокують реабсорбцію СК на рівні канальців нирок. Спектр використання цих препаратів зводиться до призначення в пацієнтів із підвищеною екскрецією СК (близько 90% хворих на подагру), однак ці засоби використовуються рідше, ніж інгібітори ксантиноксидази, і протипоказані хворим із нефролітіазом. Рекомендується використання пробенециду, бензбромарону в комбінації з інгібітором ксантиноксидази при недостатній ефективності монотерапії.
Певний урикозуричний ефект має антагоніст рецептора ангіотензіну ІІ лосартан. Його застосування доцільне в пацієнтів із ГУ, індукованою застосуванням тіазидних діуретиків.
Профілактична терапія
Відомо, що ініціація гіпоурикемічної терапії може супроводжуватися клінічним загостренням подагричного артриту, що пов’язують із можливим різким коливанням рівня СК у сироватці крові. Найбільш вираженими коливання СК бувають в перші 6 міс лікування антигіперурикемічними препартами.
З метою зменшення ризику розвитку таких загострень рекомендується розпочинати лікування антигіперурикемічними засобами з мінімальних доз (алопуринол – 50-100 мг/добу, фебуксостат – 40 мг/добу), поступово збільшуючи їх (з інтервалом 1-2 тиж залежно від динаміки рівня СК у сироватці крові), а також призначати НПЗП (у низьких дозах) або колхіцин (у низькій дозі) одночасно на 6 міс для профілактики загострення артриту.
Періодичність обстеження пацієнтів
Після встановлення діагнозу подагри пацієнт має перебувати під ретельним наглядом мультидисциплінарної команди лікарів для початкового обстеження і визначення коморбідних станів і захворювань, оцінки ризику ССЗ, необхідності застосування додаткових обстежень (серцево-судинної системи, нирок, генетичних досліджень тощо).
У разі гострого нападу артриту слід призначити огляд і лабораторне обстеження (загальний аналіз крові, рівні С‑реактивного білка, СК, загальний аналіз сечі) після зменшення/ліквідації больового синдрому.
При призначенні гіпоурикемічної терапії слід контролювати рівень СК кожні 10-14 днів із відповідною корекцією дози призначеного препарату; після досягнення цільового рівня СК необхідно контролювати цей показник щонайменше раз на 6-12 міс.
Під час підбору дози антигіперурикемічного препарату слід також щомісяця проводити контроль безпеки медикаментозної терапії (біохімічне дослідження крові з визначенням рівнів аланін- та аспартатамінотрансферази, за необхідності – креатиніну, сечовини, ШКФ), надалі – щонайменше раз на рік.
При лікуванні хронічної тофусної подагри необхідно проводити огляд пацієнта (з оцінкою стану тофусів) 1 раз на 3-6міс, а також після кожного загострення, надалі (після ліквідації тофусів) – раз на рік.
Стабільному пацієнту щороку слід проводити повний огляд із визначенням антропометричних даних, загального серцево-судинного ризику, показників ліпідограми, рівня глюкози крові, вимірюванням артеріального тиску, перевіркою стану нирок (ШКФ, ультразвукове дослідження).
Критеріями ефективності терапії є:
- зниження концентрації СК і досягнення її цільових рівнів;
- зменшення потреби в застосуванні НПЗП, колхіцину та ГК;
- зменшення частоти подагричних нападів, що призводять до втрати працездатності;
- ліквідація тонусів;
- пов’язані з рівнем СК позитивні зміни в ліпідному, вуглеводному обміні, перебігу ХХН, СКХ, АГ.
Прогноз при подагричному артриті загалом сприятливий, але у 20-50% випадків розвивається уролітіаз. Причиною смерті 18-25% хворих на подагру є ниркова недостатність.
Медична газета «Здоров’я України 21 сторіччя» № 8 (453), квітень 2019 р