18 червня, 2019
Применение декскетопрофена в хирургической практике: отечественный и зарубежный клинический опыт
С проблемой выбора метода обезболивания приходится сталкиваться специалистам любой области клинической медицины. Это особенно актуально в хирургии при проведении анестезиологического пособия при оперативных вмешательствах и в послеоперационном периоде, при выполнении болезненных диагностических и лечебных процедур, проведении обезболивания при травмах и у инкурабельных онкологических больных с хроническим болевым синдромом.
Актуальность проблемы обезболивания в хирургической практике
В последние годы значительно расширился диапазон оперативных вмешательств малоинвазивной хирургии (эндоскопическая и внутрисосудистая хирургия), и, конечно, применяемые оперативные пособия были бы невозможны без современной анестезиологической помощи [1].
Существует большое множество патологических состояний, требующих аналгезии, а именно:
- Оперативные вмешательства на органах грудной клетки, брюшной полости, урологические, проктологические, акушерско-гинекологические, операции на нижних конечностях.
- Оперативные вмешательства у больных с тяжелой сопутствующей патологией (ожирение, сердечно-сосудистые и легочные заболевания, нарушение функций печени и почек, деформация верхних дыхательных путей), у лиц пожилого и старческого возраста, у больных с «полным» желудком.
- Компонент сочетанного обезболивания.
- Тяжелые комбинированные скелетные травмы (множественные переломы ребер, костей таза, нижних конечностей).
- Послеоперационное обезболивание.
- Компонент терапии панкреатита, перитонита, кишечной непроходимости, астматического статуса.
- Острые травмы и иные состояния, сопровождающиеся болью, связанной с повреждением или острым воспалением (в частности, при стоматологических заболеваниях).
- Борьба с хроническим болевым синдромом.
В последние годы предметом клинических и научных поисков стало лечение послеоперационной боли. Почти все пациенты в послеоперационном периоде испытывают боль выраженной интенсивности, которая либо не купируется, либо корригируется недостаточно. Этому существует множество объяснений: недостаточное знание патофизиологических механизмов возникновения острой боли, а также фармакодинамических и фармакокинетических свойств анальгетиков. Более того, принято считать, что послеоперационная боль – это неизбежное естественное следствие хирургической травмы. Даже сейчас, при наличии многих эффективных анальгетиков, лечение послеоперационной боли бывает неадекватным.
С другой стороны, гораздо сложнее разработать примерную схему терапевтических алгоритмов ее лечения, которая должна учитывать различие индивидуальных характеристик пациентов, вид оперативного вмешательства, методику анестезии, возможности медицинского персонала и т. п. [2]. Неадекватное обезболивание приводит как к значительному ухудшению ближайших результатов хирургического лечения, так и к неблагоприятным отдаленным последствиям [3]. Недостаточная аналгезия у данного контингента больных, по данным литературы, в 11-65% случаев приводит к развитию хронического болевого синдрома, значительному ограничению трудоспособности, инвалидности и снижению качества жизни [4].
Послеоперационная боль усиливает нагрузку практически на все органы, оказывая влияние на послеоперационную выживаемость пациентов. В табл. 1 суммировано негативное влияние боли на жизненно важные системы организма.
Согласно современным рекомендательным документам по лечению боли (PROSPECT, рекомендации Европейской ассоциации по изучению боли) в послеоперационном периоде должны использоваться нестероидные противовоспалительные препараты (НПВП). При этом НПВП назначаются на всех ступенях так называемой анальгетической лестницы – начиная от боли малой интенсивности и заканчивая уровнем, требующим параллельного использования опиатов.
В настоящее время в клинической практике достаточно широко и успешно используется инъекционный и таблетированный анальгетик из группы НПВП декскетопрофена трометамол (Дексалгин®) (Побел Е.А., 2008). Дексалгин® является оптически чистым правовращающим изомером кетопрофена, который ингибирует циклооксигеназу‑2 (ЦОГ‑2) в 5 раз активнее по сравнению с рацемическим кетопрофеном и в 100 раз активнее по сравнению с его правовращающим изомером, что обусловливает его высокую анальгетическую эффективность. А также имеет лучший профиль гастроинтестинальной переносимости и меньшую метаболическую нагрузку на организм за счет возможности использования более низких терапевтических доз. Кроме того, важным является тот факт, что декскетопрофен метаболизируется в организме без участия цитохромов печени, что значительно снижает риск развития межлекарственного взаимодействия.
По влиянию на изоферменты циклооксигеназы декскетопрофен является сбалансированным ингибитором ЦОГ‑1 и ЦОГ‑2, в одинаковой степени блокирующим их активность.
Механизм анальгетического действия препарата Дексалгин® заключается в следующем:
- блокада выработки медиаторов боли на периферии за счет ингибирования активности ЦОГ;
- блокада проведения боли по периферическим нервам и проводящим путям ЦНС за счет деполяризации мембран нейронов;
- блокада выработки медиаторов боли в ЦНС, в том числе в коре и глубинных отделах головного мозга, за счет ингибирования активности ЦОГ в этих отделах.
Результаты отечественных и зарубежных исследований по применению декскетопрофена
На базе травматологического отделения Запорожской медицинской академии последипломного образования у пациентов с травмами опорно-двигательного аппарата в качестве послеоперационного обезболивания вместо введения наркотических средств был применен препарат Дексалгин® в дозе 50 мг внутривенно сразу после выхода больного из наркоза 1 раз в сутки (Побел Е.А., 2008). В последующие 24 ч препарат вводили 2 раза в день вместо опиатов. Анализ полученных результатов выявил следующее: в группе больных, получавших опиаты, практически все пациенты независимо от возраста, пола и тяжести повреждения отмечали повышенную заторможенность, сонливость, сохраняющуюся слабость. У троих больных отмечена задержка мочеиспускания на второй день введения наркотических анальгетиков. В основной группе больных на фоне применения Дексалгина указанных выше субъективных ощущений выявлено не было, как и не отмечено влияния препарата на функцию мочеиспускания.
В группе больных, которые получали Дексалгин®, в первые двое суток послеоперационного периода в 81% случаев было достаточно двукратного введения препарата (каждые 12 ч), что позволило заменить таким образом введение опиатов. Остальным 19% больных препарат вводился однократно. Только 2 больным в группе декскетопрофена требовалось дополнительное назначение наркотических анальгетиков для достижения адекватного обезболивания. Начиная с третьих суток после операции, уже без применения наркотических препаратов, вводили 50 мг Дексалгина внутримышечно 1 раз в сутки. У подавляющего большинства пациентов облегчение состояния наступало уже к концу первого часа после введения препарата. При этом продолжительность обезболивающего эффекта в группе получавших опиаты составляла в среднем 4,5 ч, а в группе Дексалгина – 6,5 ч.
Показатели данного исследования подтверждают данные о пролонгированном обезболивающем действии Дексалгина, что связано с блокирующим влиянием на простагландины и, как следствие, снижением воспалительной реакции [5].
Специалистами Днепропетровской центральной районной больницы была проведена сравнительная оценка применения Дексалгина как средства для профилактики и лечения послеоперационного болевого синдрома с применением других анальгетиков, в том числе опиоидов [6]. Исследования выполнены у 70 пациенток в возрасте от 18 до 75 лет, перенесших оперативное вмешательство на органах малого таза. Уменьшение боли наступало через 30,5 мин с момента введения препарата. Максимальный анальгетический эффект развивался спустя 44,3 мин. Продолжительность аналгезии после введения 50 мг Дексалгина внутримышечно составила 10,2 ч. Качество обезболивания в 1-е сутки после операции оценено как отличное у 78% пациенток, как хорошее – у 21%, удовлетворительное – у 1%, при отсутствии необходимости применения опиоидного компонента в послеоперационной аналгезии.
На одной из клинических баз НМАПО им. П.Л. Шупика было проведено исследование по изучению эффективности и переносимости аналгезии декскетопрофеном в акушерско-гинекологической практике [7]. Под наблюдением находились женщины после кесарева сечения. Все пациентки были разделены на две эпидемиологически равнозначные группы. Пациенткам исследуемой группы во время премедикации вводили Дексалгин® в дозе 50 мг (2 мл) однократно и повторно через 8 ч в той же дозе. Группу сравнения составили больные без применения Дексалгина во время премедикации и в послеоперационном периоде. Полное анальгетическое действие Дексалгина у большинства женщин исследуемой группы (92%) продолжалось более 5 ч после его введения в премедикации, 7% отмечали умеренную болевую реакцию, не требующую дополнительной коррекции. Послеоперационную боль у всех больных купировали в течение 15-20 мин после повторного введения через 8 ч. В группе сравнения у большинства (74%) пациенток преобладала боль в нижних отделах живота, а 16% указывали на боль в нескольких местах. В 73% случаев отмечена средняя интенсивность боли. Полученные результаты свидетельствуют об эффективности и целесообразности применения препарата Дексалгин® на этапе премедикации, что позволяет в 92% случаев купировать болевой синдром.
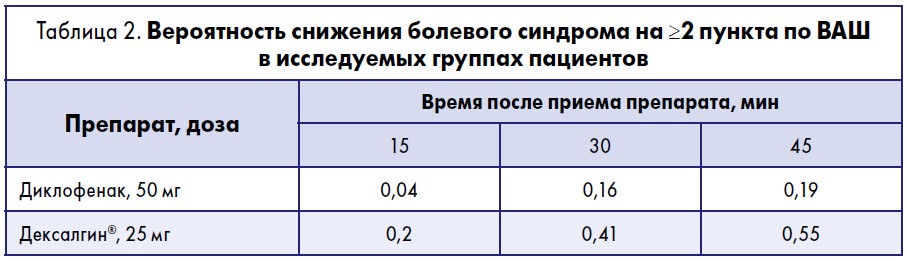
В отделении неотложной помощи больницы Св. Томаса (г. Лондон, Великобритания) P. Leman и соавт. было проведено рандомизированное контролируемое исследование по сравнению декскетопрофена и диклофенака у пациентов с травмами нижних конечностей, испытывающих выраженную боль [8]. Препараты принимали перорально, однократно, сразу же после поступления в стационар: диклофенак – в разовой дозе 50 мг, декскетопрофена трометамол – 25 мг.
Оценку динамики боли проводили каждые 15 мин в течение первого часа после приема сравниваемых препаратов по визуальной аналоговой шкале (ВАШ). При оценке по ВАШ снижение боли на 2 и более пункта в группе применения декскетопрофена было достигнуто достоверно более часто по сравнению с группой диклофенака (табл. 2). То есть Дексалгин® при купировании острой боли был более эффективен по сравнению с диклофенаком.
Учеными Берлинского медицинского университета было проведено многоцентровое двойное слепое рандомизированное клиническое исследование по изучению эффективности и безопасности внутривенно вводимого декскетопрофена трометамола и кетопрофена при лечении болевого синдрома после проведения ортопедической операции [9]. Потребность в спасительной аналгезии была высокой в обеих группах. Время достижения максимального снижения интенсивности болевого синдрома после введения декскетопрофена и кетопрофена составило 284,7 и 308,5 мин соответственно. Нежелательные явления, связанные с лечением, наблюдались у 21,3% пациентов в группе кетопрофена по сравнению с 16% в группе декскетопрофена трометамола. Большинство пациентов одновременно получали препарат низкомолекулярного гепарина (94,4%), при этом никаких геморрагических осложнений, связанных с хирургическим вмешательством, отмечено не было. Авторы пришли к заключению, что назначение декскетопрофена трометамола имеет более благоприятный профиль переносимости по сравнению с кетопрофеном.
В нейрохирургической клинике г. Стамбула было проведено еще одно сравнительное исследование, в котором оценивали анальгетическое действие парацетамола и декскетопрофена в отношении интенсивности послеоперационной боли и динамики потребления опиатов [10]. С этой целью больные, принимавшие участие в исследовании, в течение 24 ч после дискэктомии получали пациент-контролируемое обезболивание (ПКО) морфином и были рандомизированы для получения дополнительно внутривенно парацетамола в дозе 1 г, декскетопрофена – 50 мг или изотонического физиологического раствора (плацебо).
Было установлено, что интенсивность боли в группе декскетопрофена была достоверно ниже, чем в контрольной (р=0,01). В группе парацетамола подобная зависимость отсутствовала (р=0,21). В отношении накопительного потребления морфина и ассоциированных с этим побочных эффектов существенных различий между группами не выявлено. Исследование показало, что значительное (по сравнению с контрольной и группой, принимавшей парацетамол) снижение интенсивности боли в течение 24 ч после дискэктомии отмечалось в группе, получавшей декскетопрофен.
Представляет интерес исследование Z.K. Bengisun и соавт. [11], в котором изучалась эффективность применения декскетопрофена трометамола в качестве дополнительного анальгетика для ПКО трамадолом в послеоперационном периоде при выполнении лапароскопической холецистэктомии. В исследование были включены 40 пациентов. В основной группе больные получали 600 мг трамадола и 100 мг декскетопрофена трометамола, в группе контроля в дополнение к трамадолу – 100 мл 0,9% физиологического раствора для проведения ПКО. Исследование продемонстрировало, что добавление декскетопрофена трометамола статистически значимо повышает удовлетворенность пациентов лечением и снижает потребность в опиоидах. Различий в отношении частоты возникновения побочных эффектов (гипотензия, брадикардия, седации) в сравниваемых группах не отмечалось.
Таким образом, аналгезия послеоперационного периода является важным компонентом интенсивной терапии хирургического больного. При этом назначаемый анальгетик должен оказывать адекватный эффект и быть безопасным для пациента, не вызывать выраженных побочных явлений.
Препарат Дексалгин® эффективен в лечении послеоперационной боли при различных оперативных вмешательствах. В половинной дозе он обладает сопоставимым с кетопрофеном анальгетическим эффектом и в то же время – лучшим профилем безопасности в лечении послеоперационной боли. Важным преимуществом Дексалгина перед наркотическими анальгетиками является его влияние на уменьшение воспаления, жаропонижающий эффект, а также предупреждение периферической сенситизации. Эти положительные свойства препарата в сочетании с выраженным аналгезирующим эффектом позволяют успешно применять его как при травмах, различных соматических заболеваниях, так и в послеоперационном периоде.
Литература
1. Обезболивание в хирургии: Учеб. пособие / Н.П. Володченко. – Благовещенск, 2015.
2. Исраилова В.К., Айткожин Г.К., Сулейменов Б.К. Актуальность обезболивания в раннем послеоперационном периоде у больных после обширных операций на органах брюшной полости // Вестник Казанского национального медицинского университета. – 2015. – № 1.
3. Ferrante F.M., VadeBoncouer T.R. Postoperative pain management / Послеоперационная боль. – М.: Медицина, 1998. – 640 c.
4. Rawal N. Analgesia technique and post-operative morbidityт // Eur. J. Anaesthesiol. Suppl. – 1995. – № 10. – С. 47-52.
5. Побел Е.А. Сравнительное исследование препарата дексалгин и других анальгетиков, применяемых для послеоперационного обезболивания // Медицина неотложных состояний. – 2008. – № 3.
6. Богословова Ю.Е., Л.Н. Сыроватко Л.Н., Косульникова Л.Ф. Применение Дексалгина с целью профилактики и лечения болевого синдрома у пациенток после операций на органах малого таза // Здоровье женщины. – 2013. – № 7.
7. Герасимова Т.В.,Гопчук Е.Н., Чайка О.И. Декскетопрофен – аналгезия в акушерско-гинекологической практике // Здоровье женщины. – 2013. – № 2. – С.41-44.
8. Leman P., Kapadia Y., Herington J. Randomised controlled trial ofthe onset of analgesic efficacy of dexketoprofen and diclofenac in lowerlimb injury Emerg Med J. 2003 Nov; 20 (6): 511-3.
9. Zippel H., Wagenitz A. Comparison of the efficacy and safety of intravenously administered dexketoprofen trometamol and ketoprofen in the management of pain after orthopaedic surgery: A multicentre, double-blind, randomised, parallel-group clinical trial. Clin Drug Investig, 2006; 26(9):517-28.
10. Tunali Y., Akçil E.F., Dilmen O.K. et al. Efficacy of intravenous paracetamol and dexketoprofen on postoperative pain and morphine consumption after a lumbar disk surgery. J Neurosurg Anesthesiol 2013; 25 (2): 143-7.
11. Kazak Bengisun Z., Kazbek B.K. et al. The efficacy of adding dexketoprofen trometamol to tramadol with patient controlled analgesia technique in post-laparoscopic cholecystectomy pain treatment. Agri 2012; 24 (2): 63-8.
Подготовила Кристина Ружанская
Тематичний номер «Хірургія, Ортопедія, Травматологія, Інтенсивна терапія» № 1 (35), лютий 2019 р.