27 червня, 2019
Ведення дітей з кропив’янкою: доказова база та сучасні рекомендації
За різними даними, нині від алергії страждає близько 20-40% населення світу. Третину пацієнтів з алергією становлять діти. Серед найрізноманітніших проявів алергії уваги педіатрів заслуговують стани, які характеризуються ураженнями шкіри, наприклад кропив’янка. Вважається, що протягом життя кожна четверта людина хоча б один раз страждала від проявів кропив’янки. У дітей гостра кропив’янка зустрічається частіше, ніж у дорослих. Поширеність захворювання в дитячій популяції становить 2,7-6,7% (H. Pite et al., 2013). Для дітей віком до 2 років характерна гостра кропив’янка, у віці від 2 до 12 років зустрічаються як гостра, так і хронічна форми захворювання. У підлітків часто діагностується хронічна кропив’янка.
Сильний свербіж, печіння, висипання при кропив’янці негативно відображаються на повсякденному житті дитини: порушується сон, дитина стає дратівливою, знижується здатність до навчання тощо. Тому проблему кропив’янки у дітей слід трактувати не лише як медичну, а й як соціальну.
Кропив’янка – це переважно алергічне захворювання, яке характеризується появою пухирів та/або ангіонабряку внаслідок розширення та підвищення проникності судин. Пухирі мають вигляд чітко контурованих елементів різного розміру (від кількох міліметрів до 10 см та більше), зазвичай блідо-рожевого кольору з почервонінням по периферії, які локалізуються на різних ділянках шкіри та супроводжуються сильним свербежем.
При кропив’янці патологічні шкірні утворення швидко з’являються і безслідно зникають протягом 24 год, не залишаючи після себе вторинних елементів. У разі поширення патологічного процесу на глибокі шари дерми та підшкірну жирову тканину розвивається ангіонабряк, що характеризується раптовим початком, поширенням на нижні шари дерми та підшкірний шар із швидким залученням підслизової мембрани. При цьому іноді біль превалює над свербежем (тривалість клінічних симптомів – до 72 год). Ангіонабряк слід розглядати як клінічний прояв того самого механізму, що і при кропив’янці.
За тривалістю захворювання виділяють гостру (наявність висипань до 6 тижнів) і хронічну кропив’янку (наявність висипань більше 6 тижнів; пухирі можуть з’являтися майже щоденно, «світлі проміжки» без висипань становлять від кількох днів до кількох тижнів).
У дітей частіше виникає гостра кропив’янка, проте сьогодні доступні дані про випадки хронічної кропив’янки навіть у дітей раннього віку. Існує також великий перелік наукових досліджень стосовно різних аспектів ведення дітей з кропив’янкою, у тому числі з хронічною. Це ще раз спростовує твердження про те, що діагноз хронічна кропив’янка не має відношення до педіатрії.
Стратегія ведення пацієнтів із кропив’янкою на підставі даних доказової медицини
Для ведення пацієнтів з кропив’янкою в усьому світі керуються оновленими рекомендаціями European Academy of Allergy and Clinical Immunology, Global Allergy and Asthma European Network, European Dermatology Forum & World Allergy Organization (EAACI/GA2LEN/EDF/WAO) 2018 р.
Для розробки рекомендацій EAACI/GA2LEN/EDF/WAO (2018) були залучені провідні експерти з 42 національних і міжнародних товариств, які провели систематичний аналіз наукової літератури (8090 джерел) та відібрали 65 з них, що відповідали критеріям включення.
Діагностика хронічної кропив’янки
Метою обстеження пацієнтів з кропив’янкою, у тому числі хронічною, є виключення інших патологічних станів, які можуть супроводжуватися подібною клінічною картиною (уртикарний васкуліт, аутозапальні захворювання, такі як синдром Шнітцлера, кріопіринасоційований періодичний синдром, CAPS тощо), визначення активності хвороби та виявлення тригерів, що здатні спровокувати розвиток патології.
Слід пам’ятати, що немає необхідності в проведенні рутинних алерготестів у кожного пацієнта з алергією.
Важливим етапом діагностики захворювання є детальний збір анамнезу, в процесі якого необхідно визначити такі деталі:
- час початку захворювання;
- форма, розміри, частота/тривалість і поширення пухирів;
- асоційований ангіоневротичний набряк (АНН);
- інші ознаки, наприклад, біль у кістках/суглобах, лихоманка;
- сімейний анамнез та анамнез захворювання щодо пухирів і АНН;
- індукція загострень фізичними чинниками або фізичним навантаженням;
- розвиток загострень у зв’язку з вживанням певних харчових продуктів або лікарських засобів;
- алергічні реакції в анамнезі чи наявна алергія, інфекції, інші захворювання внутрішніх органів.
Лікування пацієнтів з хронічною кропив’янкою
Мета лікування – повне усунення симптомів захворювання. Терапія пацієнтів з хронічною кропив’янкою включає:
- ідентифікацію та усунення впливу основних причин;
- уникнення контакту з факторами, що зумовлюють розвиток симптомів;
- індукцію толерантності;
- використання фармакологічного лікування.
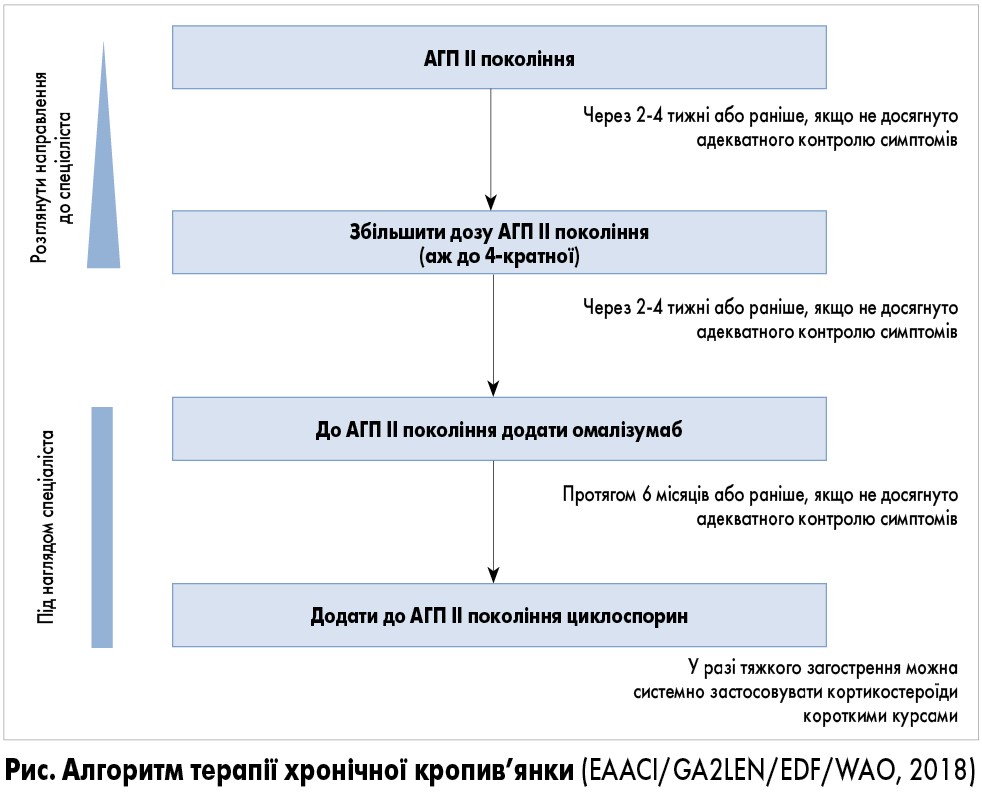
Оскільки ключовим патогенетичним механізмом виникнення пухирів є вплив гістаміну на H1-рецептори, які локалізуються на ендотеліальних клітинах і сенсорних нейронах (зумовлюють появу нейрогенного почервоніння та свербежу), найбільше значення у фармакотерапії таких пацієнтів мають H1-антигістамінні препарати (АГП) в оптимальній для конкретного клінічного випадку дозі (рис.).
Таким чином, рекомендації ґрунтуються на доказовій базі та консенсусі і розроблені за допомогою методів, рекомендованих Кокранівським співробітництвом та робочою групою Оцінювання ступеня рекомендацій та їх розробки (Grading of Recommendations Assessment, Development and Evaluation – GRADE). У попередніх рекомендаціях 2014 р. терапія кропив’янки складалася із 3 послідовних кроків, у нових рекомендаціях лікування пацієнтів представлено у вигляді 4 кроків. Також основними змінами, внесеними у попередні рекомендації EAACI/GA2LEN/EDF/WAO 2014 р., є:
- збільшення тривалості періоду спостереження за ефективністю терапії на 1-му кроці до 2-4 тижнів замість 2 тижнів;
- на 3-му – терапію АГП ІІ покоління доповнюють омалізумабом, на 4-му – циклоспорином (за попередньою редакцією рекомендацій було застосування омалізумабу, циклоспорину або монтелукасту на вибір).
Аналіз ефективності лікарських засобів, які застосовують для контролю симптомів хронічної кропив’янки у дітей
K. Kanchanapoomi et al., 2018
Мета: вивчити ефективність лікарських засобів, які використовують для контролю симптомів кропив’янки у дітей.
Методи: аналіз медичної документації 100 дітей із контрольованою хронічною кропив’янкою, які лікувалися в спеціалізованій алергологічній клініці.
Характеристика пацієнтів. Середній вік хворих становив 8 років (4-18 років), 48% пацієнтів – хлопчики. У 32% пацієнтів кропив’янка супроводжувалася розвитком ангіоневротичного набряку. Середній часовий діапазон від появи перших симптомів захворювання до встановлення діагнозу становив 5 місяців.
Етіологічний спектр захворювання. Під час вивчення медичної документації виявлено, що у 80% випадків ідентифікувати причину алергічного захворювання не вдалося. У 10 з 19 дітей отримано позитивні результати аутогомологічного шкірного тесту з аутологічною сироваткою (Autologous Serum Skin Test; ASST). У 7 дітей було припущено наявність харчової алергії, зокрема в 1 дитини виявлено патологічну реакцію на вживання яєчного білка, у 3 – креветок. На тлі елімінаційної дієти у 4 хворих дітей відмічалося покращення стану. В 1 дитини діагностовано нематодоз: після проведення антипаразитарної терапії симптоми кропив’янки значно зменшилися. У 3 дітей хронічна кропив’янка була асоційована з дією фізичних факторів.
Призначене лікування. Лікування дітей з хронічною кропив’янкою проводили відповідно до рекомендацій EAACI/GA2LEN/EDF/WAO, ключовими препаратами за якими є антигістамінні засоби ІІ покоління. Тривалість терапії – 8-12 тижнів.
Результати:
- у 44% пацієнтів терапія стандартною дозою АГП ІІ покоління була ефективною для полегшення симптомів хронічної кропив’янки; медіана часу контролю симптомів захворювання становила 8 місяців (95% довірчий інтервал – ДІ – 5,40-10,60);
- 56% пацієнтів було переведено на 2-й крок лікування кропив’янки; найпоширенішою тактикою лікування було підвищення дози АГП (19%), рідше терапію АГП ІІ покоління доповнювали іншими лікарськими засобами, такими як Н2-блокатори, АГП І покоління, антагоністи лейкотрієнових рецепторів (згідно з оновленими рекомендаціями EAACI/GA2LEN/EDF/WAO 2018 р., 2-й крок лікування кропив’янки не передбачає застосування інших препаратів, окрім АГП ІІ покоління);
- медіана часу контролю симптомів захворювання у пацієнтів, терапія яких відповідала 2-му кроку лікування, становила 10 місяців (95% ДІ 8,67-11,33);
- при аналізі медичної документації не було виявлено випадків потреби застосування засобів, передбачених 3-м та 4-м кроками терапії, та системних кортикостероїдів;
- при порівнянні медіани часу досягнення контролю симптомів хронічної кропив’янки у пацієнтів з ангіонабряком (n=32) та без нього (n=68) виявлено, що у першому випадку вона становила 10 місяців (95% ДІ 8,15-11,85), у другому – 9 місяців (95% ДІ 6,80-11,20).
Обговорення та висновки дослідження
Результати цього дослідження демонструють, що майже у половини хворих дітей (44%) контроль симптомів хронічної кропив’янки досягався завдяки застосуванню стандартних доз АГП ІІ покоління, ще у 19% – позитивна клінічна динаміка була зафіксована при підвищенні дози АГП.
Ці дані порівнянні з такими інших міжнародних досліджень. Наприклад, у недавньому багатоцентровому сліпому проспективному рандомізованому дослідженні, проведеному в 2 колумбійських містах за участю 150 хворих старше 12 років з хронічною кропив’янкою, лікування яких здійснювали згідно з рекомендаціями EAACI/GA2LEN/EDF/WAO, отримано такі результати: у 59% пацієнтів досягнуто відповідь на лікування стандартними дозами АГП ІІ покоління, у 17% – на терапію підвищеними дозами АГП ІІ покоління, у 15% хворих хороша клінічна відповідь спостерігалася на тлі застосування омалізумабу та циклоспорину (J. Sanchez et al., 2018).
Слід зазначити, що при аналізі досліджень, які стосувалися лікування дорослих та дітей, прослідковували деякі відмінності. У більшості випадків адекватний контроль симптомів кропив’янки у дорослих пацієнтів досягався на тлі введення стандартних чи відкоригованих доз АГП ІІ покоління, хоча 15-44% хворих потребували доповнення терапевтичної схеми імуномодулювальними агентами (P. Amin et al., 2015; I. Marin-Cabanas et al., 2017; J. Sanchez et al., 2018). У проспективному дослідженні Lee та співавт., проведеному в Сінгапурі за участю 98 дітей, у половини пацієнтів контроль симптомів хронічної кропив’янки був досягнутий шляхом застосування стандартних доз АГП ІІ покоління, в решти 36, 6 та 5% хворих клінічна відповідь була отримана при 2-, 3- та 4-разовому підвищенні дози препарату відповідно. Жоден з учасників дослідження не потребував застосування омалізумабу чи циклоспорину (X.H. Lee et al., 2016).
Примітно, що середній час досягнення контролю симптомів захворювання у дорослих і дітей також відрізнявся. У дослідженні Р. Amin та співавт. (2015) середній час контролю симптомів становив 1,4-2,7 року, тоді як у випробуванні Lee та співавт. на тлі лікування дітей стандартною, 2-, 3- та 4-кратно збільшеною дозою АГП ІІ покоління середній час становив 2; 8; 9,5 та 14,5 тижня відповідно. У цьому дослідженні медіана часу контролю симптомів захворювання становила 9 місяців, що значно менше, ніж у дослідженні Lee та співавт.
У низці досліджень показано, що гірша відповідь на терапію АГП спостерігається у разі виявлення у пацієнтів хронічної індукованої кропив’янки, ангіонабряку, позитивного результату аутогомологічного шкірного тесту з аутологічною сироваткою (P. Amin et al., 2015; I. Marin-Cabanas et al., 2017; E. Kocaturk et al., 2017; E. Toubi et al., 2004).
Таким чином, АГП ІІ покоління – це препарати вибору для лікування кропив’янки у дітей, у тому числі хронічної, що продемонстровано у низці досліджень і рекомендаціях EAACI/GA2LEN/EDF/WAO. Слід зазначити, що у більшості випадків для досягнення адекватного контролю симптомів хронічної кропив’янки у дітей достатнім є застосування стандартних чи підвищених доз АГП ІІ покоління.
Антигістамінні препарати ІІ покоління: який обрати?
Нові тенденції торкнулися не лише базових принципів діагностики алергічних захворювань та лікування пацієнтів з ними, а й фармакології. Блокатори Н1-гістамінових рецепторів І покоління мають деякі властивості, які обмежують їх широке застосування: антихолінергічний ефект, вплив на центральну нервову систему, також вони не можуть бути призначені для тривалого прийому.
Водночас АГП ІІ покоління позбавлені цих небажаних ефектів, тому їх поява на ринку стала справжнім проривом у лікуванні пацієнтів з алергічними захворюваннями. Серед широкого переліку цих засобів особливої уваги заслуговують активні метаболіти Н1-АГП (наприклад, левоцетиризин).
Левоцетиризин – це активний стабільний R-енантіомер цетиризину, який належить до групи конкурентних антагоністів гістаміну. Перевагами препарату є висока спорідненість з Н1-рецепторами, виражений антиалергічний, протисвербіжний, протизапальний ефекти при відсутності антихолінергічної та антисеротонінової дії, швидка та тривала дія.
Левоцетиризин – це препарат, який добре зарекомендував себе при лікуванні алергічного риніту та кропив’янки у дітей та дорослих, у тому числі й хронічної. Препарат левоцетиризину зручний для прийому – лише 1 раз на добу, його можна застосовувати тривалий час.
Сучасні стратегії лікування алергічних захворювань потребують застосування сучасних лікарських засобів. АГП ІІ покоління, зокрема їхні активні метаболіти (наприклад, левоцетиризин), безсумнівно, є оптимальними для лікування кропив’янки у дітей, зокрема і хронічної, що підтверджено даними доказової медицини.
Підготувала Ілона Цюпа
Тематичний номер «Педіатрія» №2 (49), травень 2019 р.