10 вересня, 2019
Ведение пациентов с острым коронарным синдромом с элевацией сегмента ST в свете последних рекомендаций Европейского общества кардиологов
Острый коронарный синдром (ОКС) – совокупность симптомов, которые позволяют заподозрить развитие острого инфаркта миокарда (ОИМ). Настоящая классификация ОКС основана на простом клиническом признаке (наличии элевации сегмента ST на ЭКГ), однако позволяет разделить всех пациентов на две большие группы, характеризующиеся особенностями развития, клинического течения заболевания, кратковременного и длительного прогноза. В основе ОКС с элевацией сегмента ST лежит полное закрытие коронарной артерии (КА) тромбом, которое, как правило, приводит к развитию крупноочагового повреждения миокарда (ОИМ с зубцом Q). Лечение этой категории пациентов в ранние сроки заболевания состоит в безотлагательном открытии инфарктобусловливающей КА механическим (ангиопластика) или медикаментозным (фибринолитическая терапия) методом, восстановлении микроциркуляции и защите миокарда от реперфузионного повреждения. Далее проводят профилактику и лечение осложнений ОИМ. В 2017 г. обновлены рекомендации Европейского общества кардиологов (ESC) по ведению пациентов с ОКС с элевацией сегмента ST. В статье на клиническом примере рассмотрены основные принципы ведения больного ОКС с элевацией сегмента ST в соответствии с обновленными рекомендациями.
Пациент, 68 лет, частный предприниматель, доставлен каретой скорой помощи с жалобами на интенсивные боли в грудной клетке, умеренную одышку, слабость через примерно 6 ч от развития заболевания. Боли в грудной клетке развились впервые в жизни. В анамнезе более 10 лет отмечал повышение артериального давления (АД) до 150/90 мм рт. ст., однако регулярно терапию не применял. Более пяти лет не курит, сахарный диабет (СД) ранее не диагностировался, уровень холестерина не знает. В анамнезе не было значимых кровотечений, язвенная болезнь желудка (двенадцатиперстной кишки) ранее не диагностировалась, однако отмечались явления гастрита.
На догоспитальном этапе снята электрокардиограмма (ЭКГ), выставлен диагноз ОКС с элевацией сегмента ST в области передней стенки левого желудочка (ЛЖ), и пациент в ургентном порядке был доставлен в наш центр для проведения реперфузионной терапии. До поступления в стационар больной получил 300 мг клопидогреля и 250 мг ацетилсалициловой кислоты (АСК) перорально, в/в введен НФГ в дозе 5000 МЕ. Для купирования болевого синдрома введен морфин, налажена в/в инфузия нитроглицерина.
Комментарий
В новых рекомендациях ESC четко прописана логистика оказания первой помощи пациентам с элевацией сегмента ST [1]. За точку отсчета – «нулевое» время – выбрано время первого медицинского контакта (ПМК). Именно с этого момента включается секундомер медицинского этапа оказания помощи, а соблюдение рекомендуемых временных интервалов характеризует качество предоставления медицинских услуг. Под ПМК следует понимать момент, когда пациента впервые осмотрел врач, парамедик, медсестра или другой обученный персонал, который может снять и интерпретировать ЭКГ и оказать неотложную помощь (например, выполнить дефибрилляцию). ПМК может произойти как догоспитально, так и по приезде пациента в больницу (например, в приемном покое). В соответствии с рекомендациями ЭКГ у пациента с болью в грудной клетке должна быть записана и проанализирована в течение первых 10 мин от ПМК. В дальнейшем пациент с уже подтвержденным диагнозом ОКС с элевацией сегмента ST должен быть направлен в реперфузионный центр для проведения первичного чрескожного коронарного вмешательства (ПЧКВ). При этом время от постановки диагноза до открытия коронарной артерии (КА) не должно превышать 60 мин, если пациент сразу обратился в реперфузионный центр, или 90 мин, если ПМК был вне реперфузионного центра (большинство пациентов). Максимальное время между постановкой диагноза STEMI и ПЧКВ не должно превышать 120 мин. Если это условие не может быть выполнено, независимо от причин следует немедленно (в пределах 10 мин от постановки диагноза) начать фибринолитическую терапию (при отсутствии противопоказаний).
В нашем случае временные интервалы на догоспитальном этапе были соблюдены и уже через 48 мин после регистрации первой ЭКГ пациент был госпитализирован. При поступлении АД – 140/100 мм рт. ст.; частота сердечных сокращений (ЧСС) – 81 уд./мин; сатурация кислорода по данным пульсоксиметрии (без ингаляции кислорода) – 94%. Дополнительных тонов и шумов при аускультации сердца выявлено не было. В легких определялось жесткое дыхание, влажные хрипы не выслушивались (острая левожелудочковая недостаточность [ОЛЖН], Killip I). ЭКГ на момент поступления представлена на рисунке 1.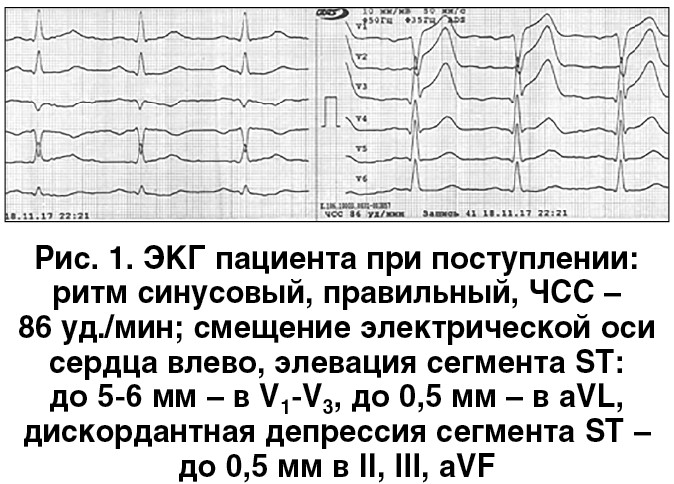
Установлен предварительный диагноз ОКС со стойкой элевацией сегмента ST, пациент помещен под мониторное наблюдение, продолжено в/в введение нитратов.
Комментарий
В новых рекомендациях ЕОК изменены показания к проведению оксигенотерапии при ОКС [1]. Оксигенотерапия должна проводиться только в случае значимой гипоксемии (SaO2 <90%, PaO2 <60 мм рт. ст.). Данные нескольких исследований свидетельствуют о том, что гипероксия может оказывать дополнительное повреждающее действие на миокард у пациентов с неосложненным инфарктом [2-4]. Поэтому рутинное назначение кислорода больным с ОКС и сатурацией SaO2 ≥90% по данным пульсоксиметрии не рекомендовано. Таким образом, оксигенотерапия нашему пациенту не проводилась.
Уже на догоспитальном этапе была начата двойная антитромбоцитарная терапия (ДАТ): даны нагрузочные дозы клопидогреля (300 мг) и АСК (250 мг). Однако у пациентов с ОКС с элевацией сегмента ST перед проведением ПЧКВ рекомендовано назначение новой генерации блокаторов P2Y12 – тикагрелора или прасугреля (класс рекомендации I, уровень доказательности А) [1]. Это обусловлено их более быстрым и сильным антитромбоцитарным эффектом, что позволяет избежать развития тромботических осложнений как во время интервенционного вмешательства, так и в ходе дальнейшего лечения [5].
В Украине на сегодня из указанных выше препаратов доступен только тикагрелор. Это синтетический антитромбоцитарный препарат, который стал родоначальником новой группы – триазолопиримидинов. В отличие от тиенопиридинов (клопидогреля, тиклопидина, прасугреля), тикагрелор является не пролекарством, а метаболически активным препаратом. Блокада тромбоцитарных рецепторов на фоне его применения имеет обратимый характер, что обусловливает постепенное восстановление функции Р2Y12-рецепторов тромбоцитов после отмены препарата. Благодаря этим свойствам тикагрелор характеризуется быстрым развитием антитромбоцитарного эффекта, а при его отмене наблюдается более быстрое восстановление функции тромбоцитов [6].
Клиническая эффективность препарата у пациентов с ОКС изучалась в исследовании PLATO, в которое были включены более 18,5 тыс. пациентов [5]. Применение тикагрелора (по сравнению с клопидогрелем) в составе ДАТ в течение года после ОКС позволяло достоверно снизить вероятность развития больших сердечно-сосудистых осложнений. Так, частота наступления первичной конечной точки исследования (комбинации «смерть от сердечно-сосудистых причин / ИМ / инсульт») была снижена на 16% (95% доверительный интервал [ДИ] 0,77-0,92; p<0,001). Прием тикагрелора также приводил к существенному уменьшению вероятности развития нефатального ИМ (относительный риск [ОР] 0,84; ДИ 0,75-0,95; p=0,005), смерти от сердечно-сосудистых причин (ОР 0,79; ДИ 0,69-0,91; p=0,001) и смерти от всех причин (ОР 0,78; ДИ 0,69-0,89; p<0,001) без значимого увеличения общего количества больших кровотечений (ОР 1,04; ДИ 0,95-1,13; p=0,43). В то же время в исследовании было показано, что прием тикагрелора как более сильного антитромбоцитарного препарата сопровождался увеличением количества спонтанных (в том числе больших спонтанных) кровотечений [7].
После изменения клинических рекомендаций в ряде стран Европы тикагрелор занял лидирующие позиции в лечении пациентов с ОКС, и результаты исследования PLATO нашли подтверждение в реальной клинической практике, по данным одноцентровых, многоцентровых и национальных регистров на большом количестве пациентов (SWEDEHEART – 45 073, SHEFFIELD RWE – 10 793, Western Denmark Heart Registry – 2335, ESTATE – 928 больных и др.) [8-10]. Анализ имеющихся данных показал, что тикагрелор одинаково эффективен и должен использоваться у пациентов с элевацией сегмента ST, которым планируется проведение ПЧКВ, а также при ОКС без элевации сегмента ST независимо от выбранной стратегии [5]. В новых рекомендациях ЕОК тикагрелор и прасугрель указаны также как препараты выбора у лиц с ОИМ с элевацией сегмента ST c поздним (более 12 ч) и очень поздним (более 48 ч от развития симптоматики заболевания) поступлением, которым проводится ЧКВ (табл. 1). Перевод на прием тикагрелора или прасугреля (вместо клопидогреля) через 48 ч после фибринолитической терапии также может рассматриваться у пациентов со STEMI, у которых применялась фармакоинвазивная стратегия реперфузии (фибринолизис с последующей ЧКВ) (табл. 2). Однако данные рандомизированных исследований на этот счет в настоящее время отсутствуют. В испытании TREAT, результаты которого опубликованы в начале 2018 г. (уже после выхода рекомендаций ESC), у больных моложе 75 лет была изучена возможность более раннего (в среднем через 11,5 ч после ТЛТ) перехода с клопидогреля на тикагрелор у этой категории пациентов [11].
Таким образом, несмотря на нагрузочную дозу клопидогреля 300 мг на догоспитальном этапе, было принято решение о переводе пациента на прием тикагрелора, начиная с нагрузочной дозы 180 мг, с последующим приемом 90 мг каждые 12 ч.
Комментарий
Тиенопиридины и тикагрелор имеют разные точки взаимодействия с P2Y12-рецепторами тромбоцитов, поэтому использование клопидогреля на постоянной основе или прием его нагрузочной дозы на предшествующих этапах оказания медицинской помощи не является противопоказанием для назначения тикагрелора. Клиническая безопасность применения тикагрелора на фоне клопидогреля была подтверждена в исследовании PLATO, в котором около половины пациентов получили клопидогрель до перевода на прием тикагрелора [5]. Данные нескольких исследований по фармакодинамике тикагрелора у лиц со стабильными формами ИБС свидетельствуют о том, что увеличить скорость наступления антитромбоцитарного эффекта препарата возможно путем предварительного (перед приемом) измельчения или тщательного пережевывания таблетки [12, 13].
На рисунке 2 представлен почасовой алгоритм ведения пациентов с ОКС с элевацией сегмента ST, которым проводится экстренное ПЧКВ в соответствии с рекомендациями ESC. В частности, отмечены время начала и длительность применения каждого из компонентов антитромбоцитарной терапии.
Использование новых сильных антитромбоцитарных препаратов предъявляет дополнительные требования к безопасности сопутствующей АКТ. Подходы к выбору антикоагулянта и длительности его назначения во многом определяются методом реперфузионной терапии. Согласно рекомендациям АКТ показана всем пациентам во время проведения ПЧКВ, причем приоритетным является использование нефракционированного гепарина (НФГ) (класс рекомендации I, уровень доказательности С), эноксапарина (IIа, А) или бивалирудина (IIа, А). НФГ вводится в/в болюсно из расчета 70-100 Ед/кг массы тела (50-70 Ед/кг массы тела при совместном использовании с блокаторами GPIIb/IIIa-рецепторов).
Возможность использования эноксапарина во время интервенционного вмешательства у больных со STEMI была доказана в исследовании ATOLL (n=910), в котором его введение в дозе 0,5 мг/кг массы тела в/в болюсно по сравнению с указанными дозами НФГ сопровождалось тенденцией к снижению частоты наступления первичной конечной точки (смерть в течение 30 дней / осложнение ИМ / неэффективность ЧКВ / большое кровотечение) (средний ОР 17%; р=0,063) и приводило к достоверному уменьшению частоты событий вторичной конечной точки (смерть / ИМ / нестабильная стенокардия / ургентная реваскуляризация – средний ОР 41%; р=0,01). При этом частота кровотечений в двух группах существенно не отличалась. Эноксапарин имел преимущества перед НФГ и по результатам метаанализа. В то же время фондапаринукс не рекомендован для использования во время ЧКВ, так как препарат повышал вероятность катетерного тромбоза во время процедуры в исследовании OASIS‑6 (класс рекомендации III, уровень доказательности B). Таким образом, нашему пациенту не назначали антикоагулянты при поступлении в отделение неотложной кардиологии (5000 МЕ НФГ догоспитально) с возможностью введения НФГ во время процедуры.
Больной при поступлении в стационар также получил 40 мг розувастатина и 40 мг пантопразола для профилактики желудочно-кишечных кровотечений (гастрит в анамнезе). Согласно схеме, представленной в рекомендациях ESC, статины рекомендованы пациентам с ОКС с элевацией сегмента ST в течение первых суток заболевания, однако после ПЧКВ (рис. 2). В то же время, полагаясь на быструю реализацию плейотропных эффектов (антитромбоцитарный, противовоспалительный, нормализация функции эндотелия и др.) статинов, а также основываясь на данных по предупреждению контраст-индуцированной нефропатии на фоне их приема у лиц с ОКС без элевации сегмента ST, мы назначаем высокие дозы аторвастатина или розувастатина всем пациентам с ОКС немедленно при поступлении в стационар [14]. Данные наших исследований подтверждают целесообразность такого подхода и свидетельствуют о лучшем восстановлении микроциркуляции после ПЧКВ и предупреждении развития синдрома no-reflow на фоне раннего назначения статинов в высоких дозах [15].
В 2018 г. опубликованы данные испытания SECURE PCI [16]. Хотя в исследовании не было показано существенного влияния на частоту сердечно-сосудистых событий раннего (до перкутанной транслюминальной коронарной ангиопластики) назначения интенсивной терапии статинами в общей группе лиц с ОКС, среди реваскуляризированных пациентов с элевацией сегмента ST применение аторвастатина в дозе 80 мг перед первичным вмешательством почти вдвое снижало вероятность событий первичной конечной точки (смерть / ИМ / инсульт / незапланированная реваскуляризация) в течение 30 дней наблюдения (ОР 0,54; 95% ДИ 0,35-0,84; p=0,01).
Высокий уровень доказательной базы на ранних этапах оказания помощи пациентам с ОКС с элевацией сегмента ST имеет также в/в назначение β-адреноблокаторов (класс рекомендации IIa, уровень доказательности А). В исследовании METOCARD-CNIC раннее (до реперфузии) в/в введение метопролола (15 мг) пациентам со STEMI передней локализации (без признаков ОЛЖН и АД >120 мм рт. ст.) ассоциировалось с уменьшением размера некроза по данным МРТ на 5-7-е сутки, более высокой фракцией выброса (ФВ) ЛЖ через 6 мес наблюдения и тенденцией к уменьшению частоты сердечно-сосудистых событий в течение двух лет наблюдения [17]. В исследовании EARLY-BAMI в/в введение меньших доз метопролола перед ПЧКВ не приводило к уменьшению размеров ИМ по данным МРТ, однако сопровождалось снижением частоты жизнеугрожающих желудочковых нарушений ритма [18]. В Украине длительное отсутствие / перебои с регистрацией в/в β-блокаторов привели к отсутствию опыта и боязни их применения у пациентов с ОКС на догоспитальном и раннем госпитальном этапах. В то же время часто назначаются пероральные β-адреноблокаторы, действие которых контролировать (при развитии блокад или гипотензии) значительно сложнее. В нашем случае пациент догоспитально получил 20 мг анаприлина, поэтому в/в введение β-блокаторов не проводилось и на раннем госпитальном этапе.
Задачами отделений неотложной кардиологии перед проведением ПЧКВ являются:
- подтверждение диагноза ОКС, а также более четкое уточнение сроков от начала заболевания;
- исключение других угрожающих жизни состояний (ТЭЛА, расслаивающая аневризма аорты, острая сердечная недостаточность [СН] и др.), которые могут сопровождаться болями в грудной клетке;
- стабилизация параметров центральной гемодинамики (по возможности);
- оценка и коррекция терапии, проведенной на догоспитальном этапе.
Мы не сторонники положения рекомендаций ESC относительно того, что пациенты с ОКС с элевацией сегмента ST должны напрямую поступать в катетеризационную лабораторию, однако поддерживаем мнение о том, что задержка времени на этом этапе должна быть минимальной. Большую помощь в решении поставленных задач на данном этапе имеет эхокрадиография (ЭхоКГ). Это исследование должно проводиться дежурным персоналом, желательно в месте первичного осмотра пациента. Зачастую достаточно проведения фокусной ЭхоКГ, нацеленной на выяснение причин неотложного состояния с качественной оценкой сократимости, что занимает в среднем до 2-4 мин времени. В данном случае диагноз ОКС не вызывал сомнений, поэтому ЭхоКГ не проводилась, а пациент без промедления был переведен в отделение интервенционной кардиологии. Задержка на этапе отделения неотложной кардиологии составила 14 мин; таким образом, общая задержка на медицинском этапе оказания помощи была 62 мин, что укладывается в рекомендованные сроки.
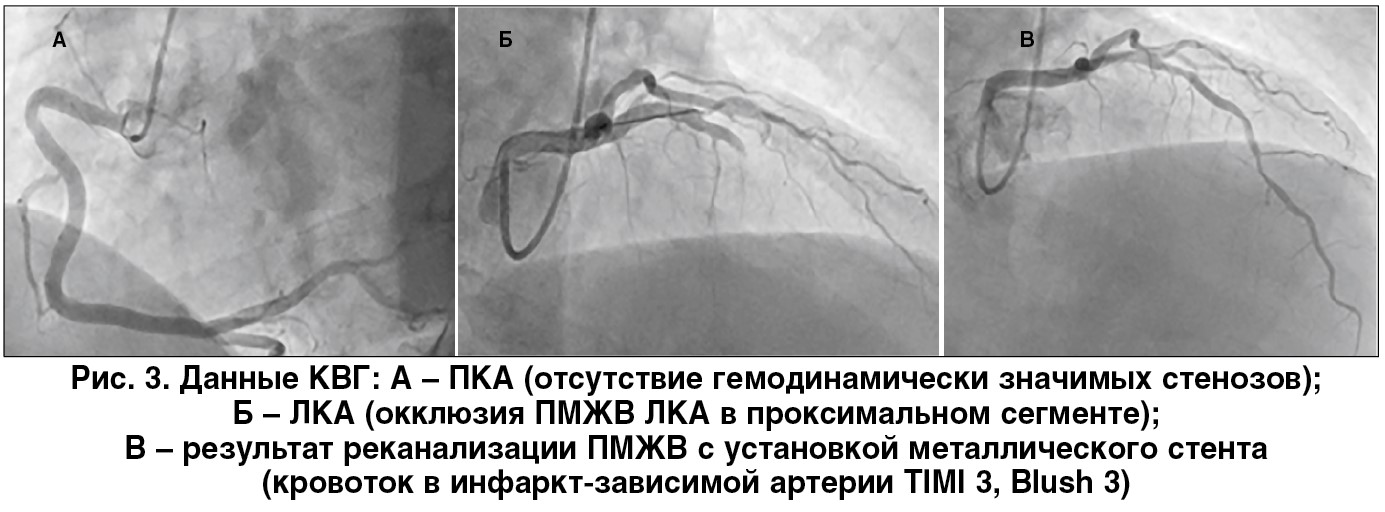
При проведении коронаровентрикулографии (рис. 3) выявлена окклюзия передней межжелудочковой ветви (ПМЖВ) в средней трети. Правая КА (ПКА) и огибающая ветвь левой (ЛКА) – без гемодинамически значимых сужений. Пациенту проведена реканализация инфарктобусловившей КА, установлен металлический стент. После открытия КА эпикардиальный кровоток соответствует TIMI 3, микроциркуляция не нарушена (Blush 3). При проведении вмешательства использовался радиальный доступ.
Комментарий
В целом ряде исследований, проведенных в последние годы (MATRIX, RIVAL, RIFLE-STEACS), были показаны преимущества данного доступа в отношении снижения вероятности кровотечений, сосудистых осложнений, а также смерти в условиях современной антитромботической терапии [19]. Поэтому, несмотря на ряд недостатков радиального доступа, связанных с большей лучевой нагрузкой (в первую очередь для медперсонала) и техническими особенностями проведения процедуры, именно радиальный доступ на сегодня является приоритетным для пациентов с ОКС (класс рекомендации I, уровень доказательности А). Преимущества покрытых стентов нового поколения перед голометаллическими, отмеченные в рекомендациях (I, А), обусловлены снижением количества повторных реваскуляризаций и тромбозов стента без существенного влияния на выживаемость больных. Поэтому в нашем центре вопрос о выборе стента решается индивидуально для каждого пациента на основании морфологических особенностей атеросклеротического повреждения и его локализации, а также сопутствующих патологий и состояния больного.
После реваскуляризации пациент в стабильном состоянии был возвращен в отделение неотложной кардиологии для дальнейшего лечения. Больной помещен под мониторное наблюдение. Продолжено применение ДАТ (тикагрелор + АСК), пантопразола, розувастатина, назначены тестирующие дозы β-блокатора и ингибитора ангиотензинпревращающего фермента. В ходе ЭхоКГ-исследования выявлено умеренное снижение ФВ ЛЖ до 42%, однако с учетом передней локализации ИМ пациенту на следующее утро назначен эплеренон в начальной дозе 25 мг/сут.
Во время проведения интервенционного вмешательства пациент дополнительно получил 10 тыс. МЕ гепарина (110 МЕ/кг массы тела), что несколько превышает рекомендованные дозы.
Комментарий
Описанные выше рекомендации по назначению АКТ касались только периода перед и во время проведения ПЧКВ. После ЧКВ рутинное назначение АКТ не показано, кроме случаев с другими показаниями для полнодозовой (ФП, механические клапаны или внутриполостное тромбообразование) или профилактической антикоагуляции (профилактика ВТЭ у лиц с пролонгированным постельным режимом). Большинство пациентов со STEMI, которые находятся на строгом постельном режиме, попадают в группу высокого риска развития венозных тромбоэмболических осложнений (оценка по шкале Падуя ≥4 или IMPROVE ≥2 баллов) и поэтому нуждаются в назначении профилактических доз антикоагулянтных препаратов. В соответствии с рекомендациями Американской коллегии торакальных хирургов (ACCP, 2012), для тромбопрофилактики у терапевтических пациентов может использоваться подкожное назначение 40 мг/сут эноксапарина, 2,5 мг/сут фондапаринукса либо низких доз НФГ [20]. Более ранняя мобилизация пациентов с неосложненным ОИМ (что также прописано в руководстве) позволяет избежать назначения антикоагулянтов после проведения ПЧКВ. Мы также часто назначаем профилактические дозы антикоагулянтов пациентам с многососудистым поражением, ОЛЖН и передней локализацией ИМ (профилактика внутриполостного тромбообразования). Нашему пациенту был назначен эноксапарин 40 мг/сут подкожно, первая доза препарата была введена через 4 ч после интервенционного вмешательства.
На фоне проводимой терапии состояние пациента стабилизировалось, боли ангинозного характера не рецидивировали, признаков СН не было. На 5-й день заболевания он переведен в плановое отделение для реабилитации. Лечение на момент перевода (суточная доза): 100 мг АСК, 90 мг тикагрелора два раза в сутки, 40 мг розувастатина, 5 мг бисопролола, 5 мг рамиприла, 25 мг эплеренона.
Комментарий
Одним из наиболее изучаемых на сегодняшний день является вопрос длительной поддерживающей антитромбоцитарной терапии у пациентов с ОКС после проведения ПЧКВ. По данным коронароангиографии (КАГ) и внутрисосудистого УЗИ лица с ОКС зачастую характеризуются дестабилизацией нескольких атеросклеротических бляшек и не только в инфарктобусловившей КА [21]. Даже после выписки из стационара эти пациенты имеют существенно более высокий риск развития тромботических осложнений в различных сосудистых бассейнах, чем таковые со стабильными формами ИБС.
Все это свидетельствует о системной предрасположенности к дестабилизации атеросклероза и позволяет говорить, скорее, не о локально нестабильной атеросклеротической бляшке, ставшей причиной ОИМ, а о нестабильном пациенте. Поэтому интенсивность и длительность антитромбоцитарной терапии у больных ОКС определяют не характеристики причинного атеросклеротического поражения и вид установленного стента, а сам факт перенесенного ОИМ. Согласно рекомендациям все пациенты с ОИМ независимо от метода реваскуляризации должны получать ДАТ в течение первых 12 мес, и сокращение этого срока до 6 мес возможно только у лиц с высоким риском кровотечений [1, 22].
В то же время использование клинических шкал для оценки риска кровотечений и тромботических событий с последующей оценкой оптимальной длительности ДАТ имеет низкий класс рекомендаций (IІb, А). Для оценки риска кровотечений рекомендовано использовать шкалу PRECISE DAPT [23]. Если пациент набирает ≥25 баллов, риск кровотечений рассматривается как высокий, что свидетельствует о том, что он может выиграть от сокращения длительности ДАТ. Тем не менее высокий риск ишемических событий (может быть оценен по шкале DAPT) рассматривается как критерий для пролонгации ДАТ свыше 1 года [24]. Такой подход тестировался в исследованиях DAPT (тиенопиридины) и PEGASUS (тикагрелор) и доказал свою эффективность [25, 26].
В соответствии с рекомендациями назначение сильного блокатора P2Y12-рецепторов (тикагрелора) рекомендовано совместно с АСК в течение как минимум 12 мес после развития ОКС с элевацией сегмента ST (при отсутствии высокого риска кровотечений). Именно такие рекомендации были даны нашему пациенту перед выпиской.
Список литературы находится в редакции.
Спецвипуск «Клінічні випадки та сценарії у невідкладній кардіології», вересень 2019 р