8 жовтня, 2019
Сучасна тактика ведення хворих на жовчнокам’яну хворобу до і після холецистектомії: роль урсодезоксихолевої кислоти
Жовчнокам’яну хворобу (ЖКХ) вважають хворобою цивілізації, поширеність якої подвоюється що 20 років. В Україні за останні 10 років її розповсюдженість збільшилася на 97,5%, а захворюваність – на 64,7%. У 80-95% випадків лікування ЖКХ закінчується оперативним втручанням. Щорічно у світі проводять 2,5 млн холецистектомій (ХЕ) (Степанов Ю. М., 2012; Гойда С. М., 2011; Томаш О. В. і співавт., 2013). У 15-40% випадків ХЕ призводить до формування симптомокомплексу, відомого як постхолецистектомічний синдром (ПХЕС), що найчастіше виявляє себе дисфункцією сфінктера Одді (Степанов Ю. М., 2012; Шевченко Б. Ф., Бабий А. М., 2013; Madácsy L. et al., 2006).
 Проблемі лікування ЖКХ до і після ХЕ було присвячено доповідь професора кафедри пропедевтики внутрішніх хвороб ДВНЗ «Ужгородський національний університет», доктора медичних наук Єлизавети Степанівни Сірчак на науково-практичній конференції з міжнародною участю «VII наукова сесія Інституту гастроентерології НАМН України. Новітні технології в теоретичній і клінічній гастроентерології» (13-14 червня, м. Дніпро).
Проблемі лікування ЖКХ до і після ХЕ було присвячено доповідь професора кафедри пропедевтики внутрішніх хвороб ДВНЗ «Ужгородський національний університет», доктора медичних наук Єлизавети Степанівни Сірчак на науково-практичній конференції з міжнародною участю «VII наукова сесія Інституту гастроентерології НАМН України. Новітні технології в теоретичній і клінічній гастроентерології» (13-14 червня, м. Дніпро).
Розрізняють три види жовчних каменів: холестеринові (до 80%) – блідо-жовтого кольору з видимими кристалами холестерину (ХС) на розрізі; пігментні (10-20%) – темно-коричневого або чорного кольору, які переважно формуються з білірубіну за умов гемолізу або цирозу печінки; вапняні, що переважно утворюються за наявності запального процесу в жовчному міхурі та складаються з вуглекислого вапна.
До факторів ризику ЖКХ належать: зрілий і старечий вік (хоча за останні роки хвороба значно «помолодшала», бо дедалі частіше трапляються пацієнти юнацького віку, котрим уже провели ХЕ); обтяжена спадковість; гормональні порушення (вагітність, клімакс); порушення харчування (надмірне вживання жирів та рафінованих вуглеводів), тривале голодування або парентеральне харчування, різкі зміни маси тіла; метаболічні розлади (дисліпідемія, ожиріння, цукровий діабет, атеросклероз); вплив лікарських засобів (пероральні контрацептиви, естрогени, сандостатин, цефтріаксон тощо).
Щодо гендерної схильності, то холестеринові конкременти у 2-3 рази частіше формуються у жінок фертильного віку, що пояснюється здатністю естрогенів посилювати секрецію ХС у жовч (Wang H. еt al., 2009). Описано навіть відповідні фенотипи жінок, окреслені формулами Дивера (п’ять «F») та Торека (сім «F»): Female (жінка), Fat (повна), Forty (40 років і більше), Fertile (фертильного віку, вагітності в анамнезі), Fair (блондинка), Flabby (з відвислим черевом), Flatulent (страждає від газів).
Як відомо, у нормі ХС у жовчі «упакований» у міцели – надмолекулярні циліндричні структури, зовнішню оболонку яких складають жовчні кислоти (ЖК), а всередині, окрім ХС, міститься щонайменше сім молекул лецитину. Порушення цілісності міцел призводить до потрапляння жиророзчинного ХС у водне середовище (адже жовч на 95% складається з води), де він спочатку утворює мікрокристали, які згодом з’єднуються в більші кристали, що з них формується конкремент. Отже, патогенетичною передумовою утворення каменів є порушення рівноваги між основними компонентами жовчі – ХС і ЖК. Сучасний стиль життя, нераціональне харчування, метаболічні розлади сприяють нагромадженню ХС та зрушенню реакції жовчі в кислий бік, що створює сприятливі умови для порушення структури міцел, випадання ХС в осад та кристалізації. Це все посилюється за умов застою жовчі та запальних змін у жовчному міхурі.
Є три способи запобігти кристалізації ХС: зниження вмісту ХС, підвищення вмісту ЖК або лецитину. Застосування урсодезоксихолевої кислоти (УДХК) забезпечує одразу два позитивні впливи – пригнічення синтезу ХС у печінці та стимуляцію синтезу ЖК, що суттєво покращує співвідношення цих речовин у складі жовчі. Як відомо, УДХК є третинною нетоксичною ЖК, холеретичний ефект якої забезпечується конкурентним витісненням токсичних ЖК. Крім того, стимулюючи мітоген-активовану протеїнкіназу, УДХК посилює утворення бікарбонатів, а також стимулює екзоцитоз шляхом кальцій-залежної протеїнкінази. Проведені дослідження свідчать, що тривале використання УДХК у дозі 12 мг/кг/добу нормалізує склад ЖК у жовчі, суттєво зменшуючи вміст літогенних ЖК та підвищуючи вміст УДХК від 1 до >50% (Roda A. et al., 1975, 1982).
Якщо йдеться про літолітичну терапію, то до неї вдаються тільки за умов неускладненого перебігу хвороби, контрастування жовчного міхура при холецистографії, при нормальній, збереженій скоротливій функції жовчного міхура, наявності рентгенопрозорих холестеринових каменів до 15 мм у діаметрі, якщо це поодинокі конкременти або ≤5 мм, якщо це множинні дрібні камені, а також при високій літогенності жовчі, резидуальному холелітіазі у хворих з високим оперативним ризиком або при категоричній відмові пацієнта від операції. Літолітична терапія передбачає УЗД‑контроль через 3-6 міс від початку проведення. Доза УДХК має становити 10-15 мг/кг. За відсутності ефекту протягом 6 міс продовжувати лікування немає сенсу, але якщо ефект позитивний, уживання УДХК треба продовжувати (тривалістю до 1-2 років).
Здебільшого лікування завершується ХЕ. Проте операція також не гарантує стовідсотково позитивного результату.
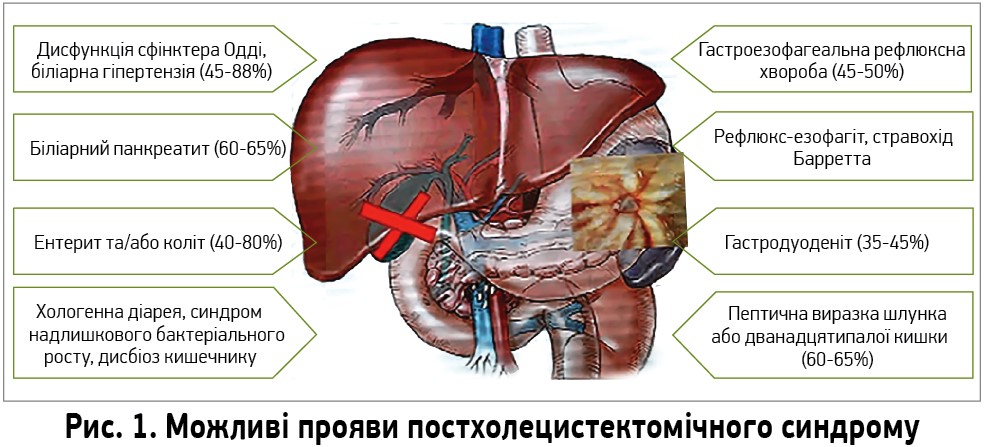
Прояви ПХЕС. Стан пацієнтів після ХЕ дуже варіабельний. Покращення спостерігається в 46% випадків. У 25% пацієнтів надалі виникають симптоми біліарної диспепсії. Погіршення стану та збільшення частоти епізодів біліарного болю можливі майже в половини прооперованих. Рецидив ЖКХ упродовж п’яти років виникає практично в кожного десятого пацієнта, а у 20-40% випадків протягом цього періоду спостерігаються прояви больового та диспептичного синдромів різного ступеня тяжкості (Губергриц Н. Б., 2013; Лазебник Л. Б. и соавт., 2004). Найчастіше прояви визначаються після видалення функціонуючого жовчного міхура. Переважають функціональні розлади (25-60% випадків), хоч у 7,6% пацієнтів можуть виникнути органічні зміни. До таких ускладнень більш схильні жінки (Степанов Ю. М., 2012; Шевченко Б. Ф., Бабий А. М., 2013; Madácsy L. et al., 2006).
Найбільш частим функціональним проявом ПХЕС є дисфункція сфінктера Одді, яку поділяють на біліарний та панкреатичний типи. Спільними ознаками останніх є диспептичні прояви та біль. У пацієнтів із біліарним типом діаметр жовчної протоки перевищує 8-12 мм, час виділення контрасту при ендоскопічній ретроградній холангіопанкреатографії становить понад 45 хв, рівні лужної фосфатази в крові та/або активність трансаміназ (АлАТ, АсАТ) у крові підвищені. При панкреатичному типі діаметр панкреатичної протоки перевищує 5 мм, час надходження секрету панкреатичною протокою до дванадцятипалої кишки (ДПК) становить >10 хв, активність амілази/ліпази в крові підвищена (Римські критерії IV, 2016).
Прояви ПХЕС переважно стосуються гастродуоденальної і панкреатичної зон (рис. 1). Найбільш поширеними механізмами їх виникнення є хронічна дуоденальна непрохідність, зумовлена гіпертензією у просвіті ДПК, дуоденогастральний та/або гастроезофагеальний рефлюкси, мікробна контамінація ДПК, порушення чи асинхронність надходження жовчі, хімусу і панкреатичного секрету в ДПК. В окремих пацієнтів такі функціональні зміни можуть спричиняти біліарний панкреатит або вторинну панкреатичну недостатність (Губергриц Н. Б., 2013; Ивашкин В. Т., 2002). Тому медикаментозна терапія ПХЕС має бути спрямована на нормалізацію функціонального стану сфінктерного апарату жовчовивідних шляхів і забезпечення адекватного відтоку жовчі і панкреатичного секрету в ДПК за допомогою міотропних спазмолітиків та УДХК; нормалізацію гастродуоденальної моторики, рН і тиску в ДПК за допомогою міотропних спазмолітиків та інгібіторів протонної помпи (ІПП); лікування і профілактику рецидивів панкреатиту, рефлюкс-індукованих уражень слизової оболонки ДПК, шлунка і стравоходу шляхом призначення ІПП, УДХК, міотропних спазмолітиків та прокінетиків; нормалізацію структурно-функціонального стану печінки, складу жовчі й жовчовиділення, що забезпечується призначенням УДХК та рослинних препаратів.
Видалення жовчного міхура разом із конкрементами не розв’язує проблеми подальшого їх утворення, тому що операція не усуває метаболічних розладів в організмі. У 15-20% пацієнтів спостерігається подальше утворення каменів у різних відділах жовчовивідної системи, зокрема в печінкових протоках, загальній жовчній протоці (холедохолітіаз) або у Фатеровому сосочку (Madácsy L. et al., 2006). Тому після операції показане постійне подальше спостереження, а основною метою лікування в післяопераційний період є нормалізація харчування та призначення препаратів, які покращують фізико-хімічний склад жовчі. Дія УДХК при захворюваннях печінки та холестатичних розладах ґрунтується на відносній заміні ліпофільних, детергентоподібних токсичних ЖК на гідрофільну, цитопротекторну нетоксичну УДХК, а також на покращенні секреторної спроможності клітин печінки та процесів імунорегуляції.
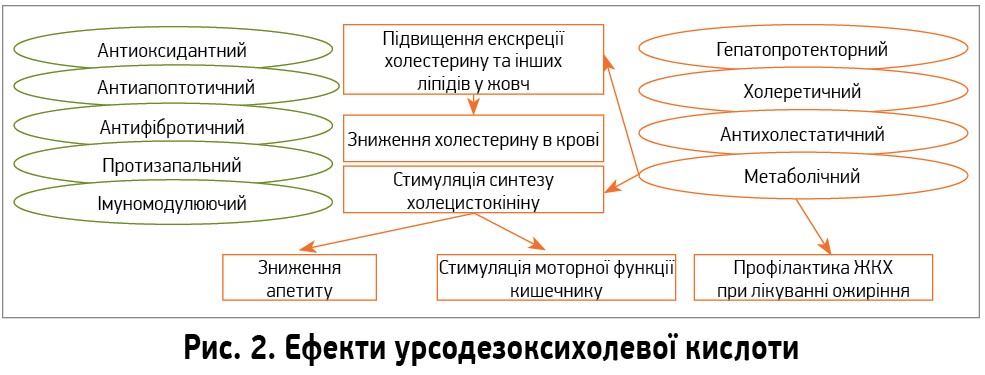
Треба зазначити багатогранність дії УДХК: гепатопротекторний, холеретичний, антиоксидантний, антиапоптотичний, імуномодулюючий, протизапальний, антифібротичний та антихолестатичний ефекти і позитивний вплив на метаболічні процеси (рис. 2). У високих дозах (>25 мг/кг) за умов уживання від 6 міс до 2 років УДХК забезпечує гіполіпідемічний та літолітичний ефекти – знижує вміст у крові загального ХС, ЛПНЩ, тригліцеридів та підвищує вміст ЛПВЩ, а також забезпечує зниження літогенності жовчі, стимулює вихід ХС із каменів у жовч, а отже, запобігає утворенню каменів (Mazella G. et al., 1992).
Отже, лікування хворих на ЖКХ має бути комплексним, поетапним і спрямованим на зменшення вираженості клінічної симптоматики та нормалізацію фізико-хімічних властивостей жовчі (препарати УДХК) як до, так і після оперативного втручання. На вітчизняному ринку УДХК представлена препаратом Урсофальк (Dr. Falk Pharma GmbH, Німеччина), який завдяки високій якості гарантує ефективність на всіх етапах ведення пацієнтів із ЖКХ – як до, так і після ХЕ. Після операції Урсофальк призначають для профілактики функціональних та органічних порушень гепато-панкреато-біліарної зони та рецидивів ЖКХ.
Підготувала Ольга Королюк
Медична газета «Здоров’я України 21 сторіччя» № 17 (462), вересень 2019 р.