8 жовтня, 2019
Эффективность и безопасность комбинированной гепатопротекции при хронических токсических поражениях печени
 В спектре острых и хронических диффузных заболеваний печени важное место занимают токсические поражения на фоне хронического злоупотребления алкоголем (алкогольная болезнь печени – АБП) и воздействия различных медикаментов (медикаментозно-индуцированные поражения печени – МИПП), частота которых в последние десятилетия растет. Так, распространенность АБП возросла с 1,38% в 1988-1994 гг. до 2,21% в 2005-2008 гг. [3].
В спектре острых и хронических диффузных заболеваний печени важное место занимают токсические поражения на фоне хронического злоупотребления алкоголем (алкогольная болезнь печени – АБП) и воздействия различных медикаментов (медикаментозно-индуцированные поражения печени – МИПП), частота которых в последние десятилетия растет. Так, распространенность АБП возросла с 1,38% в 1988-1994 гг. до 2,21% в 2005-2008 гг. [3].
В то время как смертность от рака и кардиоваскулярной патологии в развитых странах падает, стандартизированная возрастзависимая летальность вследствие АБП по сравнению с серединой 1970-х гг. возросла примерно в 5 раз. При оценке распространенности АБП лучше всего использовать термин «эпидемия», поскольку ее частота во многих странах очень высока. Это не кажется удивительным с учетом того, что хроническая алкогольная зависимость в развитых странах мира – довольно частое явление. Например, большинство населения США употребляет алкоголь, причем в 1 из 10 случаев речь идет о так называемом тяжелом пьянстве (≥3 напитков ежедневно). Цирроз печени в большинстве развитых стран в структуре причин смерти находится на 5-6-м месте. Алкогольный цирроз печени в перечне наиболее распространенных причин смерти в США занимает 6-ю позицию и является 2-й по значимости причиной летального исхода среди всех заболеваний желудочно-кишечного тракта (ЖКТ). Это очень важная проблема, поскольку многие пациенты умирают от АБП в молодом и среднем, то есть наиболее трудоспособном, возрасте [3, 12, 16]. К счастью, только у меньшинства тяжело пьющих людей развиваются клинически значимые заболевания печени. Причины этого неясны, хотя демографические и генетические факторы, такие как пол, этническая принадлежность, количество употребляемого алкоголя (≥5 напитков за один раз), алиментарный статус, включая ожирение, сопутствующие заболевания печени (например, инфекция вируса гепатита С) и полиморфизм гена пататиноподобной фосфолипазы‑3, безусловно, играют роль [12]. Недавнее исследование Бекера и соавт. показывает, что молодые люди, женщины и индивиды, склонные к тяжелому эпизодическому пьянству, также более подвержены риску развития алкогольного гепатита (АГ). Для решения этой проблемы необходимы значительные усилия со стороны как государства, так и самих пациентов.
МИПП являются достаточно широко распространенной патологией и составляют от 0,7 до 20% (в среднем 5-7%) от общего количества заболеваний печени. Актуальность проблемы поддерживается тем, что МИПП выступают ведущей причиной острой печеночной недостаточности (13-25% случаев), требующей ортотопической трансплантации печени; обусловливают до 40% острых гепатитов у пациентов старше 40 лет, а при наличии гепатоцеллюлярной желтухи дают смертность 10% [4, 5, 17, 20].
В настоящее время известно не менее 1 тыс. медикаментов, вызывающих гепатотоксические реакции, причем эта цифра не уменьшается, несмотря на то что многие препараты из-за своей гепатотоксичности изымаются из употребления или их применение существенно ограничивается [2, 6]. Более того, частота МИПП постоянно растет, что связано с увеличивающимся количеством производимых новых лекарств, случаев необоснованной полипрагмазии, ведущей к нежелательным межлекарственным взаимодействиям, а также с широким распространением растительных препаратов и многочисленных пищевых добавок, многие из которых пациентами принимаются самостоятельно без назначения врача, не проходят клиническую апробацию и обладают потенциальной гепатотоксичностью. Более 40% всех МИПП приходится на антимикробные, противотуберкулезные и противогрибковые средства, анестетики, противосудорожные, нейротропные и нестероидные противовоспалительные препараты [7-10, 14].
Одним из ключевых моментов современного лечения токсических поражений печени является устранение действия любых гепатотоксических факторов – не только алкоголя и других токсинов, но и многочисленных потенциально гепатотоксических медикаментов. Кроме того, должно быть налажено полноценное питание больного с исключением продуктов и блюд, которые являются нагрузочными для печени (жареная, жирная, копченая пища) и поступлением достаточного количества белков, витаминов и липотропных факторов. Ограничение животного белка рекомендуется только в случае развития печеночной энцефалопатии. Среди медикаментов используются кортикостероиды, в частности метилпреднизолон 24-28 мг/сут (в зависимости от тяжести течения), который применяют от 2-3 нед до нескольких месяцев (дозу каждую неделю снижают на 4 мг). Кроме того, с осторожностью могут использоваться гепатопротекторы, такие как адеметионин, препараты урсодезоксихолевой кислоты, эссенциальные фосфолипиды (ФЛ), силимарин и др. До конца не установлена эффективность детоксикационной терапии и применения лактулозы [23, 24].
Одним из новых гепатопротекторов, которые применяются при АБП и МИПП, является Лесил® – оригинальный фитосомальный комплекс силимарина с ФЛ. Силимарин и ФЛ в фитосомальном комплексе являются синергистами, потенцирующими действие друг друга [13, 22]. ФЛ – структурные компоненты клеточных мембран. При повреждении оболочек клеток фосфатидилхолиновые молекулы способствуют восстановлению целостности клеточной стенки, останавливают разрушение и дегенеративные процессы в клеточных структурах. Фосфатидилхолин активирует ферменты на мембранах, оптимизирует проникающую способность мембраны, усиливает дезинтоксикационные процессы в печени, потенцирует процессы клеточной экскреции [1].
Силимарин взаимодействует со свободными радикалами, переводя их в менее токсичные соединения, прерывает процесс перекисного окисления липидов, препятствует разрушению клеточных структур и мембран, в уже поврежденных гепатоцитах стимулирует синтез белков и ФЛ, стабилизирует клеточные мембраны, ускоряет регенерацию гепатоцитов. При пероральном приеме уровень фитосомального силибинина повышается сразу после приема и достигает пика уже через 2 ч [11, 15, 16, 18].
Таким образом, в отличие от базовых гепатопротекторов, Лесил® обеспечивает двойной механизм защиты гепатоцитов, при этом наблюдается взаимное потенцирование эффектов компонентов продукта. При приеме Лесила наблюдаются улучшение функций печени и реализация гепатопротекторного действия. Лесил работает в двух направлениях: силимарин ускоряет регенерацию, снимает воспаление и нормализует функции гепатоцита, а ФЛ являются проводниками силимарина к гепатоциту и восстанавливают его клеточную мембрану [13, 19, 22]. Фитосомальная форма доставки Лесила увеличила биодоступность силимарина в плазме крови и улучшила его абсорбцию в ЖКТ, что дает возможность применять данный фитосомальный комплекс в режиме 1 р/день [11, 15, 16].
Нами проведено открытое рандомизированное сравнительное исследование с параллельным групповым контролем по изучению эффективности комбинированного гепатопротектора Лесил® у пациентов с токсическими поражениями печени на фоне АБП и МИПП. Целью работы было изучить эффективность и безопасность комбинированного гепатопротектора Лесил® у больных АБП и МИПП в сравнении с таковыми сочетанного применения двух гепатопротекторов – силимарина и эссенциальных ФЛ.
Материалы и методы
Всего обследовано и пролечено 60 больных (37 мужчин, 23 женщины) в возрасте от 25 до 60 лет с токсическими поражениями печени на фоне АБП (n=40) и МИПП (n=20). Всем участникам проводили клинико-анамнестическое общеклиническое биохимическое исследование с определением показателей печеночных проб и липидного спектра, мультимодальное ультразвуковое исследование органов брюшной полости (УЗИ ОБП) со стеатометрией и эластографией (аппарат Sonius, компания Sonoline) до лечения, затем через 1 и 2 мес терапии. Выраженность стеатоза определялась при стеатометрии по степени затухания ультразвука (S1 – S2 – S3). Выраженность фиброза печени определялась при эластографии по степени жесткости паренхимы (F1-F4).
Диагноз АБП и АГ устанавливался на основании анамнеза (длительное злоупотребление алкоголем в опасных дозах), умеренной гепатомегалии; стойкой гипертрансаминаземии с преимущественным повышением АсАТ, повышением соотношения АсАТ/АлАТ >1, при отсутствии серологических маркеров вирусного гепатита В, С, D и аутоиммунного гепатита; выявления при мультимодальном УЗИ ОБП cо стеатометрией и эластографией стеатоза и/или фиброза печени и их выраженности.
В зависимости от проводимого лечения все участники были рандомизированы на 2 группы – основную (І) и контрольную (ІІ), в каждой по 30 пациентов. Распределение по группам осуществлялось методом простой рандомизации на основе случайных чисел, которые были получены с помощью генератора случайных чисел электронных таблиц MS Exel. В каждой группе выделяли подгруппу А (20 больных АГ) и подгруппу В (10 лиц с МИПП). После рандомизации пациентам основной группы в течение 1 мес назначался Лесил® (по 2 капсулы 1 р/день), больным контрольной – силимарин в дозировке 140 мг по 1 таблетке 3 р/день и эссенциальные ФЛ по 1 капсуле 3 р/день, также в течение 1 мес. Всем пациентам с МИПП немедленно отменяли препараты, предположительно вызвавшие МИПП, а все участники с АБП отказывавались от приема алкоголя. В качестве критериев эффективности рассматривалась динамика клинических (улучшение общего состояния, уменьшение слабости и дискомфорта в правом подреберье, уменьшение размеров печени), биохимических (нормализация уровней АлАТ, АсАТ, снижение гиперлипидемии) и ультразвуковых (уменьшение размеров печени, улучшение эхоструктуры, уменьшение выраженности стеатоза и фиброза) показателей через 1 и 2 мес.
Результаты и обсуждение
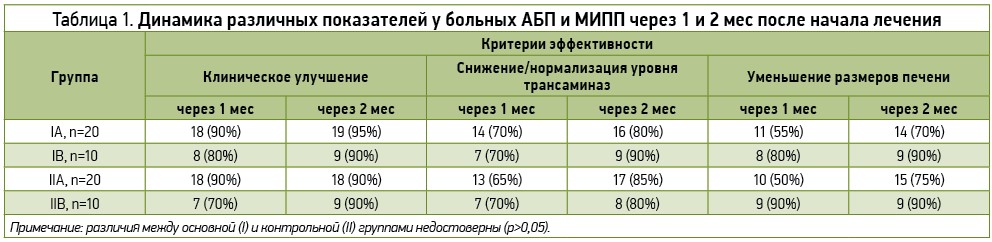
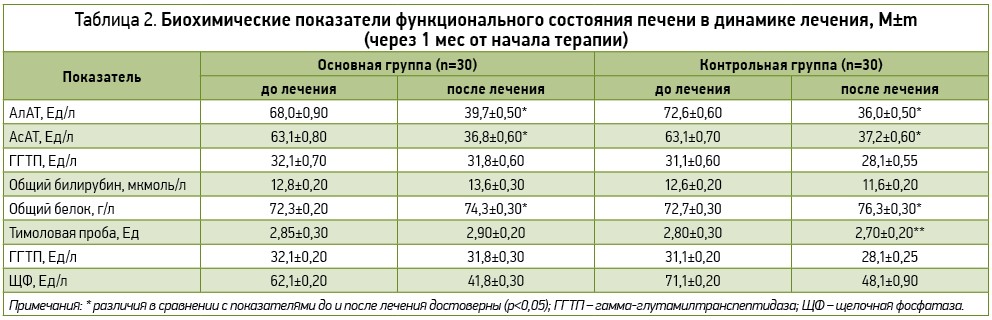
Все участники основной и контрольной групп назначенное лечение закончили полностью, перенесли хорошо, каких-либо побочных эффектов терапии у них не отмечалось. Динамика клинических, биохимических и ультразвуковых показателей, а также показателей липидного спектра в процессе лечения представлена в таблицах 1-3.
 Применение комбинированного гепатопротектора Лесил®, как и использование комплекса силимарин + эссенциальные ФЛ, привело к улучшению липидного спектра (достоверному снижению уровня общего холестерина и триглицеридов) у больных АБП. Учитывая то, что был получен как гепатопротекторный, так и гипохолестеринемический эффект, можно сделать вывод, что у данной категории пациентов применение комбинированного гепатопротектора Лесил® следует рассматривать как патогенетически обоснованный метод лечения, оказывающий многогранное действие и не провоцирующий развитие холестаза. По своей клинико-биохимической и гипохолестеринемической эффективности Лесил® был полностью сопоставим с комплексом силимарин + эссенциальные ФЛ.
Применение комбинированного гепатопротектора Лесил®, как и использование комплекса силимарин + эссенциальные ФЛ, привело к улучшению липидного спектра (достоверному снижению уровня общего холестерина и триглицеридов) у больных АБП. Учитывая то, что был получен как гепатопротекторный, так и гипохолестеринемический эффект, можно сделать вывод, что у данной категории пациентов применение комбинированного гепатопротектора Лесил® следует рассматривать как патогенетически обоснованный метод лечения, оказывающий многогранное действие и не провоцирующий развитие холестаза. По своей клинико-биохимической и гипохолестеринемической эффективности Лесил® был полностью сопоставим с комплексом силимарин + эссенциальные ФЛ.
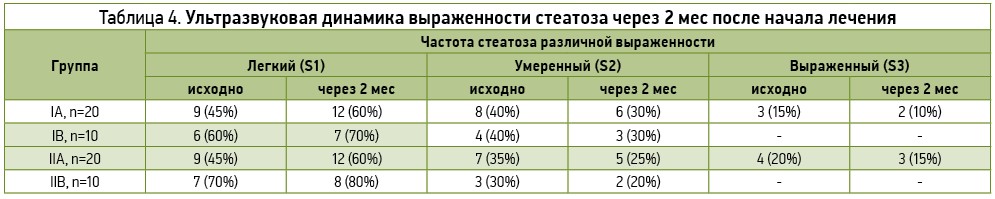
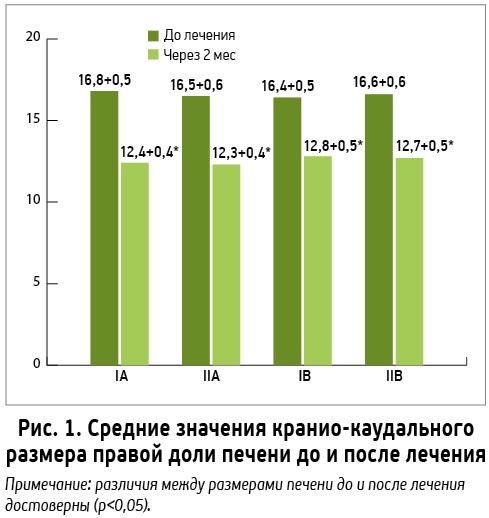
В рамках исследования всем больным проводилось УЗИ ОБП со стеатометрией и эластографией. Полученные данные представлены в таблице 4 и на рисунках 1, 2.
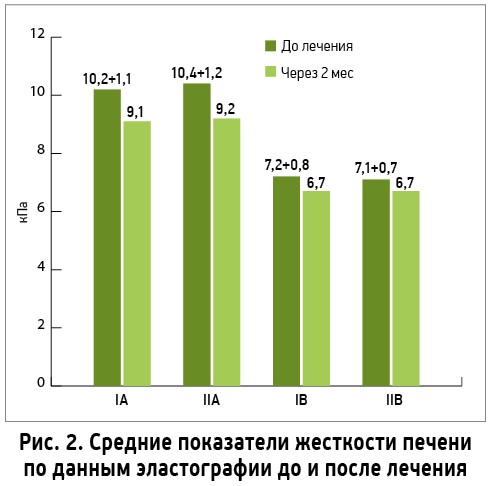 Как видно из представленных данных, на фоне позитивной динамики клинико-лабораторных показателей у обследованных больных отмечалось улучшение ультрасонографических характеристик, в частности тенденция к нормализации акустической плотности и размеров печени за счет уменьшения выраженности стеатоза и фиброза. Так, уменьшение или нормализация размеров печени через 2 мес после начала лечения Лесилом имели место у 70% больных АБП и 90% пациентов с МИПП. Если до начала терапии легкий, умеренный и выраженный стеатоз отмечались соответственно у 45, 40 и 15% больных АБП, а также у 45, 35 и 20% лиц с МИПП, то через 2 мес лечения Лесилом выраженного стеатоза не было зафиксированно ни у одного участника, а количество случаев умеренного стеатоза уменьшилось на 10%. По данным эластографии во всех группах жесткость печени, характеризующая степень выраженности фиброза, имела тенденцию к снижению, хотя различия показателей до и после лечения не достигли уровня статистической достоверности. Сходные данные были также получены и в контрольной группе больных, где применяли силимарин в сочетании с эссенциальными ФЛ.
Как видно из представленных данных, на фоне позитивной динамики клинико-лабораторных показателей у обследованных больных отмечалось улучшение ультрасонографических характеристик, в частности тенденция к нормализации акустической плотности и размеров печени за счет уменьшения выраженности стеатоза и фиброза. Так, уменьшение или нормализация размеров печени через 2 мес после начала лечения Лесилом имели место у 70% больных АБП и 90% пациентов с МИПП. Если до начала терапии легкий, умеренный и выраженный стеатоз отмечались соответственно у 45, 40 и 15% больных АБП, а также у 45, 35 и 20% лиц с МИПП, то через 2 мес лечения Лесилом выраженного стеатоза не было зафиксированно ни у одного участника, а количество случаев умеренного стеатоза уменьшилось на 10%. По данным эластографии во всех группах жесткость печени, характеризующая степень выраженности фиброза, имела тенденцию к снижению, хотя различия показателей до и после лечения не достигли уровня статистической достоверности. Сходные данные были также получены и в контрольной группе больных, где применяли силимарин в сочетании с эссенциальными ФЛ.
Выводы
Таким образом, учитывая то, что токсические поражения печени (АБП и МИПП) являются частой патологией, обусловливающей большое число всех хронических диффузных заболеваний печени, актуальность данной проблемы не вызывает сомнения. Лесил® является эффективным, безопасным и патогенетически обоснованным гепатопротекторным средством, оказывающим при АБП и МИПП достоверный клинико-биохимический (уменьшение клинических проявлений, стеатоза, фиброза, гепатомегалии, гиперферментемии) и гипохолестеринемический эффект. Кроме того, применение комбинированного гепатопротектора Лесил® способствовало уменьшению степени выраженности стеатоза и фиброза печени. На основании проведенного исследования можно сделать вывод, что по своей эффективности и безопасности Лесил® полностью сопоставим с комплексом силимарин + эссенциальные ФЛ. К несомненным преимуществам препарата Лесил® относится возможность его приема 1 р/день, что существенно повышает приверженность пациентов к лечению.
Список литературы находится в редакции.
Медична газета «Здоров’я України 21 сторіччя» № 17 (462), вересень 2019 р.