18 жовтня, 2019
Бета-блокаторы при сердечной недостаточности: пристальный взгляд на карведилол
 Современную кардиологию невозможно представить без β-адреноблокаторов (БАБ). За более чем 40-летний период эта группа препаратов заняла прочные позиции в фармакотерапии различных сердечно-сосудистых (СС) заболеваний. Польза БАБ доказана при лечении всех форм ишемической болезни сердца (ИБС) – острого инфаркта миокарда (ИМ), стабильной и нестабильной стенокардии, нарушений сердечного ритма, артериальной гипертензии. Вместе с тем при сердечной недостаточности (СН) БАБ начали применять относительно недавно. Известно, что данные препараты могут оказывать отрицательное инотропное действие, в связи с чем в течение длительного времени их считали противопоказанными при СН.
Современную кардиологию невозможно представить без β-адреноблокаторов (БАБ). За более чем 40-летний период эта группа препаратов заняла прочные позиции в фармакотерапии различных сердечно-сосудистых (СС) заболеваний. Польза БАБ доказана при лечении всех форм ишемической болезни сердца (ИБС) – острого инфаркта миокарда (ИМ), стабильной и нестабильной стенокардии, нарушений сердечного ритма, артериальной гипертензии. Вместе с тем при сердечной недостаточности (СН) БАБ начали применять относительно недавно. Известно, что данные препараты могут оказывать отрицательное инотропное действие, в связи с чем в течение длительного времени их считали противопоказанными при СН.
Обзор клинических исследований
Стоит отметить, что 1975 г. можно считать переломным в изменении наших представлений о возможности и эффективности использования БАБ у больных СН. В этом году были опубликованы результаты первой длительной (в среднем 5,4 месяца) терапии лиц с застойной кардиомиопатией с применением двух БАБ: альпренолола и практолола. Waagstein et al. впервые продемонстрировали, что лечение данными препаратами приводило к улучшению клинического состояния пациентов с хронической СН (ХСН) и положительным гемодинамическим сдвигам – повышению фракции выброса (ФВ) левого желудочка (ЛЖ) и уменьшению камер сердца [61]. Несмотря на сенсационность этих результатов, большинство клиницистов ставили под сомнение возможность использования БАБ при СН еще в течение достаточно длительного времени.
Переосмысление позиций БАБ при СН началось в начале 90-х гг. Тогда были опубликованы результаты целого ряда работ, посвященных изучению возможностей этих препаратов [12, 20, 25, 46, 50, 59, 60].
Также было проведено первое крупное многоцентровое исследование CIBIS эффектов длительной терапии (в течение двух лет) бисопрололом у 641 пациента с ХСН разной этиологии: ФВ ЛЖ <40%; функциональный класс (ФК) согласно классификации Нью-Йоркской ассоциации сердца (NYHA) III (95%) и IV (5%). В 1994 г. полученные результаты продемонстрировали достоверное улучшение ФК лиц с СН (р=0,04) и снижение частоты госпитализаций по причине прогрессирования ХСН (р<0,01) вследствие длительной терапии бисопрололом. В испытании CIBIS также были показаны данные о снижении смертности от всех причин на 20%, однако они не достигли критериев достоверности [10].
В 1996 г. опубликованы результаты еще одного многоцентрового двойного слепого плацебо-контролируемого исследования USCP при участии 1094 пациентов с СН [49]. Было показано, что 6-месячный прием карведилола, назначавшегося в дополнение к классической на то время терапии ингибиторами ангиотензинпревращающего фермента (иАПФ), дигоксином и диуретиком, уменьшал вероятность СС-госпитализаций на 27% (р=0,036), комбинированный риск СС-госпитализаций и смерти – на 38% (р<0,001), а количество летальных исходов – на 65% (!) по сравнению с плацебо [49].
В 1999 г. были завершены два крупных многоцентровых исследования CIBIS II и MERIT-HF. В CIBIS II 2647 больных с III‑IV ФК и ФВ ≤35% принимали бисопролол, а в MERIT-HF – 3991 пациент с II‑IV ФК и ФВ ≤40% – метопролола сукцинат. Оба испытания продемонстрировали значительное уменьшение смертности у лиц с СН на 34% в CIBIS II и на 38% – MERIT-HF [19, 41].
Данные метаанализов, проведенных по результатам целого ряда крупных исследований, подтвердили безопасность и эффективность БАБ при лечении пациентов с СН [17, 24, 39]. Было доказано, что дополнительное назначение БАБ к иАПФ не только приводило к улучшению гемодинамических показателей и самочувствия, но и снижало риск смерти на 37% и госпитализаций – на 41% [16, 36, 56]. Благоприятное прогностическое влияние БАБ проявлялось при длительном лечении после медианы 12 месяцев (относительный риск [ОР] 0,69; 95% доверительный интервал [ДИ] 0,56‑0,80) и не зависело от исходного ФК больных или географического региона [17, 18, 42].
Все это поставило точку в спорах об обоснованности назначения БАБ пациентам с ХСН и способствовало тому, что препараты этой группы стали одним из главных компонентов медикаментозного лечения СН. Уже в 2001 г. Европейское общество кардиологов (ESC) рекомендовало БАБ всем больным со стабильной легкой, средней тяжести и тяжелой СН II‑IV ФК согласно NYHA, со сниженной ФВ ЛЖ, независимо от этиологии синдрома, в качестве терапии СН в дополнение к диуретикам, иАПФ при отсутствии противопоказаний (уровень доказательности А) [35].
В 2004 г. были завершены два интересных рандомизированных клинических испытания. Одно из них – CARMEN – включало 572 пациента с I‑II ФК (71%) и III ФК (29%), которые были распределены на группы. Первая (n=191) получала только карведилол, вторая (n=190) – только эналаприл, а третья (n=191) – оба препарата, причем в последней группе карведилол титрировался первым, т.е. до эналаприла. Главной комбинированной точкой была оценка динамики индекса конечного диастолического объема (КДО) ЛЖ, который определяли методом трансторакальной эхокардиографии (ЭхоКГ) [54]. Фактически это первое рандомизированное исследование, показавшее возможность начала лечения с БАБ (карведилола!), а не иАПФ. Более того, оказалось, что наилучшие результаты наблюдались именно в группе комбинированной терапии, где старт был осуществлен с карведилола, и только потом титровали дозу эналаприла – по сути, к БАБ присоединяли иАПФ.
В другом пилотном исследовании с вовлечением 78 больных СН (60% – II‑III ФК) Sliwa et al. (2004) показали, что среди пациентов, у которых вначале титровали дозу карведилола, происходило более значительное улучшение ФК (Δ=1,2) и увеличение ФВ ЛЖ на 15% (!), чем в группе начинавших терапию с иАПФ (Δ =0,4 ФК; увеличение ФВ ЛЖ на 3%) [58]. Полученные результаты представляют значительный интерес еще и потому, что в исследовании были впервые затронуты вопросы достижения доз БАБ. Продемонстрировано, что использование карведилола в качестве первого лекарственного средства для титрования позволяет достигать достоверно (p=0,03) более высоких доз (43±17 мг/сут), чем второго после иАПФ (периндоприла); среднесуточная доза карведилола – 33±18 мг/сут.
Главным выводом этих двух пилотных исследований стало подтверждение новой клинической идеи – возможности старта лечения ХСН не только с иАПФ, но и с БАБ.
Предположение, что терапия, основанная на выборе БАБ в качестве первого препарата для лиц с ХСН, может обладать рядом преимуществ перед стандартным началом с иАПФ, было окончательно доказано в многоцентровом исследовании CIBIS III при участии 1010 больных с II‑III ФК (ФВ ЛЖ ≤35%). Результаты подтвердили, что старт лечения ХСН с БАБ так же эффективен и безопасен, как с иАПФ (эналаприла). Более того, оказалось, что инициирование терапии с БАБ приводило к улучшению прогноза пациентов уже на ранних этапах, хотя и сопровождалось повышением частоты госпитализаций в связи с декомпенсацией СН [62, 63]. Именно благодаря данным исследования CIBIS III БАБ стали рассматривать не просто как дополнение к иАПФ, а как препараты первого ряда (вместе с иАПФ) при лечении ХСН.
Положительное влияние БАБ при ХСН было столь очевидным, что, начиная с 2012 г., ESC стало рекомендовать их применение всем больным ХСН с ФВ ЛЖ <40% для снижения риска госпитализаций в связи с ХСН и преждевременной смерти (класс рекомендаций I, уровень доказательности A) [40]. В настоящее время в руководящих принципах ESC для лечения СН (2016) указаны четыре БАБ: метопролола сукцинат (CR/XL), бисопролол, карведилол и небиволол [7].
В рекомендациях Американской коллегии кардиологов и Американской ассоциации сердца (ACCF/AHA, 2013) указывается, что один из трех БАБ, доказавших снижение смертности (то есть бисопролол, карведилол и метопролола сукцинат с пролонгированным высвобождением) целесообразно применять у всех пациентов с СН и сниженной ФВ ЛЖ при отсутствии противопоказаний для уменьшения заболеваемости и смертности (класс рекомендаций I, уровень доказательности A) [6]. Небиволол для лечения СН не рассматривается [6]. В последних рекомендациях ACCF/AHA (2017) для терапии больных СН указаны четыре БАБ: бисопролол, карведилол, карведилол CR и метопролол CR/XL [9].
Отсутствие небиволола в рекомендациях ACCF/AHA, вероятно, обусловлено тем, что в исследовании SENIORS длительностью 21 месяц с вовлечением 2128 больных в возрасте ≥70 лет (ФВ ЛЖ ≤35%) присоединение небиволола к стандартной терапии ХСН не приводило к снижению ни риска смерти, ни числа СС-госпитализаций по сравнению с группой плацебо (р=0,21). В результате лечение небивололом у данной когорты больных ассоциировалось лишь с достоверным уменьшением значений суммарного показателя госпитализаций и летальных случаев (ОР 0,84; ДИ 0,72‑0,98; p=0,027) [29].
Вместе с тем стоит отметить, что Управление по контролю над качеством пищевых продуктов и медикаментов США (FDA) для лечения СН одобрило только два БАБ: метопролола сукцинат с пролонгированным высвобождением и карведилол [13].
Применение БАБ при ХСН в клинической практике
На сегодняшний день уже ни у кого не вызывает сомнений необходимость применения БАБ при ХСН. Доказано, что препараты данной группы снижают уровень смертности при ХСН, уменьшают количество госпитализаций, положительно влияют на ремоделирование сердца и сосудов, создавая условия для улучшения ФК больных. Однако до сих пор в клинической практике у врачей возникает ряд вопросов:
- как и когда начинать лечение БАБ при СН?
- какой БАБ назначить пациенту с СН?
- каких доз и как следует достигать у лиц с СН?
Как и когда начинать лечение БАБ при СН?
Согласно последним рекомендациям как ESC (2016), так и ACCF/AHA (2017), БАБ, эффективность которых доказана в клинических исследованиях, следует назначать:
- всем больным стабильной СН со сниженной ФВ ЛЖ при отсутствии непереносимости или противопоказаний к применению;
- как можно ранее после установления диагноза СН и даже в тех случаях, когда у пациентов удается значительно уменьшить симптомы СН в результате лечения другими препаратами; терапия БАБ способствует снижению риска прогрессирования заболевания, клинического ухудшения и внезапной смерти;
- не дожидаясь достижения целевых доз иАПФ; присоединение БАБ к терапии иАПФ даже в невысоких дозах приводит к более значимому улучшению симптомов и снижению риска смерти, чем титрация иАПФ до целевых доз, используемых в клинических исследованиях;
- желательно пациентам в состояния эуволемии; у лиц с симптомами задержки жидкости БАБ следует назначать с диуретиками, так как они необходимы для поддержания баланса натрия и жидкости и предотвращения декомпенсации, которая может сопровождать начало терапии БАБ.
Лечение БАБ следует начинать с очень низких доз с последующим постепенным увеличением, при условии хорошей переносимости предыдущей дозы. В течение всего периода титрования следует тщательно мониторить клиническое состояние больных. При таком осторожном подходе большинство пациентов (приблизительно 85%), включенных в клинические исследования, переносили лечение БАБ в целевых дозах. БАБ можно безопасно начинать применять даже у лиц, госпитализированных по поводу СН, при условии, что они не требуют внутривенной инотропной терапии для СН.
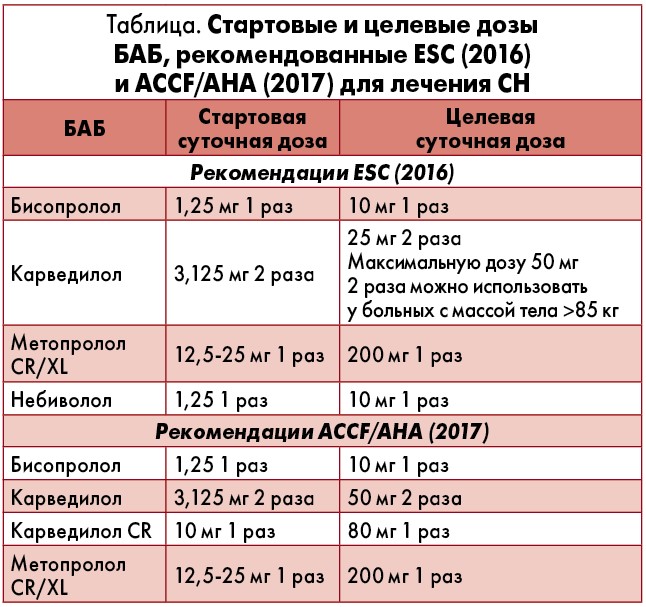 Стартовые и целевые дозы БАБ, рекомендованные ESC (2016) и ACCF/AHA (2017) на сегодняшний день для лечения СН, приведены в таблице.
Стартовые и целевые дозы БАБ, рекомендованные ESC (2016) и ACCF/AHA (2017) на сегодняшний день для лечения СН, приведены в таблице.
Какой БАБ назначить пациенту с СН?
Зачастую выбор основывается главным образом на клиническом опыте и «привязанности» врача к тому или иному препарату. Чтобы попытаться ответить на вопрос, какой БАБ выбрать, следует разобраться, есть ли различия у данных медикаментов. Как сложилось исторически, эффективность трех основных БАБ, рекомендованных в настоящее время для лечения ХСН (бисопролол, карведилол, метопролола сукцинат CR/XL), никогда не сравнивали в многоцентровых масштабных исследованиях. Поэтому можно опираться в основном на результаты субанализов или метаанализов крупных плацебо-контролируемых испытаний, посвященных изучению каждого из вышеперечисленных препаратов по отдельности: CIBIS II (бисопролол), MERIT-HF (метопролол CR/XL), USCP (карведилол) и COPERNICUS (карведилол) [19, 41, 48, 49].
Несмотря на то что CIBIS II и MERIT-HF были выполнены практически в соответствии с тем же дизайном, что и USCP, обращает внимание тот факт, что степень влияния на прогноз больных в этих исследованиях отличается. В CIBIS II и MEPIT-HF снижение смертности (34 и 38% соответственно) было почти вдвое меньше, чем в USCP (65%).
Сравнительный анализ данных, полученных в испытаниях CIBIS II, MERIT-HF и COPERNICUS, показал, что расчетное значение количества смертельных исходов, предотвращаемых в результате лечения 1 тыс. пациентов в течение года, у карведилола оказалось значительно выше (71), чем у метопролола CR/XL (38) и бисопролола (41) [26]. Анализ еще одного показателя NNT – числа больных, которых необходимо пролечить для спасения одной жизни, также выявил некоторые различия в эффективности сравниваемых препаратов. Так, в исследовании MERIT-HF значения NNT составили 28 больных при длительности терапии около года. В CIBIS-II и COPERNICUS параметры NNT были значительно ниже (18), что указывает на большую эффективность данных БАБ. Однако для достижения такого значения при лечении бисопрололом потребовалось 1,3 года, а при использовании карведилола – менее 11 месяцев.
Кроме того, нельзя обойти вниманием результаты многоцентрового исследования COMET, завершившегося в 2003 г. Это было первое прямое сравнение влияния карведилола и селективного БАБ 2-го поколения метопролола тартрата. Выбор метопролола тартрата (а не сукцината) объясняется тем, что на момент проведения исследования данная форма метопролола входила в список препаратов, рекомендованных для лечения ХСН [26, 35]. В COMET целевые дозы карведилола (50 мг/сут) и метопролола (100 мг/сут) обеспечивали фактически эквивалентный прогностический эффект.
При среднем сроке наблюдения 58 месяцев риск смерти от любых причин в группе пациентов, которые принимали карведилол, составил 34% и был достоверно ниже (ОР 0,83; ДИ 0,74‑0.93), чем у получавших метопролол (40%). При этом средний «выигрыш» в расчетной продолжительности жизни при приеме карведилола (по сравнению с метопрололом) составил 1,4 года при максимальной продолжительности наблюдения около семи лет [51].
Интерес также представляют результаты исследования MADIT-CRT, в котором изучали влияние имплантированного кардиовертера-дефибриллятора в сочетании с постоянной электрической ресинхронизацией желудочков на клинический прогноз 1820 пациентов с ХСН (ФВ ≤30%; ФК I‑II) [44]. Субанализ полученных данных подтвердил преимущества карведилола перед метопрололом. Так, комбинированный риск госпитализаций по поводу декомпенсации СН и/или смерти в группе больных на карведилоле оказался на 30% ниже, чем у принимавших метопролол (р=0,001) [55]. При этом оказалось, что положительный эффект карведилола был наиболее выражен в подгруппе пациентов с блокадой левой ножки пучка Гиса и носил отчетливый дозозависимый характер (снижение риска на 49%, р<0,001) [55].
Показательными являются результаты метаанализа восьми исследований при участии 4563 пациентов, где карведилол сравнивали с метопрололом (4 испытания), бисопрололом (2) и небивололом (2) [23]. Было показано, что уровень смертности от всех причин в результате приема «некардиоселективного» карведилола был достоверно ниже (ОР 0,85; 95% ДИ 0,78‑0,93; р=0,0006), чем в объединенной группе больных, принимавших β1-селективные БАБ (метопролол, бисопролол и небиволол).
Похожие данные были получены исследователями из Дании, которые провели ретроспективный сравнительный анализ эффектов различных БАБ (бисопролола, карведилола и метопролола) у 58 634 больных ХСН (период наблюдения – 1995‑2011 гг.) [14]. Терапия карведилолом в высоких дозах (≥50 мг/сут) оказывала более значимое положительное влияние на прогноз смертности от всех причин (ОР 0,873; ДИ 0,789‑0,966) и риск госпитализаций (ОР 0,842; ДИ 0,774‑0,915) у лиц с ХСН, чем целевыми дозами метопролола (≥200 мг/сут) или бисопролола (≥10 мг/сут).
Данные исследования MERIT-HF убедительно продемонстрировали, что внезапная смерть является ведущей у пациентов с умеренно выраженной клинической картиной ХСН (II‑III ФК NYHA), а у таковых с IV ФK – второй по частоте причиной летальных исходов после прогрессирования ХСН [41]. Доказано, что внезапная смерть – зачастую аритмическая. Поэтому способность БАБ влиять на частоту развития нарушения сердечного ритма приобретает принципиальное значение.
Результаты метаанализа семи исследований (n=11952) подтвердили антиаритмический эффект БАБ при ХСН [45]. Бисопролол, метопролол и карведилол достоверно снижали риск возникновения ФП у больных ХСН на 27% (р=0,001). Положительное влияние на развитие фибрилляции предсердий не было выявлено лишь у небиволола в испытании SENIORS [45]. Вместе с тем данные CAPRICORN (n=1959; ФВ ≤40%) показали, что терапия карведилолом приводила к значительному снижению риска появления не только суправентрикулярных аритмий (на 52%; р=0,0015), но и различных желудочковых нарушений сердечного ритма (тахикардия, фибрилляция) (на 76%; р<0,0001) [21]. На это также указывают результаты субанализа исследования MADIT-CRT, согласно которым риск возникновения желудочковых нарушений ритма у пациентов с имплантированным ресинхронизирующим устройством, принимавших карведилол, был на 20% ниже, чем у таких же больных на метопрололе [55].
Сравнительный анализ данных крупномасштабных международных испытаний CIBIS-II, MERIT-HF и USCP не только свидетельствует о положительном влиянии всех БАБ на частоту развития внезапной смерти, но и еще раз подтверждает преимущества карведилола. Так, метопролол CR/XL снижал риск развития внезапной смерти на 41%, бисопролол – на 45%, а карведилол – на 56% (!) [38]. Преимущества карведилола в этом аспекте были также подтверждены результатами исследования COMET. ОР внезапного летального исхода в группе больных ХСН, принимавших карведилол, был на 23% ниже, чем среди лечившихся метопрололом (р<0,007) [53]. Способность карведилола оказывать профилактический эффект в отношении внезапной смерти была также подтверждена в испытании CAPRICORN (снижение на 26%) [21, 56].
Гемодинамическая и прогностическая эффективность карведилола была доказана у лиц с систолической дисфункцией и ИМ в исследованиях CHAPS и CAPRICORN (n=1959; ФВ ≤40%), у больных сахарным диабетом вследствие субанализа результатов COPERNICUS и COMET [21, 43, 51, 57].
Все вышесказанное позволяет утверждать, что именно карведилол занял лидирующие позиции среди других БАБ, использующихся для лечения ХСН.
Целевые дозы – нужно ли их достигать, и как это реализовать в клинической практике?
Согласно рекомендациям ESC (2016) и ACCF/AHA (2017), в клинической практике следует прилагать все усилия, чтобы достичь целевых доз БАБ, показавших свою эффективность в крупных клинических испытаниях. Даже при отсутствии улучшения симптомов длительное лечение БАБ необходимо продолжать для улучшения прогноза таких пациентов. Целесообразно избегать отмены БАБ, поскольку это может привести к клиническому ухудшению.
То, что положительные эффекты карведилола являются дозозависимыми, одними из первых продемонстрировали данные исследования MOCHA (n=345; ФК II‑IV). Терапия высокими дозами препарата не только приводила к более выраженным изменениям гемодинамических параметров (КДО ЛЖ, ФВ и т.д.), но и в большей степени влияла на прогноз пациентов. Значительное снижение смертности наблюдалось при достижении суточной дозы ≥50 мг [15].
Дозозависимое положительное влияние БАБ на комбинированный показатель смерти от всех причин или госпитализации также подтвердили результаты испытания HF-ACTION [28]. Анализ, проведенный авторами, доказал, что более низкая смертность от СС-причин ассоциировалась с более высокой дозой БАБ и более низкой частотой сердечных сокращений. Вместе с тем результаты, полученные при проведении мультивариантной корректировки, показали, что только доза БАБ была связана со снижением риска смерти от всех причин или госпитализаций [28].
Анализ данных, полученных в исследовании BIOSTAT-CHF 2017 г., показал, что у больных СН, которые получали <50% от целевых доз иАПФ / блокатора рецепторов ангиотензина II (БРА) и БАБ, риск смерти и/или госпитализаций оказался на 24% выше, чем у принимавших более высокие дозы препаратов [47]. Еще более интересные данные были получены в отношении БАБ. Так, у пациентов, которые использовали препараты в дозах ≤49% от рекомендованных, риск смерти (ОР 1,91; 95% ДИ 1,74‑2,08) и комбинированной точки смерть/госпитализации в связи с СН (ОР 1,27; 95% ДИ 1,15‑1,39) были достоверно выше, чем у получавших ≥100% от целевых доз. Следует отметить, что риск смерти у больных, достигших 50‑99% целевых доз БАБ, также был выше (ОР 1,29; 95% ДИ 1,07‑1,51), чем у тех, кому назначали более высокие дозы (≥100% от рекомендованных) [47].
Вместе с тем данные литературы показывают, что практические рекомендации в клинической практике не всегда выполняются.
Согласно данным регистра COHERE, в который были включены 4113 больных СН, лишь 41% после периода титрования достигли средней дозы карведилола 25 мг два раза в сутки. При этом более половины пациентов принимали значительно меньшую дозу препарата [32]. По результатам еще одного регистра OPTIMIZE-HF (2008), дозы БАБ, которые использовали лица с СН после выписки из стационара, составляли ˂50% от рекомендованных, а целевые получали ˂10% больных [22, 31]. Более того, не продолжали дальнейшее титрование доз БАБ в течение трех месяцев после выписки из стационара 75% пациентов [31].
Хотелось надеяться, что за прошедшее десятилетие показатели назначения и достижения целевых доз основных препаратов, используемых при СН, поменялись. Однако в 2017 г. были опубликованы результаты исследования BIOSTAT-CHF, проведенного в 69 центрах 11 стран ЕС. Авторы изучали возможности достижения и эффекты целевых доз иАПФ и БАБ у 2100 лиц с СН и ФВ ЛЖ <40% (медиана – 21 месяц).
Полученные данные оказались достаточно неожиданными. Рекомендованных доз иАПФ/БРА достигли 22%, а целевых БАБ – всего 12% (!) больных [47].
Почему же в клинической практике не получается следовать установленным практическим рекомендациям? В этом контексте значительный интерес представляют результаты, опубликованные в 2004 г. датскими исследователями. Они изучали возможность достижения целевых доз бисопролола и карведилола за два месяца титрования у 87 больных СН (ФВ ЛЖ 28±10%; ФК NYHA III‑IV). Авторы использовали стандартную схему титрования – удвоение дозы каждые две недели. Оказалось, что через два месяца в группе бисопролола средняя суточная доза препарата составила 3,1±2,6 мг, т.е. всего 33% (!), карведилола – 13,4±14,0 мг, т.е. всего 27% (!) от рекомендованной. Хотя после выписки из стационара в обеих группах средние дозы были несколько выше – 41% (при приеме бисопролола) и 32% (при приеме карведилола) от рекомендованных. В группе бисопролола 39%, а в группе карведилола – 40% больных прекратили лечение БАБ после выписки из стационара [33].
Опыт показывает, что одной из возможных причин является именно способ титрования доз БАБ. Начиная с 2001 г., в рекомендациях ESC указывается, что при лечении СН дозы БАБ следует титровать до достижения доз, показавших эффективность в масштабных исследованиях. Дозы могут быть удвоены каждые 1‑2 недели при условии хорошей переносимости [35].
 На примере карведилола разберем, в чем «беда» такого способа титрования – удвоения каждые две недели (рис. 1)? В клинической практике основные проблемы при таком способе титрования чаще всего начинаются после достижения средних доз препарата (25 мг/сут). Дальнейшее удвоение дозы на 8-й, а тем более 12-й неделе – это фактически увеличение суточных на 25 и 50 мг соответственно. Не все пациенты способны выдержать такое повышение.
На примере карведилола разберем, в чем «беда» такого способа титрования – удвоения каждые две недели (рис. 1)? В клинической практике основные проблемы при таком способе титрования чаще всего начинаются после достижения средних доз препарата (25 мг/сут). Дальнейшее удвоение дозы на 8-й, а тем более 12-й неделе – это фактически увеличение суточных на 25 и 50 мг соответственно. Не все пациенты способны выдержать такое повышение.
В рекомендациях ESC (2016) формулировка стала более осторожной, но все еще предлагается алгоритм удвоения доз с интервалом не менее двух недель (у некоторых больных может потребоваться более медленное титрование) [8]. ACCF/AHA (2017) указывают, что повышение каждой последующей дозы БАБ должно происходить медленно, в течение 7‑14 дней [9]. Предложенный алгоритм является более безопасным, однако зависит от клинического опыта врача и индивидуальной переносимости пациента.
 В этой связи предлагаю собственный алгоритм титрования дозы карведилола, клиническая безопасность которого доказана более чем на 300 больных СН (рис. 2). Начальная доза препарата составляет 6,25 (иногда 3,125) мг дважды в сутки. Выбор исходной дозы определяют начальный уровень артериального давления и частота сердечных сокращений пациента. Повышение суточной дозы происходит один раз в неделю – на 6,25 (иногда на 3,125) мг. Данный алгоритм является безопасным и даже при наличии исходного показателя артериального давления 90/60 мм рт. ст. позволяет достигать суточной дозы карведилола 50 мг практически у 99%, а 100 мг – у 75‑80% лиц с СН.
В этой связи предлагаю собственный алгоритм титрования дозы карведилола, клиническая безопасность которого доказана более чем на 300 больных СН (рис. 2). Начальная доза препарата составляет 6,25 (иногда 3,125) мг дважды в сутки. Выбор исходной дозы определяют начальный уровень артериального давления и частота сердечных сокращений пациента. Повышение суточной дозы происходит один раз в неделю – на 6,25 (иногда на 3,125) мг. Данный алгоритм является безопасным и даже при наличии исходного показателя артериального давления 90/60 мм рт. ст. позволяет достигать суточной дозы карведилола 50 мг практически у 99%, а 100 мг – у 75‑80% лиц с СН.
Достижение таких высоких терапевтических доз карведилола позволяет добиться длительной клинической стабилизации (более 10 лет) у большинства пациентов с СН. Применение высоких доз (100 мг/сут) также является необходимым условием лечения пациентов с систолической дисфункцией, развившейся в результате воспалительного процесса в миокарде. Назначение именно карведилола у таких больных не должно подвергаться сомнению.
Благодаря сложной молекулярной структуре, карведилол обладает целым рядом свойств, выгодно отличающим его от других представителей группы БАБ.
Этот препарат способен блокировать не только β1- и β2-адренорецепторы, но и постсинаптические α1-рецепторы. Блокада β-адренорецепторов позволяет добиться более полной защиты миокарда от избыточного количества циркулирующих катехоламинов в условиях гиперактивации симпато-аденаловой системы [1]. Блокада α1-адренорецепторов способствует расширению почечные артериолы. Это обеспечивает возрастание эффективного ренального кровотока и соответствующее снижение внутриклубочкового давления, что лежит в основе нефропротекторного действия карведилола, не свойственного традиционным БАБ [11]. Именно α1-адреноблокирующий эффект карведилола определяет его благоприятное действие на утилизацию глюкозы, чувствительность тканей к инсулину, тормозящее влияние на развитие гипертрофии ЛЖ, выраженность миокардиального фиброза и, в определенной мере, антиаритмические эффекты [30, 34, 37, 52].
Помимо всего вышесказанного, карведилол и продукты его метаболизма оказывают мощный антиоксидантный эффект, что определяет ряд других свойств, присущих только данному препарату. Речь идет о его противовоспалительном и антипролиферативном действии. В отличие от других БАБ, карведилол оказывает местный противоспалительный эффект: уменьшает инфильтрацию нейтрофилами поврежденной зоны (за счет снижения экспрессии молекул адгезии), угнетает индуцируемую активными формами кислорода экспрессию апоптоз-опосредующих белков (Fas-протеина, ФНО-α), тем самым предотвращая апоптоз [27, 64]. Благодаря антиоксидантному действию карведилол также способен существенно подавлять выраженность системной иммуновоспалительной активации [1].
В исследовании, выполненном совместно с к. мед. н. Е.В. Онищенко, Н.А. Солобюковой и Е.С. Рей, было показано, что использование у пациентов с ХСН некоронарного генеза высоких терапевтических доз (до 100 мг/сут) карведилола (препарата Кориол, KRKA, Словения) приводит к значительному улучшению качества жизни и переносимости физических нагрузок. В начале нашего исследования у 60,9% больных был диагностирован III ФК по NYHA, а к концу наблюдения (19,5 месяцев) состояние 81,3% соответствовало I ФК. Согласно проведенным расчетам, 5-летняя выживаемость таких пациентов составила 88%, и 81% не нуждался в повторных госпитализациях в связи с декомпенсацией ХСН. Более того, в результате длительной терапии с использованием высоких терапевтических доз карведилола у 52,4% лиц с хроническим миокардитом и систолической дисфункцией отмечалась нормализация ФВ ЛЖ, а у 30% – полости ЛЖ [2‑5].
В заключение стоит отметить, что карведилол, благодаря сложной молекулярной структуре, обладает целым рядом свойств, выгодно отличающим его от других представителей группы БАБ. Это позволяет рассматривать препарат как один из наиболее патогенетически оправданных и клинически полезных фармакологических средств для длительного лечения ХСН, обусловленной систолической дисфункцией ЛЖ. Можно констатировать, что карведилол прочно утвердился в качестве «золотого стандарта» в фармакотерапии пациентов с ХСН [1].
Литература
- Воронков Л.Г. Карведилол: фармакодинамика и место в современной кардиологии / Л.Г. Воронков. – Л.: Четверта хвиля, 2013. – 64 с.
- Коваленко В.М., Онищенко О.В., Рей Є.С., Рябенко Д.В. Зворотне ремоделювання лівого шлуночка у хворих з хронічним дифузним міокардитом під впливом довготривалого синдромального лікування хронічної серцевої недостатності // Укр. ревматол. журнал. – 2008. – № 3 (33). – С. 52‑57.
- Коваленко В.М., Рябенко Д.В., Онищенко О.В., та співав. Безпека та особливості ефектів довготривалого лікування високими дозами карведилолу та еналаприлу у пацієнтів з ХСН різного ґенезу // Укр. мед. часопис. – 2008. – № 5 (67). – С. 108‑113.
- Рябенко Д.В. Фармакологическое лечение хронической сердечной недостаточности в XXI веке: достижения и вопросы. IІ. Почему результаты фармакотерапии остаются не столь обнадеживающими, как можно было ожидать? // Серцева недостатність. – 2014. – № 2. – С. 24‑33.
- Рябенко Д.В., Онищенко О.В., Рей Є.С., Солобюкова Н.О. Клінічна ефективність та безпечність тривалого лікування високими дозами карведилолу, еналаприлом і триметазидином у хворих із систолічною хронічною серцевою недостатністю // Укр. Кардіол. журнал. – 2008. – № 5. – С. 78‑82.
- 2013 ACCF/AHA Guideline for the Management of Heart Failure. A Report of the American College of Cardiology Foundation / American Heart Association Task Force on Practice Guidelines // J Am Coll Cardiol. – 2013; doi: 10.1016/j.jacc.2013.05.019.
- 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: The Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC) Developed with the special contribution of the Heart Failure Association (HFA) of the ESC // Eur Heart J. – 2016. – Vol. 37 (27). – P. 2129‑2200; doi.org/10.1093/eurheartj/ehw128.
- 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure – Web Addenda // European Heart Journal; doi:10.1093/eurheartj/ehw128.
- 2017 ACC/AHA/HFSA Focused Update of the 2013 ACCF/AHA Guideline for the Management of Heart Failure: A Report of the American College of Cardiology / American Heart Association Task Force on Clinical Practice Guidelines and the Heart Failure Society of America // Circulation. – 2017. – 136: e137-e161.
- A randomized trial of beta-blockade in heart failure. The Cardiac Insufficiency Bisoprolol Study (CIBIS). CIBIS Investigators and Committees // Circulation. – 1994. – Vol. 90. – P. 1765‑1773.
- Abraham W.T., Tsvetkova T, Lowes B.D. et al. Carvedilol improves renal hemodynamics in patients with chronic heart failure // Circulation. – 1998. – Vol. 98. – Р. I–378.
- Anderson J.L., Lutz J.R., Gilbert E.M. et al. A randomized trial of low-dose beta-blockade therapy for idiopathic dilated cardiomyopathy // Am J Cardiol 1984. – 55. – Р. 471‑475.
- Beta-Blockers Therapeutic Class Review (TCR); https://hhs.texas.gov/sites/default/files/…/042817‑4j.
- Bolling R., Scheller N.M., Kober L. et al. Comparison of the clinical outcome of different beta-blockers in heart failure patients: a retrospective nationwide cohort study // Eur J Heart Fail. – 2014. – Vol. 16 (6). – P. 678‑684.
- Bristow M., Gilbert EM., Abraham WT. et al. Carvedilol produces dose-related improvements in left ventricular function and survival in subjects with chronic heart failure // Circulation. – 1996. – Vol. 94. – P. 2800‑2806.
- Bristow M.R. β-Adrenergic Receptor Blockade in Chronic Heart Failure // Circulation. – 2000. – Vol. 101. – P. 558‑569.
- Chatterjee S., Biondi-Zoccai G., Abbate A., D’Ascenzo F., Castagno D., Van Tassell B. et al. Benefits of beta blockers in patients with heart failure and reduced ejection fraction: Network meta-analysis // BMJ. – 2013. – 346; doi: https://doi.org/10.1136/bmj.f55.
- Chatterjee S., Udell J.A., Sardar P., Lichstein E., Ryan J.J. Comparable benefit of beta-blocker therapy in heart failure across regions of the world: Meta-analysis of randomized clinical trials // Can J Cardiol. – 2014. – 30. – (898). – Р. 903.
- CIBIS-II Investigators and Committees. The cardiac insuffiency bisoprolol Study II (CIBIS-II): a randomized trial // Lancet. – 1999. – Vol. 353. – P. 9‑13.
- Currie PJ, Kelly MJ, McKenzie A et at. Oral beta-adrenergic blockade with metoprolol in chronic severe dilated cardiomyopathy //J Am Coll Cardiol. – 1984. – 3. – Р. 203‑209.
- Dargie HJ., Effect of carvedilol on outcome after myocardial infarction in patients with left ventricular dysfunction. The CAPRICORN randomised trial // Lancet. – 2001. – Vol. 357. – P. 1385‑1390.
- DeVore A.D., Mi X., Mentz R.J. et al. Discharge heart rate and b-blocker dose in patients hospitalized with heart failure: findings from the OPTIMIZE-HF registry //Am Heart J. – 2016. – 173. – Р. 172‑178.
- DiNicolantonio J., Lavie C., Fares H. et al. Meta-Analysis of carvedilol versus beta1-selective beta-blockers (atenolol, bisoprolol, metoprolol and nebivolol) // Am J Cardiol. – 2013. – Vol. 111. – P. 765‑769.
- Doughty R.N., Rodgers A., Sharpe N., MacMahon S. Effects of beta-blocker therapy on mortality in patients with heart failure: a systematic overview of randomized controlled trials // Eur Heart J. –1997. – 18. – Р. 560‑565.
- Engelmeier RS, O’Connel JB, Walsh R, Rad N, Scanlon PJ, Gunnar RM. Improvement in symptoms and exercise tolerance by metoprolol in patients with dilated cardiomyopathy: a double-blind, randomized, placebo- controlled trial // Circulation. – 1985. – 72. – Р. 536‑546.
- ESC Expert consensus document. Expert consensus document on Beta-adrenergic receptor blockers. The Task Force on Beta-Blockers of the European Society of Cardiology // Eur Heart J. – 2004. – Vol. 25 (15). – P. 1341‑1362.
- Feuerstein G., Yue T.L., Ma Xo L. et al. Novel mechanisms in the treatment of heart failure: inhibition of oxygen radicals and apoptosis by carvedilol // Progr Cardiovasc Dis. – 1998. – Vol. 41 (1). – P. 17‑24.
- Fiuzat M., Wojdyla D., Kitzman D. et al. Relationship of beta-blocker dose with outcomes in ambulatory heart failure patients with systolic dysfunction: results from the HF-ACTION (Heart Failure: A Controlled Trial Investigating Outcomes of Exercise Training) trial // J Am Coll Cardiol. – 2012. – 60. – Р. 208‑215.
- Flather M.D., Shibata M.C., Coats A.J. et al.: SENIORS Investigators. Randomized trial to determine the effect of nebivolol on mortality and cardiovascular hospital admission in elderly patients with heart failure (SENIORS) // Eur Heart J. – 2005. – Vol. 26 (3). – P. 215‑225.
- Fleischmann E.H., Schmieder R.E. Are all antihypertensive drug classes equal in reducing left ventricular hypertrophy? // Curr Cardiol Rep. – 2002. – Vol. 4 (6). – P. 474‑478.
- Fonarow G.C., Abraham W.T., Albert N.M. et al. Dosing of beta-blocker therapy before, during, and after hospitalization for heart failure (from Organized Program to Initiate Lifesaving Treatment in Hospitalized Patients with Heart Failure) // Am J Cardiol. – 2008. – 102. – Р. 1524‑1529.
- Fowler M.B., Lottes S.R., Nelson J.J. et al. COHERE Participant Physicians β-Blocker dosing in community-based treatment of heart failure // Am Heart J. – 2007. – 153. – Р. 1029‑1036.
- Galatius S, Gustafsson F, Atar D, Hildebrandt PR. Tolerability of b-blocker initiation and titration with bisoprolol and carvedilol in congestive heart failure: a randomized comparison // Cardiology. – 2004. – 102. – Р. 160‑165.
- Grimm D., Huber M., Jabusch H.C. et al. Extracellular matrix proteins in cardiac fibroblasts derived from rat hearts with chronic pressure overload: effects of beta-receptor blockade // J Mol Cell Cardiol. – 2001. – Vol. 33 (3). – P. 487‑501.
- Guidelines for the diagnosis and treatment of chronic heart failure Task Force for the Diagnosis and Treatment of Chronic Heart Failure, European Society of Cardiology: W.J. Remme and K. Swedberg (Co-Chairmen) // Eur Heart J. – 2001. – Vol. 22. – P. 1527‑1560.
Полный список литературы, включающий 64 пункта, находится в редакции.
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 4 (65) вересень 2019 р.



