28 жовтня, 2019
Особливості фізичного розвитку в підлітків із дифузним нетоксичним зобом
 Одним із найбільш об’єктивних інтегральних показників загального здоров’я дитини є її фізичний і статевий розвиток (ФР і СР). Серед численних факторів, що забезпечують зростання дитини на різних етапах онтогенезу, одну з провідних ролей відіграють тиреоїдні гормони. Найпоширенішою формою патології щитоподібної залози (ЩЗ) в дітей та підлітків є дифузний нетоксичний зоб (ДНЗ), частота якого залежить передусім від екологічної характеристики регіону (Алимова И.Л., 2010). Звертає увагу той факт, що в регіонах із легким дефіцитом йоду частота зоба не відповідає ступеню дефіциту цього хімічного елементу. Це зумовлено мультифакторіальною природою ДНЗ, на формування якого впливають не тільки природні та антропогенні зобогени, але й несприятливі фактори довкілля та гормональна перебудова в період статевого дозрівання (СД) на тлі спадкової обтяженості щодо патології ЩЗ (Багацька Н.В., 2012; Барышева Е.С., 2010).
Одним із найбільш об’єктивних інтегральних показників загального здоров’я дитини є її фізичний і статевий розвиток (ФР і СР). Серед численних факторів, що забезпечують зростання дитини на різних етапах онтогенезу, одну з провідних ролей відіграють тиреоїдні гормони. Найпоширенішою формою патології щитоподібної залози (ЩЗ) в дітей та підлітків є дифузний нетоксичний зоб (ДНЗ), частота якого залежить передусім від екологічної характеристики регіону (Алимова И.Л., 2010). Звертає увагу той факт, що в регіонах із легким дефіцитом йоду частота зоба не відповідає ступеню дефіциту цього хімічного елементу. Це зумовлено мультифакторіальною природою ДНЗ, на формування якого впливають не тільки природні та антропогенні зобогени, але й несприятливі фактори довкілля та гормональна перебудова в період статевого дозрівання (СД) на тлі спадкової обтяженості щодо патології ЩЗ (Багацька Н.В., 2012; Барышева Е.С., 2010).
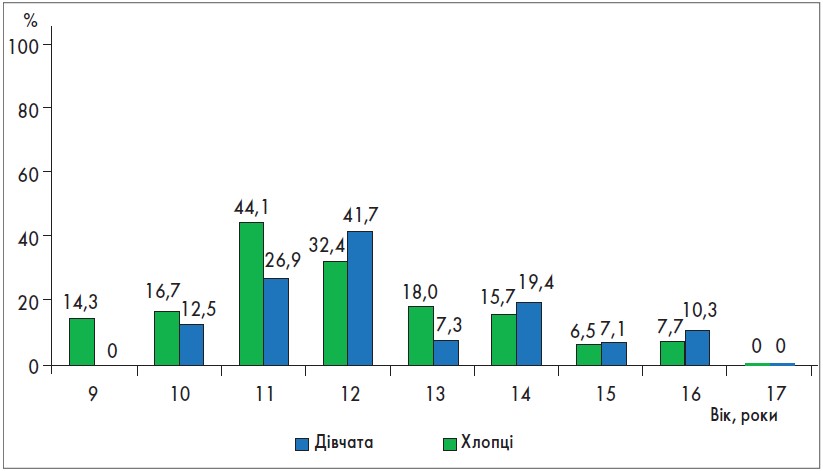
У школярів 10-17 років, що мешкають у Харкові в умовах легкого йододефіциту, проводили оцінку стану ЩЗ відповідно до Протоколів надання медичної допомоги дітям за спеціальністю «Дитяча ендокринологія». Було встановлено, що 18,0% дівчат та 16,8% хлопців мали дифузний зоб I-II ступеня. Найбільшу частоту ДНЗ реєстрували в школярів 11-12 років. Так, у 44,1% дівчат 11 років та в 41,7% юнаків 12 років діагностовано дифузне збільшення ЩЗ, що вірогідно перевищує показники в 10-річних дівчат та хлопчиків (14,3 та 12,9% відповідно). Починаючи з 13 років, як у дівчат, так і в хлопців частота ДНЗ вірогідно зменшується. У підлітків старшого віку (16-17 років) зі сформованими ознаками СР зоб діагностують лише в 6,9% дівчат і 6,2% юнаків (рис. 1).
Рис. 1. Частота ДНЗ у підлітків різного віку при ультразвуковому дослідженні ЩЗ (нормативи ВООЗ від 2001 р.)
На сьогодні доведено, що в період СД частота випадків зоба збільшується, що зумовлено впливом пубертатної імунно-гормональної перебудови на стан тиреоїдної системи. Визначення частоти ДНЗ у школярів із різним ступенем СР дало можливість встановити, що в дівчат на початку СД частота ДНЗ залежала від послідовності формування вторинних статевих ознак (ВСО). Так, у період фізіологічного перебігу пубертату, коли першою ознакою СД є збільшення молочних залоз, майже в половини (41,7%) дівчат діагностували збільшення ЩЗ. При змінах у послідовності появи ВСО, за типом інвертованого пубертату, лише в поодиноких випадках було зареєстровано ДНЗ. У дівчат із розгорнутими ознаками СД частота ДНЗ залежала від наявності менструацій. Так, за відсутності менструацій школярки з ДНЗ склали 24,1%, у дівчат із менструаціями частота зоба була вірогідно нижче (8,1%; р<0,05). У хлопців, так само як і в дівчат, найбільший відсоток ДНЗ (32,0%) реєстрували в період раннього пубертату, що набагато частіше, ніж у хлопців без ознак СД (9,9%) та підлітків із розгорнутими проявами СД (5,4%) (Турчина С.І., 2013).
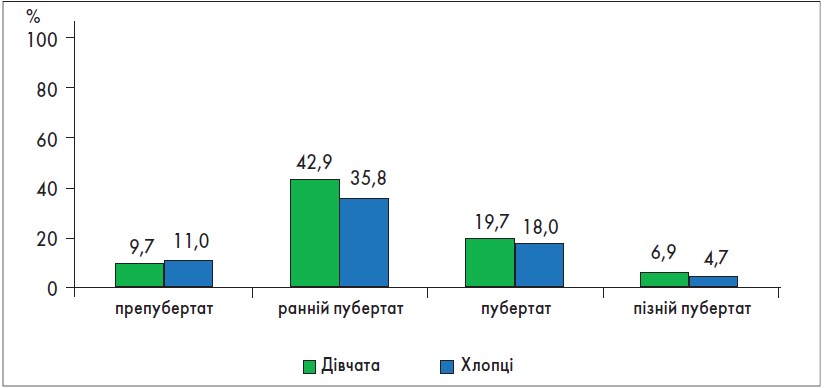
Таким чином, частота ДНЗ у підлітків, які мешкають в умовах слабкого йододефіциту у великому промисловому місті, змінюється протягом пубертату і залежить від рівня СР (рис. 2).
Рис. 2. Частота ДНЗ у дівчат і хлопців із різним рівнем СР
Незалежно від статі фізіологічний початок формування ВСО супроводжується значним збільшенням частоти зоба (42,9% у дівчат і 35,8% у хлопців) із подальшим зменшенням його частоти в пізньому пубертаті (6,9 і 4,7% відповідно).
Збільшення частоти ДНЗ протягом пубертату пов’язують зі змінами гормонального статусу та обміну йоду протягом СД, коли в період активного росту та пубертатної гормональної перебудови підвищується потреба в тиреоїдних гормонах (Буряк В.Н., 2012; Власенко М.В., 2008).
Відповідно до сучасних поглядів збільшення об’єму ЩЗ у пубертатний період визначається не тільки стимулюючим впливом тиреотропного гормону (ТТГ), але й іншими факторами:
- • скороченням періоду напіврозпаду тироксину внаслідок підвищеного метаболізму його в тканинах завдяки посиленню периферичної конверсії тироксину (Т4) у трийодтиронін (Т3);
- • збільшенням тироксинзв’язувальної здатності сироватки крові;
- • посиленням поглинання йоду ЩЗ;
- • збільшенням екскреції йоду із сечею.
Оцінюючи асоціацію між величиною екскреції йоду і СР, виділяють 3 послідовні фази, які відображають зміну інтенсивності йодного обміну:
- «Нейтральний» період дитинства (діти віком до 6 років) характеризується прискореним виведенням мікроелемента із сечею: показники на 32-44% вище, ніж у дітей 8-10 років.
- Препубертатний період (6-11 років) характеризується поступовим зниженням виведення йоду, яке досягає мінімальних показників у віці до 10 років.
- Період СД (12-14 років) супроводжується значною інтенсифікацією йодної екскреції нирками з максимальною величиною йодурії в 12 років, коли швидкість виведення мікроелемента знову починає перевищувати допубертатні (8-10 років) значення на 38-50%.
Таким чином, збільшення частоти ДНЗ у пубертатний період зумовлено гормональною перебудовою, підвищеною потребою в тиреоїдних гормонах та особливостями обміну йоду в умовах пубертатної перебудови. Незважаючи на відсутність клінічних ознак гіпотиреозу, у багатьох пацієнтів із ДНЗ зазначено збільшення рівня ТТГ як до «нормально високих» (2,0-4,0 мМО/л), так і до підвищених (>4,0 мМО/л) значень (Маменко М.Є., 2008; Турчина С.І., 2008).
На сьогодні доведено, що навіть незначуще (2,0-6,0 мМО/л) підвищення концентрації ТТГ у дітей може бути ознакою «мінімальної тиреоїдної недостатності», яка характеризується змінами в ліпідному спектрі, особливостями становлення менструальної функції в дівчаток і відхиленнями в антропометричних параметрах (Буканова С.В., 2004). У цьому разі порушення у ФР можуть бути як наслідком тиреоїдної недостатності (ТН), так і її ранньою ознакою (Камалов К.Г., 2015).
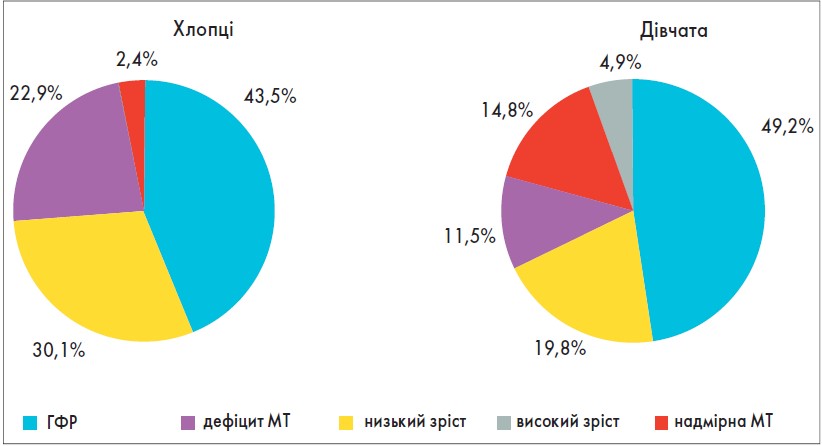
Індивідуальний аналіз росто-вагових показників у пацієнтів із ДНЗ дав змогу виявити відхилення у ФР підлітків із ДНЗ. Так, гармонійний ФР (ГФР) було діагностовано лише в 43,4% хлопців та в 49,2% дівчат. Дисгармонійний ФР був зумовлений у хлопців переважно низьким зростом (затримка темпів росту – ЗТР) та дефіцитом маси тіла (ДМТ), а в дівчат – ЗТР і надмірною МТ (рис. 3).
Рис. 3. Характер ФР у підлітків із ДНЗ
Визначення функціонального стану ЩЗ у підлітків із ДНЗ свідчить про наявність ТН, зумовленої функціональною напруженістю тиреоїдної системи в період СД, і високого ризику формування гіпотиреозу в підлітків із ДНЗ. Ураховуючи негативний вплив ТН на основні антропометричні показники, проведено індивідуальний аналіз ФР у пацієнтів із різним рівнем ТТГ і ознаками ТН і доведено існування залежності між характером тиреоїдного профілю та ФР підлітків із ДНЗ.
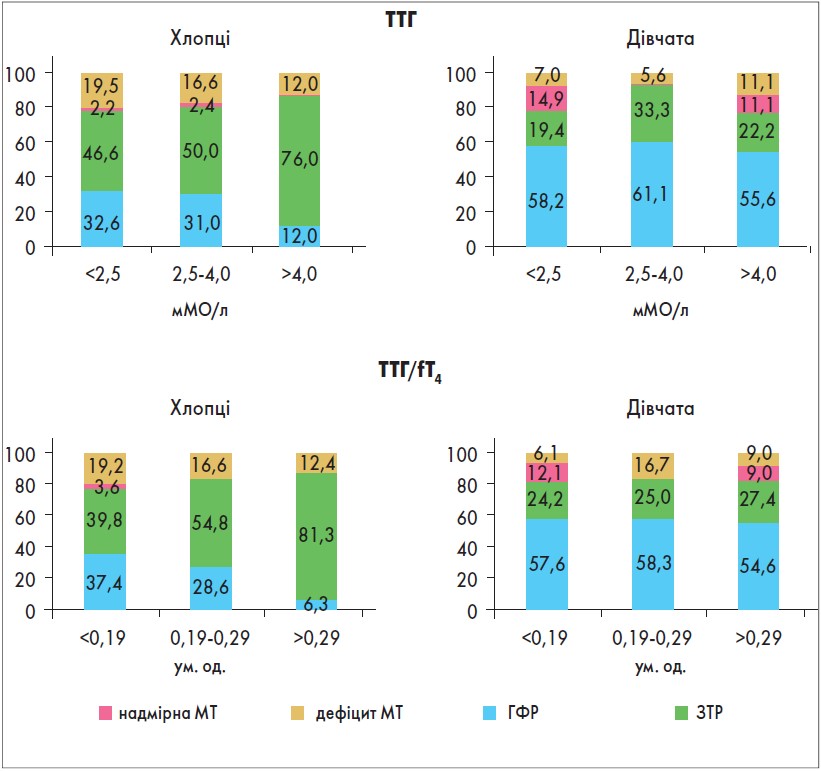
Згідно з отриманими результатами в хлопців із нормальними і «нормально високими» показниками ТТГ практично з однаковою частотою діагностували ГФР (32,6 і 31,0% відповідно) і ЗТР (46,6 і 50,0% відповідно). При збільшенні ТТГ понад 4,0 мМО/л ГФР визначали достовірно рідше (12,0%; р1<0,05 і р2<0,05). У них частіше діагностували ЗТР, яка поєднувалася з ДМТ (76,0%; р1<0,05 та р2<0,05). Водночас, зіставляючи характер ФР у пацієнтів із різними величинами індексу ТТГ/fT4 (вільний T4), який об’єктивніше віддзеркалює функціональний стан тиреоїдної системи, встановлено, що при наростанні ТН відбувається достовірне зменшення частоти хворих із ГФР і збільшення – із ЗТР (рис. 4).
Рис. 4. Характер ФР у пацієнтів із ДНЗ залежно від концентрації ТТГ і величини співвідношення ТТГ/fT4
У дівчат залежність між ТН і характером ФР простежується менш чітко, ніж у хлопців. Так, у групах із різними величинами ТТГ частота пацієнтів із ГФР достовірно не відрізнялася, хоча й зареєстровано було деяке збільшення частоти ЗТР у хворих із «нормально високими» (33,3%) та підвищеними (22,2%) значеннями ТТГ.
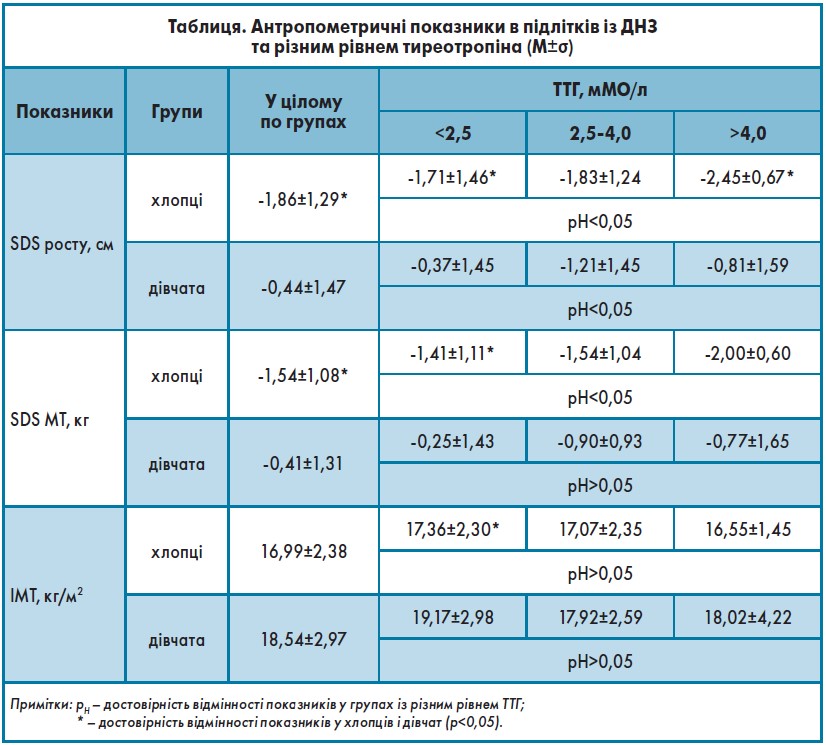
Виявлені статеві відмінності в характері впливу тиреоїдної дисфункції на ФР підлітків із ДНЗ знайшли своє відображення і в середніх по групах значеннях SDS (standard deviation score) зросту, SDS маси тіла та індексу МТ (ІМТ). Наведені в таблиці дані свідчать, що в хлопців у цілому по групі величини SDS росту і SDS МТ достовірно менші проти дівчаток (р<0,01).
Також у хлопчиків виявлена обратна кореляція між величиною ТТГ і показниками SDS росту і SDS МТ: збільшення концентрації ТТГ супроводжується достовірним зменшенням SDS росту і SDS МТ (р<0,05) і не впливає на величину ІМТ. У дівчаток – «нормально високі» і підвищені значення ТТГ поєднуються з достовірним зменшенням SDS росту і значуще не впливають на величину SDS МТ та ІМТ.
Отже, особливості ФР у підлітків із ДНЗ визначаються статтю і функціональним станом тиреоїдної системи. Так, зміни в характері ФР відбуваються на тлі формування ТН, яка характеризується не стільки підвищенням рівня ТТГ, скільки – збільшенням співвідношення ТТГ/fT4, що свідчить про напруженість тиреоїдної системі і високий ризик формування гіпотиреозу. Негативний вплив ТН на росто-вагові показники найбільш чітко проявляється в хлопців, для яких характерне зменшення SDS зросту і SDS МТ, і, як наслідок, підвищення частоти пацієнтів із ЗТР і ДМТ. Відсутність вираженого впливу на антропометричні показники ТН у дівчат із нормальним СР може бути зумовлено впливом естрогенів на процеси зросту в жіночому організмі при нормальному перебігу пубертату. Зазначене пояснює наявність статевих відмінностей у характері впливу ТН на фізичний розвиток підлітків із ДНЗ. Незважаючи на деякі статеві особливості, дисгармонійний ФР формується на тлі прогресування ознак ТН в умовах дефіциту йоду.
Відповідно до загальнодержавної програми «Національний план дій щодо реалізації Конвенції ООН про права дитини», передбачено проведення санітарно-просвітницької роботи серед населення з питань запобігання виникненню йодної недостатності та застосування препаратів калію йодиду під час групової та індивідуальної профілактики в дітей і підлітків, що дасть змогу в цілому покращити стан здоров’я дитячої та дорослої популяції України.
Для здійснення групової та індивідуальної йодної профілактики призначають препарати калію йодиду в дозах, рекомендованих ВООЗ [11, 12]. Діти грудного віку одержують йод із молоком матері, яка застосовує препарати калію йодиду в дозі 200 мкг. У разі штучного вигодовування необхідно додавати в перші 6 міс 50 мкг калію йодиду, з 7-го по 12-й міс –100 мкг калію йодиду; для дітей до 6 років – калію йодиду 90 мкг 1 раз на день; дітям 6-12 років –120 мкг калію йодиду 1 раз на день; старше 12 років – 150 мкг калію йодиду 1 раз на день.
Для лікування ендемічного зобу та ДНЗ: дітям до 6 років призначають 100 мкг калію йодиду 1 раз на день, від 6 до 12 років – 150 мкг 1 раз на день, старше 12 років – 150-200 мкг 1 раз на день, приймати постійно не менше 6 місяців.
У разі прогресування ТН і несприятливого перебігу зоба та погіршення антропометричних показників рекомендовано комплексне застосування калію йодиду в необхідних вікових дозах (препарат Йодомарин® 100 або Йодомарин® 200) та L-Тироксину (виробництва компанії «Берлін-Хемі») до отримання еутиреоїдного стану з подальшим призначенням Йодомарину у вигляді монотерапії протягом ≥6 міс (за показанням). Після досягнення позитивного терапевтичного ефекту як вторинну профілактику рекомендовано призначати препарати Йодомарин® у вікових профілактичних дозах курсами по 3 міс не менше ніж двічі на рік.
Таким чином, визначено гендерні особливості ФР у підлітків із ДНЗ, які значною мірою пов’язані зі станом тиреоїдної системи. Обґрунтовано необхідність комплексного підходу до обстеження підлітків із дисгармонійним ФР, що дасть змогу забезпечити ранню діагностику тиреоїдної дисфункції і принципово новий рівень профілактичних заходів, спрямованих на запобігання порушенням ФР і становлення репродуктивної системи у підлітковому віці.
Література
- Алимова И.Л. Структурное и функциональное состояние щитовидной железы у подростков в регионе с йодной недостаточностью [Текст] / И.Л. Алимова, С.В. Петрова, Е.И. Виноградова // Педиатрия. – 2010. – Т. 89, № 5. – С. 19-24.
- Багацька Н.В. Характеристика ендогенних та екзогенних факторів та мультифакторіальних хвороб в сім’ях хлопців і дівчат із дифузним нетоксичним зобом, які мешкають в умовах легкого йододефіциту [Текст] / Н.В. Багацька, О.І. Плехова, С.І. Турчина // Актуальні проблеми акушерства і гінекології, клінічної імунології та медичної генетики: зб. наук. праць. – 2012. – Вип. 25. – С. 411-418.
- Барышева Е.С. Роль микроэлементов в функциональном и структурном гомеостазе щитовидной железы (клинико-экспериментальное исследование) [Текст] / Е.С. Барышева / Междунар. эндокринол. журн. – 2010. – № 7 (31). – С. 15-25.
- Турчина С.И. Диффузный нетоксический зоб и половое созревание [Текст] / С.И. Турчина // Укр. журн. дитячої ендокринології. – 2013. – № 1. – С. 23-28.
- Буряк В.Н. Особенности тиреоидной патологии в детском возрасте [Текст] / В.Н. Буряк, Е.С. Мурашко // Лікарська справа. – 2012. – № 5. – С. 58-63.
- Власенко М.В. Дифузний нетоксичний зоб у підлітків: генез, діагностика, лікування [Текст]: aвтореф. дис. д-ра мед. наук: 14.01.14 / Власенко Марина Володимірівна; Державна установа «Інститут ендокринології та обміну речовин ім. В.П. Комісаренка АМН України». – К., 2008. – 39 с.
- Маменко М.Є. Вікові та статеві особливості формування тироїдної патології у дітей / М.Є. Масенко, О.І, Єрохіна // Педіатрія, акушерство та гінекологія. – 2008. – № 6. – С. 30-35.
- Турчина С.И. Изменения тиреоидного статуса подростков с диффузным нетоксическим зобом на этапах полового созревания / С.И. Турчина // Пробл. ендокрин. патології. – 2010. – № 4. – С. 19-25.
- Буканова С.В. Тиреоидный статус у детей и подростков с диффузным эндемическим зобом / Буканова С.В., Самсонова Л.Н., Ибрагимова Г.В. и соавт. // Педиатрия. – 2004. – № 3. – С. 15-18.
- Камалов К.Г. Показатели физического и полового развития мальчиков-подростков в зависимости от функционального состояния щитовидной железы / Камалов К.Г., Абусуев С.А., Газимагомедов Г.А. // Исследования и практика в медицине. – 2015. – Т. 2. – № 2. – С. 24-28.
- Протокол надання медичної допомоги дітям за спеціальністю «Дитяча ендокринологія»: наказ МОЗ України № 254 від 27.04.2006. [Текст] / МОЗ України. – Київ, 2006. – 88 с.
- Стандарти надання медичної допомоги хворим із патологічними станами щитоподібної залози в умовах дії негативних чинників довкілля (видання друге, доповнене) / Під ред. д-ра мед. наук О.В. Камінського. – К.: «Старт‑98», 2015. – 224 с.
Тематичний номер «Діабетологія, Тиреоїдологія, Метаболічні розлади» № 2 (46) 2019 р.