25 листопада, 2019
Артеріальна гіпертензія та супутні фактори кардіоваскулярного ризику: сучасне вирішення проблем
ХХ Національний конгрес кардіологів України, який відбувся 25-27 вересня в Києві, зібрав у залах НСК «Олімпійський» медичних науковців та практикуючих лікарів, і не лише кардіологів, а й терапевтів, сімейних лікарів, ендокринологів та представників інших суміжних спеціальностей. Однією з найважливіших проблем, що обговорювалися в ході конгресу, була артеріальна гіпертензія (АГ).
.jpg) Свою доповідь доктор медичних наук, професор Юрій Миколайович Сіренко (ДУ «Національний науковий центр «Інститут кардіології ім. М. Д. Стражеска» НАМН України», м. Київ) присвятив лікуванню вторинних АГ (ВАГ). Відповідно до сучасної класифікації ВАГ поділяють на вроджені (генетичні) та набуті (ренопаренхіматозні, реноваскулярні, ендокринні, ті, що розвилися під час вагітності, гемодинамічні, нейрогенні (у т.ч. мозкові), зумовлені прийомом ліків або інших речовин, пов’язані із синдромом обструктивного апное сну, СОАС). В Україні ВАГ складають 5% усіх АГ, або приблизно 600 тис випадків.
Свою доповідь доктор медичних наук, професор Юрій Миколайович Сіренко (ДУ «Національний науковий центр «Інститут кардіології ім. М. Д. Стражеска» НАМН України», м. Київ) присвятив лікуванню вторинних АГ (ВАГ). Відповідно до сучасної класифікації ВАГ поділяють на вроджені (генетичні) та набуті (ренопаренхіматозні, реноваскулярні, ендокринні, ті, що розвилися під час вагітності, гемодинамічні, нейрогенні (у т.ч. мозкові), зумовлені прийомом ліків або інших речовин, пов’язані із синдромом обструктивного апное сну, СОАС). В Україні ВАГ складають 5% усіх АГ, або приблизно 600 тис випадків.
У рекомендаціях Європейського товариства кардіологів / Європейського товариства гіпертензії з лікування АГ (2018) вказані основні характеристики, які дають можливість запідозрити ВАГ. Серед таких характеристик:
- молодий вік пацієнтів (<40 років) з АГ 2-го ступеня;
- початок АГ будь-якого ступеня в дитинстві;
- гостре погіршення (поява) АГ у пацієнтів із раніше документованою стабільною нормотензією;
- резистентна АГ;
- тяжка АГ (3-й ступінь) або невідкладний стан при гіпертензії;
- наявність виражених опосередкованих гіпертензією уражень органів-мішеней;
- клінічні або біохімічні ознаки наявності у хворого ендокринних причин АГ чи хронічної хвороби нирок (ХХН);
- клінічні ознаки СОАС;
- сімейний анамнез феохромоцитоми, клінічні ознаки, які нагадують феохромоцитому.
Поширеність різних причин ВАГ залежить від віку хворого (табл.).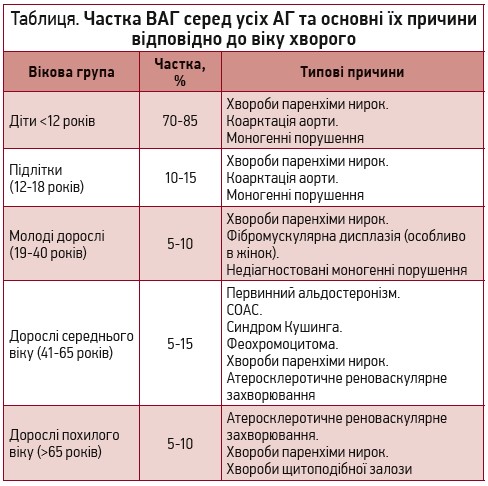
Дуже часто причиною ВАГ стає ХХН. І навпаки, АГ веде до погіршення функції нирок. Відповідно до визначення ХХН вважається наявною, якщо протягом ≥3 міс триває захворювання нирок із відповідними змінами в аналізі сечі незалежно від того, чи є зниження функції нирки чи немає; або якщо так само довго спостерігається зниження функції нирок при швидкості клубочкової фільтрації (ШКФ) <60 мл/хв незалежно від наявності змін в аналізах сечі. Авторське дослідження показало, що контроль артеріального тиску (АТ) допомагає зберегти функцію нирки, запобігаючи зниженню ШКФ. При лікуванні пацієнта з ХХН та АГ слід контролювати рівень не лише АТ та ШКФ, а й мікроальбумінурії та серцево-судинний ризик.
Препаратами першої лінії в лікуванні такого контингенту пацієнтів є блокатори ренін-ангіотензин-альдостеронової системи – інгібітори ангіотензин-перетворювального ферменту (ІАПФ) та блокатори рецепторів до ангіотензину ІІ (БРА), які здебільшого доводиться комбінувати з діуретиками або антагоністами кальцію (АК). До таких комбінацій належить, зокрема, Комбісарт (виробництва АТ «Київський вітамінний завод», Україна).
Щодо реноваскулярної АГ, то 90% цих станів спричиняє атеросклероз, 9-10% – фібромускулярна дисплазія і 1% – хвороба Такаясу. Дослідження CORAL показало, що протягом 5 років помирає майже 40% пацієнтів із атеросклеротичним ураженням ниркових артерій. Також надзвичайно часто наявний рестеноз, однак це не означає, що таких пацієнтів недоцільно лікувати. Доповнення інвазивного втручання повноцінною медикаментозною терапією дає можливість значуще покращити результат лікування.
Ще одна з важливих причин ВАГ – феохромоцитома. Основні її симптоми включають АГ, головний біль, посилене потовиділення, тахікардію, нервозність, підвищену збудливість, ортостатичні розлади, рідше – тремор, болі в животі, порушення зору. Слід зауважити, що, згідно з даними клініки Мейо, приблизно 70% виявлених у ході візуалізаційних досліджень пухлин наднирників являють собою несекреторні аденоми, які не потребують оперативного видалення. У зв’язку з цим першим кроком у діагностиці феохромоцитоми має бути визначення катехоламінів у сечі або крові в спокої або під час кризу. У разі помірного підвищення проводяться функціональні тести. Якщо результат останніх є позитивним, треба призначити візуалізаційні дослідження (комп’ютерну або магнітно-резонансну томографію), сцинтиграфію надниркових залоз або визначення катехоламінів у крові із судин наднирників.
До ендокринних причин ВАГ належить також первинний гіперальдостеронізм (ПГА), що характеризується АГ, гіпокаліємією, змінами на електрокардіограмі (ЕКГ), м’язовою слабкістю, поліурією, головним болем тощо. За підозри на ПГА на тлі гіпокаліємії слід передусім визначити рівень альдостерону та активність реніну, далі – провести пробу з дексаметазоном або візуалізаційні дослідження. Якщо ж у пацієнта наявна нормокаліємія, спочатку проводиться сольове навантаження з метою виявлення прихованої гіпокаліємії. Більшість випадків ПГА (60-70%) спричинені односторонніми альдостерон-продукуючими аденомами, що потребує хірургічного втручання. Часто також виявляються двосторонні гіперплазії (20-30%), які лікують медикаментозно.
Для діагнозу СОАС використовують полісомнографію, коли одночасно реєструють енцефалограму, ЕКГ, електроокулограму, електроміограму дихальних та глоткових м’язів, повітряний потік у дихальних шляхах, показники пульсоксиметрії.
У разі неможливості скоригувати причину ВАГ або неефективності етіотропного лікування необхідно забезпечити пацієнту лікування АГ відповідно до сучасних рекомендацій. Першим кроком основної терапевтичної стратегії медикаментозного лікування АГ є подвійна комбінація БРА/ІАПФ з АК або діуретиком (препарат Комбісарт), другим – потрійна комбінація БРА/ІАПФ з АК та діуретиком (Комбісарт Н виробництва АТ «Київський вітамінний завод»). Препарати Комбісарт та Комбісарт Н виробляються на лініях, сертифікованих відповідно до стандартів GMP (good manufacturing practice), а субстанція валсартану в цих медикаментах не містить домішок канцерогену NDMA (N-nitrosodimethylamine, N-нітрозодиметиламін).
Вітчизняне дослідження ТРИМАРАН вивчало ефективність генеричного препарату Комбісарт-Н (фіксована комбінація валсартану, амлодипіну та гідрохлортіазиду). Авторами було виявлено, що через 6 міс лікування препаратом знизився офісний систолічний АТ на 35,6 мм рт. ст., а офісний діастолічний АТ – на 22,5 мм рт. ст. Треба зауважити, що вагоме зниження відбулося вже через 1 міс лікування: АТ зменшується в середньому на 16,7/10,5 мм рт. ст.
Наприкінці виступу професор Ю. М. Сіренко зазначив, що крім нормалізації підвищеного АТ у терапії АГ надзвичайно важливою є корекція факторів серцево-судинного ризику, асоційованих із гіпертензією. Для пацієнтів із дуже високим серцево-судинним ризиком рекомендовано прийом статинів для досягнення цільового рівня холестерину ліпопротеїнів низької щільності (ХС ЛПНЩ) <1,8 ммоль/л або зниження його на ≥50%, якщо початковий рівень ХС ЛПНЩ становив 1,8-3,5 ммоль/л. Для пацієнтів із високим серцево-судинним ризиком рекомендовано прийом статинів для досягнення цільового рівня ХС ЛПНЩ <2,6 ммоль/л або зниження його на ≥50%, якщо початковий рівень ХС ЛПНЩ становив 2,6-5,2 ммоль/л. Для цього може застосовуватися препарат аторвастатину Лівостор (виробництва АТ «Київський вітамінний завод»). Для вторинної профілактики у хворих на АГ рекомендована антитромбоцитарна терапія, зокрема ацетилсаліцилова кислота в низьких дозах (препарат Магнікор виробництва АТ «Київський вітамінний завод»).
 Продовжила тему АГ доктор медичних наук, професор Тетяна Володимирівна Колесник (ДЗ «Дніпропетровська медична академія МОЗ України»). У своєму виступі Тетяна Володимирівна розповіла про проблеми контролю АТ в Україні та псевдорезистентну АГ (ПРАГ).
Продовжила тему АГ доктор медичних наук, професор Тетяна Володимирівна Колесник (ДЗ «Дніпропетровська медична академія МОЗ України»). У своєму виступі Тетяна Володимирівна розповіла про проблеми контролю АТ в Україні та псевдорезистентну АГ (ПРАГ).
АГ стає найбільш частою причиною передчасної смерті пацієнтів, однак у всьому світі АТ контролюють лише 32,5% хворих на гіпертензію. На початок 2012 р. в Україні було зареєстровано 12 292 642 пацієнти з АГ, що становить приблизно 31,5% дорослої популяції країни (Коваленко В. М., 2012). Міжнародний багатоцентровий проект із виявлення 20 факторів ризику серцево-судинних захворювань у дорослих 30-69 років з’ясував, що поширеність АГ становить 46%. Антигіпертензивні препарати (АГП) приймають 74% хворих, але регулярно – лише 46%. Цільового АТ досягає 14% пацієнтів з АГ, що надзвичайно мало (Митченко Е. И. и соавт., 2014). Реєстр 2964 хворих, які звернулися до кардіолога, демонструє, що тих, хто зміг досягти цільових показників АТ, ще більш мала частка – 10% (Целуйко В. И., 2016). За результатами дослідження за участю 10 158 пацієнтів з АГ, проведеного Ю. М. Сіренком та Г. Д. Радченко, до лікування АГ прихильні лише 27,2% молодих пацієнтів та 24,8% хворих старшого віку, що може почасти пояснювати такий низький рівень досягнення нормотензії.
Відповідно до результатів дослідження EUROASPIRE III неконтрольована АГ спостерігається в 40-50% хворих з АГ. Лікування АГ є особливо складним у разі резистентної АГ (РАГ) (2-5% усіх пацієнтів із підвищеним АТ), ПРАГ (5-20%) та ВАГ (3-5%). Відповідно до визначення РАГ – це така АГ, при якій лікування, що включає модифікацію способу життя та раціональну комбіновану антигіпертензивну терапію трьома препаратами в максимально прийнятних дозах (ІАПФ/БРА, АК, діуретик), не призводить до досягнення цільового рівня АТ <140 мм рт. ст. та/або <90 мм рт. ст. Крім того, перед встановленням діагнозу РАГ потрібно підтвердити високі показники АТ за допомогою добового моніторування та перевірити прихильність пацієнта до лікування. Необхідно також виключити основні причини псевдорезистентності, які включають синдром білого халата, неправильне вимірювання АТ (у т.ч. застосування манжети меншого, ніж потрібно, розміру), ожиріння, СОАС, прийом ліків, що сприяють підвищенню АТ чи затримці натрію, значна кальцифікація плечової артерії (в осіб похилого віку), клінічна інерція (призначення неадекватних доз або нераціональних комбінацій АГП).
Факторами способу життя, здатними спричиняти РАГ, є звичка пересолювати їжу, затримка натрію та води, зловживання алкоголем, ожиріння чи надмірна маса тіла, низька фізична активність. Якщо ці фактори відсутні, за умови справжньої РАГ слід оцінити прийом речовин, здатних підвищувати АТ; з’ясувати рівень прихильності до лікування; оптимізувати фармакотерапію; направити на консультацію до вузького спеціаліста.
Для оцінки прихильності застосовують звіти пацієнтів, упаковки ліків з електронним контролем, визначення концентрації препарату в крові чи сечі, домашнє вимірювання АТ та прийом ліків у присутності медичного персоналу. У разі задовільної прихильності та недосягнення цільового АТ необхідно оптимізувати фармакотерапію шляхом застосування фіксованих комбінацій для зменшення поліпрагмазії та покращання комплаєнсу. За неефективності комбінованої терапії трьома препаратами (БРА/ІАПФ + АК + діуретик) рекомендовано додати спіронолактон, а за його непереносимості – еплеренон (препарат Еплепрес виробництва АТ «Київський вітамінний завод»), амілорид, більш високі дози тіазидних/тіазидоподібних діуретиків, петльовий діуретик, β- чи
Так, додавання еплеренону до ІАПФ або БРА забезпечує додаткове зниження АТ на 5,9 та 6,8 мм рт. ст. відповідно (Krum H., 2001). Метааналіз G. Liu та співавт. (2015) показав, що в контрольованих дослідженнях антагоністи мінералокортикоїдних рецепторів знижували АТ на 16,5/4,1 мм рт. ст., а в неконтрольованих – на 19,7/9,1 мм рт. ст. Необхідно зазначити, що включення еплеренону до схеми лікування РАГ дає можливість зменшити жорсткість артерій, таким чином покращуючи якість лікування.
Наприкінці своєї доповіді професор Т. В. Колесник наголосила, що є декілька основних умов покращання лікування пацієнтів з РАГ: обов’язково досягти цільового рівня АТ; переконатися в правильності вимірювання АТ; не забувати про можливість недостатньої прихильності. Надзвичайно важливими компонентами є здатність лікаря переконати пацієнта в необхідності змін способу життя та застосування медикаментозної терапії, а також взаємна довіра.
Підготувала Лариса Стрільчук
Медична газета «Здоров’я України 21 сторіччя» № 20 (465), жовтень 2019 р.


