30 листопада, 2019
Ефективність та безпека препарату Арлеверт® порівняно з бетагістином (48 мг/добу) в пацієнтів із периферичним вестибулярним запамороченням: проспективне міжнародне багатоцентрове подвійне сліпе клінічне дослідження
Запаморочення (вертіго) – ілюзія руху власного тіла та/або руху оточуючих об’єктів – належить до числа симптомів, на які найчастіше скаржаться пацієнти в щоденній клінічній практиці [1, 2]. За даними проведеного в Німеччині репрезентативного опитування, поширеність запаморочення протягом життя в загальній популяції дорослих становить 7,4%. При цьому вертіго достовірно частіше зустрічається в жінок та осіб похилого й старечого віку [3-5].
Запаморочення зумовлює істотні обмеження щоденної активності пацієнтів і, як наслідок, знижує якість життя, пов’язану зі здоров’ям [3, 4]. Отже, симптоматичне лікування запаморочення є вкрай важливим для негайного полегшення стану пацієнтів, навіть якщо фонові вестибулярні розлади, що зумовили появу цього симптому, поки не є чітко діагностованими. Наразі для симптоматичного лікування вестибулярного запаморочення доступні різні препарати, з-поміж них найчастіше призначається бетагістину гідрохлорид, зазвичай у дозі 16 мг тричі на добу. Бетагістин є аналогом гістаміну, який діє як слабкий агоніст Н1-рецепторів і потужний агоніст Н3-рецепторів [11]. Препарат схвалений для лікування хвороби Мен’єра та периферичного вестибулярного запаморочення. Лікарі первинної ланки охорони здоров’я часто призначають бетагістин у випадку неспецифічної симптоматики й етіології запаморочення [10].
Понад три десятиліття в лікуванні запаморочення різного походження також успішно застосовується препарат на основі фіксованої дозової комбінації (ФДК) цинаризину (20 мг) та дименгідринату (40 мг) (Арлеверт®, Hennig Arzneimittel). Його ефективність при запамороченні базується на подвійному механізмі дії. Цинаризин як специфічний блокатор кальцієвих каналів діє переважно на периферичну вестибулярну систему шляхом інгібування інфлюксу кальцію у вестибулярні волоскові клітини, таким чином регулюючи аферентну вестибулярну передачу сигналів у них [15, 16]. Антигістамінний засіб дименгідринат чинить позитивний ефект щодо усунення запаморочення та блювання шляхом інгібування функцій гістамінових і холінергічних рецепторів у вестибулярних ядрах та блювотному центрі довгастого мозку [17, 18]. Обидва активні компоненти препарату синергічно доповнюють дію один одного [19]. Ефективність і безпека препарату Арлеверт® були продемонстровані в декількох рандомізованих плацебо-контрольованих дослідженнях та в дослідженнях з активним контролем, участь у яких брали пацієнти з різними типами запаморочення [19-28], а також у метааналізі 5 окремих рандомізованих контрольованих досліджень [29].
Це дослідження було сплановане для подальшого вивчення ефективності та безпеки препарату Арлеверт® у пацієнтів із запамороченням, спричиненим периферичними вестибулярними розладами, – патологією, яка часто зустрічається в щоденній клінічній практиці та асоціюється з істотним погіршенням пов’язаної зі здоров’ям якості життя пацієнтів. Мета дослідження полягала в доведенні ефективності препарату Арлеверт® й обґрунтуванні його застосування як потенційно корисної альтернативи бетагістину гідрохлориду в пацієнтів із запамороченням, пов’язаним із різноманітними периферичними вестибулярними розладами.
Пацієнти та методи
До дослідження були включені 306 амбулаторних пацієнтів жіночої (60,1%) та чоловічої статі (віком ≥18 років, середній вік – 53,5 років) із периферичним вестибулярним запамороченням різного генезу (включно з досить неспецифічною або нез’ясованою патологією). У дослідження не були включені пацієнти з більш чітко визначеними периферичними вестибулярними розладами, для яких доступне специфічне лікування (підтверджена хвороба чи синдром Мен’єра, доброякісне позиційне пароксизмальне запаморочення, білатеральна вестибулопатія), а також із гострими периферичними вестибулярними розладами, наявність яких потребувала госпіталізації. Діагнози периферичного вестибулярного запаморочення встановлювалися лікарями-дослідниками (всі вони були досвідченими невроотологами) переважно на підставі даних анамнезу та клінічних обстежень,
Дизайн дослідження
Це було рандомізоване подвійне сліпе міжнародне клінічне дослідження в паралельних групах. Воно проводилося з липня 2013 р. по квітень 2015 р. на базі 8 ЛОР‑клінік, розташованих в Австрії, Чеській Республіці, Болгарії та Росії. Включені до дослідження пацієнти були рандомізовані (в співвідношенні 1:1) для отримання ФДК цинаризину (20 мг) / дименгідринату (40 мг) (Арлеверт®, Hennig Arzneimittel; n=152) або бетагістину дигідрохлориду 16 мг (Бетаверт® N, Hennig Arzneimittel; n=154) протягом 4 тиж (28±2 дні). Кожний препарат призначався в поєднанні з плацебо у формі таблеток, ідентичних відповідному активному препарату порівняння за своїм розміром, масою, кольором, формою та смаком; тобто фактично всі пацієнти приймали 2 таблетки 3 р/добу (зранку та ввечері після їди) – 1 таблетку активного цинаризину/дименгідринату + 1 таблетку плацебо, що імітувала бетагістин (група цинаризину/дименгідринату), або 1 таблетку активного бетагістину + 1 таблетку плацебо, що імітувала цинаризин/дименгідринат (група бетагістину).
Оцінки ефективності та безпеки
Первинною кінцевою точкою ефективності була зміна середнього значення бальної оцінки запаморочення (mean vertigo score, MVS) за комбінованою шкалою з 12 пунктів на тлі застосування препарату Арлеверт® та бетагістину – від вихідного стану до завершення лікування (4 тиж; 28±2 дні). Вторинні кінцеві точки оцінки ефективності включали зміну середнього значення бальної оцінки запаморочення (MVS) від вихідного значення до значення на 2-му візиті (1 тиж; 7±2 дні), середню зміну оцінки за 2-ма субшкалами із 6 пунктів кожна (6 симптомів запаморочення; запаморочення внаслідок дії 6 тригерних факторів), здатність пацієнта до виконання повсякденних видів діяльності, а також оцінку загальної ефективності лікування самими пацієнтами та лікарями. Протягом усього дослідження здійснювалася реєстрація небажаних явищ (НЯ) зі встановленням їхнього ступеня тяжкості та ймовірності зв’язку з прийомом досліджуваного препарату.
Результати
Популяція аналізу згідно з протоколом охопила 294 пацієнти, які завершили дослідження. До аналізу безпеки увійшли дані всіх рандомізованих пацієнтів. Найчастішим діагнозом був «симптомокомплекс, подібний до такого при синдромі/хворобі Мен’єра» – неспецифічний стан, що включає пацієнтів, які страждають на вестибулярне запаморочення, асоційоване з різними ступенями шуму у вухах та/або втратою слуху, але не включає пацієнтів з підтвердженим діагнозом хвороби чи синдрому Мен’єра. Наступними за частотою встановлення діагнозами були: «інше периферичне запаморочення» (в тому числі «неуточнене периферичне запаморочення»), а також «лабіринтна дисфункція». Між групами лікування не зафіксовано достовірних розбіжностей за вихідними демографічними та клінічними характеристиками.
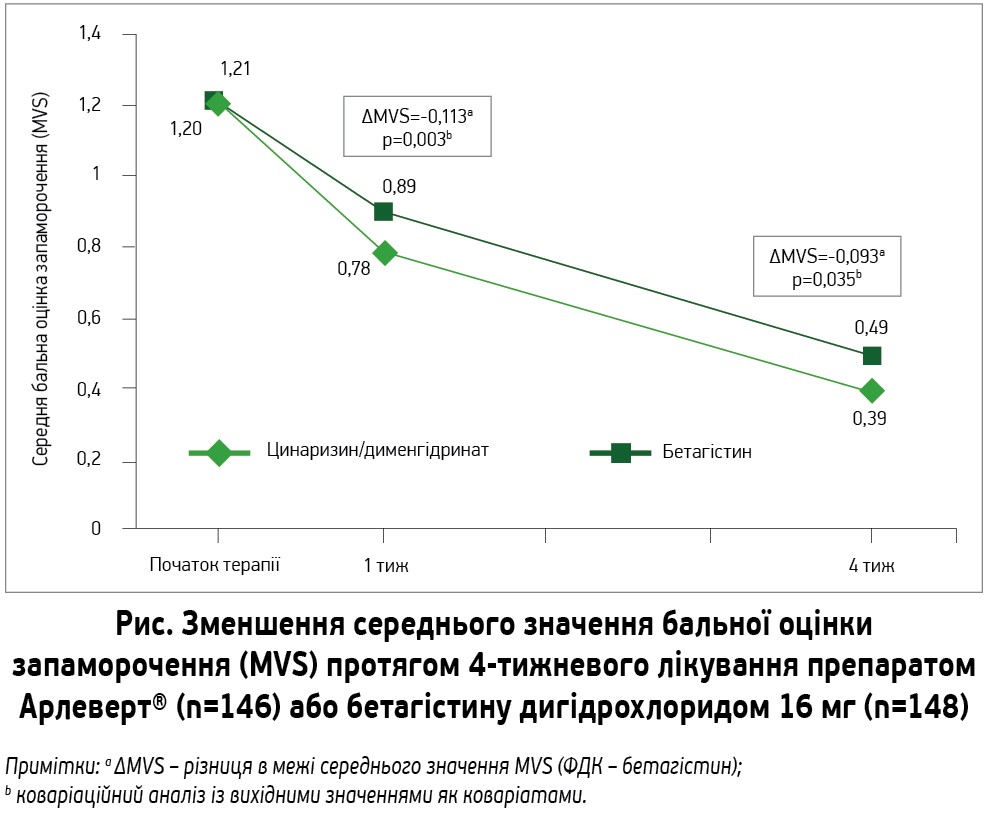
Як показано на рисунку, симптоми запаморочення в обох групах лікування достовірно ослабли в ході 4-тижневого лікування (p<0,001). Межа середнього значення MVS через 4 тиж становила 0,395 для препарату Арлеверт® та 0,488 для групи бетагістину, різниця між групами дорівнювала -0,093 (95% ДІ -0,180; -0,007). Отже, 95% ДІ для різниці в межі середнього значення MVS між препаратами був не тільки повністю нижчим за граничне значення 0,3, а й нижчим за нуль, надаючи докази переваги досліджуваного препарату Арлеверт® перед бетагістином через 4 тиж лікування (p=0,035; первинна кінцева точка). Порівняно з первинним аналізом протокольної популяції (n=294), результати ITT‑аналізу (аналіз даних усіх рандомізованих пацієнтів згідно з призначеним лікуванням, n=303) навіть дещо більше свідчили на користь препарату Арлеверт® – із різницею в MVS через 4 тиж лікування, що дорівнювала -0,117 (95% ДІ -0,210; -0,025; p=0,013).
Що стосується вторинних кінцевих точок оцінки ефективності, то були отримані докази переваги препарату Арлеверт® перед бетагістином у зменшенні середньої бальної оцінки запаморочення (MVS, межа середнього значення) вже через 1 тиж лікування (рис.): розрахована різниця становила -0,113 (95% ДІ -0,188; -0,037; p=0,003). Те саме було відзначено й щодо комбінованої бальної оцінки лише 6 (неспровокованих) симптомів запаморочення (тобто без впливу тригерних факторів) як через 1 тиж (різниця межі середнього значення -0,146; 95% ДІ від -0,232 до -0,059; p=0,001), так і через 4 тиж (різниця межі середнього значення -0,111; 95% ДІ від -0,199 до -0,023; p=0,013).
Через 1 тиж прийому препаратів 49,3% пацієнтів у групі цинаризину/дименгідринату оцінили загальну ефективність лікування як «дуже значне покращення» або як «значне покращення» порівняно з 21,6% пацієнтів у групі бетагістину. На момент закінчення 4-тижневого курсу терапії ці показники збільшилися до 71,2% та 62,8% відповідно, проте без статистично достовірної різниці між групами лікування (p=0,138).
Як засвідчив аналіз даних щодо безпеки, лише у 12 (3,9%) із 306 рандомізованих пацієнтів (у 4 пацієнтів (2,6%) у групі цинаризину/дименгідринату та у 8 пацієнтів (5,2%) у групі бетагістину) було зареєстровано загалом 13 несерйозних НЯ, 7 з яких були кваліфіковані дослідниками як «можливо» або «ймовірно» пов’язані з лікуванням. На момент завершення дослідження 61,1% пацієнтів у групі цинаризину/дименгідринату оцінили переносимість препарату як «дуже хорошу» порівняно із 49,3% у групі бетагістину. Решта (за винятком трьох) пацієнтів у кожній групі лікування оцінили переносимість препаратів як «хорошу» (36,9% та 48,6% відповідно). Оцінки переносимості терапії з боку лікарів-дослідників були практично ідентичні наданим пацієнтами.
Обговорення
Загалом більш високу ефективність препарату Арлеверт® порівняно з бетагістином можна пояснити ширшим спектром активності комбінованого препарату з огляду на той факт, що цинаризин і дименгідринат чинять фармакологічний вплив на різні ділянки вестибулярної системи, а також синергічно доповнюють дію один одного. Цинаризин переважно впливає на периферичну вестибулярну систему, а дименгідринат – на центральну вестибулярну систему. Завдяки цьому подвійному механізму дії Арлеверт® ефективно полегшує запаморочення, спричинене різноманітними вестибулярними розладами. Бетагістин, що є структурним аналогом гістаміну, як вважається, діє переважно на периферичну вестибулярну систему, хоча точний механізм його дії ще належить з’ясувати.
Препарат Арлеверт® виявився більш ефективним, ніж бетагістин, з погляду зменшення середньої бальної оцінки запаморочення (MVS) як через 4 тиж (p=0,035; первинна кінцева точка ефективності), так і через 1 тиж лікування (p=0,003).
Висновки
Препарат Арлеверт® виявився більш ефективним, ніж бетагістин у дозі 48 мг на добу, в лікуванні периферичного вестибулярного запаморочення, асоційованого з різними патологіями. Враховуючи високий і більш сприятливий профіль безпеки препарату Арлеверт®, цей комбінований препарат є потужною й оптимальною альтернативою бетагістину в лікуванні пацієнтів із зазначеним типом запаморочення.
Стаття друкується в скороченні.
Повний список літератури, що включає 35 джерел, знаходиться в редакції.
Scholtz A. W., Hahn A., Stefflova B. et al. Efficacy and Safety of a Fixed Combination of Cinnarizine 20 mg and Dimenhydrinate 40 mg vs Betahistine Dihydrochloride 16 mg in Patients with Peripheral Vestibular Vertigo: A Prospective, Multinational, Multicenter, Double-Blind, Randomized, Non-inferiority Clinical Trial. Clinical Drug Investigation. Published online: 30 September 2019. https://doi.org/10.1007/s40261-019-00858-6
Переклала з англ. Олена Зотова
Медична газета «Здоров’я України 21 сторіччя» № 21 (466), листопад 2019 р.