30 листопада, 2019
Ведення пацієнтів із неклапанною фібриляцією передсердь після перенесеного внутрішньочерепного крововиливу: тандем невролога та кардіолога
25-27 вересня в Києві відбувся XX Національний конгрес кардіологів України – щорічний масштабний форум, який традиційно викликає активну зацікавленість як науковців, так і лікарів-практиків. Цього року наукова програма конгресу охоплювала широке коло міждисциплінарних клінічних проблем, і однією з найважливіших стали кардіоцеребральні порушення. Зокрема, багато доповідей було присвячено практичним аспектам ведення пацієнтів із неклапанною фібриляцією передсердь (НФП), яка наразі є загальновизнаним фактором ризику розвитку мозкового інсульту.
Розглянути зазначену проблему з позицій невролога та кардіолога учасникам конгресу запропонували керівник інсультного центру Універсальної клініки «Оберіг», кандидат медичних наук Юрій Володимирович Фломін і старший науковий співробітник відділу аритмій ДУ «ННЦ «Інститут кардіології ім. М. Д. Стражеска» НАМН України», кандидат медичних наук Таїсія В’ячеславівна Гетьман.
 Керівник інсультного центру Універсальної клініки «Оберіг», кандидат медичних наук Ю.В. Фломін навів клінічний випадок ведення пацієнта з НФП та супутньою патологією, який переніс внутрішньочерепний крововилив (ВЧК).
Керівник інсультного центру Універсальної клініки «Оберіг», кандидат медичних наук Ю.В. Фломін навів клінічний випадок ведення пацієнта з НФП та супутньою патологією, який переніс внутрішньочерепний крововилив (ВЧК).
– Пацієнт Ж., чоловік віком 66 років, колишній офіцер. Увечері 18.06.2019 р. впав у ванній кімнаті, коли приймав душ. Коли пацієнт, який зміг самостійно піднятися на ноги, вийшов звідти, його дружина звернула увагу, що він не відповідав на її запитання. Пацієнт самостійно попрямував до спальні та ліг відпочивати. Уранці 19.06.2019 р. жінка помітила в чоловіка порушення вимови і слабкість правих кінцівок та наполягла на госпіталізації в Олександрівську лікарню м. Києва. Того ж дня пацієнту була виконана комп’ютерна томографія голови, під час якої в глибоких відділах лівої півкулі головного мозку був виявлений крововилив. При падінні пацієнт отримав забій у ділянці правого кульшового суглоба, де утворилася велика гематома м’яких тканин.
З анамнезу відомо, що протягом 20 років пацієнт страждає на панкреатогенний цукровий діабет (ЦД) та отримує лікування інсуліном. Протягом 13 років має медикаментозно контрольовану артеріальну гіпертензію (АГ) (артеріальний тиск (АТ) 120-130 мм рт. ст.). З 2011 р. зазначається НФП, з 2017 р. – у постійній формі, через що було призначене лікування ривароксабаном у дозі 15 мг 1 раз на добу.
Після 2 тиж лікування (04.07.2019 р.) пацієнта перевели в Універсальну клініку «Оберіг». Під час огляду були констатовані: наявність тяжких когнітивних порушень та психомоторного збудження; незадовільне виконання словесних інструкцій; помірна сенсомоторна афазія; помірний правобічний геміпарез; правобічна гемігіпестезія. Ходити самостійно пацієнт не міг, потребував сторонньої допомоги в повсякденній життєдіяльності.
Лабораторні дослідження (10.07.2019 р.): МНС – 1,44, АЧТЧ – 28,1 с, тропонін I високочутливий – 6,2 нг/л, D‑димер (гепаринізована кров) – 0,561 мкг/мл, креатинін – 88 мкмоль/л, кліренс креатиніну (формула Кокрофта-Голта) – 99 мл/хв.
Магнітно-резонансна томографія (МРТ) головного мозку (10.07.2019 р.) – ознаки внутрішньомозкового крововиливу в глибоких відділах лівої півкулі.
Консультативний висновок кардіолога: ішемічна хвороба серця: дифузний кардіосклероз. Постійна форма ФП. АГ, III ст., 1 ст., ризик дуже високий. Серцева недостатність I ст.
Консультативний висновок ендокринолога: ЦД, панкреатогенний (інсулінопотребуючий), тяжка форма в стані компенсації. Хронічна діабетична хвороба нирок G2/A1. Діабетична мікро- та макроангіопатія нижніх кінцівок. Облітеруючий атеросклероз нижніх кінцівок.
Консультативний висновок хірурга: нагноєна гематома правого стегна, стан після хірургічного лікування.
Слід зазначити, що пацієнт Ж. став одним із перших хворих у нашій практиці, в якого виник ВЧК на тлі лікування новими прямими оральними антикоагулянтами (ПОАК), а саме – ривароксабаном у дозі 15 мг. Для того щоб вірно визначити подальшу тактику лікування такого хворого, необхідно відповісти на наступні важливі питання:
- Чи обґрунтоване було призначення ривароксабану в цілому?
- Чи були достатніми підстави для вибору саме такої дози ривароксабану – 15 мг 1 раз на добу?
- Яким є ризик інсульту та кровотеч у цього пацієнта після перенесеного ВЧК та забою м’яких тканин?
- Які засоби вторинної профілактики треба призначити пацієнту?
- Як знизити ризик геморагічних ускладнень?
 Оскільки зазвичай ці складні питання обговорюються неврологами в тандемі з кардіологами, наведений клінічний випадок прокоментувала старший науковий співробітник відділу аритмій серця ДУ «ННЦ «Інститут кардіології ім. М. Д. Стражеска» НАМН України», кандидат медичних наук Т. В. Гетьман – ФП уперше була діагностована в пацієнта Ж. у 2011 р., а ривароксабан призначений у 2017 р. – тобто коли пацієнту виповнилося 64 роки. Щоби визначити, наскільки обґрунтованим було призначення ривароксабану, варто ретроспективно оцінити ризик інсульту та кровотеч у пацієнта у 2017 р. за шкалами CHA2DS2-VASc та HAS-BLED відповідно. За шкалою CHA2DS2-VASc оцінка складала 3 бали (наявність таких критеріїв, як гіпертензія, ЦД, судинне захворювання – облітеруючий атеросклероз нижніх кінцівок), за шкалою HAS-BLED – 0 балів. Тобто на момент призначення ривароксабану пацієнт Ж. мав високий ризик ішемічного інсульту та низький ризик кровотеч. Згідно з рекомендаціями Європейського товариства кардіологів (ESC, 2016) через високий ризик ішемічного інсульту (оцінка ≥2 бали за шкалою CHA2DS2-VASc) призначення ПОАК пацієнту Ж. було однозначно показане. На той момент був зроблений вибір на користь призначення ривароксабану. Але з огляду на те що в пацієнта Ж. був нормальний кліренс креатиніну, згідно з інструкцією для медичного застосування хворий мав отримувати цей препарат у дозі 20 мг, а не 15 мг (доза 15 мг призначається в разі значень кліренсу креатиніну в діапазоні 15-50 мл/хв). Проспективні дані щодо зниження дози ПОАК за наявності факторів ризику кровотеч доступні тільки для дабігатрану та едоксабану. Що ж до ривароксабану та апіксабану, то в рекомендаціях Європейської асоціації серцевого ритму (EHRA) із застосування ПОАК чітко вказується на небезпеку порушення інструкцій для медичного застосування та необґрунтованого зниження дози цих препаратів («off-label»), оскільки це асоціюється зі збільшенням ризику інсульту, при цьому ризик кровотеч ніяк не змінюється (Yao Х. et al., 2017). Таким чином, слід уникати «off-label» зниження дози ПОАК за відсутності показань.
Оскільки зазвичай ці складні питання обговорюються неврологами в тандемі з кардіологами, наведений клінічний випадок прокоментувала старший науковий співробітник відділу аритмій серця ДУ «ННЦ «Інститут кардіології ім. М. Д. Стражеска» НАМН України», кандидат медичних наук Т. В. Гетьман – ФП уперше була діагностована в пацієнта Ж. у 2011 р., а ривароксабан призначений у 2017 р. – тобто коли пацієнту виповнилося 64 роки. Щоби визначити, наскільки обґрунтованим було призначення ривароксабану, варто ретроспективно оцінити ризик інсульту та кровотеч у пацієнта у 2017 р. за шкалами CHA2DS2-VASc та HAS-BLED відповідно. За шкалою CHA2DS2-VASc оцінка складала 3 бали (наявність таких критеріїв, як гіпертензія, ЦД, судинне захворювання – облітеруючий атеросклероз нижніх кінцівок), за шкалою HAS-BLED – 0 балів. Тобто на момент призначення ривароксабану пацієнт Ж. мав високий ризик ішемічного інсульту та низький ризик кровотеч. Згідно з рекомендаціями Європейського товариства кардіологів (ESC, 2016) через високий ризик ішемічного інсульту (оцінка ≥2 бали за шкалою CHA2DS2-VASc) призначення ПОАК пацієнту Ж. було однозначно показане. На той момент був зроблений вибір на користь призначення ривароксабану. Але з огляду на те що в пацієнта Ж. був нормальний кліренс креатиніну, згідно з інструкцією для медичного застосування хворий мав отримувати цей препарат у дозі 20 мг, а не 15 мг (доза 15 мг призначається в разі значень кліренсу креатиніну в діапазоні 15-50 мл/хв). Проспективні дані щодо зниження дози ПОАК за наявності факторів ризику кровотеч доступні тільки для дабігатрану та едоксабану. Що ж до ривароксабану та апіксабану, то в рекомендаціях Європейської асоціації серцевого ритму (EHRA) із застосування ПОАК чітко вказується на небезпеку порушення інструкцій для медичного застосування та необґрунтованого зниження дози цих препаратів («off-label»), оскільки це асоціюється зі збільшенням ризику інсульту, при цьому ризик кровотеч ніяк не змінюється (Yao Х. et al., 2017). Таким чином, слід уникати «off-label» зниження дози ПОАК за відсутності показань.
У наведеному клінічному випадку виникли питання щодо необхідності призначення пацієнту з НФП вторинної профілактики вже після перенесеного ВЧК та термінів її початку. Згідно із сучасними рекомендаціями для аргументованого вибору тактики подальшого ведення таких хворих необхідно час від часу переоцінювати ризики інсульту та кровотеч за відповідними шкалами. Станом на 2019 р. після перенесеного ВЧК оцінка за шкалою CHA2DS2-VASc у пацієнта Ж. склала вже 6 балів (наявність гіпертензії, ЦД, інсульту в анамнезі, судинного захворювання, а також вік 65-74 роки), а оцінка за шкалою HAS-BLED – 3 бали (інсульт, кровотечі, похилий вік – >65 років). Якщо врахувати ще 2 ймовірні фактори ризику кровотеч – неконтрольовану АГ і прийом лікарських засобів, то оцінка ризику кровотечі за шкалою HAS-BLED узагалі зросте до 5 балів. Отже, наразі можна констатувати, що пацієнт Ж. має високий ризик не лише ішемічного інсульту, а й кровотеч.
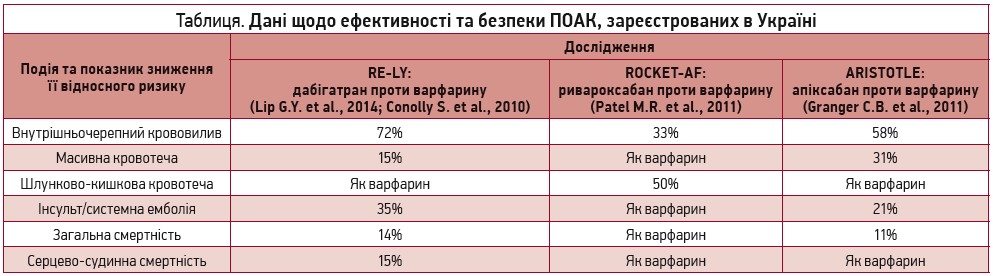
Для здійснення вторинної профілактики інсульту за наявності НФП керівництво ESC (Kirchhof Р. et al., 2016) чітко рекомендує віддавати перевагу ПОАК (апіксабан, дабігатран, ривароксабан, едоксабан) перед антагоністами вітаміну К (клас рекомендацій I, рівень доказовості А). Треба звернути особливу увагу на те, що антитромбоцитарна терапія не рекомендована для запобігання інсульту незалежно від ступеня його ризику (клас рекомендацій III (шкода), рівень доказовості А). Метааналіз 4 рандомізованих контрольованих досліджень з оцінки застосування ПОАК (Ruff С. Т. et al., 2014) продемонстрував достовірне зниження ризику ВЧК (приблизно на 50%), а також смертності внаслідок усіх причин (приблизно на 10%) на тлі прийому цих препаратів порівняно з варфарином. Тому у вторинній профілактиці в пацієнтів, що перенесли ВЧК, віддається перевага саме ПОАК. Сьогодні всі нові ПОАК визнані високоефективними лікарськими засобами, що достовірно знижують ризик як ВЧК, так і ішемічного інсульту (табл.) (Connolly S. J. et al., 2009; Lip G. Y. et al., 2014; Patel M. R. et al., 2011; Lopes R. D. et al., 2012; Giugliano R. P. et al., 2013; Granger С. В. et al., 2011).
За результатами дослідження ARISTOTLE ризик розвитку масивних кровотеч був достовірно нижчим (на 31%) на тлі застосування апіксабану, тому саме цьому ПОАК доцільно віддавати перевагу при веденні хворих із високим ризиком кровотеч (оцінка за шкалою HAS-BLED ≥3 бали). Дослідження ARISTOTLE також переконливо продемонструвало зниження частоти інсультів та системних емболій у пацієнтів із високим ризиком інсульту (оцінка за шкалою CHA2DS2-VASc ≥3 бали) на тлі терапії апіксабаном порівняно із варфарином (Lopes R. D. et al., 2012).
Стосовно питання про терміни поновлення прийому ПОАК після перенесеного ВЧК слід зазначити, що оцінка необхідності відновлення антикоагуляції має проводитися індивідуально для кожного пацієнта. Це рішення ухвалює мультидисциплінарна команда фахівців. Якщо фактори ризику кровотечі усунені, відновлення прийому ПОАК можливе вже через 4-8 тиж після ВЧК. Більш пізній початок (не раніше ніж через 8 тиж) зазвичай практикується в пацієнтів із додатковими факторами ризику кровотеч (масивний ВЧК, одразу декілька церебральних крововиливів, похилий та старечий вік, продовження кровотечі після припинення прийому ПОАК або її виникнення на тлі прийому цих препаратів в адекватній/зниженій дозі, неконтрольована АГ, зловживання алкоголем тощо). Перш ніж знов призначати ПОАК пацієнтам, які перенесли ВЧК, украй важливо забезпечити адекватний контроль АТ. У рекомендаціях ESH/ESC із ведення пацієнтів з АГ та НФП (2018) наголошується, що застосування пероральних антикоагулянтів потребує особливої уваги за наявності високого АТ (систолічний АТ (САТ) ≥180 мм рт. ст. та/або діастолічний АТ ≥100 мм рт. ст.); цільовим є рівень САТ принаймні <140 мм рт. ст., бажаним – <130 мм рт. ст.
Отже, призначаючи пацієнту з НФП той чи інший ПОАК, лікар прагне захистити пацієнта від інсульту та водночас – мінімізувати ризик розвитку кровотеч. Згідно з результатами доказових клінічних досліджень високої якості (зокрема, дослідження ARISTOTLE) такий ПОАК, як апіксабан, дає можливість успішно вирішити обидва ці завдання, оскільки він доведено знижує ризик інсульту та системних емболій та є більш безпечним щодо ризику розвитку масивних кровотеч та ВЧК порівняно з варфарином.
***
По закінченні дискусії Ю. В. Фломін зазначив, що аналіз наведеного клінічного випадку яскраво продемонстрував, як саме кардіологи та неврологи використовують у своїй повсякденній практиці результати останніх наукових досліджень щодо ведення пацієнтів із НФП. Юрій Володимирович підкреслив, що у випадку з пацієнтом Ж. первинно обраний ПОАК був призначений правильно, але не в адекватній дозі. На жаль, деякі лікарі помилково вважають, що призначення ривароксабану в зниженій дозі (15 мг) робить лікування безпечнішим – насправді ж така точка зору не має під собою достатнього наукового підґрунтя. Тому дозування всіх доступних нині ПОАК має здійснюватися лише згідно з відповідними інструкціями для медичного застосування.
Що ж до подальшої долі пацієнта Ж., то, безумовно, через наявність постійної форми НФП хворий потребує проведення адекватної антикоагулянтної терапії і після перенесеного ВЧК. У цьому клінічному випадку вдалося досягнути надійного медикаментозного контролю АТ (≤130/80 мм рт. ст.), і вже через 6 тиж від появи перших симптомів ВЧК пацієнту був призначений апіксабан у дозі 5 мг 2 рази на добу. Цей препарат було обрано відповідно до проведеної оцінки ризику кровотеч, а також побоювань пацієнта та його родини щодо продовження прийому саме того ПОАК, на тлі застосування якого виник ВЧК. Окрім апіксабану хворий отримував також раміприл, амлодипін, бісопролол, метформін та препарати інсуліну тривалої дії. Пацієнту були надані рекомендації з корекції способу життя та призначений наступний візит до судинного невролога й ендокринолога з попереднім виконанням лабораторних аналізів, а також розроблена індивідуальна програма фізичної реабілітації. Уже після призначення апіксабану пацієнту була виконана повторна МРТ головного мозку, за результатами якої констатована стабільність внутрішньомозкової гематоми без збільшення її розмірів. Під час контрольного візиту 1,5 міс потому лікар констатував виражену позитивну динаміку неврологічного відновлення після перенесеного ВЧК та засвідчив високу прихильність пацієнта до прийому апіксабану в якості антикоагулянтного препарату для вторинної профілактики.
Підготувала Анжела Томічева
Стаття друкується за підтримки компанії «Пфайзер».
PP-ELI-UKR-0047
Медична газета «Здоров’я України 21 сторіччя» № 21 (466), листопад 2019 р.