31 липня, 2015
Уніфікований клінічний протокол первинної, вторинної (спеціалізованої) медичної допомоги дорослим та дітям «Вірусний гепатит С»

Содержание статьи:
- І. Паспортна частина.
- ІІ. Загальна частина.
- ІІІ. Основна частина.
- ІV. Опис етапів медичної допомоги.
- VІІІ. Додатки.
І. Паспортна частина
1.1. Діагноз
Гострий вірусний гепатит С
Хронічний вірусний гепатит С
1.2. Коди захворювання за МКХ-10
B17 Інші гострі вірусні гепатити
B17.1 Гострий гепатит С
B18 Хронічний вірусний гепатит
B18.2 Хронічний вірусний гепатит С
1.8. Коротка епідеміологічна інформація
За даними ВООЗ, Україна належить до країн із середньою поширеністю вірусного гепатиту С (ВГС) – інфіковано приблизно 3% громадян, що становить близько 1 170 000 осіб. Однак, за результатами вибіркового моніторингу груп ризику, рівень інфікування ВГС серед деяких з них значно перевищує середньостатистичні показники і сягає 40–60%.
За ступенем негативного впливу на здоров’я населення та масштабами захворюваності вірусні гепатити в Україні посідають домінуюче місце в структурі інфекційної патології разом із грипом та гострими інфекційними захворюваннями верхніх дихальних шляхів.
В останні роки помітна тенденція до збільшення захворюваності на ВГС, у тому числі частоти випадків хронічних форм захворювання. За даними ВООЗ, на хронічний ВГС страждає близько 150 млн осіб, а 350 тис. щорічно помирають унаслідок ураження печінки вірусом гепатиту С (HCV). Захворюваність та летальність внаслідок гепатитів В і С на планеті прогресивно збільшуються та, за даними експертів, подвояться до 2015–2020 рр. Вже зараз загальна кількість хворих на гепатити у світі в 14–15 разів перевищує кількість ВІЛ-інфікованих. Вірусні гепатити є у 50–100 разів більш заразними, ніж ВІЛ-інфекція.
Вірусні гепатити з гемоконтактним механізмом передачі збудників, перш за все, ВГС, є важливою проблемою сучасної медичної науки і практичної охорони здоров`я усіх країн світу. Це обумовлено широкою поширеністю, високим рівнем захворюваності, вираженим поліморфізмом клінічних проявів, численністю шляхів та факторів передачі збудників, а також надзвичайно несприятливими наслідками, до яких можуть призвести гепатити, – формуванням хронічних уражень печінки, в тому числі цирозу і гепатоцелюлярної карциноми (ГЦК).
За оцінками ВООЗ, 57% випадків цирозу печінки і 78% випадків первинного раку печінки зумовлені впливом вірусів гепатиту В або С. Окрім цього, гепатити В та С мають багато позапечінкових проявів, що ускладнює їх діагностику та може перешкоджати призначенню відповідного лікування.
1.9. Етіологія та характеристика епідемічного процесу
HCV являє собою однониткову РНК та належить до сімейства Flaviviridae. Нині виділяють 11 генотипів вірусу, понад 100 його субтипів та велику кількість так званих квазівидів. Останні відіграють основну роль у формуванні стійких до лікування штамів вірусу. Генотипи 1а, 1b, 2а, 2b, 2с і 3а становлять понад 90% усіх ізолятів вірусу, що отримані у Північній та Південній Америці, Європі, Росії, Китаї, Японії, Австралії та Новій Зеландії. Генотипи 4, 5а та 6 відповідно виявляють у Центральній та Південній Африці, Південно-Східній Азії. У нашій країні та інших країнах колишнього СНД відмічається переважання генотипів 1b (близько 70%) та 3a. Генотип не впливає на наслідок захворювання, але дає змогу спрогнозувати ефективність та тривалість лікування. З генотипами 1 та 4 частіше пов’язана низька відповідь на інтерферонотерапію; з 3-м генотипом частіше пов’язаний стеатоз печінки.
Джерелом інфекції є хворі на гострий чи хронічний ВГС та вірусоносії. У крові вірус з’являється через 1–3 тиж після інфікування.
Провідним механізмом передачі ВГС є гемоконтактний; можливий вертикальний механізм передачі. До запровадження тестування крові на наявність HCV найбільше епідеміологічне значення мало переливання крові та її компонентів. Нині найактуальнішим є інфікування при вживанні парентеральних наркотичних речовин (у 87,5% споживачів ін’єкційних наркотиків виявляють антитіла проти HCV, частіше 3а генотипу), а також через маніпуляції в лікувальних закладах (оперативні втручання, стоматологічні процедури тощо). Передавання збудника при гетеро- і гомосексуальних контактах, від інфікованої матері до новонародженого може мати місце, але реалізується значно рідше, ніж, наприклад, при вірусному гепатиті В (ВГВ). Так, ризик інфікування дитини серопозитивною жінкою в середньому становить 2% та зростає до 7% за наявності в крові вагітної РНК HCV. Якщо жінка під час вагітності продовжує споживати ін’єкційні наркотичні речовини, ризик інфікування дитини зростає до 10%, при ко-інфекції з ВІЛ – до 20%. Групами ризику також є хворі, які страждають на гемофілію, та ті, що перебувають на гемодіалізі.
Дані щодо стійкості вірусу в навколишньому середовищі обмежені. На відміну від ВГВ, забруднення навколишніх предметів кров’ю не є вагомим фактором ризику передачі інфекції, за винятком відділень гемодіалізу. Середній відсоток сероконверсії (поява антитіл проти HCV) після випадкової трансшкірної експозиції від інфікованого джерела становить у середньому 1,8%, до того ж у більшості випадків передавання здійснювалось через порожнисті голки. Не було задокументовано випадків передачі вірусу через непошкоджені шкіру та слизові оболонки.
Природна сприйнятливість людей до HCV висока. Антитіла, що їх виявляють у організмі інфікованої людини, не мають захисних властивостей, їх наявність не захищає від повторного інфікування HCV як гомологічного, так і іншого штаму.
Гострий ВГС характеризується: чітким контактом з інфекцією та позитивною РНК HCV за 6 міс, або значним зростанням рівня аланінамінотрансферази (АЛТ) у сироватці крові, або сероконверсією, при якій противірусні антитіла та/або РНК HCV відсутні в першому і наявні в другому зразку.
Хронічний ВГС – безперервне захворювання на ВГС поза гострою фазою.
ІІ. Загальна частина
ІІІ. Основна частина
3.1. Для установ, що надають первинну медичну допомогу
3.1.1. Профілактика
Обґрунтування:
Доведено, що знання пацієнтом свого вірусного статусу уповільнює прогресування ВГС; рання діагностика дає можливість своєчасно розпочати лікування.
Застосування бар’єрних контрацептивів, засобів разового використання (шприци, голки тощо), засобів індивідуального захисту (рукавички) запобігає інфікуванню ВГС.
Існує низький ризик передачі інфекції від інфікованих HCV членам їх сімей, близьким або статевим партнерам.
Необхідні дії лікаря:
Проводити роз’яснювальну роботу щодо профілактики захворювання на вірусні гепатити серед громади; рекомендувати щеплення проти ВГА, ВГВ.
Роз’яснювати пацієнтам суть первинної та вторинної профілактики (див. 4.1).
Оцінювати належність кожного пацієнта до груп ризику щодо розвитку ВГС (див. 4.2).
Кожного пацієнта розглядати як потенційно інфікованого HCV (користуватися засобами індивідуального захисту при безпосередньому контакті з пацієнтом, біологічними тканинами чи рідинами, не допускати потрапляння біологічних тканин та/чи рідин у навколишнє середовище).
3.1.2. Організація діагностично-лікувального процесу
Обґрунтування:
Доведено, що вдосконалення допомоги пацієнтам з ВГС можливе завдяки мультидисциплінарній інтеграції.
Доведено, що в немовлят існують особливості, пов’язані з перинатальним ризиком інфікування від інфікованої матері, особливостями імунної відповіді у дітей раннього віку та грудним вигодовуванням (див. 4.4).
Доведено, що виключно клінічна оцінка тяжкості захворювання пацієнтів має тенденцію до недооцінювання тяжкості змін у печінці. Біохімічні маркери можуть використовуватися як альтернатива біопсії печінки для діагностування цирозу або прямого скринінгу ускладнень фіброзу.
Необхідні дії лікаря:
Пацієнтам, які мають скарги на загальну втомлюваність, зниження працездатності, проводити анкетування (див. Додаток 1). У разі позитивного результату анкетування направляти на попередню діагностику (див. Додаток 4 ).
Пацієнтів з груп ризику (див. 4.2) один раз на рік направляти на попередню діагностику.
Направляти пацієнтів з позитивним результатом попередньої діагностики протягом 7 днів до інфекціоніста.
Направляти пацієнтів до суміжних спеціалістів за наявності у пацієнта з ВГС факторів, що обтяжують перебіг хвороби (див. 4.5).
Обстежувати немовлят, народжених від HCV- та/чи ВІЛ-позитивних матерів, відповідно до алгоритму обстеження немовлят (див. Додаток 5).
Сприяти виконанню призначень та рекомендацій інфекціоніста для дітей, у яких визначається РНК HCV.
Клінічне ведення дітей, інфікованих HCV, проводити разом з педіатричною службою.
Оцінюючи тяжкість захворювання, спиратися на оцінку стану печінки та позапечінкові прояви.
3.1.3. Лікування
3.1.3.А. Лікування гострого ВГС
Обґрунтування:
Нині доведено неефективність превентивного лікування; відкладене лікування ВГС на 3–6 міс не знижує відповідь на лікування, а відкладене вже на 1 рік – знижує.
Лікування призначається інфекціоністом відповідно до пункту 4.6.
Необхідні дії лікаря:
Сприяти виконанню пацієнтом усіх рекомендацій інфекціоніста.
Сприяти здійсненню інфекціоністом клінічного моніторингу пацієнтів з гострим ВГС протягом 3 міс після встановлення діагнозу; обстеженню на РНК HCV через 3 міс після встановлення діагнозу гострого ВГС. У разі виявлення РНК HCV пацієнта направити до інфекціоніста.
3.1.3.Б. Лікування хронічного ВГС
Пацієнти з хронічним ВГС підлягають оцінці противірусного та симптоматичного лікування.
Противірусне лікування хронічного ВГС призначається інфекціоністом.
Лікування жінкам призначається після виключення вагітності.
Пацієнти під час лікування потребують оцінки стану та виявлення побічних реакцій, а також факторів, що впливають на ефективність противірусного лікування (див. табл. 6).
Необхідні дії лікаря:
Сприяти виконанню пацієнтом усіх рекомендацій спеціаліста.
Інформувати пацієнта, що ефективність лікування залежить від дотримання призначень, а також факторів, що обтяжують лікування.
Інформувати пацієнта про негативний вплив противірусного лікування на розвиток плода. Рекомендувати під час лікування та впродовж 6 міс після нього дотримуватися подвійної контрацепції – застосування чоловіками презервативів та оральних контрацептивів жінками.
Пацієнтам, у яких виникли побічні реакції під час противірусного лікування, надавати рекомендації відповідно до наведеного переліку побічних реакцій (див.табл. 7).
Під час лікування проводити моніторинг психічного статусу пацієнтів, у яких до того мали місце психічні розлади; направляти до психіатра за наявності психічних розладів.
Перед початком, під час та після лікування всіх пацієнтів потрібно обстежувати щодо депресії.
Роз’яснювати пацієнтам, що важливо продовжувати відвідувати ЗОЗ з метою контролю їх стану здоров’я та корекції лікування.
Проводити моніторинг стану пацієнтів з нирковою недостатністю під час противірусного лікування.
3.1.3.В. Лікування запущених стадій ВГС
Обґрунтування:
Доведено, що пізня діагностика та, відповідно, пізній початок лікування хронічного ВГС призводить до запущеного ВГС, ознаками якого є ГЦК та цироз. Лікування пацієнтів із запущеним ВГС має свої особливості (див. 4.6.5).
Рання діагностика ГЦК можлива, якщо проводити УЗД печінки раз на 6 міс та визначати рівень α-фетопротеїну раз на рік.
Необхідні дії лікаря:
Сприяти виконанню призначень інфекціоніста.
Проводити моніторинг клінічного стану пацієнтів, які отримують противірусне лікування; відстежувати побічні реакції фармакотерапії у встановленому порядку.
3.1.4. Харчування, підтримувальна терапія та додаткові методи лікування
Обґрунтування:
Доведено, що одужання пацієнтів залежить від того, який спосіб життя вони ведуть, наприклад, надлишкова вага та неповноцінне харчування знижують шанси на одужання. З іншого боку, противірусне лікування знижує стійкість до фізичного навантаження, а застосування додаткових лікарських засобів може призвести до негативних наслідків.
Необхідні дії лікаря:
Консультувати пацієнтів щодо адекватного харчування, фізичного навантаження та необхідності підтримання нормальної маси тіла.
Пацієнтів з цирозом печінки стадій B, С за Чайлд-П’ю (Сhild-Pugh) направляти на консультацію до дієтолога.
Застерігати пацієнтів щодо певних загроз, пов’язаних із застосуванням додаткових лікарських засобів.
3.2. Для установ, що надають вторинну неінфекційну медичну допомогу
3.2.1. Профілактика
Обґрунтування:
Застосування бар’єрних контрацептивів, засобів разового використання (шприци, голки тощо), засобів індивідуального захисту (рукавички) запобігає інфікуванню ВГС.
Необхідні дії лікаря:
Кожного пацієнта розглядати як потенційно інфікованого (користуватися засобами індивідуального захисту при безпосередньому контакті з пацієнтом, біологічними тканинами чи рідинами, не допускати потрапляння біологічних тканин та/чи рідин у навколишнє середовище).
3.2.2. Організація лікувального процесу
Необхідні дії лікаря:
Консультувати пацієнтів з ВГС, які звертаються за направленнями від сімейного лікаря чи спеціаліста.
3.2.3. Особливості ВГС у дітей
Обґрунтування:
У немовлят існують особливості, що пов’язані з перинатальним ризиком інфікування від інфікованої матері, особливостями імунної відповіді у дітей раннього віку та грудним вигодовуванням (див. 4.4).
Необхідні дії лікаря:
Акушерам-гінекологам дотримуватися ведення вагітності за відповідним протоколом.
Педіатрам раз на півроку проводити обстеження дітей (старше 12 міс), у яких визначається РНК HCV, або за направленням сімейного лікаря чи спеціаліста.
3.2.4. Харчування, підтримувальна терапія та додаткові методи лікування
Обґрунтування:
Одужання пацієнтів багато в чому залежить від того, який спосіб життя вони ведуть. Наприклад, надлишкова вага та неповноцінне харчування знижують шанси на одужання. З іншого боку, противірусне лікування знижує стійкість до фізичного навантаження, а застосування додаткових лікарських засобів може призвести до негативних наслідків.
Необхідні дії лікаря:
Консультувати пацієнтів щодо адекватного харчування, фізичних навантажень та необхідності підтримання нормальної маси тіла, щодо певних загроз, пов’язаних із застосуванням додаткових лікарських засобів (див. 4.7).
3.3. Для установ, що надають вторинну інфекційну медичну допомогу
3.3.1. Організація діагностично-лікувального процесу
Обґрунтування:
Доведено, що вдосконалення допомоги пацієнтам з ВГС можливе завдяки мультидисциплінарній інтеграції.
Організація своєчасної діагностики ВГС та адекватного специфічного противірусного лікування є вирішальними факторами одужання та запобігання розвитку ускладнень. Інформування та навчання пацієнтів є одним із засобів припинення подальшого поширення HCV.
Необхідні дії лікаря:
Співпрацювати із сімейним лікарем пацієнта.
Призначати обстеження та лікування пацієнта відповідно до вимог цього протоколу, що заснований на сучасних наукових доказах.
3.3.2. Діагностика
Обґрунтування:
Доведено, що своєчасна діагностика захворювання дає змогу розпочати лікування в строки, що максимально сприяють одужанню.
Доведено, що виключно клінічна оцінка тяжкості захворювання пацієнтів має тенденцію до недооцінювання тяжкості змін у печінці.
Біохімічні маркери фіброзу та фіброеластографія можуть використовуватися як альтернатива біопсії печінки.
Необхідні дії лікаря:
Обов’язкові:
Проведення подальшої діагностики та диференційної діагностики у пацієнтів з позитивними результатами попередньої діагностики.
Оцінюючи тяжкість стану пацієнта, спиратися на оцінку стану печінки та позапечінкові прояви.
Направляти пацієнта на обстеження: АЛТ, α-фетопротеїн, фібротест; у разі необхідності використовувати додаткові методи обстеження.
Встановлювати діагноз відповідно до пункту 4.3.
Забезпечити передачу інформації сімейному лікарю про пацієнтів, які консультувались з приводу ВГС.
Бажані:
Направляти пацієнта на проведення фіброеластографії.
3.3.3. Вторинна профілактика
Обґрунтування:
Доведено, що знання пацієнтом свого вірусного статусу уповільнює прогресування ВГС; рання діагностика дає можливість своєчасно розпочати лікування.
Застосування бар’єрних контрацептивів, засобів разового використання (шприци, голки тощо), засобів індивідуального захисту (рукавички) запобігає інфікуванню ВГС.
Існує низький ризик передачі інфекції від інфікованих HCV до членів їх сімей, близьких або статевих партнерів.
Необхідні дії лікаря:
Проводити роз’яснювальну роботу щодо вторинної профілактики захворювання на вірусні гепатити; рекомендувати щеплення проти ВГА, ВГВ (див. 4.1).
Кожного пацієнта розглядати як потенційно інфікованого (користуватися засобами індивідуального захисту при безпосередньому контакті з пацієнтом, біологічними тканинами чи рідинами, не допускати потрапляння біологічних тканин та/чи рідин у навколишнє середовище).
3.3.4. Особливості ВГС у дітей
Обґрунтування:
У немовлят існують особливості інфікування, що пов’язані з перинатальним ризиком інфікування від інфікованої матері, особливостями імунної відповіді у дітей раннього віку та грудним вигодовуванням (див. 4.4).
Необхідні дії лікаря:
Обстежувати немовлят, народжених від HCV- та/чи ВІЛ-позитивних матерів відповідно до алгоритму обстеження немовлят (див. Додаток 5).
Проводити огляд РНК-HCV-позитивних дітей кожні 6 міс.
Проводити моніторинг HCV-позитивних дітей з метою виявлення тих, хто має підвищений ризик прогресування фіброзу печінки та можуть потребувати противірусного лікування (проводити моніторинг спільно із сімейним лікарем та педіатром).
3.3.5. Лікування ВГС
Обґрунтування:
Не доведено ефективності превентивного лікування ВГС.
Доведено, що після інфікування впродовж 3 міс >30% осіб одужують.
Лікування проводиться противірусними препаратами відповідно до генотипу вірусу та супутньої патології у пацієнта.
При гострому ВГС противірусне лікування матиме максимальний ефект, якщо розпочати його з 3-го по 6-й місяць після інфікування.
Доведено, що існують модифіковані та немодифіковані фактори, що впливають на перебіг хвороби (див. 4.5).
Активність АЛТ не є показником тяжкості стану печінки при ВГС.
Особам з ВГС рекомендовані щеплення проти ВГА та ВГВ.
Противірусне лікування протипоказане вагітним.
Існують фактори, що впливають на противірусне лікування (див. табл. 5).
Противірусне лікування супроводжується побічними реакціями.
Існують оптимальні терміни та схеми лікування пацієнтів у залежності від генотипу вірусу, відповіді на лікування (див. 4.6 та Додатки 6–9).
Необхідні дії лікаря:
Володіти інформацією про тих, хто проходить обстеження на ВГС.
Проводити клінічний моніторинг пацієнтів з гострим ВГС протягом 3 міс після встановлення діагнозу.
Призначити обстеження на РНК HCV на початку 4-го місяця після встановлення діагнозу гострого ВГС.
Пацієнтам, у яких протягом 3 міс після інфікування не відбулось кліренсу вірусу HCV:
- визначити генотип вірусу;
- призначати основну схему лікування відповідно до пункту 4.6;
- при потребі розглядати застосування додаткових лікарських засобів.
Інформувати пацієнтів про залежність перебігу хвороби від модифікованих та немодифікованих факторів (див. 4.5).
Проводити моніторинг активності АЛТ кожні 3 міс.
Пропонувати пацієнтам з ВГС щеплення проти ВГА та ВГВ.
Рекомендувати пацієнтам під час противірусного лікування та впродовж 6 міс після нього дотримуватися подвійної контрацепції (презервативи та оральні контрацептиви).
Проводити моніторинг під час противірусного лікування психічного статусу пацієнта, який до того мав психічні розлади; направляти до психіатра за наявності психічних розладів.
Обстежувати всіх пацієнтів на предмет депресії перед початком, під час та після лікування.
Роз’яснювати пацієнтам важливість продовження відвідування ЗОЗ з метою контролю їх стану здоров’я та корекції лікування.
Проводити моніторинг стану пацієнтів з нирковою недостатністю.
3.3.5.1. Лікування запущеної інфекції
Обґрунтування:
Доведено, що наслідком хронічного ВГС може бути ГЦК та цироз печінки.
УЗД печінки раз на 6 міс підвищує імовірність своєчасного виявлення ГЦК. Скринінговим маркером ГЦК є також α-фетопротеїн.
Лікування пацієнтів з цирозом не менш токсичне, ніж пацієнтів без цирозу.
Необхідні дії лікаря:
Проводити відбір кандидатів на консервативне та оперативне лікування.
Проводити УЗД печінки раз на 6 міс та визначення рівня α-фетопротеїну – раз на рік.
При розвитку ГЦК вести пацієнта разом з онкологом.
Кандидатів на трансплантацію печінки направляти на консультацію трансплантолога.
3.3.5.2. Особливості лікування пацієнтів у ситуаціях, коли пегільований інтерферон протипоказаний
Для лікування пацієнтів з гематологічними змінами (нейтропенія, тромбоцитопенія як наслідок лікування ВГС), онкогематологічною патологією, вагітністю, дітей перших років життя доцільно розглянути використання непегільованого α-інтерферону (α-ІФН).
3.3.6. Харчування, підтримувальна терапія та додаткові методи лікування
Обґрунтування:
Одужання пацієнтів багато в чому залежить від того, який спосіб життя вони ведуть. Наприклад, надлишкова вага та неповноцінне харчування знижують шанси на одужання. З іншого боку, противірусне лікування знижує стійкість до фізичного навантаження, а застосування додаткових лікарських засобів може призвести до негативних наслідків.
Необхідні дії лікаря:
Консультувати пацієнтів щодо адекватного харчування; фізичних навантажень та необхідності підтримання нормальної маси тіла (див. 4.7).
Пацієнтам із запущеною хворобою печінки призначати відповідну нутритивну підтримку.
Інформувати пацієнтів про певні загрози, пов’язані із застосуванням додаткових лікарських засобів.
ІV. Опис етапів медичної допомоги
4.1. Первинна та вторинна профілактика інфікування ВГС
Первинна профілактика спрямована на запобігання інфікуванню особи, а в разі інфікування – на своєчасну діагностику і початок лікування, що є запорукою одужання. Первинна профілактика інфікування полягає в обізнаності населення щодо проблеми ВГС та дотримання певної поведінки. Така поведінка передбачає: утримання від контактів з рідинами організму іншої людини (кров, міжтканинна рідина, сперма): треба практикувати безпечний секс (застосовувати бар’єрні контрацептиви – презервативи), користуватися засобами разового (шприци, голки, крапельні системи, гінекологічні оглядові дзеркала тощо) та індивідуального (зубні щітки, леза для гоління, контактні лінзи) призначення, засобами індивідуального захисту (рукавички, окуляри, фартухи тощо), стерильним інструментом багаторазового призначення (манікюрний, стоматологічний, хірургічний, лабораторний інструмент, інструмент для пірсингу й татуажу тощо); працівникам, які мають контакт з рідинами та тканинами організму, не допускати забруднення навколишнього середовища останніми та користуватися засобами індивідуального захисту.
Особам, які мали (або не виключають) контакт з рідинами організму іншої людини, звертатися до сімейного лікаря з приводу своєчасної діагностики захворювання, оскільки чим раніше буде встановлений діагноз, тим швидше можна буде прийняти рішення стосовно лікування (якщо воно буде потрібно та не матиме протипоказань) і тим більші шанси одужати.
Вторинна профілактика спрямована на запобігання поширенню вірусу в навколишнє середовище інфікованою особою та зменшення тяжкості перебігу хвороби шляхом модифікації способу життя і проведення щеплень проти ВГА та ВГВ.
Суть вторинної профілактики: інфікована особа має усвідомлювати суть свого захворювання (етіологія, шлях передачі вірусу, наслідки хвороби для організму) і, як сумлінний член суспільства, поводити себе безпечно по відношенню до інших людей, пам’ятаючи про те, що саме вона може інфікувати іншого.
Згідно з чинним законодавством, інфікована особа несе відповідальність за поширення інфекції серед інших.
Інфіковані особи повинні не брати участь у програмах донорства (крові, органів, сперми тощо); не працювати на роботах, що передбачають контакт з рідинами організму (хірургічні, акушерсько-гінекологічні, стоматологічні, лабораторні маніпуляції; маніпуляції в салонах пірсингу й татуажу тощо); не користуватися спільними засобами для ін’єкцій; не практикувати небезпечний секс (без застосування бар’єрних контрацептивів – презервативів).
Інфіковані HCV породіллі мають забезпечити можливість обстеження своєї новонародженої дитини в строк, зазначений лікарем.
Інфікованим особам рекомендовано щепитися від ВГА та ВГВ, оскільки ко-інфекція з ВГА та/чи ВГВ значно обтяжує перебіг хвороби і зменшує шанси на одужання.
Немає доказів можливості інфікування немовлят (діти до 18 міс) через грудне молоко інфікованих матерів-годувальниць.
4.2. Групи ризику, що підлягають обстеженню на ВГС
- Реципієнти крові/тканин.
- Пацієнти на гемодіалізі.
- Медичні працівники, діяльність яких передбачає проведення процедур, що становлять ризик інфікування (хірурги, травматологи, акушери-гінекологи, лаборанти, маніпуляційні медсестри та ін.), а також працівники служб надзвичайних ситуацій у разі поранення гострими інструментами або потрапляння на слизові оболонки крові, що інфікована HCV.
- Пацієнти з підвищеною активністю АЛТ нез’ясованої етіології.
- Особи, які споживали/споживають ін’єкційні наркотики.
- Особи, які є ВІЛ-позитивними.
- Особи, які перебували в закладах позбавлення волі.
- Діти, мати яких інфікована HCV.
- Особи, які отримали медичну чи стоматологічну допомогу в країнах, де ВГС є поширеним, а інфекційний контроль – низьким.
- Особи, у яких є татуювання або пірсинг.
- Особи, які мали статевого партнера/побутові контакти з особою, що інфікована HCV.
4.3. Діагностика
4.3.1. Попередня діагностика (ІФА та ПЛР)
Первинна діагностика має на меті встановлення інфікованості пацієнта.
Попередня діагностика має дати відповідь на два запитання:
а) Чи є на даний час у пацієнта антитіла до HCV?
Треба пам’ятати, що антитіла до вірусу можуть не вироблятися, особливо коли імунітет особи пригнічений.
Антитіла до HCV можуть виявлятися протягом певного часу в крові неінфікованих немовлят (материнські антитіла, що з часом зникнуть).
Особи з позитивним результатом тесту на антитіла до HCV і повторно негативною РНК ВГС не потребують подальшого активного ведення ВГС.
б) Чи визначається РНК HCV у крові пацієнта?
Для виявлення РНК HCV необхідно проводити тестування нуклеїновими кислотами, що є достатньо чутливим для виявлення 50–100 МО/мл вірусу.
РНК HCV може бути виявлена вже на 1–2-му тижнях після інфікування, в той час як антитіла можуть бути виявлені на 7–8-му тижнях після інфікування.
Після гострого перебігу інфекції результат виявлення РНК HCV може коливатися між позитивними та негативним значеннями впродовж кількох місяців. Результати зразків, що відібрані у даний період, можуть бути хибними. В особи, що позитивна на антитіла до HCV, але негативна на РНК HCV, необхідно провести аналіз другого зразка для підтвердження попереднього діагнозу, особливо коли в більшості випадків дата інфікування невідома.
Особи з позитивним результатом тесту на антитіла до HCV і повторно негативною РНК HCV не потребують подальшого активного ведення ВГС.
Медичних працівників, які контактували з кров’ю пацієнта, хворого на ВГС, обстежувати на РНК HCV на 6-, 12- та 24-му тижнях з обстеженням на антитіла до HCV на 12- та 24-му тижнях.
Пацієнта з позитивним результатом необхідно направити на консультацію до інфекціоніста з метою уточнення діагнозу, генотипування вірусу, встановлення ступеня тяжкості захворювання, ураження печінки, забезпечення додаткових методів обстеження, диференційної діагностики, призначення лікування.
4.3.2. Генотипи HCV
Генотип HCV визначається методом полімеразної ланцюгової реакції (ПЛР).
Генотипування HCV має проводитися у випадку, коли розглядається питання призначення противірусної терапії.
4.3.3. Ступені тяжкості ураження печінки
Основний компонент визначення тяжкості перебігу хронічного гепатиту – це гістологічна оцінка, що ґрунтується на ступені вираженості некрозу і запального процесу в печінці. На основі гістологічних досліджень пунктатів печінки можна також оцінити стадії більш значного ураження печінки – фіброзу і цирозу.
Рекомендованою є інтерпретація результатів гістоморфологічного дослідження біоптатів печінки за шкалою оцінок METAVIR як найбільш інформативної та об’єктивної, що дає змогу окремо враховувати як ступінь запалення, так і ступінь розвитку фіброзу печінки (табл. 1).
Таблиця 1. Система оцінок активності запалення та фіброзу печінки за шкалою METAVIR
|
Показники активності (А) |
Лобулярне запалення |
|||
|
Відсутнє 0 |
Помірне 1 |
Тяжке 2 |
||
|
Часточкові |
Відсутні 0 |
А 0 |
А 1 |
А 2 |
|
Мінімальні 1 |
А 1 |
А 1 |
А 2 |
|
|
Помірні 2 |
А 2 |
А 2 |
А 3 |
|
|
Тяжкі 3 |
А 3 |
А 3 |
А 3 |
|
|
Показники фіброзу (F) |
Гістоморфологічні зміни |
|||
|
F 0 |
Відсутність портального фіброзу |
|||
|
F 1 |
Незначний портальний фіброз без септ (відсутні порушення цитоархітектоніки печінкових часточок) |
|||
|
F 2 |
Помірний портальний фіброз з окремими септами (поодинокі порушення цитоархітектоніки печінкових часточок) |
|||
|
F 3 |
Значний портальний фіброз, багато септ, але без ознак цирозу |
|||
|
F 4 |
Цироз |
|||
Шкала METAVIR побудована на окремій оцінці запально-некротичних (А – активність) та інших змін, що характеризують стадії фіброзу (F). Відповідно до неї результати гістоморфологічного дослідження біоптатів печінки оцінюють наступним чином:
1. Оцінка активності гепатиту:
А 0 – відсутня гістологічна активність;
А 1 – мінімальна активність;
А 2 – помірна активність;
А 3 – значна активність.
2. Оцінка стадії фіброзу печінки:
F 0 – фіброз відсутній;
F 1 – портальний фіброз без септ (мінімальний);
F 2 – портальний фіброз із поодинокими септами (помірний);
F 3 – численні септи без цирозу (значний);
F 4 – цироз (з градацією його активності).
Ступені фіброзу печінки
Достатньо простими і водночас досить точними є критерії печінкової недостатності та стадії цирозу печінки, що наведені у класифікaції Чайлд-П’ю (Child-Pugh), на основі клінічних ознак та лабораторних показників (табл. 2).
Таблиця 2. Шкала Чайлд-П’ю для визначення класу (стадії) цирозу печінки
|
Клінічні та біохімічні параметри |
Оцінка у балах |
||
|
1 |
2 |
3 |
|
|
Білірубін (мкмоль/л) |
<34 |
34-50 |
>50 |
|
Альбумін (г/л) |
>35 |
28-35 |
<28 |
|
Асцит |
Відсутній |
Помірний |
Значний / |
|
Енцефалопатія |
Відсутня |
Помірна |
Тяжка |
|
Протромбіновий індекс (у %) або протромбіновий час, МНО |
>60 <1,70 |
40-60 1,71-2,20 |
<40 >2,20 |
Інтерпретація результатів оцінки:
клас А: 5–6 балів (компенсований цироз);
клас В: 7–9 балів (субкомпенсований цироз);
клас С: 10–15 балів (декомпенсований цироз).
4.4. Особливості ВГС у дітей
Ризик розвитку цирозу печінки у дітей збільшується з віком. Дітей, народжених від матерів, у яких визначається РНК HCV, необхідно обстежити методом ІФА до HCV на 12-му місяці життя. Якщо результат потрібен раніше, можна обстежувати на РНК HCV після 2-го місяця життя; в разі негативного результату обстеження повторити після 12-го місяця життя. У разі позитивного результату проводити обстеження на РНК HCV. Обстеженню на РНК HCV підлягають діти, народжені від матерів з ко-інфекцією ВІЛ.
Позитивний результат тесту на РНК HCV треба підтверджувати додатковим тестуванням на РНК HCV.
Ризик передачі інфекції дитині від матері, у якої визначається РНК HCV (внутрішньоутробно або під час пологів), становить приблизно 5%, а у випадку ко-інфекції з ВІЛ ризик вдвічі вищий; ризик інфікування дитини не залежить від шляху народження чи вигодовування. Тому ведення вагітних, у яких визначається РНК HCV, не має відрізнятися від ведення інших вагітних; грудне вигодовування не протипоказане.
Неінфіковані немовлята стають ІФА-негативними щодо HCV в період з 6-го по 20-й місяць після народження (близько 80% стають негативні до 1-го року життя). Немовлята, народжені від жінок ІФА-позитивних і РНК-негативних щодо HCV, не потребують обстеження на ВГС.
У деяких інфікованих немовлят не виявляється РНК HCV до 12-го місяця життя та навіть довше.
Ризик розвитку цирозу у дітей <5%; з віком відсоток збільшується.
Існує потенційна загроза порушення ендокринних функцій унаслідок використання Пег-ІФН для лікування дітей. Комбіноване лікування Пег-ІФН+рибавірин дає стійку вірусологічну відповідь (СВВ) у 50–60% випадків.
Клінічне ведення дітей, хворих на ВГС, має здійснюватись разом із педіатром.
Алгоритм обстеження немовлят зазначено в Додатку 5.
4.5. Фактори, що обтяжують перебіг хвороби
Доведено, що такі фактори, як вік, стать, етнічне походження впливають на перебіг захворювання.
Існують фактори, модифікація яких можлива. Прискорювати прогресування ВГС можуть тютюнопаління та вживання алкоголю, навіть помірне, а також надмірна вага.
Ко-інфекція з ВІЛ обтяжує перебіг хвороби.
Ко-інфекція з ВГВ чи ВГА в анамнезі обтяжують перебіг ВГС.
Доведено, що пацієнти з хронічним ВГС можуть мати підвищені показники заліза (ППЗ), але немає єдиної думки з приводу того, чи це чинить вплив на захворювання. Сатурація сироватки феритином та трансферином збільшена у 20–60% пацієнтів і корелює з активністю АЛТ. Кровопускання окремим пацієнтам з маркерами ППЗ до початку монотерапії ІФН може покращити стійку СВВ. Пацієнти із суттєво ППЗ потребують подальшого обстеження з метою виключення станів, що призводять до перевантаження залізом.
4.6. Лікування
4.6.1. Показання до противірусної терапії ВГС:
- Наявність маркерів реплікації вірусу (РНК HCV).
- Виражений фіброз ( ≥F2 згідно з METAVIR) та наявність некрозозапальних змін у тканині печінки незалежно від активності трансаміназ. У таких випадках призначення лікування є обов’язковим.
- Відсутність автоімунних, неврологічних, психічних захворювань та некомпенсованих хвороб внутрішніх органів.
- Лікування дорослих призначається в залежності від генотипу HCV, ступеня ураження печінки, факторів, що обтяжують перебіг хвороби, та факторів, що впливають на противірусне лікування; відповіді на лікування та побічних реакцій, що можуть виникнути під час лікування та з урахуванням строків лікування – див. 4.5; табл. 3, 6, 7; Додатки 6–9.
- Лікування дітей призначається відповідно до ступеня тяжкості захворювання та генотипу вірусу (див. табл. 4).
Таблиця 3. Строки лікування дорослих з ВГС
|
Генотип HCV |
Тривалість лікування (тиж) |
|
|
Мінімально |
Максимально |
|
|
1 |
24 |
48 |
|
2, 3 |
12 |
24 |
|
4, 5, 6 |
– |
48 |
Таблиця 4. Лікування дітей відповідно до тяжкості захворювання та генотипу HCV
|
Ступінь тяжкості |
Генотип HCV |
|||||
|
1 |
2 |
3 |
4 |
5 |
6 |
|
|
Легкий |
Зважити ризики лікування |
Лікування |
Зважити ризики лікування |
|||
|
Помірний |
Лікування |
|||||
|
Тяжкий |
||||||
Лікування дітей з генотипом 1 HCV з використанням додаткових лікарських засобів слід розглядати тільки в контексті клінічних випробувань.
4.6.2. Термінологія, що використовується для позначення вірусологічної відповіді
Велике прогностичне значення в лікуванні вірусних гепатитів має відповідь організму пацієнта на противірусне лікування. Практичне значення має рівень РНК HCV у певні терміни після початку лікування в залежності від генотипу збудника. Для зручності інфекціоністи використовують певну термінологію (див. табл. 5)
Таблиця 5. Термінологія, що пов’язана з вірусологічною відповіддю
|
Термін |
Визначення |
|
Швидка вірусологічна відповідь |
Рівень РНК HCV, що не визначається на 4-му тижні терапії |
|
Рання вірусологічна відповідь |
Зниження рівня РНК HCV на 12-му тижні лікування більше ніж на 2 log10 |
|
Вірусологічна відповідь у кінці лікування |
Рівень РНК HCV, що не визначається в кінці лікування |
|
Стійка вірусологічна відповідь |
Рівень РНК HCV, що не визначається через 24 тиж після початку лікування |
|
Нульова відповідь |
Зниження рівня РНК HCV на 12-му тижні лікування менше ніж на 2 lоg10 в порівнянні з початковим рівнем |
|
Часткова відповідь |
Зниження рівня РНК HCV більше ніж на 2 lоg10 від початкового рівня на 12-му тижні лікування, але водночас такий його рівень, що визначається |
|
Вірусологічний прорив |
Повторна поява РНК HCV упродовж лікування, в той час коли був досягнутий рівень РНК HCV, що не визначався |
|
Рецидив |
Повторна поява РНК HCV у разі, коли після закінчення лікування було досягнуто такого рівня РНК HCV, що не визначався |
4.6.3. Фактори, що впливають на противірусне лікування
Відповідь пацієнта на противірусне лікування ВГС залежить від певних факторів. Лікарі мають інформувати пацієнтів про такий вплив (табл. 6).
Таблиця 6. Фактори, що впливають на противірусне лікування ВГС
|
Фактор |
Вплив |
|
Вік старше 40 років |
Ефективність лікування погіршується |
|
Чоловіча стать |
|
|
Вага тіла понад 75 кг |
|
|
Етнічне походження |
|
|
Кількість спожитого алкоголю |
|
|
Ниркова недостатність |
Ефективність лікування обтяжується. Призначається тільки лікування Пег-ІФН |
|
Пацієнти з психічними розладами |
У відповідь на лікування можуть спостерігатися погіршення психічного стану |
4.6.4. Побічні реакції противірусного лікування ВГС
Противірусне лікування ВГС може супроводжуватися побічними реакціями. Лікарі мають відслідковувати такі реакції та оцінювати можливість подальшого лікування. Рекомендації щодо корекції деяких побічних реакцій наводяться в табл. 7.
Таблиця 7. Передбачувані побічні реакції противірусного лікування ВГС
|
Реакція |
Рекомендації |
|
Грипоподібні реакції |
Приймати парацетамол, вживати достатньо рідини, ін’єкції інтерферону у вихідні дні |
|
Анемія та нейтропенія |
Призначення гранулоцитарного колонієстимулювального фактора має розглядатися окремо у кожного пацієнта, в якого розвинулася значна нейтропенія під час лікування хронічного ВГС Пег-ІФН+рибавірином, щоб запобігти відміні або зниженню дози Пег-ІФН. Необхідно розглядати можливість призначення еритропоетину у пацієнтів з хронічним ВГС, які приймають Пег-інтерферон+рибавірин і в яких розвинулася анемія, щоб запобігти відміні або зниженню дози рибавірину. У пацієнтів, які отримували додаткові лікарські засоби в поєднанні з Пег-ІФН+рибавірином, слід розглянути зниження дози рибавірину в якості альтернативи до додавання еритропоетину для контролю анемії |
|
Депресія |
Перед початком, під час та після лікування всіх пацієнтів потрібно обстежувати на предмет депресії |
|
Дерматити |
Усі пацієнти повинні бути поінформовані щодо відповідної гігієни шкіри та її зволоження, утримання від перебування на сонці, зміни місць ін’єкцій; за потреби – використання топічних стероїдів |
|
Дисфункція щитоподібної залози |
Базовий моніторинг функції (ТТГ, вільний Т3, вільний Т4) щитоподібної залози має проводитися перед початком терапії, на 12-му тижні лікування та у будь-який час, коли виникає підозра щодо дисфункції щитоподібної залози |
|
Диспное |
Пацієнти, які лікуються Пег-ІФН+рибавірином і у яких спостерігається диспное, що не пов’язане з анемією, мають негайно пройти медичне обстеження з метою виявлення пневмокардіальних захворювань |
|
Ретинопатія |
Офтальмологом мають бути оглянуті пацієнти з гіпертонією та діабетом (перед початком терапії), будь-який пацієнт, що скаржиться на порушення зору протягом лікування Пег-ІФН+рибавірином |
|
Алопеція |
Пацієнтам необхідно повідомити, що після припинення лікування волосся знову відросте |
|
Безсоння, втома, зниження концентрації, хвороби ротової порожнини, зміни смаку, нудота, симптоми абстиненції, анальний/ректальний дискомфорт |
Проінформувати пацієнта про можливість розвитку під час лікування таких побічних ефектів, як безсоння, втома, зниження концентрації, хвороби порожнини рота, зміна смаку, нудота, симптоми абстиненції, анальний/ректальний дискомфорт. Надавати пацієнтам консультації з приводу симптоматичного лікування відповідних станів |
4.6.5.А. Лікування запущеної інфекції
Доведено, що наслідком хронічного ВГС може бути ГЦК та цироз печінки; інколи потрібна трансплантація печінки. Якщо має місце трансплантація печінки, ГЦК чи цироз, то ми говоримо про запущену інфекцію.
Пацієнти з цирозом печінки, які отримують ІФН, мають значно менший ризик захворіти на ГЦК. Лікування Пег-ІФН+рибавірином пацієнтів із цирозом печінки не є токсичнішим, ніж пацієнтів без цирозу, хоча й менш ефективне.
Пацієнтам з ВГС та одночасною операбельною ГЦК та/чи асоційованою хворобою печінки пропонувати трансплантацію печінки. Показники виживання ВГС-позитивних та ВГС-негативних пацієнтів, які перенесли трансплантацію печінки, еквівалентні. Деякі пацієнти в післятрансплантаційний період (у випадках рецидиву) потребують противірусного лікування. Після трансплантації противірусна терапія переноситься погано, але безпечна з точки зору відторгнення трансплантату.
УЗД печінки раз на 6 міс діє змогу своєчасно виявити ГЦК. Скринінговим маркером ГЦК є також α-фетопротеїн.
4.7. Харчування та додаткові методи лікування
Неадекватне харчування чинить негативний вплив на нутритивний статус, якість життя та виживання. Пацієнти із запущеними формами хвороби повинні отримувати нутритивну підтримку. Водночас, надлишкова вага (ІМТ>25) пов’язана зі стеатозом печінки, призводить до тяжкої форми фіброзу. З іншого боку, зменшення маси тіла слід рекомендувати в тому разі, коли пацієнт стабільний з точки зору ведення ВГС, не отримує противірусну терапію при ВГС.
Пацієнти, які отримують противірусне лікування, мають знижену стійкість до фізичних навантажень. Тому таким пацієнтам показане легке та помірне фізичне навантаження.
Прийом пацієнтом інших лікарських засобів (що не показані для лікування ВГС) під час противірусного лікування ВГС може спричинити погіршення стану. Лікарі мають застерігати пацієнтів з ВГС щодо прийому додаткових лікарських засобів.
VІІ. Список літератури
- Адаптована клінічна настанова, заснована на доказах. «Вірусний гепатит С», 2013.
- Наказ МОЗ України від 23.02.2000 року № 33 «При штатні нормативи та типові штати закладів охорони здоров’я».
- Наказ МОЗ України від 14.02.2012 року № 110 «Про затвердження форм первинної облікової документації та інструкцій щодо їх заповнення, що використовуються у закладах охорони здоров’я незалежно від форми власності та підпорядкування», зареєстрований в Міністерстві юстиції України 28.04.2012 року за № 661/20974.
- Наказ МОЗ України від 23.02.2012 року № 132 «Про затвердження Примірного табеля оснащення лікувально-профілактичних підрозділів закладів охорони здоров’я, що надають первинну медичну (медико-санітарну) допомогу».
- Наказ МОЗ України від 29.03.2013 року № 251 «Про затвердження п’ятого випуску Державного формуляра лікарських засобів та забезпечення його доступності».
- Наказ МОЗ України від 02.03.2011 року № 127 «Про затвердження примірних табелів оснащення медичною технікою та виробами медичного призначення центральної районної (районної) та центральної міської (міської) лікарень».
- Наказ МОЗ України від 31.10.2011 року № 734 «Про затвердження табелів оснащення медичною технікою та виробами медичного призначення структурних підрозділів лікарні планового лікування».
- Наказ МОЗ України від 31.10.2011 року № 735 «Про затвердження табелів оснащення медичною технікою та виробами медичного призначення структурних підрозділів лікарні інтенсивного лікування».
- Наказ МОЗ України від 31.10.2011 року № 739 «Про затвердження табелів оснащення медичною технікою та виробами медичного призначення структурних підрозділів консультативно-діагностичного центру».
- Наказ МОЗ України від 28.09.2012 року № 751 «Про створення та впровадження медико-технологічних документів зі стандартизації медичної допомоги в системі Міністерства охорони здоров’я України», зареєстрований в Міністерстві юстиції України 29.11.2012 року за № 2001/22313.
- Наказ МОЗ України від 16.09.2011 року № 595 «Про порядок проведення профілактичних щеплень в Україні та контроль якості й обігу медичних імунобіологічних препаратів», зареєстрований в Міністерстві юстиції України 10.10.2011 року за № 1159/19897.
- Наказ МОЗ України від 19.08.2005 року № 415 «Про удосконалення добровільного консультування і тестування на ВІЛ-інфекцію», зареєстрований в Міністерстві юстиції України 22.11.2005 року за № 1404/11684.
- Наказ МОЗ України від 21.12.2010 року № 1141 «Про затвердження Порядку проведення тестування на ВІЛ-інфекцію та забезпечення якості досліджень, форм первинної облікової документації щодо тестування на ВІЛ-інфекцію, інструкцій щодо їх заповнення», зареєстрований в Міністерстві юстиції України 14.03.2011 року за № 319/19057.
VІІІ. Додатки
Розробники протоколу:
1. Хобзей М.К., директор Департаменту реформ та розвитку медичної допомоги Міністерства охорони здоров’я України, д.м.н., професор (голова).
2. Голубовська О.А., завідувач кафедри інфекційних хвороб Національного медичного університету імені О.О. Богомольця, д.м.н., професор (заступник голови з клінічних питань), головний позаштатний спеціаліст МОЗ України зі спеціальності «Інфекційні хвороби».
3. Ліщишина О.М., директор Департаменту стандартизації медичних послуг Державного підприємства «Державний експертний центр Міністерства охорони здоров’я України», к.м.н. (заступник голови з методичного супроводу).
4. Андрейчин М.А., завідувач кафедри інфекційних хвороб з епідеміологією, шкірними та венеричними хворобами Тернопільського державного медичного університету імені І.Я. Горбачевського, президент Асоціації інфекціоністів України.
5. Боднарук Н.М., заступник начальника управління спеціалізованої медичної допомоги – начальник відділу спеціалізованої медичної допомоги Департаменту реформ та розвитку медичної допомоги Міністерства охорони здоров’я України.
6. Бреднева Л.Ю., лікар-інфекціоніст Комунальної установи «Центральна міська лікарня № 1» м. Житомир, обласний позаштатний інфекціоніст Департаменту охорони здоров’я Житомирської ОДА (за згодою).
7. Герасун Б.А., професор кафедри інфекційних хвороб та епідеміології Львівського державного медичного університету імені Данила Галицького, д.м.н.
8. Донченко Т.М., директор Департаменту з питань якості медичної та фармацевтичної допомоги Міністерства охорони здоров’я України, к.м.н.
9. Дубинська Г.М., завідувач кафедри інфекційних хвороб з епідеміологією ВДНЗ України «Українська медична стоматологічна академія».
10. Козько В.М., завідувач кафедри інфекційних хвороб Харківського національного медичного університету.
11. Матюха Л.Ф., завідувач кафедри сімейної медицини Національної медичної академії післядипломної освіти імені П.Л.Шупика, д.м.н., головний позаштатний спеціаліст МОЗ України зі спеціальності «Загальна практика – сімейна медицина».
12. Мороз Л.В., завідувач кафедри інфекційних хвороб Вінницького Національного медичного університету імені М.І. Пирогова, д.м.н., професор.
13. Мостовенко Р.В., завідувач дитячого інфекційного відділення Національної дитячої спеціалізованої лікарні «ОХМАТДИТ», головний позаштатний спеціаліст МОЗ України зі спеціальності «Педіатрія».
14. Нетяженко В.З., завідувач кафедри пропедевтики внутрішніх хвороб № 1 Національного медичного університету імені О.О. Богомольця, д.м.н., професор, головний позаштатний спеціаліст МОЗ України зі спеціальності «Терапія».
15. Пришляк О.Я., професор кафедри інфекційних хвороб та епідеміології Івано-Франківського національного медичного університету, д.м.н.
16. Рябоконь О.В., завідувач кафедри інфекційних хвороб з епідеміологією Запорізького державного медичного університету.
17. Сергеєва Т.А., провідний науковий співробітник лабораторії епідеміології, парентеральних вірусних гепатитів та ВІЛ-інфекції Державної установи «Інститут епідеміології та інфекційних хвороб імені Л.В. Громашевського», д.м.н.
18. Терещенко А.В., заступник директора Департаменту – начальник Управління охорони материнства, дитинства та санаторного забезпечення Департаменту реформ та розвитку медичної допомоги Міністерства охорони здоров’я України.
19. Федорченко С.В., завідувач відділу ВІЛ-інфекції та вірусних гепатитів Державної установи «Інститут епідеміології та інфекційних хвороб імені Л.В. Громашевського» (за згодою).
20. Хаджинова Н.А., начальник відділу санаторно-курортного лікування Управління охорони материнства, дитинства та санаторного забезпечення Департаменту реформ та розвитку медичної допомоги Міністерства охорони здоров’я України.
21. Харченко Н.В., завідувач кафедри гастроентерології і дієтології, декан терапевтичного факультету Національної медичної академії післядипломної освіти імені П.Л. Шупика, член-кореспондент НАМН України, д.м.н., професор, головний позаштатний спеціаліст МОЗ України зі спеціальності «Гастроентерологія».
22. Шкурба А.В., професор кафедри інфекційних хвороб Національного медичного університету імені О.О. Богомольця.
Методичний супровід та інформаційне забезпечення:
1. Горох Є.Л., начальник відділу якості медичної допомоги та інформаційних технологій Державного підприємства «Державний експертний центр Міністерства охорони здоров’я України».
2. Мельник Є.О., начальник відділу доказової медицини Державного підприємства «Державний експертний центр Міністерства охорони здоров’я України».
3. Шилкіна О.О., начальник відділу методичного забезпечення нових технологій в охороні здоров’я Державного підприємства «Державний експертний центр Міністерства охорони здоров’я України».
4. Мігель О.В., завідувач сектору економічної оцінки медичних технологій Департаменту стандартизації медичної допомоги Державного підприємства «Державний експертний центр Міністерства охорони здоров’я України».
Рецензенти:
1. Зайцев І.А., завідувач кафедри інфекційних хвороб та епідеміології Донецького національного медичного університету імені М. Горького, д.м.н., професор.
2. Дикий Б.М., професор кафедри інфекційних хвороб з курсом епідеміології Івано-Франківського національного медичного університету, д.м.н., заслужений діяч науки і техніки України.
Адреса для листування: Департамент стандартизації медичних послуг Державного підприємства «Державний експертний центр МОЗ України», м. Київ, електронна адреса: medstandards@dec.gov.ua.
Друкується в скороченому обсязі
Електронну версію документа можна завантажити
на офіційному сайті Міністерства охорони здоров’я України:
http://www.moz.gov.ua та
за посиланням http://www.dec.gov.ua/mtd/index.html
Додаток 1
до Уніфікованого клінічного протоколу первинної, вторинної (спеціалізованої)
медичної допомоги «Вірусний гепатит С»
Анкета скринінгового опитування пацієнта
Шановний пацієнт, у зв’язку з тим, що вірусний гепатит С має тяжкі наслідки для здоров’я людини і важко виявляється, МОЗ України вживає заходи для покращення виявлення цього захворювання. Заповнивши цю анкету, ви допоможете лікарю своєчасно направити вас чи вашу дитину на обстеження.
Відповідь «Так» хоча б на одне запитання означатиме, що вам чи вашій дитині необхідно пройти обстеження на ВГС. Від своєчасного обстеження залежатиме ваше чи вашої дитини здоров’я, а інколи і життя.
Ця анкета не може розглянути всіх випадків, які могли б стати причиною інфікування людини.
Ви маєте розуміти, що можете бути інфіковані, якщо хоч якась частина крові чи тканинної рідини від хворої людини потрапить крізь шкіру чи слизову оболонку до вашого організму.
Якщо вам відомі такі випадки – повідомте про це свого лікаря. Це може врятувати вам життя.
Додаток 2
до Уніфікованого клінічного протоколу первинної, вторинної (спеціалізованої)
медичної допомоги «Вірусний гепатит С»
Пам’ятка пацієнту стосовно ВГС
Що таке ВГС?
ВГС – це захворювання, що спричинюється вірусом, який може передаватися через кров від однієї людини до іншої. Захворювання в основному вражає печінку.
Коли ваша печінка вражається вірусом, вона може пошкоджуватися, і зрештою виникнуть труднощі з виконанням її різноманітних і життєво важливих функцій. Протягом тривалого часу це може прогресувати до серйозного пошкодження печінки (наприклад фіброзу і цирозу) або, в деяких випадках, до раку печінки (ГЦК).
Як хвороба впливає на людей?
Потенційно це захворювання загрожує життю людини і може вплинути на вас фізично й емоційно. Захворювання може погіршити якість вашого життя. У багатьох випадках за умови відповідного лікування ВГС можна вилікувати.
Які симптоми захворювання на ВГС?
Деякі люди не мають жодних симптомів захворювання протягом багатьох років, тоді як інші можуть відчувати підвищену стомлюваність, пітливість (особливо вночі), ломоту та болі, втрату апетиту і концентрації уваги. Симптоми можуть з’являтися і зникати. На більш пізніх стадіях захворювання, коли печінка пошкоджена більш серйозно, можуть бути такі симптоми, як жовтяниця, свербіж, внутрішня кровотеча і закреп.
Мені це загрожує?
Фактори ризику, коли кров інфікованої ВГС особи може потрапити в кровотік іншої особи, є наступними:
- переливання крові, хірургічне втручання за кордоном або в Об’єднаному Королівстві до 1991 р., продукти крові в Об’єднаному Королівстві до 1987 р. (переливання та продукти крові у Об’єднаному Королівстві зараз безпечні з точки зору ВГС);
- отримання медичної або стоматологічної допомоги в країнах, де гепатит є поширеним захворюванням, а інфекційний контроль – неякісним;
- спільне використання будь-якого обладнання при споживанні ін’єкційних або інгаляційних наркотиків;
- спільне використання таких речей, як леза для гоління, зубні щітки або речі, що можуть подряпати шкіру;
- пірсинг, татуювання або косметичні ін’єкційні процедури (наприклад ботокс), якщо обладнання використовується повторно;
- статеві відносини, хоча ризик дуже низький, якщо немає загрози кровотечі;
- контакт з кров’ю на роботі, наприклад, поранення голкою, порізи, прибирання крові, робота на місці жорстоких подій з наявністю крові;
- передавання від матері до дитини в момент народження.
Мені треба здати аналізи?
Якщо ви вважаєте, що належите до групи ризику, необхідно отримати попередню консультацію в лікаря. Чим раніше почати лікування, тим більша вірогідність вилікування інфекції. Якщо ви знаєте, що маєте позитивний результат тесту на інфекцію, ви можете уникнути зараження інших.
Що мається на увазі «позитивний» чи «негативний»?
Є три типи тестів. Перший тип тесту (тест на антитіла до HCV) визначає, чи ви коли-небудь були інфіковані вірусом. Деякі люди позбавляються вірусу природним шляхом, без медичної допомоги. Другий тип (ПЛР) вказує, чи вірус наявний у даний момент у вашому організмі (тобто чи інфіковані ви HCV). Якщо тест ПЛР позитивний, додаткове тестування покаже генотип (штам) вірусу. Генотип визначає лікування, яке ви отримуватимете.
Як щодо конфіденційності?
Конфіденційне тестування доступне в сімейних лікарів та інших. Результати цього тесту є конфіденційними і не будуть передані третім особам без вашого дозволу. Сімейні лікарі лише передадуть інформацію про позитивні тести страховій компанії, якщо ви подали заяву на страхування і дали свою згоду на передавання медичної інформації. Негативні результати не розголошуватимуться.
Ви можете знайти інформацію про служби гепатиту по всій Шотландії, відвідавши сайт Hepatitis Scotland (див. розділ 13.1).
Це загрожує моїй родині та друзям? Мені треба їм розповісти?
Підтримка родини і друзів має вирішальне значення, тому варто сказати їм про ваш діагноз і те, якими можуть бути результати і побічні ефекти лікування. Ви не можете заразити членів вашої сім’ї і друзів під час повсякденної діяльності, такої як спільне використання посуду, обійми та поцілунки.
Аби не заразити інших:
- не використовуйте спільно такі предмети побуту, як зубні щітки або бритви;
- очищуйте будь-які плями крові слабким розчином хлорки;
- не використовуйте спільно будь-яке приладдя для вживання ліків (наприклад, трубки, голки та шприци, воду тощо).
Ризик передачі інфекції статевим шляхом є дуже низьким у разі відсутності інших ускладнюючих чинників, таких як:
- кров від менструації або анального сексу;
- виразки на геніталіях, тобто від інфекцій, що передаються статевим шляхом, таких як гонорея, герпес або генітальні бородавки.
Як це вплине на мою роботу і кар’єрні перспективи?
Багато людей з ВГС почуваються досить добре, щоб працювати, але вам, можливо, доведеться внести деякі корективи у вашу повсякденність, якщо у вас є надмірна втомлюваність або інші симптоми.
Як правило, ви не зобов’язані повідомляти своєму роботодавцю, що у вас ВГС (якщо ви не медичний працівник, який бере участь у процедурах, що можуть включати контакт з кров’ю, наприклад деякі операції). Проте, побічні ефекти від лікування можуть призвести до того, що ви почуватиметесь погано і будете не в змозі працювати протягом певного часу. Може бути корисно розказати, що ви перебуваєте на лікуванні. Наприклад, вас можуть підтримати, змінивши робочі години або фізичну діяльність, що пов’язана з вашою роботою, впродовж періоду лікування.
Як позитивний діагноз вплине на моє страхування життя?
Як і будь-яке серйозне захворювання, діагноз ВГС матиме вплив на страхування життя. Є багато видів страхування життя, так що варто перевірити будь-які поліси, які у вас є, оскільки, можливо, вам доведеться сказати страховику, якщо є зміни у стані вашого здоров’я. Важливо пам’ятати, що будь-яка інформація, яку ви надаєте вашим страховикам, є складовою частиною правового договору. Якщо інформація є неточною або невірною, угода може бути недійсною.
Якщо ви подаєте заяву на страхування та згоду на передачу медичної інформації, людина, яка проводила тестування, зобов’язана передати інформацію про позитивний результат тесту, якщо страхова компанія звернеться з таким проханням.
Ви повинні прочитати дрібний шрифт на поточних або нових договорах страхування, перш ніж підписувати.
Як вплине на моє страхування життя негативний діагноз?
Лікарі не повинні надавати страховикам жодної інформації про негативний діагноз. Страховики можуть тільки запитувати інформацію, чи має хтось позитивний результат або проходить курс лікування.
Що відбувається впродовж тестування?
Перед тестуванням лікар повинен обговорити з вами, що відбувається. Це допоможе вам зрозуміти процес тестування, результати тестування та конфіденційність.
Зразки крові будуть відправлені на лабораторне дослідження. Якщо Ваш контакт з вірусом відбувся в останні 6 міс, Вас можуть попросити повернутися для повторного тесту. Це відбувається через те, що існує «вікно» після контакту, поки тест не стає позитивним.
Якщо тест негативний, команда лікарів дасть Вам поради про те, як не піддавати себе ризику в майбутньому. Якщо тест позитивний, вони пояснять, що це означає і направлять Вас у спеціалізовану клініку для оцінки.
Що відбувається далі?
Оцінка включатиме в себе аналізи крові, такі як тест на печінкові проби, тест на генотип (штам HCV), клінічне обстеження, дискусії про спосіб життя, інші захворювання та ліки, що Ви приймаєте, УЗД, еластографію і, в окремих випадках, біопсію печінки. Біопсія печінки означає забір невеликого шматка печінки для лабораторного аналізу. Це робиться під місцевою анестезією, але не обов’язково до початку лікування.
По завершенню оцінки Ваш лікар говоритиме з Вами про лікування. Лікування дуже ефективне і побічних ефектів можна уникнути при гарному догляді та підтримці. Ваша клініка повинна допомогти Вам знайти підтримку, що є частиною Вашого лікування. Лікування не підходить для всіх і залежить від інших захворювань або ускладнень, які Ви можете мати.
У той час як Ви або Ваш партнер знаходитесь на лікуванні, і протягом від 6 до 12 міс після цього, Ви повинні використовувати контрацепцію, щоб уникнути вагітності, оскільки ці препарати можуть бути шкідливі для майбутньої дитини.
Життя з ВГС?
Є багато речей, що стосуються стилю життя, які можуть полегшити життя з ВГС.
Не вживайте алкоголь. Алкоголь і ВГС можуть призвести до пошкодження печінки, а їх поєднання робить значно прискорює цей процес. Існує спеціальна професійна підтримка, щоб допомогти вам зменшити або припинити споживання алкоголю;
Збалансована дієта є життєво важливою. Зменшіть споживання надмірно жирних та солодких продуктів. Втрата надлишкової маси тіла допоможе знизити навантаження на печінку. Проте, втрата ваги може бути побічним ефектом лікування, тому можуть бути необхідні харчові добавки. Професійна допомога в плануванні здорової збалансованої дієти стане вам у нагоді.
Якщо у вас поганий апетит, намагайтеся їсти малими порціями, але частіше.
Регулярні помірні фізичні вправи зменшують стрес або депресію, тонізують, допомагають зміцнити імунну систему.
Якщо у вас ВГС, припиніть палити. Відмова від куріння знижує ризик захворіти на рак. Для припинення паління можна звернутися за допомогою.
Поговоріть з вашим лікарем з приводу щеплень проти ВГА і ВГВ. Інші типи інфекції печінки, особливо якщо у вас вже є ВГС, спричиняють набагато більше навантаження на печінку і можуть уповільнити або зупинити відновлення для всіх типів гепатиту. Ви також маєте переконатися, що отримуєте сезонне щеплення проти грипу як додатковий захід обережності, коли імунна система може бути ослаблена.
Існує дуже мало доказів користі застосування додаткових лікарських засобів, але багато пацієнтів вважають їх корисними у вирішенні багатьох різних симптомів, пов’язаних з цим захворюванням. Перш ніж почати їх вживання, необхідно отримати професійну консультацію.
Яку підтримку я можу отримати?
Існують різні спеціалізовані служби підтримки для людей з ВГС, такі як консультування, підтримка осіб з подібним діагнозом, адвокації для допомоги у прийнятті рішень.
ВГС може змусити людей відчувати себе ізольованими, а тому емоційна підтримка є дуже важливою. Пацієнти повинні сподіватися на:
- підтримку багатопрофільних служб, що забезпечують добру комунікацію з пацієнтом;
- якісні інформаційні послуги;
- залучення пацієнта на всіх стадіях допомоги та лікування;
- поступовий перехід до паліативної допомоги, якщо це необхідно; та
- регулярну оцінку потреб.
Додаток 3
до Уніфікованого клінічного протоколу первинної, вторинної (спеціалізованої)
медичної допомоги «Вірусний гепатит С»
Форма добровільної поінформованої згоди пацієнта
Я, _______________________________________________________________________, __________________________ року народження, проживаю за адресою: ___________________________________________________________________________________________________ , даю добровільну поінформовану згоду на діагностику та лікування вірусного гепатиту С.
Я отримав(ла) інформацію від лікаря про суть проблеми, методи діагностики, лікування, побічні реакції, що можуть виникнути під час лікування. Я мав(ла) можливість обсудити з лікарем всі запитання, що мене цікавили. Я отримав(ла) листок «Інформація для пацієнта».
Я усвідомлюю, що результати діагностики можуть вплинути на моє подальше життя.
Я проінформований(на) про те, що хвора на ВГС людина є джерелом інфікування інших людей; усвідомлюю, що в разі виявлення у мене ВГС моя поведінка, як сумлінного члена суспільства, має змінитися так, щоб я не наражав(ла) на ризик інфікування інших людей; усвідомлюю, що навмисне інфікування інших тягне за собою відповідальність згідно з чинним законодавством України.
Я згоден(на) співпрацювати з лікарями і негайно інформувати їх про будь-які відхилення від мого стану здоров’я. Зобов’язуюсь, у разі підтвердження діагнозу проходити етапні обстеження на РНК вірусу гепатиту С на 4- та 12-му тижнях противірусного лікування, а в разі необхідності (за призначенням лікаря) – на 24-, 48-, 72-му тижнях.
Я усвідомлюю, що результати мого обстеження та лікування мають бути доступні певному колу лікарів, а тому мають відображатися в медичній документації.
Я усвідомлюю, що під час лікування стан мого здоров’я може погіршитися і лікарі можуть змінити лікування та/або направити мене до закладу вищого рівня; усвідомлюю, що лікування може не мати позитивного результату.
Я усвідомлюю, що вживання будь-яких додаткових лікарських засобів, навіть тих, що відпускаються без рецепта, або заборонених препаратів може бути причиною небезпечної взаємодії з противірусними лікарськими засобами.
Я усвідомлюю, що інформація про мій інфекційний статус є конфіденційною, але в деяких випадках, відповідно до чинного законодавства України, може бути доступна третім особам (_______________).
Згоду на обстеження та лікування даю добровільно, без будь-якого тиску з боку лікарів чи інших осіб. Цю добровільну згоду скріплюю власноручним підписом.
Прочитав і погоджуюсь з цим текстом.
Дата ____________________________ Підпис _________________________________
Додаток 4
до Уніфікованого клінічного протоколу первинної, вторинної (спеціалізованої)
медичної допомоги «Вірусний гепатит С»
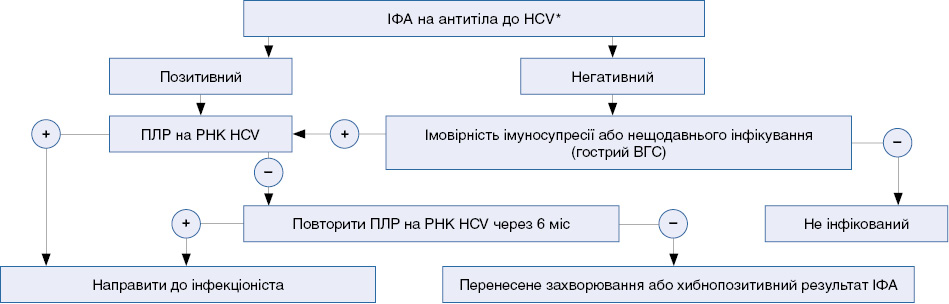
Алгоритм попередньої діагностики ВГС
* Вірус гепатиту С
Додаток 5
до Уніфікованого клінічного протоколу первинної, вторинної (спеціалізованої)
медичної допомоги «Вірусний гепатит С»
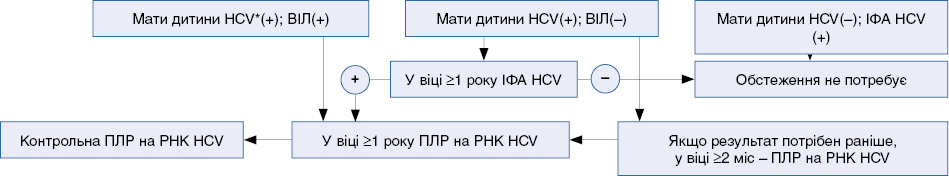
Алгоритм обстеження немовлят
* Вірус гепатиту С
Додаток 6
до Уніфікованого клінічного протоколу первинної, вторинної (спеціалізованої)
медичної допомоги «Вірусний гепатит С»
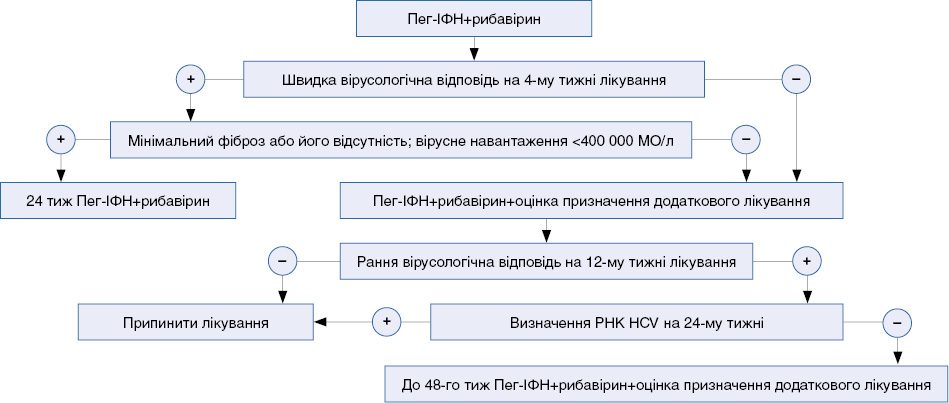
Алгоритм лікування пацієнтів з ВГС 1-го генотипу
Додаток 7
до Уніфікованого клінічного протоколу первинної, вторинної (спеціалізованої)
медичної допомоги «Вірусний гепатит С»
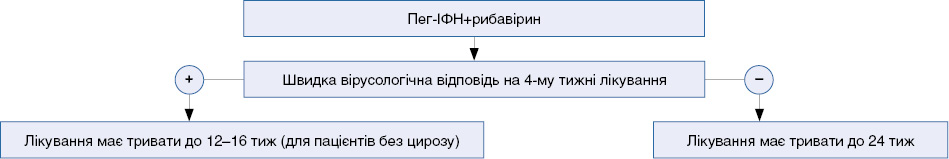
Алгоритм лікування пацієнтів з ВГС 2- та 3-го генотипу
Додаток 8
до Уніфікованого клінічного протоколу первинної, вторинної (спеціалізованої)
медичної допомоги «Вірусний гепатит С»
Алгоритм лікування пацієнтів з ко-інфекцією ВІЛ
Додаток 9
до Уніфікованого клінічного протоколу первинної, вторинної (спеціалізованої)
медичної допомоги «Вірусний гепатит С»
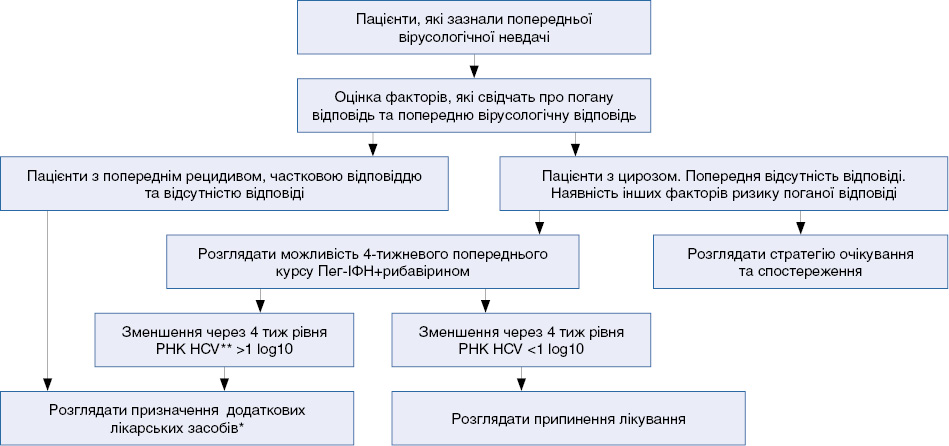
Алгоритм застосування додаткових лікарських засобів* у пацієнтів, інфікованих HCV 1-го генотипу, які зазнали попереднього невдалого лікування
* Інгібітори протеази; ** вірус гепатиту С