27 грудня, 2019
Оцінка ефективності та безпеки застосування сиропу Пектолван® Ц у комплексному лікуванні пацієнтів із ХОЗЛ
 Хронічне обструктивне захворювання легень (ХОЗЛ) – це прогресуюче гетерогенне захворювання, що характеризується стійкими респіраторними симптомами й обмеженням прохідності дихальних шляхів у зв’язку з патологічними змінами. Запобігання виникненню та раціональне лікування цієї патології є одними з пріоритетних завдань сучасної пульмонології.
Хронічне обструктивне захворювання легень (ХОЗЛ) – це прогресуюче гетерогенне захворювання, що характеризується стійкими респіраторними симптомами й обмеженням прохідності дихальних шляхів у зв’язку з патологічними змінами. Запобігання виникненню та раціональне лікування цієї патології є одними з пріоритетних завдань сучасної пульмонології.
ХОЗЛ характеризується прогресуючим перебігом, втратою працездатності, високим рівнем інвалідизації та смертності. За останні десятиліття загальна смертність і смертність від серцево-судинних захворювань знизилася, тоді як смертність від ХОЗЛ зросла на 28%; за прогнозами, до 2030 року ХОЗЛ стане третьою за значущістю причиною смерті в усьому світі. Розвиток захворювання може бути спадково детермінованим при вродженому дефіциті α1-антитрипсину, але частіше ХОЗЛ спричиняють активне куріння, забруднення повітря, тривалий вплив професійних факторів, несприятливе навколишнє середовище. Сумно, що висока захворюваність на ХОЗЛ насамперед зумовлена значною поширеністю куріння (80-90% випадків). Доведено, що максимальні показники смертності від ХОЗЛ спостерігаються саме в курців. Захворювання частіше розвивається до 40-50 років.
Основними клінічними проявами ХОЗЛ є різного ступеня кашель і задишка, продукція й виділення мокротиння. Їх вираженість залежить від стадії, швидкості прогресування хвороби й переважного рівня ураження бронхіального дерева. Першими ознаками, з якими пацієнти зазвичай звертаються до лікаря, є кашель і задишка, іноді вони супроводжуються свистячим диханням із виділенням мокротиння. Ці симптоми більш виражені вранці. Їх ступінь варіює від задишки при інтенсивному фізичному навантаженні й епізодичного кашлю до задишки в спокої з ознаками правошлуночкової недостатності та постійного кашлю. Задишка, що відчувається при фізичному навантаженні, виникає в середньому на 10 років пізніше появи кашлю. Проте в низці випадків можливий дебют захворювання із задишки. Мокротиння виділяється в невеликій кількості (не більш ніж 60 мл/добу) вранці, має слизовий характер. Хронічний кашель і продукція мокротиння часто на багато років передують розвитку обмеження повітряного потоку, хоча не в усіх пацієнтів із продуктивним кашлем розвивається ХОЗЛ. Згідно з даними Всесвітньої організації охорони здоров’я, на ХОЗЛ страждає 210 млн осіб і через десять років ця кількість збільшиться на 30%. Ще одним дуже важливим фактором, який зумовлює актуальність проблеми ХОЗЛ, є висока вартість лікування для системи охорони здоров’я та суспільства в цілому. Витрати на лікування ХОЗЛ утричі перевищують витрати на лікування бронхіальної астми (Мостовий Ю. М., 2016). Це патологія, для котрої характерна епізодичність проявів із чергуванням періодів ремісії та загострень, які є найбільш небезпечною фазою й зумовлюють тяжкість прогнозу. Часті загострення різко збільшують витрати на лікування хворого та негативно впливають на якість життя пацієнтів, що пояснюється ескалацією режимів терапії ХОЗЛ, особливо за потреби госпіталізації (Гашинова К. Ю., 2014).
Завданнями терапії ХОЗЛ є: запобігання прогресуванню хвороби, зменшення вираженості клінічних симптомів, досягнення кращої переносимості фізичного навантаження та підвищення якості життя хворих, запобігання ускладненням і загостренням, а також зниження смертності.
Специфічна фармакотерапія ХОЗЛ допомагає запобігти та контролювати симптоми, зменшити частоту й тяжкість загострень, поліпшити стан здоров’я та переносимість фізичного навантаження. Нині для лікування ХОЗЛ головними фармакологічними препаратами є бронхолітики (основа патогенетичної терапії ХОЗЛ), глюкокортикоїди та муколітики.
Бронхолітики тривалої дії посідають центральне місце у фармакологічному лікуванні ХОЗЛ стабільного перебігу, покращують показник об’єму форсованого видиху за 1-шу секунду (ОФВ1), зменшують задишку та гіперінфляцію легень, покращують якість життя, підвищують толерантність до фізичного навантаження, запобігають розвитку загострень. Хоча при ХОЗЛ має місце незворотна бронхіальна обструкція, застосування бронхолітиків дає змогу зменшити вираженість задишки й інших симптомів приблизно в 40% хворих і збільшити толерантність до фізичного навантаження. Наразі найкращим вважається застосування комбінованих препаратів із подвійною бронходилатацією (комбінація β2-агоністів тривалої дії та холінолітиків).
Згідно зі статистичними даними, у світі понад 80% пацієнтів із ХОЗЛ приймають інгаляційні глюкокортикоїди (ІГК) у комбінації з β2-агоністами тривалої дії. Проте в більшості хворих на ХОЗЛ головну роль у запаленні дихальних шляхів відіграють макрофаги й нейтрофіли, а ІГК – найефективніші для лікування пацієнтів з еозинофільним запаленням. Отже, величезна кількість хворих на ХОЗЛ отримують неадекватне лікування.
Одним із ланок патогенезу ХОЗЛ є порушення дренажної функції легень, що пов’язано з надмірним утворенням і підвищенням в’язкості бронхіального секрету, а також із погіршенням його евакуації. При цьому перистальтичні рухи дрібних бронхів і «мерехтіння» миготливого епітелію великих бронхів і трахеї не в змозі забезпечити адекватний дренаж бронхіального дерева.
Сигаретний дим, дефіцит α1-антитрипсину, токсини мікроорганізмів спричиняють руйнування та зменшення кількості війчастих клітин, зниження активності війок. У відповідь на це відбувається гіперпродукція слизу келихоподібними клітинами й залозами підслизового шару, що стає не захисним, а патогенним фактором. Змінюється реологія бронхіального слизу: збільшуються її в’язкість і адгезивність, знижується еластичність, що також призводить до погіршення мукоциліарного кліренсу, мукостазу, а отже, розвитку мікробної колонізації, порушення бронхіальної прохідності, прогресування дихальної недостатності. Відзначено, що чим вище в’язкість слизу, тим нижче швидкість її просування респіраторним трактом. Погіршення реологічних властивостей бронхіального секрету призводить також до порушення рухливості війок миготливого епітелію, що блокує їх очисну функцію. З підвищенням в’язкості швидкість руху мокротиння сповільнюється чи зовсім припиняється. Підвищення в’язкості, уповільнення швидкості просування бронхіального секрету сприяє фіксації, колонізації та глибшому проникненню мікроорганізмів у товщу слизової оболонки бронхів, що призводить до збільшення запального процесу, наростання бронхіальної обструкції, формування оксидативного стресу. Усе це зумовлює розвиток центрилобулярної емфіземи, дихальної недостатності. Формування емфіземи спричиняє поступову втрату оборотного компонента бронхіальної обструкції та наростання її незворотного компонента. Отже, гіперпродукція слизу при ХОЗЛ призводить до її накопичення в дихальних шляхах, у результаті чого формується сприятливе середовище для розвитку бактеріальної інфекції, що в підсумку зумовлює чергове загострення.
З огляду на цей патогенетичний механізм, при лікуванні ХОЗЛ необхідно використовувати препарати, що покращують або полегшують відділення зміненого бронхіального секрету, запобігають мукостазу й поліпшують мукоциліарний кліренс. Це досягається значною мірою завдяки застосуванню муколітичних (мукорегуляторних) препаратів. Мета муколітичної терапії – зменшення кашлю та полегшення відходження мокротиння. Основний терапевтичний ефект муколітиків полягає в безпосередньому розрідженні патологічно в’язкого секрету за допомогою зміни складу та кількості глікопротеїну слизу, що секретують клітини епітеліальної вистілки дихальних шляхів. Останнім часом у терапії ХОЗЛ активно обговорюється доцільність тривалого використання мукорегуляторних препаратів. Отримані результати їх застосування суперечливі. Ефективність муколітиків доведена тільки у хворих із легким перебігом ХОЗЛ (ОФВ1 >50% від належного) в низці короткотривалих (2-6 міс) досліджень. Результати систематичного Кокранівського огляду показують, що застосування муколітиків асоційоване з меншою на 29% частотою раптових загострень ХОЗЛ. Згідно з рекомендаціями Національного інституту здоров’я та вдосконалення медичної допомоги Великої Британії (NICE), муколітичну терапію слід проводити пацієнтам із хронічним продуктивним кашлем і продовжувати її при ослабленні симптоматики. У разі мінливого характеру продуктивного кашлю (наприклад, переважно в зимові місяці) тривалість прийому муколітиків становить 3-6 міс. Доцільно проведення початкового пробного лікування, коли муколітики призначають на 4-6 тиж у початковій встановленій дозі та здійснюється спостереження за пацієнтом протягом зазначеного періоду. При цьому критерії спостереження досить суб’єктивні та ґрунтуються на власній оцінці пацієнтом змін характеру кашлю з мокротинням. Зазвичай пролонговане лікування муколітичними препаратами клінічно ефективно в разі неодноразових, затяжних або тяжких загострень ХОЗЛ. Підставою для тривалого застосування муколітичних препаратів є зниження частоти та скорочення термінів загострень захворювання. При лікуванні хворих на ХОЗЛ хорошого результату можна досягти, призначаючи поєднання муколітичних препаратів і бронхолітиків. Наявність в’язкого мокротиння перешкоджає доступу інгаляційних препаратів до слизової бронхів. Тому забезпечення експекторації та звільнення слизової бронхів від слизу сприяють посиленню ефективності препаратів і зменшенню їх дози. Іншою точкою прикладання муколітичної терапії є загострення ХОЗЛ при впливі інфекційних чинників, що потребує призначення антибактеріальних засобів. За умови проведення антибактеріальної терапії помітно підвищується в’язкість мокротиння внаслідок вивільнення ДНК через лізис мікробних тіл і лейкоцитів. Окрім того, густа в’язка мокрота є значною перешкодою для проникнення антибіотиків у слизову бронхів і бронхіальний секрет. У зв’язку з цим потрібне проведення заходів, які спрямовані на поліпшення реологічних властивостей мокротиння і сприяють її кращому відходженню. Це досягається значною мірою завдяки застосуванню муколітичних (мукорегуляторних) препаратів, таких як Пектолван® Ц.
Пектолван® Ц являє собою комбінований муколітичний і відхаркувальний засіб, який містить збалансовану комбінацію двох медичних інгредієнтів – амброксолу та карбоцистеїну.
Амброксол є активним метаболітом бромгексину, але більш ефективним. Збільшує секрецію залоз дихальних шляхів, сприяє розрідженню в’язкого бронхіального секрету та полегшує відходження за рахунок збільшення мукоциліарного кліренсу, змінює співвідношення серозного та слизового компонентів мокротиння. Він стимулює клітини Клара й активізує гідролізуючі ферменти, що також сприяє зниженню в’язкості мокротиння. Амброксол має секретомоторну властивість – стимулює роботу миготливого епітелію бронхів, відновлює дренажну функцію дрібних бронхів і бронхіол. Препарат стимулює утворення ендогенного сурфактанту, не спричиняє надмірного утворення секрету, зменшує спастичну гіперреактивність бронхів. Кашель і кількість мокротиння значно зменшуються. Амброксолу гідрохлорид продемонстрував протизапальну дію in vitro. Дослідження in vitro виявили, що амброксолу гідрохлорид значно зменшує вивільнення цитокінів із крові та тканинне зв’язування мононуклеарних і поліморфнонуклеарних клітин.
Карбоцистеїн проявляє муколітичну й відхаркувальну дію, шляхом розриву дисульфідних містків глікопротеїнів забезпечує розрідження надмірно в’язкого секрету бронхів, сприяє виведенню мокротиння. Мукорегуляторний ефект карбоцистеїну пов’язаний з активацією сіалової трансферази – ферменту келихоподібних клітин слизової оболонки бронхів. Препарат нормалізує кількісне співвідношення кислих і нейтральних сіаломуцинів, що сприяє зменшенню в’язкості бронхіального секрету. Крім того, полегшує відходження мокротиння за рахунок підвищення мукоциліарного кліренсу, має антиоксидантну та пневмопротекторну властивості, що зумовлено здатністю сульфгідрильних груп зв’язувати вільні радикали; це особливо важливо для завзятих курців і хворих похилого віку, в яких активуються окисні процеси та знижується антиоксидантна активність сироватки крові. Карбоцистеїн сприяє регенерації слизової оболонки, нормалізує її структуру та зменшує гіперплазію келихоподібних клітин і, як наслідок, зменшує продукцію слизу. Він активує діяльність миготливого епітелію, відновлює секрецію IgA (специфічний захист) і кількість сульфгідрильних груп компонентів слизу (неспецифічний захист). Має протизапальний ефект завдяки кінін-інгібуючій дії сіаломуцинів, що забезпечує зменшення набряку та бронхообструкції. Результати нещодавно проведених досліджень свідчать про потенційні властивості карбоцистеїну запобігати патологічним процесам у бронхіальних епітеліальних клітинах, спричинених впливом тютюнового диму.
Мета дослідження: оцінити ефективність і безпеку застосування сиропу Пектолван® Ц у комплексному лікуванні пацієнтів із ХОЗЛ.
Критерії включення: чоловіки та жінки з наявністю верифікованого діагнозу ХОЗЛ згідно з міжнародними й національними стандартами, в стабільному стані, з частими загостреннями ХОЗЛ (≥1 епізодів загострень протягом року); ОФВ1 >50% від належного.
Критерії виключення: інші клінічно значущі захворювання легень; інша тяжка супутня патологія.
Матеріали та методи
У дослідженні брали участь 42 пацієнти (28 чоловіків і 14 жінок) віком від 42 до 72 років (середній вік – 62,45±10,16 року), тривалість захворювання становила від 1,5 до 15 років (у середньому 7,67±4,12 року), показник ОФВ1 – 63,12±9,61% від належного. Усі хворі були на той час або раніше курцями із середнім індексом куріння 29,44±15,2 пачко-років. При комплексній оцінці ХОЗЛ з урахуванням симптомів і ризику загострень (відповідно до рекомендацій Глобальної ініціативи з ХОЗЛ, 2011-2018) до групи А належали 0 хворих, до групи В – 19, до групи С – 0 і до групи D – 23 пацієнти зі стабільною ХОЗЛ.
Усі пацієнти отримували базисну терапію ХОЗЛ згідно з міжнародними та національними стандартами. Терапія була стабільною протягом 3 міс до включення в дослідження. У 24 пацієнтів застосовували тіотропію бромід / олодатерол по 2 дози 1 р/день, у 8 пацієнтів – умеклідиніум/вілантерол по 1 дозі 1 р/день, у 3 пацієнтів – форматерол/будесонід по 1 дозі 2 р/день, у 5 пацієнтів – сальметерол/флутиказон по 1 дозі 2 р/день. Для негайного полегшення всі пацієнти отримували сальбутамол 100 мкг по 1-2 дозі при симптомах ХОЗЛ.
Хворі були розподілені на 2 групи:
- група 1 (30 осіб) – отримували сироп Пектолван® Ц (амброксол/карбоцистеїн) по 10 мл 3 р/добу перорально та продовжували застосовувати базисну терапію ХОЗЛ;
- група 2 (12 осіб) – не отримували сироп Пектолван® Ц (амброксол/карбоцистеїн), застосовували тільки базисну терапію ХОЗЛ.
Тривалість терапії становила 3 міс. За ступенем вираженості симптомів ХОЗЛ, показниками функції зовнішнього дихання, кількістю щорічних загострень групи 1 і 2 статистично не відрізнялися (Р>0,05). Оцінювався стан пацієнтів при включенні в дослідження та через 3 міс.
Стан пацієнтів визначали шляхом оцінювання:
- вираженості задишки за шкалою Борга. Це 10-бальна шкала зі словесними описами ступеня тяжкості, що відповідають кожному балу. Додаткові пояснення на початку та наприкінці шкали позначають реакцію на навантаження, що полегшує оцінку переносимості фізичного навантаження та робить можливим порівнювати результати в різних людей;
- толерантності до фізичного навантаження за допомогою тесту з 6-хвилинною ходьбою (6MWT), який дає змогу об’єктивно оцінити рівень щоденної активності хворих, оскільки передбачає використання навантаження під час ходьби на субмаксимальному рівні з оцінкою навантаження тієї сили, котру зазвичай дозволяє собі пацієнт у повсякденному житті. Хворі повинні були пройти максимально можливу дистанцію за 6 хв, після чого реєструвалася пройдена відстань. Тест проводили в ранкові години. Використовувався коридор довжиною 25 м із непомітними для пацієнта розмітками через кожні 3 м дистанції;
- самопочуття за опитувальником САТ, який дає змогу оцінити вплив ХОЗЛ на самопочуття й повсякденне життя хворих. Опитувальник містить 8 пунктів, які характеризують погіршення статусу здоров’я при ХОЗЛ. Загальна сума балів може становити від 0 (найкращий показник) до 40 (найгірший показник);
- тяжкості задишки в умовах повсякденної активності пацієнта за модифікованою шкалою Британської медичної ради (mMRC) – опитувальник із 5 запитаннями з форматом відповідей «так/ні» щодо недавніх симптомів задишки. Пацієнта просять визначити рівень своєї активності, що спричиняє задишку, а в наступні візити повторюють тест, щоб визначити, збільшується рівень активності хворого чи зменшується. Рівні шкали перебувають у межах від 0 до 4, при цьому найвищий бал відповідає тяжчій задишці;
- ОФВ1 у відсотках від належного значення, прийнятого за 100%. Спірометрія проводилася на спірографі «Спіроком професійний» № 258 (Україна) за загальноприйнятими стандартами.
Ефективність і переносимість лікування оцінювали за зміною результатів анкетного тестування хворих і динамікою функціональних параметрів на момент включення в дослідження і через 3 міс.
Статистичну обробку проводили із застосуванням програми Statistiсa 6.0 for Windows Microsoft, методів параметричної (одно- та двосторонній t-тест Стьюдента) й непараметричної (одно- та двовибірковий критерій Вілкоксона) статистики. Результати представляли у вигляді кількості обстежених хворих у групі (n), середньо- арифметичного значення (М) і середнього відхилення (SD). Обчислення критеріальних значень проводилося при заданому рівні значущості р≤0,05.
Результати та їх обговорення
В обох групах загострень ХОЗЛ, позапланових візитів до лікаря, звернень по невідкладну допомогу не було. Реакції гіперчутливості, алергічні реакції, інші можливі побічні ефекти терапії не спостерігалися. Усі пацієнти відзначали хорошу переносимість препарату.
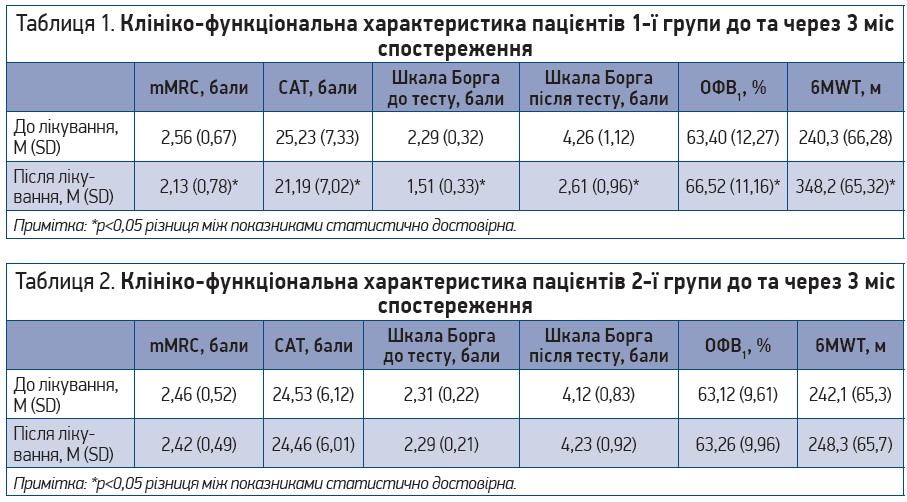
У пацієнтів групи 1 на тлі застосування сиропу Пектолван® Ц через 3 міс підвищилася толерантність до фізичного навантаження відповідно до показників шкали Борга з 4,26±1,12 до 2,61±0,96 (р<0,05), покращилися показники якості життя згідно з опитувальником САТ із 25,23±7,33 до 21,19±7,02 (р<0,05), зменшився ступінь тяжкості задишки за шкалою mMRC із 2,56±0,67 до 2,13±0,78 (р<0,05) (табл. 1).
Пацієнти групи 1 також відзначали зменшення частоти й інтенсивності кашлю, кількості мокротиння, епізодів хрипів при диханні, потреби в застосуванні препаратів для негайного полегшення. Як видно з даних, наведених у таблиці 2, вищевказані показники практично не змінилися в пацієнтів 2-ї групи.
У результаті проведеного лікування в 1-й групі відзначено достовірне поліпшення бронхіальної прохідності – приріст ОФВ1 через 3 міс лікування з 63,40±12,27 до 66,52±11,16 (р<0,05) (табл. 1). У 2-й групі бронхіальна прохідність практично не змінилася (табл. 2).
Висновки
Призначення сиропу Пектолван® Ц (амброксол/карбоцистеїн) пацієнтам із ХОЗЛ на додачу до базисної терапії має низку переваг:
- послаблення вираженості основних симптомів ХОЗЛ – кашлю, виділення мокротиння, хрипів при диханні, задишки;
- зменшення кількості загострень;
- покращення показників бронхіальної прохідності;
- зниження потреби в отриманні терапії для негайного полегшення.
Отже, сироп Пектолван® Ц є ефективним і безпечним препаратом і може бути рекомендований як додатковий засіб для базисної терапії ХОЗЛ.