26 лютого, 2020
Сприятливі наслідки профілактичної статинотерапії у пацієнтів із фібриляцією передсердь після кардіоемболічного інсульту
Захворюваність на ішемічний інсульт, який є провідною причиною смерті та інвалідності серед дорослого населення, зростає з віком. Фібриляція передсердь (ФП) може виникати у 20‑25% пацієнтів, що перенесли інсульт, а її частота в осіб після 80 років становить до 36% (Sienkiewicz-Jarosz et al., 2011; Kotlęga et al., 2012; Gołąb-Janowska et al., 2014). Статини – це група препаратів, які широко застосовують у хворих після інсульту. Сприятливий вплив препаратів зумовлений їхніми гіполіпідемічними та плейотропними властивостями. D. Kotlęga et al. провели дослідження, метою якого було встановити потенційну користь застосування статинів у пацієнтів із ФП, які перенесли ішемічний інсульт. До вашої уваги представлено огляд отриманих результатів, опублікованих у журналі Archives of Medical Science (2019; 15 (2): 385‑392).
За доступними даними, наявність ФП підвищує частоту розвитку інсульту в п’ять разів; цей показник більший, ніж у пацієнтів з ішемічною хворобою серця (ІХС), артеріальною гіпертензією або серцевою недостатністю. Для осіб з емболічними інсультами характерний вищий ризик смерті, втрати працездатності та внутрішньомозкового крововиливу при тромболітичній терапії (Saposnik et al., 2013).
Терапія статинами сприяє зниженню частоти розвитку інсульту (відносний ризик 0,80; 95% довірчий інтервал [ДІ] 0,74‑0,87; p<0,00001) (Wang, Zhang, 2014). Відповідно до рекомендацій Національної освітньої програми з виявлення, оцінки та лікування високого рівня холестерину в дорослих у США, у первинній профілактиці інсульту доза статинів для осіб без будь-яких факторів ризику має становити <4,1 ммоль/л (NCEP, 2001). У настановах Американської асоціації кардіологів та Американської асоціації інсульту (AHA/ASA, 2014) йдеться про доцільність застосування інтенсивної терапії статинами у пацієнтів з інсультом унаслідок атеросклеротичного ураження судин мозку, навіть якщо рівень холестерину (ХС) ліпопротеїдів низької щільності (ЛПНЩ) становить <2,59 ммоль/л,
Автори зазначають: із часом все очевиднішим стає те, що чим нижчий рівень ХС ЛПНЩ, тим більшими є переваги для пацієнтів, які перенесли інсульт. Незважаючи на сприятливі ефекти інтенсивної терапії статинами для профілактики інсульту, доведені у випробуванні SPARCL, такий підхід до лікування не слід узагальнювати, поширюючи на хворих із неатеросклеротичним ураженням, адже особи з кардіоемболічним інсультом були виключені з дослідження (Collins et al., 2004; Amarenco et al., 2006). Автори також припустили, що не слід розпочинати застосування статинів у пацієнтів із кардіоемболічним інсультом, якщо немає інших серцево-судинних показань (Furie, 2012).
Frustaci et al. (1997) провели перші спостереження, що пов’язували гістологію та наявність запалення при ФП. Було встановлено, що маркери запалення, серед яких С-реактивний білок, корелюють із ФП та прогнозують майбутній розвиток аритмій. Проте достеменно не відомо, чи розвиток ФП активує прямі запальні ефекти, а чи виникле раніше системне запалення сприяє подальшій персистенції ФП [19]. До того ж наявні дані досліджень, в яких оцінювали ефективність терапії статинами у хворих на ФП. Потенційно сприятливі ефекти препаратів щодо смертності та рецидиву ФП не спостерігалися у пацієнтів із пароксизмальною ФП (Watanabe et al., 2011). Після
Мета дослідження D. Kotlęga et al. (2019) полягала в аналізуванні впливу застосування статинів з метою профілактики інсультів на клінічні наслідки та госпітальну смертність у пацієнтів із кардіоемболічним інсультом.
Матеріали й методи дослідження
Характеристики пацієнтів
У дослідженні було ретроспективно проаналізовано медичні дані пацієнтів з ішемічним інсультом (n=2000), обстежених на підставі анамнезу ФП. Додатковий критерій включення/виключення: наявність/відсутність інформації щодо використання статинів перед інсультом. Усі пацієнти були представниками європеоїдної раси. Із 565 хворих, що перенесли кардіоемболічний інсульт, 334 приєднали до спостереження після виключення інших відомих причин розвитку інсульту та кардіоемболії.
Учасників розподілили на дві групи: до першої увійшов 181 пацієнт, який лікувався статинами безпосередньо перед епізодом інсульту, до другої – 153 особи, які не отримували такої терапії. Розмір вибірки був достатнім для проведення аналізу з очікуваною частотою розвитку ФП 25%, рівнем достовірності 95% і ДІ 5%. Смерть як кінцеву точку використовували в основній групі лікування, яка передбачала наявність даних щонайменше 536 пацієнтів.
Аналіз проводили на основі інформації, наявної в анамнезі пацієнтів, результатів додаткових тестувань та інших медичних записів. Історії хвороби отримували з медичної документації та самозвітів хворих. Учасники пройшли стандартний фізикальний огляд, лабораторні й додаткові обстеження. Пацієнти отримували лікування згідно з тими ж рекомендаціями, що й у звичайній клінічній практиці. Смертність і неврологічний дефіцит на госпітальному етапі та після виписки були проаналізовані за допомогою шкали інсульту Національного інституту охорони здоров’я США (NIHSS). Поняття «інсульт» використовували відповідно до термінології ВООЗ (Adams et al., 2007). ФП визначали як будь-який тип ФП, виявлений під час госпіталізації або підтверджений попередніми медичними записами. Були застосовані три типи статинів: аторвастатин, симвастатин та розувастатин.
Статистичний аналіз
Мета випробування полягала у дослідженні гіпотези про те, що використання статинів для профілактики інсульту позитивно впливає на клінічні наслідки та смертність пацієнтів із кардіоемболічним інсультом у стаціонарі. Для оцінки рівності дисперсій змінних, як-от вік, вміст загального ХС, ХС ЛПНЩ, ХС ліпопротеїдів високої щільності (ЛПВЩ), тригліцеридів (ТГ), бал за NIHSS, перед їхнім порівнянням використовували тест Брауна – Форсайта. Дані обох груп порівнювали за допомогою U-критерію Манна – Уїтні та точного критерію Фішера. Моделі логістичної регресії, що включали вік, стать пацієнта, артеріальну гіпертензію, ІХС, цукровий діабет, куріння, попередні інфаркт міокарда, інсульт або транзиторну ішемічну атаку, використання антикоагулянтів у минулому, вихідний ліпідний профіль та міжнародне нормалізоване відношення (МНВ) як незалежні змінні, були взяті для визначення незалежних предикторів відсутності поліпшення, прогресування погіршення чи смерті. Значення р<0,05 вказувало на статистичну значимість результатів. Статистичний аналіз проводили за допомогою програмного забезпечення Statistica 12.
Результати дослідження
Значно нижчий рівень ХС ЛПНЩ, загального ХС і ТГ у плазмі крові спостерігався у групі терапії статинами. Різниця у концентрації ХС ЛПВЩ між групами виявилася незначущою. Відмінностей щодо інших серцево-судинних факторів ризику в групах не було. Статинотерапію продовжували у всіх пацієнтів, що отримували ці препарати раніше, а також розпочали у 60,3% пацієнтів із групи порівняння, які потребували її згідно з їхніми ліпідними профілями. У 93,6% хворих групи терапії статинами і 93,9% пацієнтів, що не отримували такої профілактики, показники за шкалою для прогнозування ризику ішемічного інсульту та системної тромбоемболії при фібриляції передсердь (CHA2DS2-VASc) становили принаймні 2 бали (різниця незначуща).
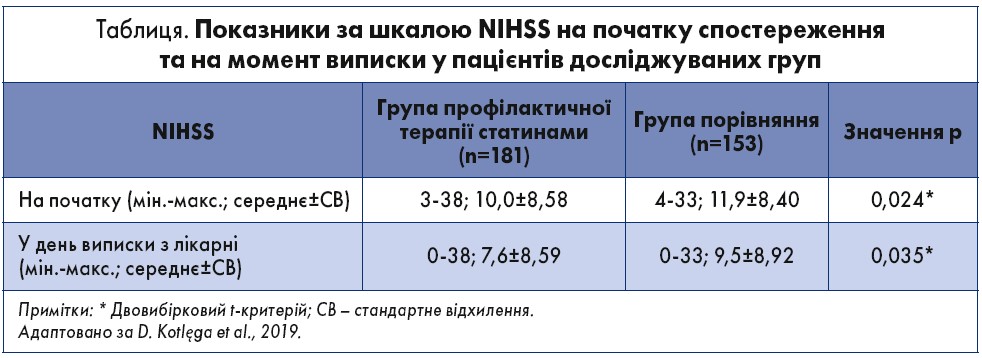
Суттєво нижчий неврологічний дефіцит за шкалою NIHSS при госпіталізації та виписці з лікарні мав місце у пацієнтів, що приймали статини профілактично, ніж у групі порівняння (таблиця). Учасники, що не отримували профілактику статинами, мали вищі бали за NIHSS на початку та при виписці (10 проти 11,9, р<0,05; 7,6 проти 9,5, р<0,05 відповідно). Поліпшення показника за NIHSS було суттєвішим у групі профілактичного лікування статинами (73,5% проти 59,5%, р<0,01). Ступінь відновлення хворих після інсульту на госпітальному етапі, з урахуванням зіставної оцінки за NIHSS на початку та при виписці, виявився значно вищим у пацієнтів із ФП, які отримували статини до розвитку інсульту (рисунок). Госпітальна летальність становила 9,9 та 18,3% у групах профілактичної терапії статинами і порівняння.
 Був також проведений багатофакторний логістичний регресійний аналіз для визначення незалежних предикторів відсутності поліпшення, погіршення неврологічних показників або смерті. Так, жіноча стать та ІХС виявилися предикторами відсутності змін або погіршення неврологічного стану за NIHSS під час госпіталізації у групі профілактики статинами, тоді як вік та попередній інсульт – серед пацієнтів, що не отримували такого лікування. Предикторами смерті під час госпіталізації були вік, ІХС, цукровий діабет у хворих групи профілактичної статинотерапії та вік – у групі порівняння.
Був також проведений багатофакторний логістичний регресійний аналіз для визначення незалежних предикторів відсутності поліпшення, погіршення неврологічних показників або смерті. Так, жіноча стать та ІХС виявилися предикторами відсутності змін або погіршення неврологічного стану за NIHSS під час госпіталізації у групі профілактики статинами, тоді як вік та попередній інсульт – серед пацієнтів, що не отримували такого лікування. Предикторами смерті під час госпіталізації були вік, ІХС, цукровий діабет у хворих групи профілактичної статинотерапії та вік – у групі порівняння.
Обговорення
Автори зауважують, що в контексті дослідження ефективності статинотерапії основну увагу загалом приділяли вивченню патогенезу атеросклерозу. Однак наявні дані, що дозволяють припустити потенційно важливу роль цих препаратів у хворих на кардіоемболічний інсульт. Їхній сприятливий вплив може бути зумовлений плейотропними властивостями, які відображають взаємодію клітин імунної системи та молекул запалення. Плейотропний ефект статинів, імовірно, був причиною значного поліпшення неврологічного стану серед пацієнтів, які приймали ці препарати (Heart Protection Study Collaborative Group, 2002). Такий вплив на функціональні результати виявився особливо помітним у хворих після інсульту з низьким вихідним рівнем ХС ЛПНЩ, які пізніше стали отримувати статини, порівняно із групою осіб, що не застосовували цих ліків (Stead et al., 2009).
У процесі дослідження D. Kotlęga et al. (2019) відзначали нижчу частоту госпітальної смертності серед хворих групи профілактичної статинотерапії, ніж у групі порівняння (різниця виявилася статистично значущою). Також до цих результатів можна додати дані, отримані після проведення аналізу даних пацієнтів з інсультом, за якими спостерігали протягом 22,2 місяця (Choi et al., 2014). Частка летальних наслідків була меншою у пацієнтів, що приймали статини, ніж у тих, хто не отримував такого лікування (Ntaios et al., 2014). Крім того, D. Kotlęga et al. (2019) виявили, що профілактичне застосування статинів пацієнтами, у яких згодом розвинувся інсульт, корелювало з нижчою частотою недостатності кровообігу як причини смерті, що може бути пов’язане з кардіопротекторним ефектом статинів. Варто зауважити, що дія статинів не залежала від застосування оральних антикоагулянтів, адже відмінностей між групами щодо частоти досягнутого терапевтичного МНВ не виявлено. Лікування антикоагулянтами до госпіталізації хворих у групі профілактичної статинотерапії використовували дещо частіше, але без суттєвої різниці.
Обмеженням представленого дослідження автори вважають відсутність аналізу впливу на результати тривалості приймання статинів, дозувань та типів використовуваних препаратів. Різниця у фармакокінетиці статинів та дозах могла вплинути на результати. Розмір груп також був імовірною причиною недостатньо достовірних даних аналізу смертності. Розмір вибірки, можливо, зумовив появу деяких факторів, що впливали на отримані показники.
Висновки
З-поміж численних факторів, які можуть чинити вплив на виживання пацієнтів після перенесеного інсульту та його наслідки, виділяють і терапію статинами. D. Kotlęga et al. (2019) довели, що використання статинів із метою профілактики інсульту знижує ризик неврологічного дефіциту та смерті у гострій фазі інсульту. Незважаючи на частіше використання статинів у осіб з атеротромботичним інсультом, продемонстровано їхній позитивний ефект у пацієнтів із кардіоемболічним інсультом. Показано, що ця група препаратів чинить різноспрямовану фармакологічну дію, зокрема, щодо утворення активних форм кисню, запобігання тромбоутворенню та поліпшення пластичності мозку (Kotlęga et al., 2015). Автори вважають, що всі пацієнти з фібриляцією передсердь потребують детального аналізу серцево-судинних показників для визначення необхідності в терапії статинами з метою первинної та вторинної профілактики інсульту.
Підготувала Олена Коробка
Спецвипуск «Інсульт». Додаток до № 1 (52), 2020 р.