26 лютого, 2020
Современное состояние вопроса распространенности умеренных когнитивных нарушений и деменции
При изучении вопроса о возраст-зависимых заболеваниях среди лиц 60 лет и старше на этапе первичной медико-санитарной помощи на приеме у невропатолога выявлено, что зачастую пациенты жалуются на снижение памяти, проявляющееся просьбой повторить несколько раз одну и ту же информацию, растущей зависимостью от письменных напоминаний и ухудшение запоминания событий на текущий период времени, трудности с решением проблем или планированием. Все это относят к первым симптомам умеренных когнитивных нарушений (УКН), которые ассоциируются с повышением риска развития синдрома деменции.
Начиная со второй половины XX века, во всем мире наблюдается изменение возрастной структуры населения с постоянным увеличением в популяции доли лиц пожилого и старческого возраста. Поэтому в современной медицине все большее значение приобретают профилактика и лечение множества возраст-зависимых заболеваний. Среди последних одно из ведущих мест занимают неврологические и нервно-психические нарушения, обусловленные как первичными расстройствами нервной системы, так и различными соматическими патологиями [1]. Когнитивные нарушения, включая деменцию, вызывают повышенный интерес мирового медицинского сообщества и врачей в связи с растущей тенденцией продолжительности жизни и старением населения в мире.
На сегодняшний день издается множество клинико-эпидемиологических трудов по выявлению причин когнитивных отклонений и развития синдрома деменции. Ведется поиск профилактических, диагностических мер и лечения данных нарушений. Около 60‑80% в структуре деменции занимает болезнь Альцгеймера, однако авторы публикаций последних лет все чаще утверждают о смешанном генезе синдрома деменции, вынося первично цереброваскулярные нарушения. Сегодня насчитывается более 46 млн человек, страдающих деменцией, во всем мире, что превышает численность населения Испании. По прогнозам Всемирной организации здравоохранения (ВОЗ), к 2050 г. этот показатель возрастет до 131,5 млн [2].
Во многих частях мира растет озабоченность населения касательно синдрома деменции (старческого слабоумия). Так, 94% лиц, живущих с деменцией в странах с низким и средним уровнем дохода, заботятся о себе дома. Это регионы, в которых система здравоохранения часто предоставляет ограниченную помощь или вовсе не поддерживает людей, живущих с деменцией, и/или их семьи. Говоря о синдроме деменции среди лиц старше 60 лет, необходимо отметить, что развитие деменции (сенильного, старческого слабоумия) приходит не в одночасье. По данным всемирной литературы, существует промежуточная стадия – додементная, когда у человека (или членов его семьи) есть время обратиться к специалистам за медицинской помощью. Данная стадия характеризуется легкими или умеренными когнитивными нарушениями.
Под когнитивным функционированием принято понимать наиболее сложные функции головного мозга, с помощью которых осуществляется процесс рационального познания мира, – память, гнозис, речь, праксис и интеллект [3]. Для оценки когнитивных функций используются нейропсихологические методы исследования. Они представляют собой различные тесты и пробы на запоминание и воспроизведение слов и рисунков, узнавание образов, решение интеллектуальных задач, исследование движений и т.д. [3, 4]. Полное нейропсихологическое исследование позволяет выявить клинические особенности когнитивных нарушений и поставить топический диагноз. Умение диагностировать когнитивные нарушения на ранней стадии становится все более важной задачей для врачей. В 2001 г. R.C. Petersen et al. в журнале American Academy of Neurology опубликовали статью «Практические параметры: раннее выявление деменции: умеренные когнитивные нарушения (обзор литературы, основанный на доказательной базе)», которая показала потребность в своевременной идентификации УКН, так как они являются промежуточной стадией синдрома деменции [5].
Цель данного обзора литературы – освятить проблему старения головного мозга, а именно необходимость в раннем выявлении УКН и деменции.
Материалы и методы исследования
Был проведен поиск литературы в девяти электронных базах данных: CINAHL, MEDLINE, Embase, Cochrane Collaborative Library, Thomson Reuters Web of Science, PsycINFO, LILACS, ALOIS и Pubmed. Материалы были опубликованы с декабря 2000 по февраль 2017 гг. Соответствующие статьи выявлены путем поиска названий и рефератов с применением ключевых слов, таких как деменция, ранняя диагностика деменции, когнитивные нарушения, умеренные когнитивные нарушения, легкие когнитивные нарушения, додементные формы когнитивных нарушений, васкулярная деменция. Используемые ключевые слова в небольшой степени различались между базами данных в зависимости от требований каждой поисковой системы.
Критерии приемлемости
Критерии включения были следующими: исследования с вовлечением любых участников в возрасте 60 лет и старше; тема работ – выявление когнитивных расстройств; языки поиска – русский и английский [6‑8]. Количество респондентов составляло 300 человек и более. Исследования были основаны на знаниях, которые предоставили четкое описание набора участников, критериев УКН и того, как они были введены в действие. Критерии исключения: исследования с возрастным диапазоном от 18 до 64 лет; работы с узким возрастным диапазоном ≥90 лет, поскольку ограничивали обобщаемость (generalizability); более ранние испытания с использованием определений когнитивных нарушений, которые не согласовывались с текущим определением УКН (доброкачественная забывчивость, возрастные нарушения памяти, возрастной когнитивный спад) [9‑13].
Скрининг и отбор исследований
Были получены и проанализированы полнотекстовые версии статей, представлявших интерес.
Анализ данных
Данные для всех включенных исследований были выделены и обобщены при ссылке на среднюю величину, стандартное отклонение, медиану. Объединенный анализ не проводили из-за большого различия в дизайне и популяциях испытаний.
Распространенность УКН
УКН являются важной проблемой общественного здравоохранения из-за повышенного риска прогрессирования деменции и увеличения смертности. Однако некоторые проблемы препятствуют клинической постановке диагноза. В частности, определение УКН варьирует в широких диапазонах, и синдром УКН неоднороден. Различные цифры показателей распространенности, частоты заболеваемости и темпов прогрессирования деменции подчеркивают необходимость признать эту гетерогенность и разработать стандартизированные критерии диагностики УКН, которые легко вводятся в действие, имеют высокую надежность и достоверность в клинических условиях. Клиническая польза биомаркеров визуализации и цереброспинальной жидкости в диагностике УКН еще не установлена. Таким образом, предстоит провести немало исследований, прежде чем биомаркеры станут использоваться для диагностики УКН в повседневной клинической практике.
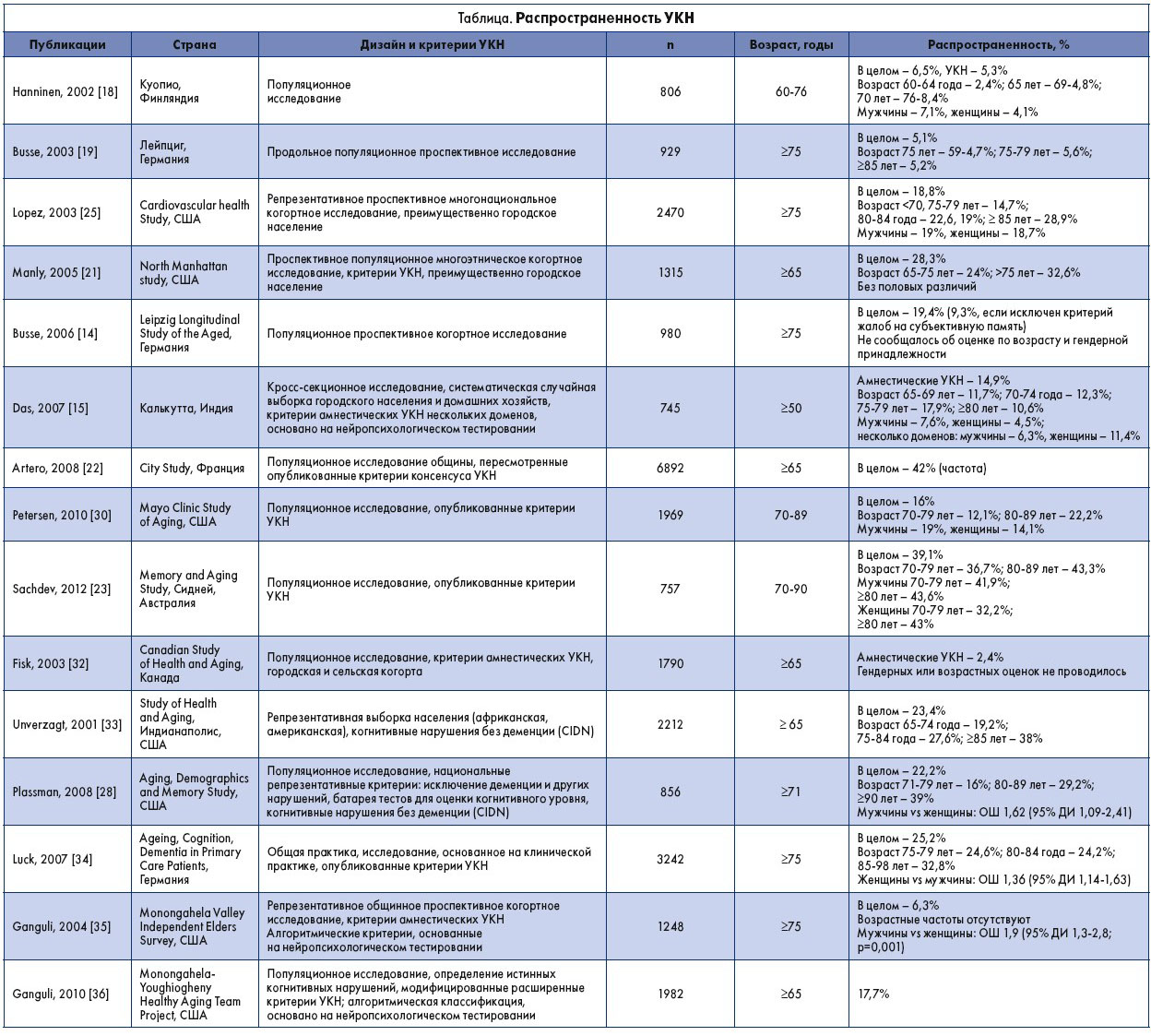
Оценка распространенности УКН различна по всему миру (таблица) [14‑16]. Эта вариабельность может быть вызвана изучаемой популяцией, распределением по возрасту и размером выборки, а также применением различных критериев УКН. В частности, в исследованиях были использованы проспективные и ретроспективные надлежащие диагностические критерии, нейропсихологические алгоритмы, клиническая консенсусная диагностика, разные типы когнитивных инструментов, глубина и широта собственных оценок и нормативные данные [17].
Так, например, исследования в Европе, а именно Финляндии и Германии, показали более низкие оценки распространенности, чем проведенные в США [18‑20]. В США рост показателей наблюдался в испытаниях, выполненных в более крупных городах [21, 22]. Различия в том, как применялись критерии УКН, возможно, привели к более высоким значениям распространенности в исследовании старения, выполненном в Австралии [23]. Шведские ученые в проекте Kungsholmen использовали глобальные и доменные когнитивные меры оценок, вследствие чего получили распространенность 11,1% населения в выборке из 379 субъектов в возрасте 75‑95 лет [16]. В исследовании, проведенном в Лейпциге (Германия), применяли комбинированный инструмент с 55 точками; общий показатель распространенности составил 19,2% у лиц в возрасте 75 лет и старше [23]. В исследовании сердечно-сосудистой системы (The Cardiovascular Health Study) была выявлена общая встречаемость 19% у лиц в возрасте 75 лет и старше [24]. Ретроспективное многонациональное и многокультурное исследование в Северном Манхэттене (Нью-Йорк, США) показало оценку распространенности УКН в диапазоне 21,8 и 26,9% [25].
Распространенность УКН в настоящем исследовании была сопоставима с таковой когнитивных нарушений в канадском исследовании здоровья и старения (16,8%), а также американском исследовании старения, демографии и памяти (22,2%) [26, 27]. Общая встречаемость УКН (aмнестических и неамнестических) в продольном испытании Einstein Aging Study составила 21,5% [28]. Этот показатель аналогичен цифрам других работ, выполненных в США [29, 30]. Таким образом, в большинстве исследований сообщалось о распространенности УКН в диапазоне 11‑20% [29].
Высокий уровень прогрессирования деменции среди субъектов с УКН подчеркивает необходимость определения методов предотвращения УКН, снижения бремени УКН и выявления лиц с повышенным риском развития УКН, которые могут извлечь выгоду из ранних вмешательств. С учетом того, что высокую долю факторов риска можно предотвратить, крайне важно, чтобы врачи и медицинский персонал:
- обучили пациентов, как уменьшить вероятность возникновения УКН с помощью диетических мер, физических упражнений, участия в когнитивно-стимулирующих действиях, профилактики инсульта;
- выявлять и уменьшать факторы риска, обеспечивать адекватный контроль факторов и результатов сердечно-сосудистых заболеваний;
- инициировать нетерапевтические и терапевтические вмешательства, когда они становятся доступными.
Эти меры потенциально могут снизить риск развития УКН и предотвратить переход УКН в деменцию [31].
Выводы
УКН – это этап, который поддается вмешательствам, способным предотвратить дальнейшее развитие синдрома деменции на стадии когнитивных нарушений, оказывающего существенное негативное влияние на повседневную жизнь. Классификация УКН со временем улучшается, а включение изображений и других биомаркеров может дополнительно улучшить обнаружение лиц с УКН. Это позволит облегчить сравнение между исследованиями, будет способствовать повышению качества выбора направлений для клинических испытаний, обеспечит лучшее понимание результатов УКН и более раннее выявление субъектов с УКН. Лица с УКН смогут извлечь пользу из вмешательств, которые снизят риск прогрессирования деменции, и получать лечение с помощью болезнь-модифицирующих препаратов, предотвращающих дальнейшее снижение когнитивных функций и развитие синдрома деменции.
Литература
- Яхно Н.Н., Захаров В.В., Локшина А.Б., Коберская Н.Н., Мхитарян Э.А. Деменция: руководство для врачей / 4-е изд. – М.: МЕДпресс-информ, 2013. – С. 7.
- Alzheimer’s Disease International: World Alzheimer report, 2015.
- Lezak M.D. Neuropsychology assessment. N.Y.: University Press, 1983. – P. 768.
- Лурия А.Р. Высшие корковые функции человека. – М.: изд-во МГУ, 1969.
- Petersen R.C., Stevens J.C., Ganguli M. et al. Practice parameter. Early detection of dementia: mild cognitive impairment (an evidence-based review). Report of the Quality Standards Subcommittee of the American Academy of Neurology // Neurology. – 2001. – Vol. 56. – P. 1133‑1142.
- Petersen R.C. Mild cognitive impairment as a diagnostic entity // J Intern Med. – 2004. – Vol. 256. – P. 183‑194.
- Winblad B., Palmer K., Kivipelto M. et al. Mild cognitive impairment-beyond controversies, towards a consensus: report of the International Working Group on Mild Cognitive Impairment // J Intern Med. – 2004. – Vol. 256. – P. 240‑246.
- Petersen R.C. Does the source of subjects matter?: absolutely! // Neurology. – 2010. – Vol. 74. – P. 1754‑1755.
- Jungwirth S., Weissgram S., Zehetmayer S. et al. VITA: subtypes of mild cognitive impairment in a community-based cohort at the age of 75 years // Int J Geriatr Psychiatry. – 2005. – Vol. 20. – P. 452‑458.
- Pioggiosi P.P., Berardi D., Ferrari B., et al. Occurrence of cognitive impairment after age 90: MCI and other broadly used concepts // Brain Res Bull. – 2006. – Vol. 68. – P. 227‑232.
- Kral V.A. Senescent forgetfulness: benign and malignant // Can Med Assoc J. – 1962. – Vol. 86. – P. 257‑260.
- Crook T., Bartus R., Ferris S. et al. Age associated memory impairment: proposed diagnostic criteria and measures of clinical change: report of a National Institute of Mental Health Work Group // Dev Neuropsychol. – 1986. – Vol. 2. – P. 261‑276.
- Levy R. Aging-associated cognitive decline. Working Party of the International Psychogeriatric Association in collaboration with the World Health Organization. International psychogeriatrics // IPA. – 1994. – Vol. 6. – P. 63‑68.
- Busse A., Hensel A., Guhne U., Angermeyer M.C., RiedelHeller S.G. Mild cognitive impairment: long-term course of four clinical subtypes // Neurology. – 2006. – Vol. 67. – P. 2176‑2185.
- Das S.K., Bose P., Biswas A. et al. An epidemiologic study of mild cognitive impairment in Kolkata, India // Neurology. – 2007. – Vol. 68. – P. 2019‑2026.
- Palmer K., Backman L., Winblad B., Fratiglioni L. Mild cognitive impairment in the general population: occurrence and progression to Alzheimer disease // Am J Geriatr Psychiatry. – 2008. – Vol. 16. – P. 603‑611.
- Tschanz J.T., Welsh-Bohmer K.A., Lyketsos C.G. et al. Conversion to dementia from mild cognitive disorder: the Cache County Study // Neurology. – 2006. – Vol. 67. – P. 229‑234.
- Hanninen T., Hallikainen M., Tuomainen S. et al. Prevalence of mild cognitive impairment: a population-based study in elderly subjects // Acta Neurol Scand. – 2002. – Vol. 106. – P. 148‑154.
- Busse A., Bischkopf J., Riedel-Heller S.G. et al. Mild cognitive impairment: prevalence and incidence according to different diagnostic criteria. Results of the Leipzig Longitudinal Study of the Aged (LEI‑LA75+) // Br J Psychiatry. – 2003. – Vol. 182. – P. 449‑454.
- Ward A., Arrighi H.M. Michels S. et al. Mild cognitive impairment: disparity of incidence and prevalence estimates // Alzheimers Dement. – 2012. – Vol. 8. – P. 14‑21.
- Manly J.J., Bell-McGinty S., Tang M.X. et al. Implementing diagnostic criteria and estimating frequency of mild cognitive impairment in an urban community // Arch Neurol. – 2005. – Vol. 62. – P. 1739‑1746.
- Artero S., Ancelin M.L., Portet F. et al. Risk profiles for mild cognitive impairment and progression to dementia are gender specific // J Neurol Neurosurg Psychiatry. – 2008. – Vol. 79. – P. 979‑984.
- Sachdev P.S., Lipnicki D.M., Crawford J. et al. Risk profiles for mild cognitive impairment vary by age and sex: the sydney memory and ageing study // Am J Geriatr Psychiatry. – 2012. – Vol. 20. – P. 854‑865.
- Busse A., Hensel A., Guhne U., Angermeyer M.C., Riedel-Heller S.G. Mild cognitive impairment: long-term course of four clinical subtypes // Neurology. – 2006. – Vol. 67. – P. 2176‑2185.
- O.L., Jagust W.J., DeKosky S.T. et al. Prevalence and classification of mild cognitive impairment in the Cardiovascular Health Study Cognition Study: part 1 // Arch Neurol. – 2003. – Vol. 60. – P. 1385‑1389.
- Manly J.J., Tang M.X., Schupf N., Stern Y., Vonsat-tel J.P., Mayeux R. Frequency and course of mild cognitive impairment in a multiethnic community // Ann Neurol. – 2008. – Vol. 63. – P. 494‑506.
- Graham J.E., Rockwood K., Beattie B.L. et al. Prevalence and severity of cognitive impairment with and without dementia in an elderly population // Lancet. – 1997. – Vol. 349. – P. 1793‑1796.
- Plassman B.L., Langa K.M., Fisher G.G. et al. Prevalence of cognitive impairment without dementia in the United States // Ann Intern Med. – 2008. – Vol. 148. – P. 427‑434.
- Katz M.J. et al. Age and sex specific prevalence and incidence of mild cognitive impairment, dementia and Alzheimer’s dementia in blacks and whites: A report from the Einstein Aging Study // Alzheimer disease and associated disorders. – 2012. – Vol. 26.– № 4. – P. 335.
- Petersen R.C., Roberts R.O., Knopman D.S. et al. Prevalence of mild cognitive impairment is higher in men. The mayo clinic study of aging // Neurology. – 2010. – Vol. 75. – P. 889‑897.
- Manly J.J., Tang M.X., Schupf N. et al. Frequency and course of mild cognitive impairment in a multiethnic community // Ann Neurol. – 2008. – Vol. 63. – P. 494‑506.
- Fisk J.D., Merry H.R., Rockwood K. Variations in case definition affect prevalence but not outcomes of mild cognitive impairment // Neurology. – 2003. – Vol. 61. – P. 1179‑1184.
- Unverzagt F.W., Gao S., Baiyewu O. et al. Prevalence of cognitive impairment: data from the Indianapolis Study of Health and Aging // Neurology. – 2001. – Vol. 57. – P. 1655‑1662.
- Luck T., Riedel-Heller S.G., Kaduszkiewicz H. et al. Mild cognitive impairment in general practice: age-specific prevalence and correlate results from the German study on ageing, cognition and dementia in primary care patients (AgeCoDe) // Dement Geriatr Cogn Disord. – 2007. – Vol. 24. – P. 307‑316.
- Ganguli M., Dodge H.H., Shen C., et al. Mild cognitive impairment, amnestic type: an epidemiologic study // Neurology. – 2004. – Vol. 63. – P. 115‑121.
- Ganguli M., Chang C.C., Snitz B.E. et al. Prevalence of mild cognitive impairment by multiple classifications: The Monongahela-Youghiogheny Healthy Aging Team (MYHAT) project // Am J Geriatr Psychiatry. – 2010. – Vol. 18. – P. 674‑683.
Статья печатается в сокращении
Нейрохирургия и неврология Казахстана. – 2018. – № 1 (50). – С. 47‑53.
Спецвипуск «Інсульт». Додаток до № 1 (52), 2020 р.