16 квітня, 2020
Меланома шкіри
Клінічні настанови Європейського товариства медичної онкології щодо діагностики, лікування та подальшого спостереження пацієнтів
 Захворюваність на злоякісну меланому в Європі коливається в межах від 3-5 (країни Середземномор’я) до 12-35 (північні країни) на 100 тис. населення. Захворюваність на меланому постійно зростає протягом останніх 40 років з тенденцією до стабілізації смертності, крім чоловіків похилого віку [1]. Пік захворюваності на меланому припадає на вік 65 років [2]. Також спостерігається зростання співвідношення смертності до захворюваності у східноєвропейських країнах порівняно із країнами Західної Європи [3].
Захворюваність на злоякісну меланому в Європі коливається в межах від 3-5 (країни Середземномор’я) до 12-35 (північні країни) на 100 тис. населення. Захворюваність на меланому постійно зростає протягом останніх 40 років з тенденцією до стабілізації смертності, крім чоловіків похилого віку [1]. Пік захворюваності на меланому припадає на вік 65 років [2]. Також спостерігається зростання співвідношення смертності до захворюваності у східноєвропейських країнах порівняно із країнами Західної Європи [3].
Cкорочення
AJCC – Американський об’єднаний комітет з раку
BRAFi – інгібітори протоонкогена B-Raf
CLND – повна дисекція лімфатичних вузлів
CTLA‑4 – цитотоксичний T-лімфоцитасоційований антиген 4
DeCOG-SLT – Дерматологічна об’єднана онкологічна група з дослідження селективної лімфаденектомії
EORTC – Європейська організація з вивчення та лікування онкологічних захворювань
IO – імунотерапія
MDLL – максимальний діаметр найбільшого ураження
MEKi – інгібітори мітогенактивованої протеїнкінази кінази 1
MSLT – багатоцентрова селективна лімфаденектомія
NRAS – протоонкоген NRAS
PD‑1 – білок програмованої клітинної смерті 1
PD-L1 – ліганд рецептора програмованої клітинної смерті 1
SNB – біопсія сторожового лімфатичного вузла
SND – дисекція сторожових лімфатичних вузлів
SPECT – однофотонна емісійна томографія
SRS – стереотаксична променева хірургія
TKI – інгібітори тирозинкінази
T-VEC – талімоген лагерпарепвек
WT – «дикий» тип мутації
УФ – ультрафіолетовий
УФ-опромінення визначено як основний канцероген, що бере участь у генезі меланоми. Пов’язане з УФ-опроміненням виражене пошкодження ДНК та високий рівень мутацій на мегабазу [4]. Найкращою профілактикою меланоми є захист від УФ‑променів адаптованими предметами одягу. У рандомізованому дослідженні встановлено, що запобігання впливу УФ‑опромінення, включаючи регулярне використання сонцезахисного крему, сприяє зменшенню захворюваності на первинну меланому шкіри в населення Австралії [5].
Діагностика
Підозрілі пігментні утворення шкіри аналізуються за правилом ABCD: А – асиметрія, В – нерівність країв, С – гетерогенність забарвлення, D – динаміка чи еволюція кольору, форми або розміру. Сьогодні багато меланом мають діаметр менше 5 мм [7]. Дерматоскопія, виконана досвідченим лікарем, підвищує точність діагностики (II, B) [9]. Автоматизована відеодерматоскопічна система покращує точність діагностики у пацієнтів із множинними атиповими невусами під час їх спостереження. Застосування візуалізації всього тіла фотографіями високої роздільної здатності також підвищує частоту раннього виявлення [10]. За допомогою алгоритмів машинного навчання, тренованих на стандартних або дерматоскопічних зображеннях, отримують змогу правильно діагностувати пігментні ураження шкіри. Частота коректних результатів таких досліджень зіставна з висновками панелі 21 сертифікованого дерматолога [11]. Однак застосування орієнтованих на пацієнта діагностичних приладів без медичного нагляду не рекомендоване.
Діагностика має ґрунтуватися на даних ексцизійної повностінної біопсії шкіри з мінімальними краями резекції (V, A). Дослідження первинної пухлини досвідченими патоморфологами згідно з міжнародними рекомендаціями є обов’язковим. Висновок гістологічного дослідження має відповідати 8-й версії класифікації TNM AJCC та містити: максимальну товщину в міліметрах (Breslow), вказану до найближчих 0,1 мм (заокруглення починаються з 0,05 мм), наявність звиразкування та чистоту меж хірургічного поля (II, A) [12]. Рекомендується оцінювати рівень мітозів і регресування пухлин для меланом усіх категорій товщини незважаючи на те, що ця інформація більше не включається до 8-ї версії класифікації AJCС [12].
Інформація про анатомічну ділянку розташування пухлини (зокрема й поза шкірою, наприклад, слизова оболонка, кон’юнктива) та ступінь ураження навколишньої шкіри від сонця є необхідною. Також потрібно вказати тип меланоми: поверхнево поширена, lentigo maligna, акральна лентигінозна, вузлова меланома та ін. У рідкісних випадках меланома може походити з дермальних меланоцитів (меланома, що виникає з гігантського вродженого невуса, злоякісного синього невуса і spitzoid ураження) [13]. Атипові spitzoid пухлини слід диференціювати від spitzoid меланоми, оскільки вони не мають метастатичного потенціалу. У меланом цього типу прогностична значимість товщини пухлини та ураження лімфатичного вузла є сумнівними.
Молекулярна характеристика
Визначення цільових мутацій є обов’язковим для пацієнтів із резектабельною або нерезектабельною меланомою III чи IV стадії (I, A) і настійно рекомендується пацієнтам IIC стадії з високим ризиком, але не рекомендується для осіб із I та IIA-IIB стадіями. Визначення BRAF-статусу є обов’язковим (I, А). Якщо меланома має мутацію BRAF WT на локусі V600 (BRAF клас I), необхідно провести секвенування локусів інших відомих незначних мутацій BRAF (BRAF клас II та III) і мутацій NRAS та c-kit (II, C) [14]. Хоча на сьогодні не існує прийнятної таргетної терапії, асоційованої з цими мутаціями, це необхідно для глибшої ідентифікації пацієнтів з метою подальшого включення у клінічні дослідження. Визначено мутації, характерні для певних підтипів меланоми [15]:
- BRAF, CDKN2A, NRAS і TP53 – меланома шкіри;
- BRAF, NRAS, NF1 та KIT – акральна меланома (зустрічається з меншою частотою, ніж меланома шкіри);
- SF3B1 – меланома слизової оболонки.
Незважаючи на дуже обмежене клінічне використання, рекомендується додатково визначати PD-L1, представлений як відсоток позитивних клітин пухлини, для всіх резектабельних і нерезектабельних пухлин III та IV стадій (I, B) та мутаційне навантаження пухлини (IV, C) [16].
Стадіювання та оцінка ризику
Пацієнти з меланомою низького ризику метастазування (pT1a) не потребують додаткових досліджень. Пацієнтам з пухлинами pT1b-pT4b необхідно провести ультразвукове дослідження регіонарних лімфатичних вузлів та/або комп’ютерну томографію перед хірургічним втручанням та біопсією сторожового лімфатичного вузла. Магнітно-резонансну томографію головного мозку та позитронно-емісійну томографію/комп’ютерну томографію проводять тільки для пацієнтів з меланомою високого ризику (pT3b і вище; III, С). Для стадіювання краще користуватися 8-ю версією класифікації AJCC [12].
Лікування локальної та місцевопоширеної хвороби
Алгоритм лікування пацієнтів з меланомою I-III стадії представлений на рисунку 1. Широке місцеве висічення пухлини на відстані 0,5 см виконують у разі меланоми in situ, 1 см – пухлин товщиною до 2 мм, 2 см – більших пухлин (II, B) [17]. Пацієнтам з акральною меланомою чи меланомою обличчя можна застосовувати модифіковане хірургічне лікування з меншим відступом від пухлини технікою Mohs [18, 19].
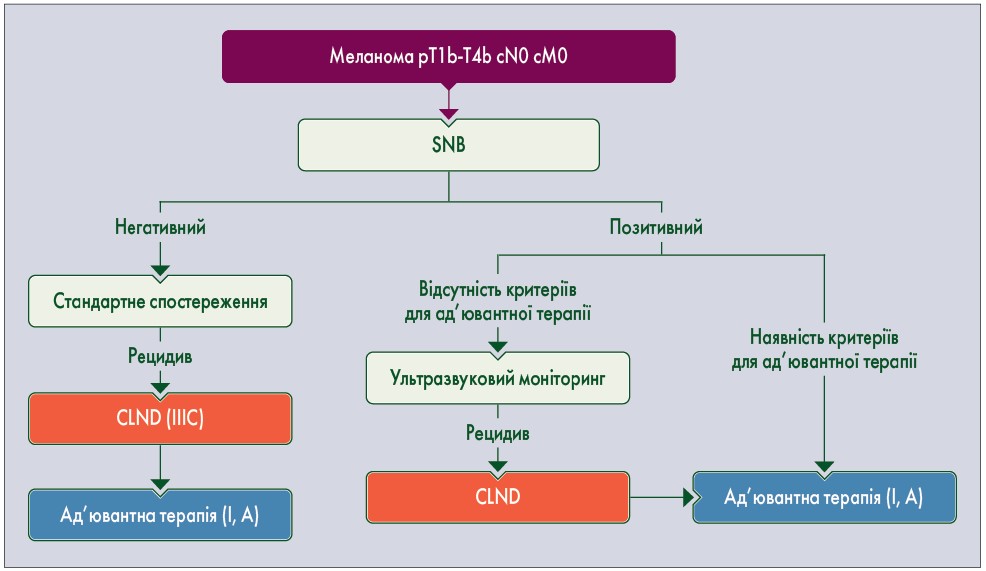 Рис. 1. Алгоритм лікування меланоми I-III стадії
Рис. 1. Алгоритм лікування меланоми I-III стадії
При lentigo maligna променева терапія може бути альтернативою операційному лікуванню [20].
Променеве лікування меланоми як самостійний метод розглядається лише у рідкісних паліативних випадках, коли операція неможлива через тяжкі супутні захворювання пацієнта (кінцева стадія серцево-судинних захворювань, старечий вік тощо) чи коли імовірність ускладнень після операції є занадто високою. Вибіркова дисекція лімфатичних вузлів або первинне вибіркове опромінення регіонарних лімфатичних вузлів не показані (II, B) [21-24].
SNB рекомендована для точнішого стадіювання пухлин розміром pT1b (за 8-ю версією класифікації AJCC), тобто пухлин товщиною >0,8 мм або товщиною <0,8 мм зі звиразкуванням (II, B) [25]. SNB не рекомендується при меланомах розміром pT1a [26]. SNB має здійснюватися лише у центрах з досвідом виконання такого дослідження [30]. Критерії якості SNB [31]:
- огляд і порівняння результатів первинного гістологічного дослідження і SNB рекомендується у тяжких випадках;
- гістологічна оцінка SNB відповідно до клітинної морфології та імунного профілю первинного вогнища;
- SNB проводиться одночасно з ре-резекцією країв меланоми, щоб уникнути модифікацій лімфовідтоку;
- SNB та ре-резекція країв меланоми проводиться досвідченим хірургічним колективом;
- позначення рубця під час консультації, бажано з фотодокументуванням;
- застосування SPECT у разі невідомої локалізації сторожового лімфатичного вузла.
Пухлинне навантаження сторожового лімфатичного вузла оцінювали по-різному, і всі оцінювальні методи додають точності прогнозу [32, 33]. Найчастіше використовують метод встановлення MDLL за критеріями Роттердам, затвердженими EORTC [34-36]. MDLL 1 мм було використано як точку відсікання у клінічних дослідженнях, присвячених ад’ювантному лікуванню. Тому, хоч формально MDLL не входить до 8-ї версії класифікації AJCC, рекомендується вносити критерії EORTC/Роттердам у звітність про пухлинне навантаження сторожового лімфатичного вузла.
CLND для пацієнтів з ураженим сторожовим лімфатичним вузлом донедавна була стандартом лікування. Однак, зважаючи на ускладнення рутинного застосування CLND, ця тактика більше не рекомендується (I, E) [39-41].
У разі ізольованого локального, регіонарного, клінічно визначеного метастазу у лімфатичному вузлі показана його дисекція (III, C); видалення тільки клінічно змінених лімфатичних вузлів є недостатнім [42].
Пацієнти з резектабельними сателітними пухлинами або транзиторними метастазами можуть бути кандидатами на операцію, хоча поява високоефективної системної терапії зараз змінює такий підхід.
Пацієнтам з нерезектабельними сателітними пухлинами, транзиторними метастазами або неоперабельними первинними пухлинами кінцівок без віддалених метастазів можна виконувати ізольовану перфузію кінцівки з використанням мелфалану та/або фактора некрозу пухлини (III, C).
Як засіб для альтернативного лікування T-VEC забезпечував кращий рівень тривалої відповіді на лікування порівняно з підшкірним введенням гранулоцитарного макрофагального колонієстимулювального фактора, особливо у пацієнтів з меланомою стадії IIIB/C, IVM1a (7-ма версія класифікації AJCC; I, B) [43, 44].
Такі методи місцевого лікування або потребують великих операцій, або використання онколітичних вірусів, і тому їх мають застосовувати досвідчені фахівці у відповідних центрах. Під час клінічних досліджень також можуть бути запропоновані променева терапія, електрохіміотерапія, лазерне опромінення діоксидом вуглецю (СО2) або інша внутрішньопухлинна терапія (V, D) [16, 45-47].
Ад’ювантна променева терапія для місцевого контролю пухлини може розглядатися у разі нерадикальної межі резекції lentigo maligna, резекції R1 або після резекції об’ємної хвороби (III, B). Променева терапія не застосовується з ад’ювантною метою (III, D).
Терапія анти-PD‑1-препаратами, ніволумабом (I, A; оцінка за ESMO-MCBS v1.1: A), пембролізумабом (І, A; оцінка за ESMO-MCBS v1.1: A) або дабрафенібом/траметинібом (I, A; оцінка за ESMO-MCBS v1.1: A) є кращими варіантами ад’ювантного системного лікування.
Не рекомендуються як ад’ювантне лікування інтерферон альфа, іпілімумаб, монотерапія BRAFi.
Лікування місцевопоширеної та метастатичної меланоми
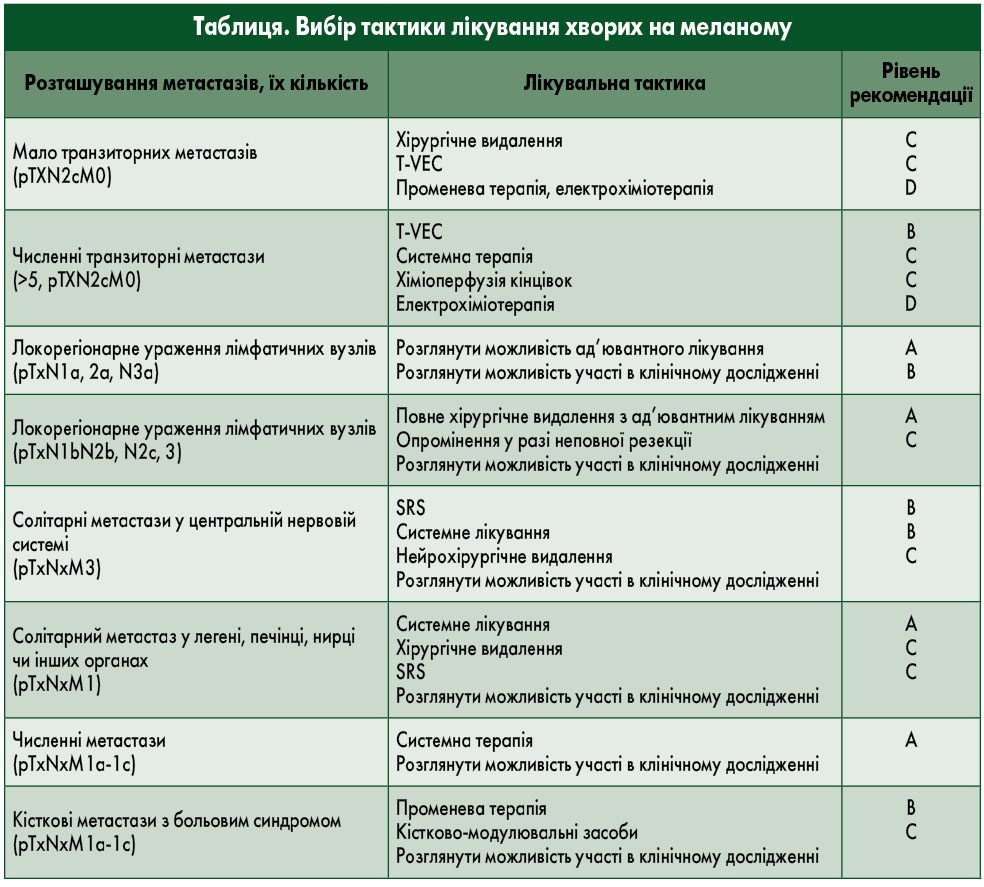
Хірургічне або абляційне лікування резектабельної меланоми IV стадії
Деякі пацієнти з IV стадією мають резектабельні олігометастази. Хоча значення хірургічних або абляційних променевих методів у таких клінічних умовах не було підтверджено в перспективних дослідженнях ІІІ фази, доступні дані дослідження II фази [73]. Хірургічне видалення або SRS локорегіонарного рецидиву чи поодинокого віддаленого метастазу слід розглядати у функціонально придатних пацієнтів (III, C). Хірургічне втручання залишається варіантом лікування для певної групи хворих, переважно в поєднанні з ад’ювантною системною терапією (див. вище і таблицю).
Системне лікування нерезектабельної меланоми III та IV стадії
Імунотерапія та мішенева терапія забезпечують помітне покращення виживаності порівняно з хіміотерапією. Незважаючи на прогрес у лікуванні запущених захворювань, багато запитань залишаються без відповіді, а для більшості хворих на меланому прогноз залишається поганим. Тому включення таких пацієнтів у клінічні дослідження залишається пріоритетом.
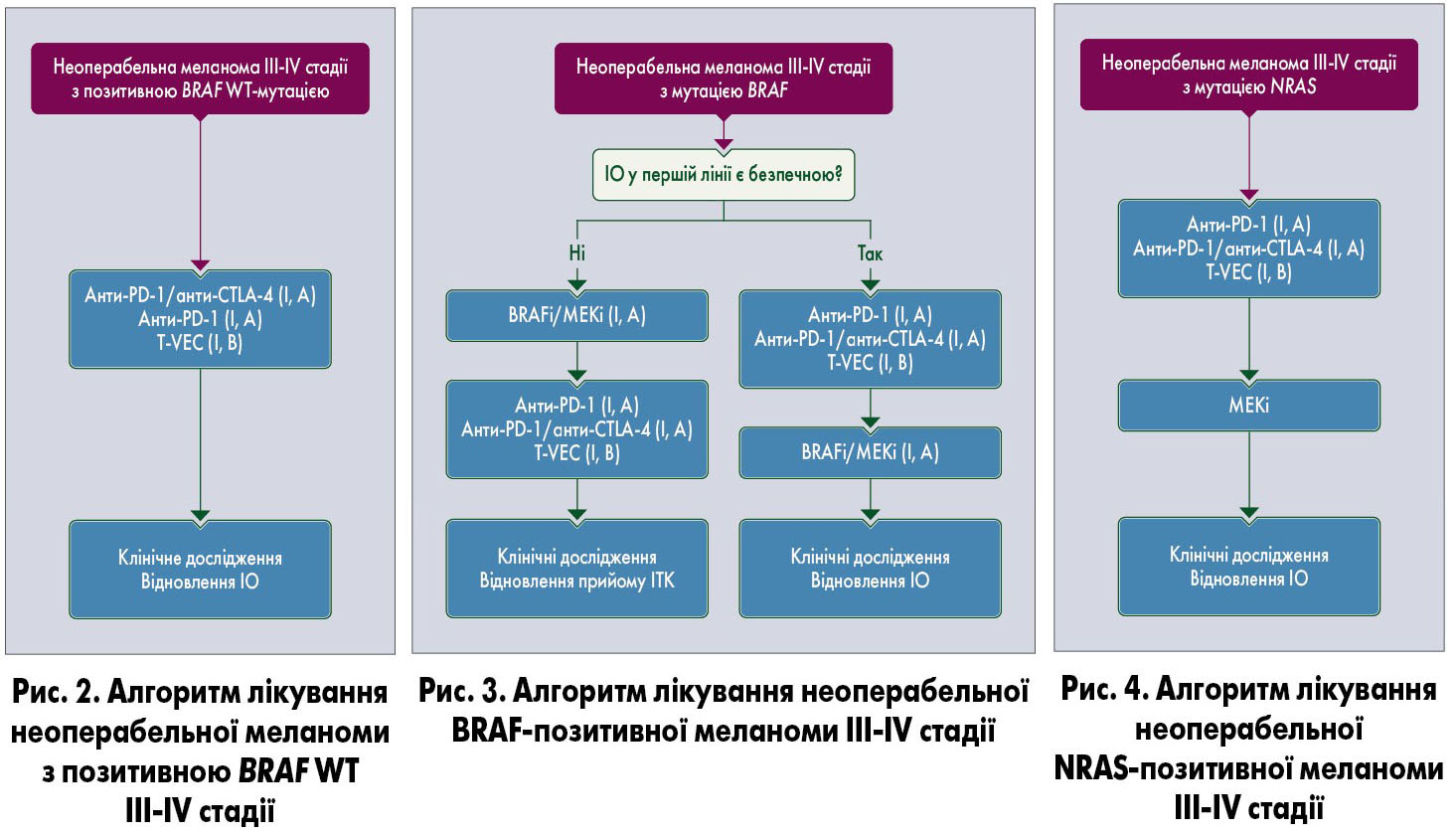
Алгоритми системного лікування меланоми IV стадії представлені на рисунках 2-5.
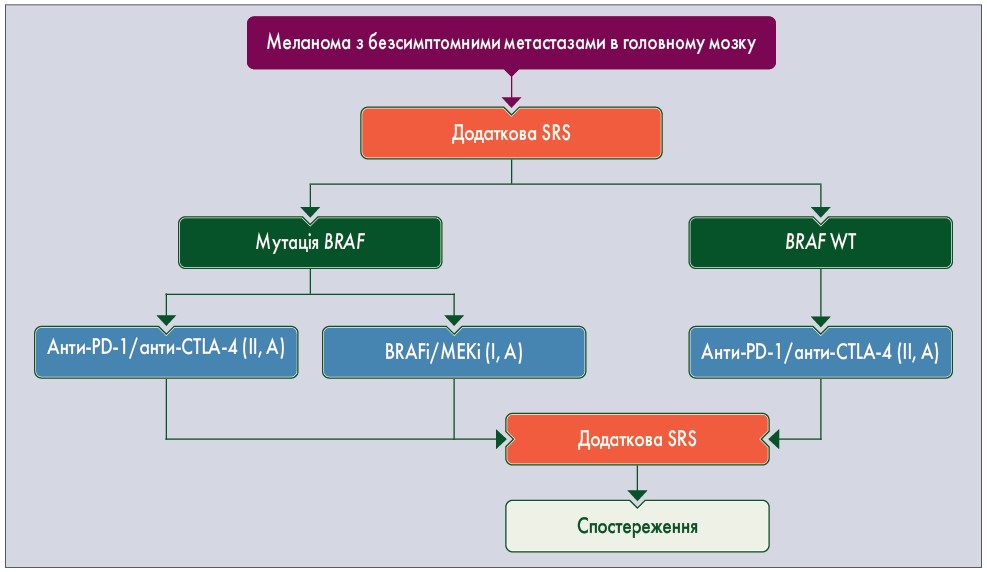 Рис. 5. Алгоритм лікування меланоми з безсимптомними метастазами в головному мозку
Рис. 5. Алгоритм лікування меланоми з безсимптомними метастазами в головному мозку
У пацієнтів з метастатичною меланомою необхідно визначати мутації BRAF V600 у тканині метастазів (бажано) або в первинній пухлині. Лікування має включати антитіла до PD‑1 (пембролізумаб, ніволумаб), PD‑1 та іпілімумаб для всіх пацієнтів та комбінацію інгібіторів BRAF і MEK для пацієнтів із мутацією BRAF (II, B). Інгібітори PD‑1 у монотерапії або в поєднанні з іпілімумабом сьогодні є стандартом першої лінії лікування в усіх пацієнтів, незалежно від їх BRAF-статусу (I, A).
Для пацієнтів з нерезектабельною пухлиною стадії IIIB/C, IVM1a варіантом лікування є T-VEC (I, B).
При BRAF-WT позитивних меланомах можливості другої лінії лікування дуже обмежені, і слід обговорити включення таких пацієнтів до клінічних досліджень та/або персоналізацію терапії. Якщо перша лінія включала монотерапію анти-PD‑1, друга лінія лікування може бути представлена іпілімумабом (II, B), а також іпілімумабом/ніволумабом (IV, B).
При BRAF-позитивних меланомах всі варіанти терапії, доступні для меланоми WT, теж можуть бути застосовані з додаванням інгібіторів BRAF/MEK, якщо вони не використовувались у першій лінії лікування.
У разі меланоми з мутацією NRAS через обмежену ефективність інгібіторів МЕК перша лінія імунотерапії ідентична лікуванню меланоми WT.
Якщо участь у клінічних дослідженнях або зареєстровані нові препарати є недоступними, можна застосовувати цитотоксичні препарати, такі як дакарбазин або темозоломід (II, C).
Для лікування метастазів у мозку надається перевага комбінації іпілімумаб/ніволумаб як лікуванню першої лінії також у пацієнтів без симптомів з позитивним BRAF-статусом (III, A). Для пацієнтів з невеликою кількістю безсимптомних метастазів (<5-10), необ’ємною хворобою (<3 см) SRS є лікуванням першого вибору. У інших пацієнтів слід спочатку розглянути можливість системного лікування, застосовуючи SRS у разі резистентності пухлинних вогнищ. Для пацієнтів, у яких системне лікування було невдалим, SRS можна розглядати як терапію порятунку, якщо загальна кількість прогресуючих пухлинних вогнищ становить <5-10, а їх максимальний розмір <3 см.
Подальше спостереження, довгострокові наслідки та виживаність
Пацієнтів з меланомою слід проінструктувати щодо уникнення сонячних опіків, тривалого сонячного чи штучного УФ-опромінення. Необхідно наголосити на потребі регулярного самообстеження шкіри та периферичних лімфатичних вузлів протягом усього життя (III, B). Пацієнти мають також знати, що у членів їх сімей наявний підвищений ризик розвитку меланоми (III, B).
Під час подальшого спостереження проводять клінічний моніторинг з метою якнайшвидшого виявлення рецидиву та додаткових пухлин шкіри, особливо вторинних меланом (III, B).
Немає консенсусу щодо оптимальної схеми спостереження, застосування візуалізаційних обстежень чи аналізу крові для пацієнтів після хірургічного видалення меланоми. Рекомендації варіюють від відвідування через кожні 3 місяці протягом перших 3 років і через кожні 6-12 місяців надалі до відсутності організованого спостереження.
Пацієнти з ураженими сторожовими лімфатичними вузлами регулярно мають проходити ультразвукове дослідження.
Підвищення рівня сироваткового білка S100 є найточнішим маркером при спостереженні за хворими на меланому, якщо взагалі рекомендується аналіз крові (IV, D).
Michielin O., van Akkooi A.C.J., Ascierto P.A., Dummer R., Keilholz U. Cutaneous melanoma: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Annals of Oncology. 2019; 30: 1884-1901. doi:10.1093/annonc/mdz411.
Переклав з англ. Назар Лукавецький
Тематичний номер «Онкологія. Гематологія. Хіміотерапія» № 1 (62), 2020 р.