16 квітня, 2020
Сучасна гормональна та хіміотерапія при метастатичному кастраційно-резистентному раку передміхурової залози
Рак передміхурової залози (РПЗ) є одним із найпоширеніших онкологічних захворювань чоловічного населення в Україні. За даними Національного канцер-реєстру, РПЗ посідає друге місце у структурі онкологічної захворюваності (44,8 на 100 тис. чоловічого населення) та третє – у структурі смертності від злоякісних новоутворень (19,7 на 100 тис. чоловічого населення). Загалом станом на 2018 р. в Україні на обліку перебував 39 891 хворий на РПЗ.
За даними світової літератури, у більшості (80%) пацієнтів РПЗ діагностують на стадії локального поширення, у 12% – на стадії місцевого поширення. Віддалені метастази на момент діагностики наявні у 5% пацієнтів, проте зумовлюють третину летальних випадків. В Україні пацієнти з І-ІІ стадією складають 42,6% з-поміж уперше виявлених, з ІІІ стадією – 22,4%, з IV стадією – 22,3%, з невизначеною стадією захворювання – 12,5%.
Андрогендеприваційна терапія
Андрогендеприваційна терапія (АДТ) – стандарт лікування при метастатичному РПЗ. Її метою є зниження концентрації тестостерону до рівня менш ніж 50 нг/дл. Значний біохімічний результат спостерігається майже у всіх пацієнтів, проте він транзиторний – медіана його тривалості становить 18 міс до розвитку кастраційно-резистентної форми захворювання, що зумовлює потребу доповнення АДТ хімотерапією чи препаратами з групи інгібторів андрогенного сигналу.
За даними Європейської асоціації урології (EUA, 2019) критеріями кастраційної резистентності є рівень тестостерону сироватки крові <50 нг/дл (0,7 нмоль/л), зростання вмісту простатичного специфічного антигену (ПСА) >2 нг/мл, або >50% від надиру 3 рази поспіль з інтервалом 1 тиждень. При виникненні кастраційної резистентності обов’язково слід відмінити антиандрогени першого покоління (флутамід, бікалутамід), що в багатьох випадках сприяє зниженню рівня ПСА і покращенню стану пацієнта, АДТ при цьому не припиняють [7].
Доцетаксел
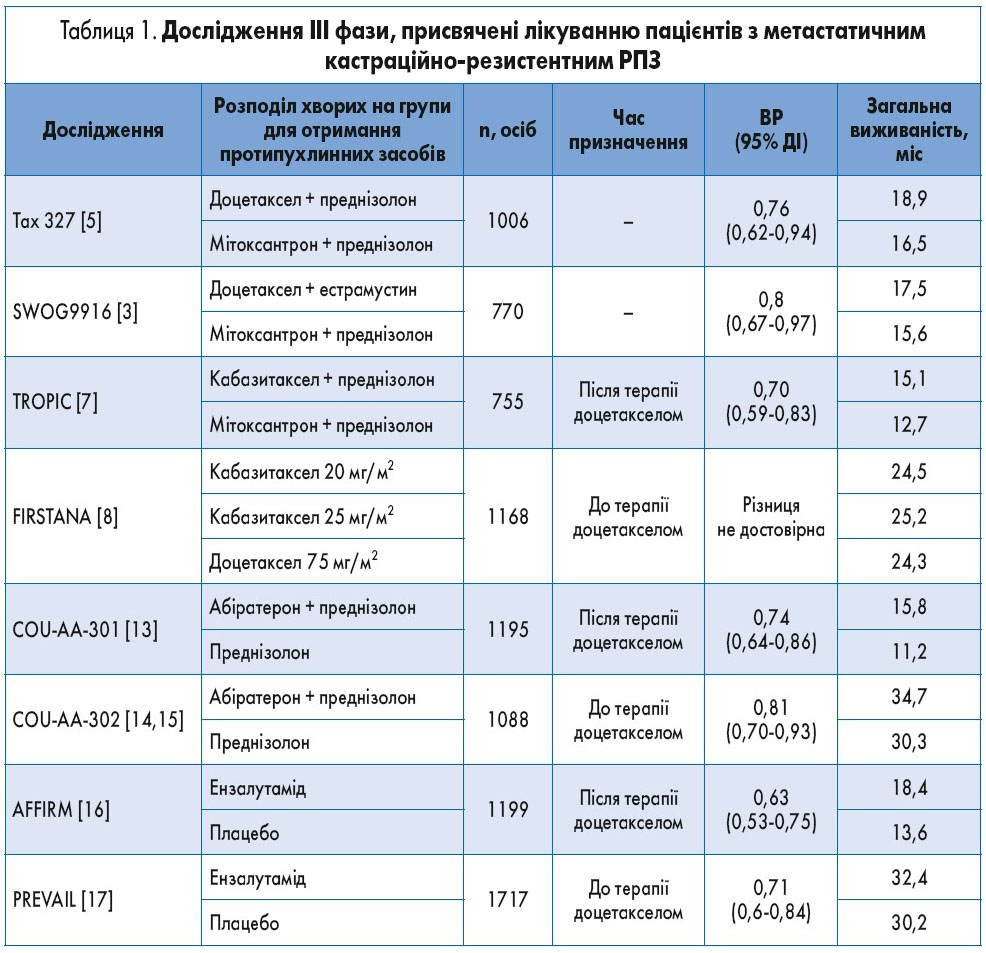
Історично першим протипухлинним засобом, який забезпечував значне покращення виживаності пацієнтів з метастатичним кастраційно-резистентним РПЗ (мКРРПЗ), що доведено у двох рандомізованих дослідженнях ІІІ фази, був доцетаксел (табл. 1). У дослідженні TAX 327 пацієнти (n=1006) були рандомізовані в групу доцетакселу 75 мг/м2 (1 раз на 21 день) та контрольну групу. У дослідженні SWOG9916 пацієнти отримували доцетаксел з естрамустином. В обох випадках учасники контрольної групи отримували мітоксантрон. Медіана загальної виживаності в групі доцетакселу (TAX 327) становила 18,9 проти 16,5 міс у контрольній групі (відношення ризиків – ВР – 0,76; 95% довірчий інтервал – ДІ – 0,62-0,94; р=0,009) зі значним зменшенням вираженості больового синдрому та покращенням якості життя. Аналогічні показники за даними D.P. Petrylak та співавт. (2004) становили 17,5 проти 15,6 міс (ВР 0,8; 95% ДІ 0,67‑0,97; р=0,02).
Через 12 міс терапії доцетакселом у значної кількості хворих спостерігався розвиток хіміорезистентного РПЗ, що потребувало корекції лікування. Для раннього виявлення цього стану необхідно вже протягом перших тижнів оцінити відповідь пацієнта на хіміотерапію: рівень ПСА, радіологічна оцінка пухлини.
Кабазитаксел
Дериватом доцетакселу є напівсинтетичний представник таксанів кабазитаксел. За результатами рандомізованого дослідження ІІІ фази TROPIC за участю пацієнтів з мКРРПЗ, які отримували доцетаксел, кабазитаксел був значно ефективнішим порівняно з мітоксантроном (медіана загальної виживаності становила 15,1 та 12,7 міс відповідно; ВР 0,70; 95% ДІ 0,59‑0,83; р<0,0001). В іншому клінічному дослідженні ІІІ фази FIRSTANA продемонстровано відсутність статистично значимої різниці виживаності у пацієнтів з мКРРПЗ, які не отримували хіміотерапїї, та пацієнтів, лікованих кабазитакселом (20 або 25 мг/м2) чи доцетакселом (75 мг/м2). Подібний результат було отримано у дослідженні ІІІ фази PROSELICA при порівнянні різних доз кабазитакселу (20 проти 25 мг/м2).
Сучасна гормональна терапія мКРРПЗ включає препарати групи інгібіторів андрогенного сигналу. Абіратерон та ензалутамід входять до рекомендацій EUA, Європейського товариства медичної онкології (ESMO), Національної онкологічної мережі США (NCCN) тощо з лікування як пацієнтів з мКРРПЗ, котрі отримували хіміотерапію, так і тих, кому її не проводили.
Абіратерон
Цей препарат є незворотним високоселективним інгібітором цитохрому P450 (CYP) 17А1, що в результаті призводить до зниження внутрішньопухлинної продукції андрогенів і синтезу андрогенів наднирковими залозами та яєчками. Абіратерон був схвалений у 2011 р. для лікування мКРРПЗ у пацієнтів, які отримали лікування доцетакселом, а у 2013 – для хворих, які не отримували хіміотерапії.
У рандомізованому подвійному сліпому плацебо-контрольованому дослідженні ІІІ фази COU-AA‑301 вивчали ефективність абіратерону з преднізолоном у пацієнтів (n=1195), які попередньо отримували лікування доцетакселом. Преднізолон призначали з метою профілактики гіпертензії, гіпокаліємії, затримки рідини, які можуть виникати через надлишок мінералокортикоїдів унаслідок пригнічення цитохрому P450. Остаточні результати дослідження COU-AA‑301 (медіана спостереження – 20,2 міс) свідчили про те, що медіана загальної виживаності була значно більшою в досліджуваній групі (абіратерон + преднізолон та АДТ), ніж у групі плацебо (лише АДТ) (15,8 проти 11,2 міс; ВР 0,74; 95% ДІ 0,64‑0,86; р<0,0001). У рандомізоване плацебо-контрольоване дослідження COU‑AA‑302 включали хворих без симптомів або з мінімальними симптомами, які раніше не отримували цитостатичних препаратів. Пацієнти (n=1088) були розподілені на групу абіратерону та преднізолону в комбінації з АДТ та групу плацебо, що отримувала тільки АДТ. Під час проміжного аналізу відмічено 25% зниження ризику смерті при застосуванні абіратерону (ВР 0,75; 95% ДІ 0,61‑0,93; р=0,01). Після спостереження з медіаною 49,4 міс зафіксовано значну перевагу у загальній виживаності, відповідні показники становили 34,7 проти 30,3 міс (ВР 0,81; 95% ДІ 0,70-0,93; р=0,0033).
Ензалутамід
Ензалутамід – нестероїдний інгібітор андрогенових рецепторів другого покоління, який пригнічує андрогенові рецептори не тільки на поверхні клітини, а і їх транслокацію всередину клітини та передачу сигналу поділу від андрогенових рецепторів до ДНК ядра клітини. Відомо, що при застосуванні антиандрогенів першого покоління (флутамід, бікалутамід) часто можлива конверсія дії препарату з антагоністів у агоністи андрогенових рецепторів, з антиандрогенами другого покоління ця реакція асоціюється значно рідше. Результати двох рандомізованих досліджень ІІ фази засвідчили вищу ефективність ензалутаміду порівняно з біклутамідом. Трайл TERRAIN включав 375 нелікованих хворих із мКРРПЗ. За його результатами медіана часу до прогресування захворювання становила 15,7 міс при лікуванні ензалутамідом + АДТ та 5,8 міс при лікуванні біклутамідом + АДТ (ВР 0,44; 95% ДІ 0,34‑0,57).
Дослідження STRIVE охопило 396 пацієнтів з метастатичним і неметастатичним кастраційно-резистентним РПЗ. Ензалутамід сприяв зниженню ризику прогресування чи смерті на 76% порівняно з бікалутамідом (ВР 0,24; 95% ДІ 0,18‑0,32).
Ензалутамід застосовується для лікування мКРРПЗ у хворих, у яких було прогресування захворювання на тлі використання доцетакселу або яким лікування доцетакселом не показане.
Рандомізоване подвійне сліпе плацебо-контрольоване багатоцентрове дослідження ІІІ фази AFFIRM включало 1199 хворих на мКРРПЗ, які отримували попереднє лікування доцетакселом. Ензалутамід забезпечив покращення медіани загальної виживаності на 4,8 міс (18,4 проти 13,6 міс; ВР 0,63; 95% ДІ 0,53‑0,75; р<0,001) та зниження ризику смерті на 37%. Окрім цього, ензалутамід показав кращий ефект, ніж плацебо (лише АДТ), щодо зниження рівня ПСА (54 проти 2%; р<0,001), відповіді м’яких тканин (29 проти 4%; р<0,001), якості життя (43 проти 18%; р<0,001), часу до наростання ПСА (8,3 проти 3,0 міс; ВР 0,25; р<0,001), часу до розвитку першого негативного наслідку з боку кісткової системи (16,7 проти 13,3 міс; ВР 0,69; р<0,001).
Інше плацебо-контрольоване подвійне сліпе дослідження ІІІ фази PREVAIL охопило 1717 хворих на кастраційно-резистентний РПЗ, які не отримували хіміотерапії. Призначення ензалутаміду супроводжувалося зниженням ризику смерті на 29% (ВР 0,71; 95% ДІ 0,60-0,84; р<0,001), покращенням радіологічної безрецидивної виживаності через 1 рік після початку терапії ензалутамідом (65 проти 14%; ВР 0,19; 95% ДІ 0,15-0,23), подовженням часу до початку хіміотерапії та часу до першої пов’язаної зі скелетом події.
Вищезазначені результати досліджень застосування ензалутаміду сприяли його схваленню для лікування мКРРПЗ у пацієнтів, які отримували доцетаксел, у 2012 р., і для хворих, які не отримували хіміотерапію доцетакселом, у 2014 р.
На сьогодні відсутні прямі порівняльні дослідження, у яких безпосередньо порівнювалися б ензалутамід з абіратероном. W. Zhang та співавт. виконали систематичний огляд і провели метааналіз багатьох рандомізованих досліджень із метою порівняти ефективність цих препаратів у лікуванні мКРРПЗ. За результатами непрямого порівняння статистично значима різниця у загальній виживаності відсутня (ВР 0,9; 95% ДІ 0,73-1,11 для пацієнтів, які проходили хіміотерапію; ВР 0,85; 95% ДІ 0,68-1,07 для пацієнтів без попередньої хіміотерапії). Ензалутамід може бути більш ефективним, ніж абіратерон, до та після хіміотерапії щодо часу до прогресування за рівнем ПСА (ВР 0,34; 95% ДІ 0,28-0,42; ВР 0,40; 95% ДІ 0,30-0,53), безрецидивної виживаності за даними радіологічних методів дослідження (ВР 0,37; 95% ДІ 0,28-0,48; ВР 0,61; 95% ДІ 0,50-0,74) та рівнем відповіді ПСА (ВР 18,29; 95% ДІ 11,20-29,88; ВР 10,69; 95% ДІ 3,92-29,20).
У 90% пацієнтів з мКРРПЗ досягається відповідь на терапію новими гормональними препаратами при призначенні їх у першій лінії [3, 4]. Ензалутамід у разі призначення в першій лінії має переваги перед абіратероном за рахунок кращої відповіді ПСА, нижчої частоти побічних ефектів з боку серцево-судинної системи та печінки, відсутності необхідності прийому кортикостероїдів і спеціального моніторингу [5].
Побічна дія
Щодо побічних реакцій, зумовлених прийомом інгібіторів андрогенного сигналу, то вони розвиваються з однаковою частотою у разі застосування ензалутаміду та абіратерону, але мають свої особливості. Поширеними (>5%) побічними явищами, пов’язаними з використанням абіратерону, були слабкість (39%), біль у кістках і м’язах (28-32%), периферичні набряки (28%), діарея, нудота та запори (22%), гіпокаліємія (17%), гіпофосфатемія (24%), фібриляція передсердь (4%) та серцеві розлади (19%), припливи (22%), інфекції сечових шляхів і дизуричні явища, ніктурія, кашель, гіпертензія (22%), підвищення рівня амінотрансфераз (11-12%). Саме внаслідок клінічних ефектів, що пов’язані з прийомом преднізолону, пацієнти, які приймають абіратерон, потребують постійного моніторингу. Найчастішими побічними явищами, що спостерігались при лікуванні ензалутамідом, були слабкість (34%), діарея (21%), припливи (20%), головний біль (12%) та запаморочення (0,6%).
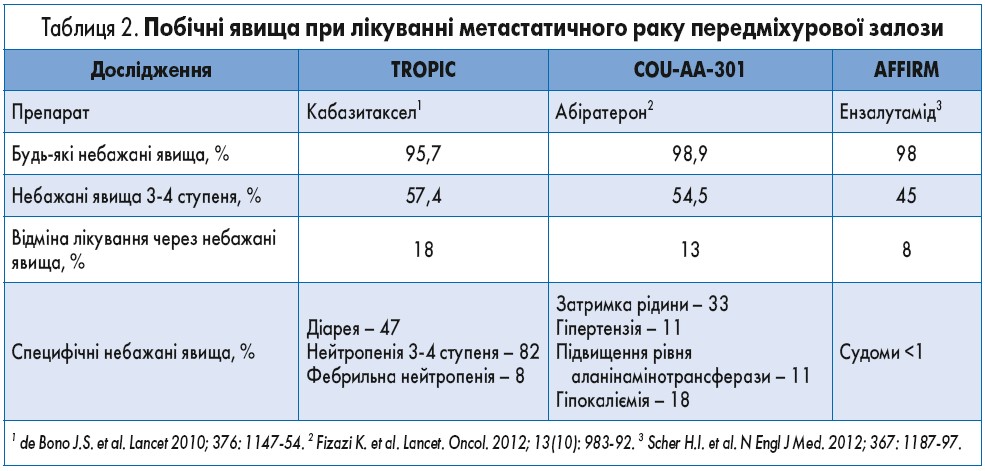
За даними R. de Wit та співавт. (2019), після попередньої терапії доцетакселом частота побічних явищ будь-якого ступеня (94,4 проти 98,4%) та, зокрема, 3 ступеня тяжкості (52,4 проти 56,3%) була дещо вищою у групі кабазитакселу, ніж у групі абіратерону чи ензалутаміду (табл. 2).
Інші засоби гормональної терапії
Апалутамід у рандомізованому подвійному сліпому плацебо-контрольованому багатоцентровому клінічному дослідженні III фази TITAN (1052 пацієнтів) продемонстрував свою ефективність порівняно з плацебо при метастатичному гормоночутливому РПЗ (мГЧРПЗ).
У 2018 р. погоджено застосування апалутаміду для лікування хворих на неметастатичний кастраційно-резистентний РПЗ (нмКРРПЗ) на основі збільшення безметастичної виживаності хворих, які отримували апалутамід + АДТ порівняно з плацебо (лише АДТ; III фаза SPARTAN).
Даролутамід (ODM‑201) є новим представником інгібіторів андрогенного сигналу. У трайлах І-ІІ фази ARADES препарат продемонстрував свою ефективність і безпеку у лікуванні мКРРПЗ. Продовжуються активні дослідження ІІІ фази із застосування даролутаміду при мГЧРПЗ та нмКРРПЗ.
Ортеронел (ТАК‑700) – нестероїдний зворотний селективний інгібітор 17,20-ліази. Цей препарат у двох дослідженнях ІІІ фази не забезпечував подовження загальної виживаності при мКРРПЗ. Севітеронел (VT‑464) також є нестероїдним інгібітором 17,20-ліази. Препарат вивчають у трайлах ІІ фази.
Біполярна андрогенотерапія
Ця методика була запропонована M.T. Schweizer та співавт., які використовували ін’єкції тестостерону з конкурентною АДТ з метою досягнення швидкої зміни максимального і мінімального рівнів тестостерону. Такий підхід у комбінації з етопозидом забезпечив обнадійливий результат у пацієнтів з мКРРПЗ. Проводиться декілька досліджень, присвячених вивченню цього парадоксального феномену з препаратами другого покоління антиандрогенів, хіміотерапевтичними й імунотерапевтичними засобами. У дослідження ІІІ фази TRANSFORMER (NCT02286921) включили пацієнтів з мКРРПЗ та рефрактерністю до абіратерону з метою вивчення застосування у них ензалутаміду та біполярної андрогенотерапії. Результатів поки не оприлюднювали.
Висновки
Гормонотерапія та хіміотерапія відіграють важливу роль у лікуванні хворих на мКРРПЗ. Сьогодні відсутні міжнародні рекомендації, які б на основі принципів доказової медицини визначали кращу послідовність препаратів для лікування мКРРПЗ. Перевага надається лікарським засобам, що підвищують кастраційноспецифічну виживаність, при цьому враховуються профіль їхньої токсичності й індивідуальні характеристики здоров’я пацієнта. Вибір терапії першої лінії має базуватися на соматичному статусі, симптомах захворювання, локалізації та ступені поширеності захворювання, а також видах лікування, які були використані при вперше виявленому метастатичному РПЗ у конкретного пацієнта [2].
Тривають дослідження й активне розроблення новітніх лікарських засобів (у тому числі PARP-інгібіторів, імунопрепаратів, PI3K-інгібіторів і таргетних препаратів до простатичного специфічного мембранного антигену).
Головним завданням дослідників і клініцистів залишається забезпечення максимально можливої тривалості життя пацієнта при збереженні його якості.
Література
- Hou X, Flaig TW. Adv Urol 2012; 2012: 978351.
- Mottet N et al. EAU Guidelines on Prostate Cancer 2019. Available from: http://uroweb.org/guideline/prostate-cancer.
- Ryan et al. Lancet Oncol. 2015;16: 152-160.
- Beer TM et al. N Engl J Med 2014; 371: 424-33.
- Chopra et al. Prostate. 2017 May; 77(6):639-646. doi: 10.1002/pros.23309. Epub 2017 Jan 19.
- Рекомендації EAU2019 з приводу послідовності терапії у пацієнтів з мКРРПЗ.
- EAU Guidelines 2019 EAU=European Association of Urology.
Підготувала Олена Поступаленко
Тематичний номер «Онкологія. Гематологія. Хіміотерапія» № 1 (62), 2020 р.