24 квітня, 2020
Альтернативные гликированному гемоглобину маркеры контроля СД
Сахарный диабет (СД) – это хроническое метаболическое заболевание, вызванное абсолютной или относительной недостаточностью инсулина, нарушением чувствительности тканей к инсулину, что проявляется гипергликемией. В настоящее время заболеваемость СД приобрела характер эпидемии и является проблемой для здравоохранения во всем мире. На сегодня, согласно статистическим данным, 415 млн человек болеют СД. По прогнозу Международной федерации диабета (IDF), к 2040 г. количество больных составит 642 млн.
Основной причиной развития осложнений СД является поражение сосудов. Прежде всего страдает микроциркуляция, то есть нарушается кровоснабжение по мельчайшим сосудам. Симптомы диабетических нарушений проявляются в виде нефропатии, ангиопатии, ретинопатии, нейропатии. Эти симптомы обнаруживаются слишком поздно, что обрекает человека на гибель, в лучшем случае – на инвалидность. Несмотря на то что уровень глюкозы является основным фактором и диагностическим маркером для СД, существует жизненно важная необходимость на время забыть о глюкозе и искать дополнительные биомаркеры, которые помогли бы диагностировать диабет с безошибочной точностью, а также прогнозировать риск развития осложнений.
Золотой стандарт гликемического контроля
Повышение концентрации глюкозы в крови значительно увеличивает ее поступление в клетки за счет инсулиннезависимых механизмов. В результате этого неферментативно происходит гликилирование гемоглобина, альбумина, трансферрина, аполипопротеинов, коллагена, белков эндотелия, хрусталика и некоторых других белков. Степень гликирования разных белков неодинакова и в каждом случае зависит не столько от степени повышения концентрации глюкозы, сколько от времени жизни конкретного белка, то есть от скорости его обновления. В медленно обменивающихся (так называемых долгоживущих) белках накапливается больше модифицированных аминогрупп, тогда как в короткоживущих – меньше. Поэтому при присоединении глюкозы функции белка могут нарушаться вследствие изменения заряда белковой молекулы, нарушения ее конформации или по причине блокирования активного центра. Это приводит к многочисленным осложнениям диабета. Гликированный гемоглобин (HbA1c) – самый значимый параметр, используемый в повседневной клинической практике как золотой стандарт гликемического контроля. HbA1c является эталонным тестом для гликемического мониторинга, так как он напрямую отражает среднюю гликемию и имеет сильную корреляцию с отдаленными осложнениями СД.
Преимущества теста HbA1c
HbA1c, являющийся адекватным показателем уровня гликемии, позволяет надлежащим образом оценить риск развития осложнений. Тест стандартизирован, стабилен, имеет низкую вариабельность. Нет необходимости в частых измерениях и проведении последних исключительно натощак. Содержание HbA1c не зависит от питания, времени суток, приема лекарственных препаратов, физических нагрузок, стресса. Поскольку период полужизни эритроцитов составляет 60 сут, то принимают, что этот параметр является усредненной характеристикой, отражающей карбогидратный баланс в течение предыдущих 2 мес в виде усредненной ежедневной концентрации глюкозы.
Ограничения теста HbA1c
Тест HbA1c используется в диабетологии с 1976 г., при этом он имеет определенные ограничения. Так, с учетом возраста и индекса массы тела (ИМТ) более высокие зачения HbA1c наблюдаются у мужчин (на 0,3%) и женщин (0,4%) негроидной расы без диабета по сравнению с представителями европеоидной расы соответствующего пола. Переменные, которые могут влиять на гликемию (возраст, пол, ИМТ, давление крови, пре- и постпрандиальная гликемия, деятельность β-клеток, инсулинорезистентность, уровень гематокрита) были рассмотрены при использовании метода множественной линейной регрессии. Показано, что афро- и латиноамериканцы имели более высокие уровни HbA1c по сравнению с европейцами. Ложное повышение HbA1c наблюдались в случае дефицита витамина В12, фолиевой кислоты, железодефицитной анемии, а также при хронической болезни почек, гипербилирубинемии, приеме в больших дозах ацетилсалициловой кислоты, у лиц, употребляющих опиаты, у пациентов после спленэктомии и с патологической структурой эритроцитов. И наоборот, ложное снижение отмечено у пациентов, которые получали препараты железа, витамин В12, фолиевую кислоту, эритропоэтин, витамины С и Е. Похожие эффекты наблюдались у лиц с укороченным периодом продолжительности жизни эритроцитов: при массивных кровопотерях, гемолитической анемии, гемоглобинопатии, спленомегалии, хронической алкогольной зависимости, а также у пациентов с гипертриглицеридемией, ревматоидным артритом, больных, получающих ретровирусную терапию.
Фетальный гемоглобин (HbF) является основным гемоглобином во время внутриутробного развития и составляет до 90% при рождении. В течение первого года жизни концентрация HbF снижается до значений, наблюдаемых у взрослых, что составляет примерно 1%. Увеличение уровня HbF может происходить при патологических состояниях, таких как лейкемия, анемия, талассемия, или при наследственной персистенции фетального гемоглобина, в результате чего его значения достагают 30%. Это состояние является бессимптомным, что может повлиять на концентрацию HbA1c. Более того, HbA1c не является хорошим маркером контроля гликемии у детей с неонатальным диабетом из-за присутствия фетального гемоглобина. Ложное снижение значения HbA1c может возникнуть у пациентов с диабетом и нарушенной функцией почек, что связано с уменьшением продолжительности жизни эритроцитов при использовании препаратов рекомбинантного человеческого эритропоэтина или на фоне терапии железом. Уремия, изменения рН крови или наличие карбамилированного гемоглобина, а также необходимость трасфузии у пациентов с прогрессирующим повреждением почек приводит к снижению значений HbA1c независимо от изменений уровня гликемии.
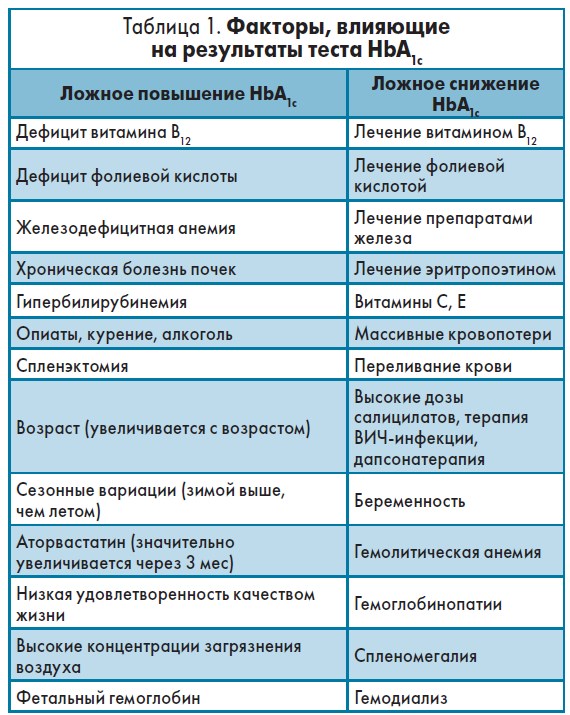 Факторы, влияющие на результаты теста HbА1c, представлены в таблице 1.
Факторы, влияющие на результаты теста HbА1c, представлены в таблице 1.
Необходимо отметить, что тест HbA1c является широко распространенным в клинической практике для осуществления мониторинга уровня глюкозы в крови больных СД. Однако в ряде случаев, когда проведение его затруднено по различным причинам, могут довольно успешно использоваться другие методы. Так, на практике применяются такие тесты, как фруктозамин, гликированные сывороточные белки (GSP) и гликированный альбумин (ГА).
Фруктозамин
Фруктозамин образуется в процессе неферментативного гликирования карбонильной группы глюкозы с аминогруппами циркулирующих сывороточных белков, в основном альбуминов. В связи с более коротким периодом полужизни сывороточных белков по сравнению с продолжительностью жизни эритроцитов концентрация фруктозамина является краткосрочным маркером и позволяет проводить ретроспективную оценку концентрации глюкозы за период 10-14 дней, а по данным некоторых авторов – за 21 день, что служит альтернативой, когда результаты HbA1c не могут быть достоверными. Это также полезно при мониторинге пациенток с гестационным диабетом, поскольку данный тест показывает динамику изменения и контроля гликемии за короткий промежуток времени. Тем не менее фруктозамин не является идеальным маркером, так как на него влияют изменения концентрации сывороточных белков, дислипопротеинемии. Ложное снижение содержания фруктозамина может быть связано с более низким уровнем белка и/или альбумина в результате потери с мочой, например при нефротическом синдроме, при нарушении поглощения белка в пищеварительном тракте, например при мальабсорбции или нарушении синтеза белка при циррозе печени. Данный тест не выполняется, если концентрация альбумина в сыворотке ниже 30 г/л. Фруктозамин используется реже из-за его более низкой чувствительности, зависимости от концентрации белка в крови и метаболизма, уровня гидратации, концентрации билирубина в сыворотке или гемолиза. Вместе с тем различные исследования у лиц с хронической болезнью почек (стадии 3 и 4) показали хорошую корреляцию между уровнем фруктозамина и гликемией у диабетических пациентов и у находящихся на гемодиализе больных.
Метод определения фруктозамина
Гликилированные белки крови способны превращать нитросиний тетразолий (NBT) в щелочной среде в формазан с образованием пурпурного окрашивания с максимумом поглощения при λ=530 нм. Для определения фруктозамина используют стабильный NBT реагент и калибратор на основе человеческой сыворотки. Образец добавляют к реагенту и инкубируют. Через 10 и 15 мин измеряют абсорбцию. Изменения в абсорбции сравнивают со стандартом и рассчитывают концентрацию фруктозамина. Референсные значения для женщин составляют 161-351 мкмоль/л, для мужчин – 118-282 мкмоль/л.
Применение теста для определения фруктозамина, а не гликированного гемоглобина является более эффективным в следующих случаях:
- при внесении резких изменений в план лечения СД фруктозамин позволяет оценить эффективность применяемой коррекции лечения в течение нескольких недель вместо нескольких месяцев;
- в период беременности, когда в организме матери происходят значительные изменения, контроль уровня глюкозы у пациенток с СД приобретает особенно важное значение. Анализ на фруктозамин можно проводить одновременно с анализами на глюкозу, чтобы правильно подобрать дозу инсулина;
- при снижении количества эритроцитов тест на HbA1c не будет достаточно точным (гемолитическая анемия или кровопотери).
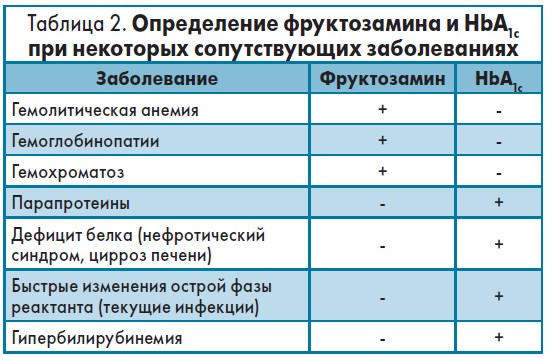 Присутствие некоторых форм гемоглобина также может оказывать влияние на применяемые методы его измерения. В таких случаях фруктозамин является единственным показателем, адекватно отражающим уровень глюкозы в крови (табл. 2).
Присутствие некоторых форм гемоглобина также может оказывать влияние на применяемые методы его измерения. В таких случаях фруктозамин является единственным показателем, адекватно отражающим уровень глюкозы в крови (табл. 2).
Метод определения фруктозамина на основе колориметрического теста с использованием нитросинего тетразолия применяется в повседневной лабораторной практике, однако он имеет ряд недостатков. Так, на концентрацию фруктозамина оказывают влияние витамин С, билирубин и глутатион. Это в конечном итоге приводит к неточным результатам.
Гликированные сывороточные белки
Учитывая недостатки теста с использованием нитросинего тетразолия при определении фруктозамина, был разработан альтернативный простой, чувствительный и быстрый тест для контроля гликемии, в котором используется высокоспецифичный фермент фруктозил-амино-оксидаза для элиминирования интерферирующих веществ. Набор под названием Glycated Serum Protein LiquiColor® Assay (EKF Diagnostics Inc., США) специфичен для всех гликированных белков, включая альбумин, гемоглобин и др.
 Новый анализ гликированных белков сыворотки LiquiColor получил одобрение Управления по контролю качества продуктов питания и лекарственных средств США (FDA), регуляторных органов Европейского союза (имеет знак CE).
Новый анализ гликированных белков сыворотки LiquiColor получил одобрение Управления по контролю качества продуктов питания и лекарственных средств США (FDA), регуляторных органов Европейского союза (имеет знак CE).
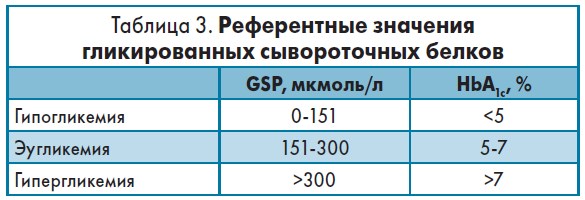
Референтные значения GSP представлены в таблице 3.
«Пробел в гликировании»
Исследования показывают, что комбинация результатов GSP с измерением HbA1c обеспечивает лучшую оценку риска долгосрочного осложнения диабета. GSP заполняет так называемый пробел в гликировании, который представляет собой разницу между фактически измеренным значением HbA1c и предсказанным HbA1c значением GSP в сыворотке крови (рис. 1). Это дает возможность надежно прогнозировать осложнения диабета, включая нефропатию и ретинопатию
GSP как гликемический маркер может использоваться у пациентов при таких клинических состояниях, как терминальная стадия почечной недостаточности и гемодиализ; гемоглобинопатии; лечение эритропоэтином; гемолитическая анемия; острая кровопотеря; беременность; любое состояние/лечение, которое влияет на продолжительность жизни эритроцитов.
Гликированный альбумин
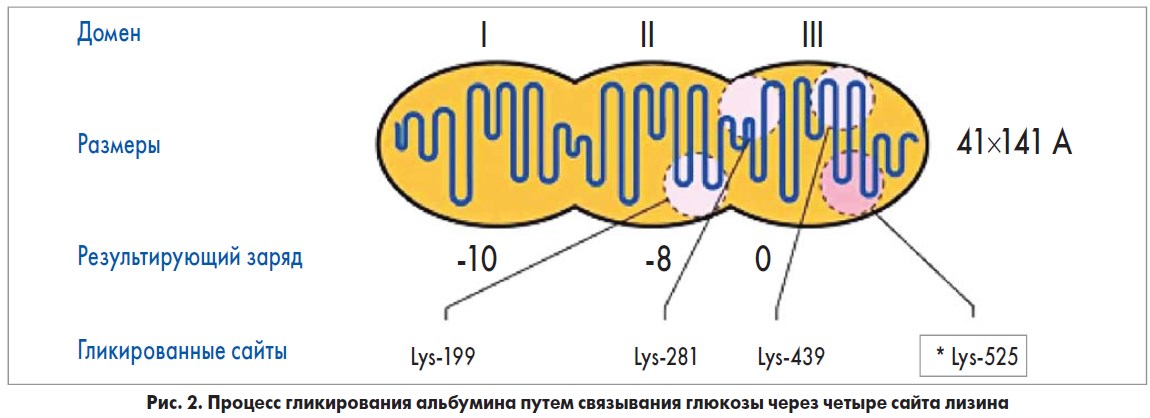
Альбумин – высокомолекулярный белок с молекулярной массой 66,7 кДа, состоящий из одной полипептидной цепи, которая содержит 585 аминокислот, 17 дисульфидных мостиков и 3 гомологичных домена, связанные в спиральную структуру. Это основной белок плазмы, который составляет около 60% от общего белка крови с концентрацией от 35 до 50 г/л и периодом полураспада от 14 до 20 дней. Структура альбумина способствует выполнению его физиологических функций, таких как поддержание рН и осмотического давления. Кроме того, альбумин действует как мощный антиоксидант и основной транспортер продуктов метаболизма, ионов, питательных веществ, гормонов и жирных кислот. Подобно другим белкам, альбумин принимает участие в физиологическом процессе гликирования. Гликирование (реакция Mailard) является неферментативной спонтанной реакцией, в которой глюкоза связывается со свободной аминогруппой (обычно лизин или аргинин), присутствующей в белке. Первый шаг этой реакции включает образование нестабильного и обратимого продукта, известного как основание Шиффа, между карбонильной группой ациклического углевода и N-концом аминокислоты. Этот промежуточный продукт подвергается коформационным изменениям и приводит к стабильному и необратимому продукту, известному как Амадори продукт, который представляет собой фруктозолизин, то есть реакцию между глюкозой и лизином, встречающийся на 59 сайтах лизина в альбумине. Лизин 525 был идентифицирован как самый большой сайт гликирования альбумина, что подтверждается в экспериментах in vivo и in vitro (рис. 2).
Кетоамины, образованные неферментативным гликированием, имеют химическое название «фруктозамин». Среди фруктозаминов сыворотки ГА является основным компонентом и составляет около 80% от общих гликилированных белков плазмы. Концентрация глюкозы и время экспозиции между белком и глюкозой считаются определяющими факторами гликирования, которое происходит в течение жизни белка, то есть гликирование зависит от степени и длительности гипергликемии. Внеклеточный белок, каким является альбумин, более восприимчив к Амадори перестройке, чем внутриклеточный белок гемоглобин. Это объясняет различия в скорости гликирования альбумина, которая в 9-10 раз выше, чем у гемоглобина. В экспериментах было доказано, что синтез ГА был примерно в 4,5 раза больше, чем HbA1c, после добавления известных концентраций глюкозы в образцы здоровых добровольцев. Эти данные показывают, что даже при одинаковом гликировании в условиях in vitro ГА синтезируется быстрее, чем HbA1c.
Гликированный альбумин для мониторинга глюкозы
В отличие от долгосрочного образования HbA1с (средняя продолжительность жизни эритроцитов – около 120 дней) ГА образуется в течение периода от 2 до 4 нед. Это повышает чувствительность ГА к быстрым изменениям уровня глюкозы. Поэтому измерение ГА больше подходит для мониторинга начала медикаментозной терапии при СД, а также для контроля дозирования или замены лекарственного препарата, так как его уровни при интенсивном лечении изменяются быстрее, чем HbA1c.
Лабораторный метод измерения ГА
Исторически фруктозамин использовался в клинической практике, когда была необходимость в краткосрочной оценке гликемии. При этом данный тест имеет низкую точность, так как на его результат влияют многие молекулы, присутствующие в крови, такие как билирубин, мочевая кислота и низкомолекулярные вещества. Не существует также международных стандартов его применения.
Методы оценки ГА были разработаны в 1980-х годах с использованием сыворотки или плазмы крови. Эти методы имели многочисленные недостатки из-за сложности выполнения, высокой стоимости и/или неточности. Отсутствие стандартизации данного теста привело к непопулярности ГА, и все внимание было направлено на HbA1c. ГА может быть измерен с помощью ионообменной высокоэффективной жидкостной хроматографии (ВЭЖХ), боронат-аффинной хроматографии, иммуноанализом, колориметрическим методом с тиобарбитуровой кислотой и ферментативными методами с использованием протеиназы и кетаминоксидазы. Однако эти методы не доступны в рутинной лабораторной практике.
Новый набор Lucica® Glycated Albumin-L (Asahi-Kasei Pharma Corporation, Япония) представляет собой ферментативный метод для определения ГА с быстрым временем исследования и упрощенной процедурой; может выполняться как вручную, так и на автоматических биохимических анализаторах.
Метод определения ГА включает 3 этапа. На первом этапе гликированные аминокислоты высвобождаются из ГА посредством действия альбумин-специфичной протеазы. Кетоаминоксидаза расщепляет ГА на свободные аминокислоты и глюкозон, который является промежуточным продуктом реакции Амадори. Окрашивание прямо пропорционально количеству ГA в образце. На втором этапе альбумин плазмы реагирует с бромкрезоловым зеленым в кислой среде, в результате чего образуется окрашенное соединение, которое напрямую связано с общей концентрацией альбумина. Третий этап состоит в математическом расчете с определением процента ГA с учетом двух предыдущих реакций.
Референтные значения ГА
В 2006 г. Японское диабетическое общество установило референтный интервал для ГA от 12,3 до 16,9%. Несколько лет спустя в более крупном исследовании (n=1575) опубликован референтный интервал для ГA от 12,2 до 16,5%. Кроме того, это исследование показало, что cut-off для ГА ≥15,5% имеет хорошую чувствительность и специфичность для выявления СД с использованием глюкозы натощак и HbA1c (≥7,0 ммоль/л и ≥6,5% соответственно) в качестве контрольных тестов.
Ограничения при использовании ГА
В некоторых случаях нарушение метаболизма альбумина может влиять на значение ГА. Не рекомендуется использовать ГА как маркер при гипер- и гипотиреозе, циррозе печени, нефротическом синдроме с массивной протеинурией. Концентрация ГА зависит от возраста, ИМТ, наличия/отсутствия воспаления (повышенный уровень С-реактивного белка) и гипертриглицеридемии, статуса курения. В связи с этим при интерпретации уровней ГА в некоторых клинических ситуациях необходимо проявлять осторожность.
Выводы
Лабораторные исследования для определения HbA1c и гликированных белков необходимы в первую очередь для мониторинга уровня глюкозы крови у больных СД. Хотя анализ на гликированный гемоглобин является более распространенным, в ряде случаев, когда его проведение затруднено, может успешно использоваться анализ на гликированные белки. Особенно это важно для пациентов, находящихся на гемодиализе. Во многих исследованиях было показано, что определение ГА имеет хорошую диагностическую точность и тесно связано с диабетическими микрососудистыми осложнениями. Несмотря на все свои преимущества, ГА не заменяет использование HbA1c, так как и тот и другой тест имеют свои достоинства и недостатки.
Список литературы находится в редакции.